国際特許分類[C07C253/14]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | 非環式化合物または炭素環式化合物 (64,036) | カルボン酸ニトリルの製造 (747) | ハロゲン原子のシアノ基による置換を伴う,シアン化物とハロゲン含有化合物との反応によるもの (19)
国際特許分類[C07C253/14]に分類される特許
1 - 10 / 19
ニトリル化合物の製造方法
【課題】金属触媒を使用することなく、芳香族化合物の無置換位置に直接シアノ基を導入することが可能な、芳香族ニトリル化合物の製造方法を提供する。
【解決手段】芳香族化合物と、ホルムアミド化合物と、強塩基性化合物と、アンモニア水と、ヨウ素化剤とを混合することにより、上記芳香族化合物をワンポットでシアノ化するか、芳香族化合物と強塩基性化合物とを混合して反応させた後、ホルムアミド化合物とアンモニア水とヨウ素化剤とを更に混合することにより、上記芳香族化合物をシアノ化する。
(もっと読む)
シクロプロピルアミド誘導体及びそれに関連する中間体の製造方法
式Iのシクロプロピルアミド誘導体、及び/又はその製薬学的に許容される塩の製造方法、及びそれに関連する中間体が提示されている。式Iの少なくとも1つのシクロプロピルアミド誘導体、又はその製薬学的に許容される塩は、少なくとも1つのヒスタミンH3受容体が関連する状態を処置するのに有用である。 (もっと読む)
1−(2−ハロビフェニル−4−イル)−シクロプロパンカルボン酸の誘導体の調製方法
本発明は、式(IA)で示される化合物を調製する方法に関する。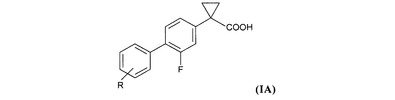
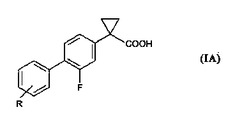 (もっと読む)
(もっと読む)
2−アミノ−5−シアノ安息香酸誘導体を調製するための方法
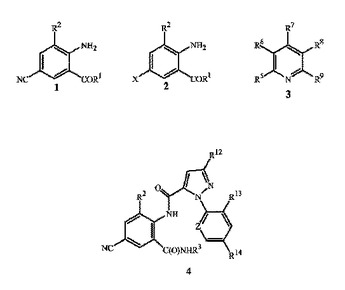
式2の化合物を、金属シアン化物試薬、銅(I)塩試薬、ヨウ化物塩試薬および式3の少なくとも1種の化合物
【化1】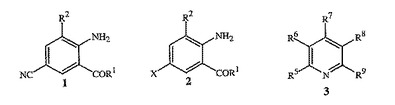
(式中、R1はNHR3またはOR4であり;R2はCH3またはClであり;R3は、H、C1〜C4アルキル、シクロプロピル、シクロプロピルシクロプロピル、シクロプロピルメチルまたはメチルシクロプロピルであり;R4はHまたはC1〜C4アルキルであり;Xは、BrまたはClであり;ならびに、R5、R6、R7、R8およびR9は、開示中に定義されているとおりである)
と接触させる工程を含む式1の化合物を調製する方法が開示されている。
式1の化合物を上記に開示の方法により調製する工程、または、上記に開示の方法により調製した式1の化合物を用いる工程により特徴付けられる、式1の化合物を用いて、R12、R13、R14およびZが開示中に定義されているとおりである式4の化合物を調製する方法もまた開示されている。
【化2】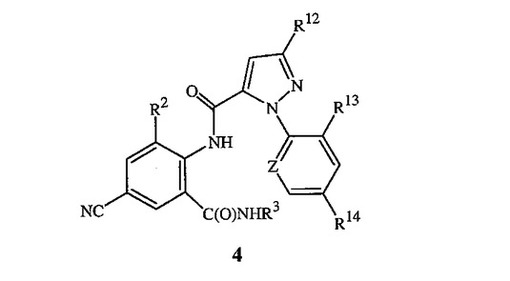
 (もっと読む)
(もっと読む)
ヨウ化物と、それを用いた酸化的不斉スピロ環形成方法
【課題】新規ヨウ化物と、それを用いた酸化的不斉スピロ環形成方法の提供。
【解決手段】式(I)で表わされるヨウ化物またはその塩、式(II)で表わされるヨウ化物またはその塩である。また、式(X)で表わされる化合物に、(i)前記式(I)で表わされるヨウ化物もしくはその塩の光学活性体を触媒量および、酸化剤とを、または(ii)前記式(II)で表わされるヨウ化物もしくはその塩の光学活性体とを反応させ、式(XI)で表わされる化合物の光学活性体を得る工程を含む酸化的不斉スピロ環形成方法。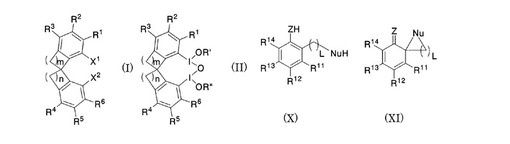 (もっと読む)
(もっと読む)
炭素−ヘテロ原子間及び炭素−炭素間結合の銅を触媒とした形成
【課題】安価な銅を触媒とした、広範囲な炭素−ヘテロ原子間及び炭素−炭素間結合形成法を提供する。
【解決手段】いくつかの実施態様では、アミド、アミンアシルヒドラジン部分の窒素原子と、ハロゲン化もしくはスルホン化アリール、ヘテロアリール、又はビニルの活性化炭素との間に炭素−窒素間結合を形成する銅触媒方法。更なる実施態様では、インドール、ピラゾール、及びインダゾールなどの窒素含有複素環式芳香族の窒素原子と、上記と同様な活性化炭素との間に炭素−窒素間結合を形成する銅触媒法。いくつかの実施態様では、アルコールの酸素原子と、上記と同様な活性化炭素との間に炭素−酸素間結合を形成する銅触媒法。さらに、エノラート陰イオン又はマノレート陰イオンなどの求核性炭素原子を含む反応体と、上記と同様な活性化炭素との間に炭素−炭素間結合を形成する銅触媒法。
(もっと読む)
2−アミノ−5−シアノ安息香酸誘導体を調製するための方法
式2の化合物と、少なくとも1種の式3のアルカリ金属シアン化物および式4の化合物とを接触させる工程を含む式1の化合物を調製する方法が開示されている。
【化1】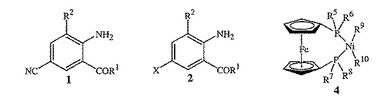
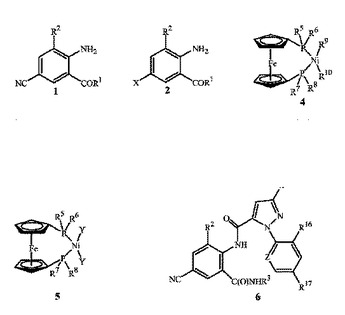
式中、R1はNHR3またはOR4であり;R2はCH3またはClであり;R3は、H、C1〜C4アルキル、シクロプロピル、シクロプロピルシクロプロピル、シクロプロピルメチルまたはメチルシクロプロピルであり;R4はHまたはC1〜C4アルキルであり;Xは、Br、ClまたはIであり;ならびに、R5、R6、R7、R8、R9およびR10は本開示中に定義されているとおりである。
また、YがCl、BrまたはIである式5の化合物と、シクロアルカジエン二座リガンド、少なくとも1種の金属還元剤およびニトリル溶剤とを接触させる工程を含む、R9およびR10が一緒になってシクロアルカジエン二座リガンドである式4の化合物を調製する方法もまた開示されている。
また、式5の化合物と、シクロアルカジエン二座リガンドおよび少なくとも1種の金属還元剤とを接触させることにより式4の化合物を調製する工程、次いで、式4の化合物を含むこの反応混合物と式2の化合物および式3の少なくとも1種のアルカリ金属シアン化物とを接触させる工程を含む式1の化合物を調製する方法も開示されており;ならびに、式1の化合物を上記に開示の方法により調製することを特徴とする、R15、R16、R17およびZが式1の化合物を用いて本開示中に定義されているとおりである式6の化合物を調製する方法がさらに開示されている。
【化2】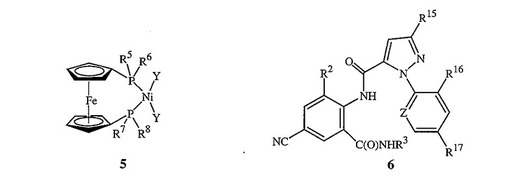
 (もっと読む)
(もっと読む)
(7−メトキシ−1−ナフチル)アセトニトリル合成のための新規な方法及びアゴメラチンの合成における用途
本発明は、式(I)の化合物の工業的合成方法に関連する。本発明は、アゴメラチンの合成に使用することができる。 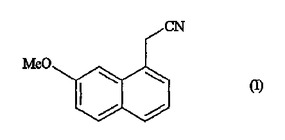 (もっと読む)
(もっと読む)
2−アミノ−5−シアノ安息香酸誘導体の製造方法
(1)式2の化合物を、(2)少なくとも1つのシアン化アルカリ金属および(3)少なくとも1つの式4
【化1】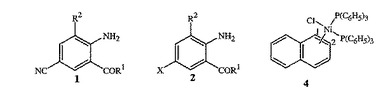
[式中、R1はNHR3またはOR4であり、R2はCH3またはClであり、R3はH、C1〜C4アルキル、シクロプロピル、シクロプロピルシクロプロピル、シクロプロピルメチルまたはメチルシクロプロピルであり、R4はHまたはC1〜C4アルキルであり、XはBr、ClまたはIである]の化合物と接触させることを含む式1の化合物の製造方法を開示する。
また(i)少なくとも1つの式9の化合物と(ii)少なくとも1つの金属還元剤との混合物を、(iii)ジクロロビス(トリフェニルホスフィン)ニッケルと接触させることを含む式4の化合物の製造方法も開示する。さらに式1の化合物とのニッケル不純物の混合物からニッケル不純物を除去するための方法であって、シアン化物水溶液の存在下で、混合物を酸素と接触させることを含む方法を開示する。加えて式5
【化2】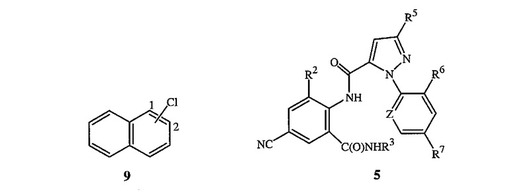
[式中、R5、R6、R7およびZは開示中に定義されるとおりである]の化合物を、式1の化合物を使用して製造する方法であって、上記開示された方法によって式1の化合物を製造することを特徴とする方法を開示する。 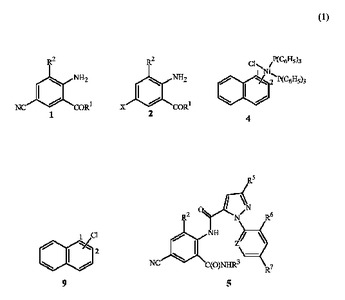 (もっと読む)
(もっと読む)
芳香族または複素芳香族ニトリルを触媒的に製造する方法
【課題】芳香族または複素芳香族ニトリルを触媒的に製造する方法を提供する。
【解決手段】一般式(I)Ar−CNの、場合により置換された芳香族または複素芳香族ニトリルを、一般式(II)Ar−X(式中、Xは塩素、臭素、ヨウ素、トリフラート、ノナフラート、メシラートまたはトシラートであり、そしてArは場合により置換された芳香族または複素芳香族基である)の対応するハロゲン化アリールを反応させることによって触媒的に製造する方法であって、反応が、パラジウム化合物、一般式(III)または(IV)
(式中、Rはアルキル基であり、そしてR’、R’’およびR’’’はそれぞれアルキル基またはアリール基またはヘテロアリール基であり、そしてAはアルキレン基またはアリーレン基である)のホスフィン、ならびにヘキサシアノ鉄(II)酸カリウムまたはヘキサシアノ鉄(III)酸カリウムの存在下に、場合により溶媒中でおよび場合により塩基を添加して行われることを特徴とする方法が記載される。
(もっと読む)
1 - 10 / 19
[ Back to top ]