国際特許分類[C07C29/40]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | 非環式化合物または炭素環式化合物 (64,036) | 6員芳香環に属していない炭素原子に結合している水酸基またはO―金属基をもつ化合物の製造 (1,729) | 水酸基の生成を伴う炭素原子数の増加する反応によるもの。水酸基の誘導体,例.O―金属基,を中間体として経由する場合も含む (102) | アルデヒドまたはケトンとの反応によるもの (89) | 炭素―金属結合を含有する化合物とのもの (41)
国際特許分類[C07C29/40]に分類される特許
1 - 10 / 41
新規パーフルオロアルキル化剤及びそれを用いたパーフルオロアルキル基含有化合物の製造方法
【課題】新規なパーフルオロアルキルマグネシウム−ジルコニウムアート錯体を提案する。
【解決手段】パーフルオロマグネシウムハライドと、下記一般式(2)
(式中Mはチタン原子またはジルコニウム原子を示し、Xはハロゲン原子を示す)で表されるメタロセンジハライド及びパーフルオロアルキルアイオダイドを反応させることにより調製されるパーフルオロアルキル化剤及びそれを用い各種パーフルオロアルキル基含有化合物を調製する。
(もっと読む)
2−(置換フェニル)−1−ハロ−1,1−ジフルオロプロパン−2−オール化合物及びその製造法
【課題】有害生物防除剤として有用な置換イソキサゾリン化合物の新規な製造中間体の提供。
【解決手段】式(2)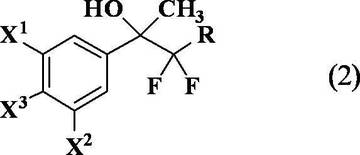
[式中、X1は、ハロゲン原子、C1〜C6アルキル等を表し、X2は、ハロゲン原子、C1〜C6ハロアルキル等を表し、X3は、水素原子、ハロゲン原子等を表し、Rは、ハロゲン原子を表す。]で表される2−(置換フェニル)−1−ハロ−1,1−ジフルオロプロパン−2−オール化合物及びその製造方法、並びに2−(置換フェニル)−3−ハロ−3,3−ジフルオロプロペン化合物の製造方法。
(もっと読む)
新規含フッ素有機マグネシウムアルコキシド及びそれを用いた含フッ素化合物の製造方法
【課題】新規なパーフルオロアルキルマグネシウムアルコキシド又はパーフルオロアリールマグネシウムアルコキシドを提供する。
【解決手段】下式(1)で表されるアルキルマグネシウムハライドと、下式(2)で表されるカリウムアルコキシド類又はアルコール類から調製される、下式(3)で表されるアルキルマグネシウムアルコキシドに、下式(4)で表されるハロゲン化物を添加し調製される、下式(5)で表されるパーフルオロアルキルマグネシウムアルコキシド又はパーフルオロアリールマグネシウムアルコキシド。
R1MgX(1);R2OA(2);R1MgOR2(3);RfX(4);RfMgOR2(5)[式中、R1はメチル基、エチル基等を表し、Xはハロゲン原子を表し、R2はメチル基、エチル基等を表し、Aはカリウム原子又は水素原子を表し、Rfはパーフルオロアルキル基又はパーフルオロアリール基を表す。]
(もっと読む)
パーフルオロアルキル(有機亜鉛)−リチウム錯体及びそれを用いたパーフルオロアルキル基含有アルコール類の製造方法
【課題】 パーフルオロアルキル基を各種有機化合物に導入可能な新規なパーフルオロアルキル(有機亜鉛)−リチウム錯体を提案する。
【解決手段】 有機亜鉛、アルキルリチウム及びパーフルオロアルキルハライドより調製される下記式(4)
[RfZnR2]−Li+ (4)
(式中、R2はメチル基、エチル基又はフェニル基を示し、Rfは、炭素数1〜8の直鎖、分岐若しくは環式のパーフルオロアルキル基を示す)
で表されるパーフルオロアルキル(有機亜鉛)−リチウム錯体。
(もっと読む)
モンテルカストナトリウム中間体の合成方法
大量生産に適したモンテルカストナトリウム中間体の合成方法の提供を目的とする。
【解決手段】この目的を達成するため、本発明は大規模な生産に好適なモンテルカストナトリウム中間体2−(2−(3−(2−(7−クロロ−2−キノリニル)エテニル)フェニル)−3−オキソプロピル)フェニル)プロピルアルコールの製造方法を提供する。この製造方法は、7−クロロキナルジン及び3−シアノベンズアルデヒドを出発原料として縮合させた後、ハロゲン化化合物2−(2−o−(2−ハロゲン化エチル)フェニルプロピル)テトラヒドロピランエーテルと反応させることを特徴とする。
(もっと読む)
1−ヒドロキシ−1,3,3,5,5−ペンタメチルシクロヘキサンを調製する方法
1-ヒドロキシ-1,3,3,5,5-ペンタメチルシクロヘキサンを調製する方法であって、ステップ(ii)からなる方法。ステップ(ii):塩化メチルマグネシウムを用いて3,3,5,5-テトラメチルシクロヘキサノンを1-ヒドロキシ-1,3,3,5,5-ペンタメチルシクロヘキサンに変換する。得られる1-ヒドロキシ-1,3,3,5,5-ペンタメチルシクロヘキサンは、1-アミノ-1,3,3,5,5-ペンタメチルシクロヘキサン(ネラメキサン)またはその薬剤学的に許容可能な塩の調製に用いることができる。 (もっと読む)
ネラメキサンの製造方法
【課題】1−アミノ−1,3,3,5,5−ペンタメチルシクロヘキサン又はその薬理学的に許容される塩を製造する方法であって、次のステップ(i)から(iv)から選択される二つ以上のステップを具備する方法;ステップ(i)においては、塩化メチルマグネシウム存在下でイソフォロンを3,3,5,5−テトラメチルシクロヘキサノンに変換する;ステップ(ii)においては、塩化メチルマグネシウム存在下で3,3,5,5−テトラメチルシクロヘキサノンを1−ヒドロキシ−1,3,3,5,5−ペンタメチルシクロヘキサンに変換する;ステップ(iii)においては、酸性溶液中でクロロアセトニトリル存在下で1−ヒドロキシ−1,3,3,5,5−ペンタメチルシクロヘキサンを1−クロロアセトアミド−1,3,3,5,5−ペンタメチルシクロヘキサンに変換する;ステップ(iv)においては、水中でチオ尿素存在下で1−クロロアセトアミド−1,3,3,5,5−ペンタメチルシクロヘキサンを1−アミノ−1,3,3,5,5−ペンタメチルシクロヘキサンに変換する。 (もっと読む)
オクタフルオロブチレン構造を有する化合物およびその製造方法
【課題】ジシクロヘキシルオクタフルオロブチレン構造を有する含フッ素液晶化合物の製造に有用なハロゲン化合物、該化合物を用いる上記含フッ素液晶化合物の汎用性が高く簡便かつ効率的な製造方法および中間体化合物の提供。
【解決手段】上記ハロゲン化合物は、式R1−(A1−Z1)a−(A2−Z2)b−Ch−(CF2)4−X1(I)で表される。式中、Chは1,4−シクロヘキセン基、X1はヨウ素原子または臭素原子、a,bは0または1である。R1は水素原子、ハロゲン原子、−CN、−NCS、−SF5、炭素数1〜18のアルキル基または式(C1k)として表される基;A1,A2は、トランス−1,4−シクロへキシレン基、1,3−シクロブチレン基、1,2−シクロプロピレン基、ナフタレン−2,6−ジイル基、1,2,3,4−テトラヒドロナフタレン−2,6−ジイル基、デカヒドロナフタレン−2,6−ジイル基または1,4−フェニレン基;Z1,Z2は単結合または炭素数1〜4のアルキレン基などを示す。
(もっと読む)
光学活性アルコールの製造方法
【課題】有機亜鉛化合物とカルボニル化合物とを反応させ、高収率・高エナンチオ選択的に光学活性アルコールを得ることができる光学活性アルコールの製造方法を提供する。
【解決手段】本発明の光学活性アルコールの製造方法は、ZnCl2、NaOMe、及びRMgClを反応させて、有機亜鉛化合物を得る工程と、ホスホロアミド化合物(1a)又は(1b)及びN,N,N’,N’−テトラメチルエチレンジアミン(TMEDA)の存在下、カルボニル化合物と、上記有機亜鉛化合物とを反応させる工程と、を備える。
【化1】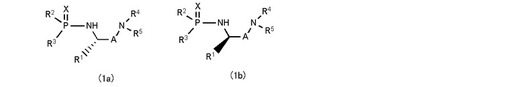
(R1〜R5は、それぞれ独立して一価の炭化水素基である。R2及びR3は、それぞれ直接又は炭素原子以外の原子を介してリン原子と結合している。Xは酸素原子又は硫黄原子である。Aはメチレン基又はカルボニル基である。)
(もっと読む)
α付加型アリル化反応による選択的ホモアリルアルコール誘導体の製造法
【課題】高収率で、高立体選択的に光学活性なα付加型アリル化反応によるホモアリル化合物を製造する方法の提供。
【解決手段】水と有機溶媒との混合溶媒中で、金属触媒の存在下で、かつリガンドの存在下又は不存在下で、アリルボラン化合物と、カルボニル化合物やそのヒドラゾン誘導体とを反応させる触媒的不斉α付加型アリル化反応により、立体選択的にα付加型アリル化化合物を製造する。例えば、カルボニル化合物の場合、Zn金属と2,9−ジメチルフェナントロリン(Ligand3)の存在下に、下式の反応によりα付加体4a化合物が高収率で得られる。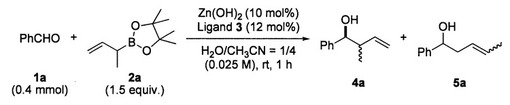 (もっと読む)
(もっと読む)
1 - 10 / 41
[ Back to top ]

