国際特許分類[C07D501/24]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | 複素環式化合物 (108,186) | 5−チア−1−アザビシクロ−[4.2.0]オクタン環系,すなわち,式「図」の環系を含む化合物,例.セファロスポリン;このような上記環系に,たとえば2,3位で,酸素,窒素,または硫黄を含む複素環がさらに縮合した環系 (95) | 7位に直接結合する窒素原子をもつ化合物 (80) | 2位および3位との間に二重結合を有するもの (77) | アシル基がカルボン酸に由来する,7―アシルアミノセファロスポラン酸または置換7―アシルアミノセファロスポラン酸 (66) | 3位に結合する,異種原子または複素環で置換された炭化水素基を有するもの (40)
国際特許分類[C07D501/24]の下位に属する分類
酸素原子で置換されたメチレン基;2―カルボキシル基をもつそのラクトン (4)
硫黄原子で置換されたメチレン基 (8)
窒素原子で置換されたメチレン基;2―カルボキシル基を有するそのラクタム;環の窒素原子により結合している窒素含有複素環で置換されたメチレン基;その第4級化合物 (4)
複素環で置換されたメチレン基 (17)
国際特許分類[C07D501/24]に分類される特許
1 - 7 / 7
セフェム化合物の製造方法
【課題】セファロスポリン系抗生物質の合成中間体として有用なセフェム化合物のZ体を、選択的にかつ高収率で製造する方法を提供すること。
【解決手段】下記一般式(I)で表される3−[(トリフェニル−ホスホラニリデン)メチル]−3−セフェム化合物と、下記式(II)で表される4−メチルチアゾール−5−カルボアルデヒドとを、塩素化炭化水素と低級アルコールとを体積比(前者:後者)10:1以下で混合してなる混合溶剤中で、+5℃〜−50℃で反応させて、下記一般式(A)で表される3−[2−(4−メチルチアゾール−5−イル)ビニル]−3−セフェム化合物(A)を得る。下記化学式中、R1、R2は芳香族炭化水素基を示す。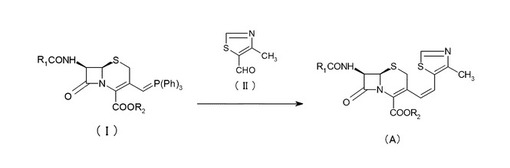 (もっと読む)
(もっと読む)
広帯域β−ラクタマーゼ阻害薬
広帯域スペクトルβ−ラクタマーゼ阻害薬。いくつかの阻害薬は、また、β−ラクタマーゼの阻害に加えて強力な抗菌活性を示す。本発明の化合物は、β−ラクタム環の開裂により、β−ラクタマーゼを不活性化することのできる反応性部分を生じるように設計される。このような阻害を示すβ−ラクタマーゼ阻害薬の製造方法及びβ−ラクタム系抗生物質も提供される。さらに、細菌感染症を治療又は予防するための医薬組成物、及びこのような感染症の治療方法が提供される。 (もっと読む)
セフェム化合物
本発明は、新規セフェム化合物、およびその化合物の製造方法に関するものであり、その方法は発酵段階、化学的段階、および/または生体内変換段階を含む可能性がある。式(I)で表される本発明のセフェム化合物またはその塩若しくはそのエステル(式中、Rは(カルボキシメチルチオ)プロピオニル、(カルボキシエチルチオ)プロピオニル、Y−CH2−CO15からなる群から選択され、式中、Yはフェニル、フェノキシまたはテトラゾリルHOOC−X−COであり、式中、Xは(CH2)4と定義されるか、あるいは式中、Xは(CH2)P−A−(CH2)qと定義され、式中、pおよびqはそれぞれ個別に0、1、2、3または4であり、AはCH=CH、C≡C、CHB、C=O、O、S、NHであり、窒素は置換されてもよく、または硫黄は酸化されてもよく、Bは水素、ハロゲン、C1−3アルコキシ、ヒドロキシル、または置換されてもよいメチルであり、但し、AがCH=CHまたはC≡Cのとき、p+qは2または3であり、またはAがCHB、C=O、O、SまたはNHのとき、p+qは3または4であり、あるいは式中、Xは(CH2)m−CH=A−(CH2)nまたは(CH2)m−C≡C−(CH2)nであり、式中、mおよびnはそれぞれ個別に0、1、2または3であり、m+n=2または3であり、AはCHまたはNであるか、あるいは式中、Xは(CH2)p−CH=CH−CH=C−(CH2)qであり、式中、pおよびqはそれぞれ個別に0または1であり、p+q=0または1であり、かつ式中、R’は、OH、アルキルが直鎖または分枝鎖であり得るO−(アルキル1〜6C)およびアルキル基が直鎖または分枝鎖であり得るO−C(アルキル1〜6C)−O−(アルキル1〜6C)からなる群から選択される)を、とりわけ本発明による発酵技術により、特に適当なアシル−6−アミノペニシラン酸を所望の化合物に変換するのに必要な遺伝子を有するか、またはその遺伝子で形質転換された適切な微生物を用いて調製することができる。 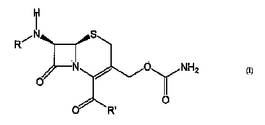 (もっと読む)
(もっと読む)
蛍光プローブ
蛍光プローブであって、下記の式(I):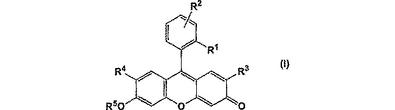
(式中、R1は水素原子、カルボキシル基、又はスルホン酸基以外の一価の置換基を示し;R2は水素原子又は一価の置換基を示し;R3及びR4はそれぞれ独立に水素原子又はハロゲン原子を示し;R5は測定対象物質との接触により切断される一価の基を示し、ただし、R1及びR2の組み合わせは、それらが結合するベンゼン環の酸化電位が、(1)上記切断の前には、式(I)で表される化合物が実質的に無蛍光性になるように、かつ(2)上記切断の後には、式(I)で表される化合物に由来する切断後の化合物が実質的に高い蛍光性になるように選ばれる。)で表される蛍光プローブ。 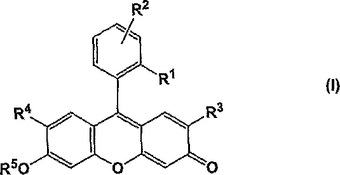 (もっと読む)
(もっと読む)
セファロスポリン化合物の製造方法
【課題】
セフジトレンの安価な新しい製造法を提供すること。
【解決手段】
次式(I)
【化1】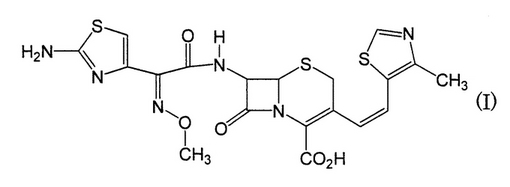
で表される7-[2-メトキシイミノ-2-(2-アミノチアゾール-4-イル)アセトアミド]-3-[2-(4-メチルチアゾール-5-イル)ビニル]-3-セフェム-4-カルボン酸(セフジトレン)の製造方法であって、次式(IV)
【化2】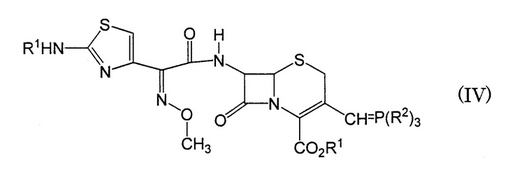
〔式中、R1はシリル保護基、R2は低級アルキル基またはアリール基である〕で示される化合物と次式(V)
【化3】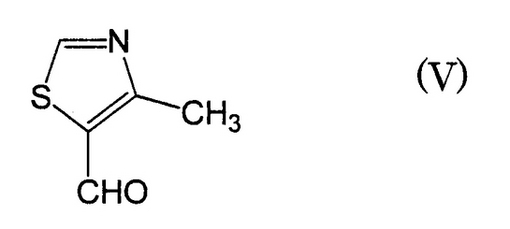
で示される化合物とを反応させることを含む方法を提供するものである。
(もっと読む)
アミノキノリンをQとし、抗生物質残基をAとする混成分子QA、その合成及び抗菌剤としての使用
アミノキノリンをQとし、抗生物質残基をAとする混成分子QA、その合成、及び抗菌剤としての使用。本発明は、一般式 (1) により定義される、アミノキノリンと抗生物質のハイブリッド化合物を対象とし、Q - (Y1)p - (U)p’ - (Y2)p’’ - A (I)、式中、- Q は1個のアミノキノリンを表し、 (Y1)p - (U)p’ - (Y2)p’’ - は場合により用いられるスペーサー・アーム1本であり、Aは抗生物質残基1つである。本発明は、抗生物質残基の活性の予期せぬ向上を可能にする。 (もっと読む)
3−クロロメチル−3−セフェム誘導体の製造方法
工業的に有利な3−クロロメチル−3−セフェム誘導体結晶の製造方法を提供する。 チアゾリンアゼチジノン誘導体(1)と、スルホニルハライド(2)とを酸の存在下に溶媒中で反応させて、アゼチジノン誘導体(3)を得る第一工程、該アゼチジノン誘導体(3)と塩素化剤とを有機溶媒中で反応させて、塩素化アゼチジノン誘導体(4)を得る第二工程、該塩素化アゼチジノン誘導体(4)と、アルコラート(5)をアルコールとエーテルを含む溶媒中でpH8以下で反応させて、3−クロロメチル−3−セフェム誘導体(6)を結晶として回収する第三工程を含む3−クロロメチル−3−セフェム誘導体の製造方法。 (もっと読む)
1 - 7 / 7
[ Back to top ]