不全角化及び表皮増殖異常三次元皮膚モデルの作製方法
【課題】不全角化及び/又は表皮増殖異常三次元皮膚モデル、好ましくはヒト細胞由来の不全角化三次元皮膚モデルの提供。
【解決手段】ケラチノサイト及び繊維芽細胞を含んで成る三次元皮膚モデルに対し、UVBを下記の条件において照射することで、不全角化及び/又は表皮増殖異常三次元皮膚モデルを作製する方法:5≦X×Y/Z≦15(式中、XはUVBの強度(mJ)、YはUVB照射回数、そしてZはUVB照射時間を表し、但し、10≦Xであるか、又はX≦10のとき、2≦Yである。)。
【解決手段】ケラチノサイト及び繊維芽細胞を含んで成る三次元皮膚モデルに対し、UVBを下記の条件において照射することで、不全角化及び/又は表皮増殖異常三次元皮膚モデルを作製する方法:5≦X×Y/Z≦15(式中、XはUVBの強度(mJ)、YはUVB照射回数、そしてZはUVB照射時間を表し、但し、10≦Xであるか、又はX≦10のとき、2≦Yである。)。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、不全角化及び/又は表皮増殖異常三次元皮膚モデルの作製方法及びその方法により作製された不全角化及び/又は表皮増殖異常三次元皮膚モデルを提供する。
【背景技術】
【0002】
皮膚が正常の角化を行うと顆粒層から角層へと移行する段階で核が消滅する「脱核」が生ずる。表皮細胞は基底層で増殖し、上層に移行して成熟し角層となる。しかしながら、例えば乾癬、炎症性異常角化症、アトピー性皮膚炎といった皮膚病に罹り、正常な角化が行われない肌荒れした皮膚においては、角質細胞に核が未消化のまま残り、角質細胞が核を有した未熟な状態で角層中に存在することがあり、これを「不全角化」又は「錯角化」(parakeratosis)という(J. Am. Acad. Dermatol. Vol.50, No.1, pp.77-84 (2004):非特許文献1)。不全角化の現象は古くから知られているものの、不全角化が生じるメカニズムや生化学的な指標についてはよく知られていなかった。不全角化は肌荒れの顕著な状態であり、その治療・予防に有効な薬剤の評価方法、新規の不全角化改善薬剤の研究・開発が求められ、そのために有効な不全角化モデルの出現が望まれている。
【0003】
紫外線照射、乾燥、界面活性剤など皮膚に有害な外部刺激による皮膚傷害、アトピー性皮膚炎、乾癬、接触性皮膚炎などといった種々の皮膚疾患に見られる肌荒れ症状においては、皮膚バリアー機能が低下し、表皮増殖異常が起こることが報告されている。皮膚の皮膚機能の低下による表皮増殖異常を防止するために有効な新規の皮膚バリアー機能回復促進剤に開発が求められ、そのために有効な表皮増殖異常モデルの出現が望まれている。
【0004】
不全角化モデルの作成方法としては例えばマウスなどの動物モデルの皮膚にオレイン酸溶液を繰り返し塗布することで不全角化を人為的に起こさせる手法がある(非特許文献1)。また、表皮増殖異常モデルの作成方法としては例えばマウスなどの動物モデルに粘着テープを貼り/剥がすといった工程を繰り返す行うことによりの表皮の肥厚化を人為的に起こさせる手法(いわゆるテープストリッピング法[特開2000−159666:非特許文献2])がある。しかしながら、このような方法は動物愛護の観点から敬遠され、またマウスなどの皮膚細胞とヒトの細胞との間には表皮細胞の角質化に関与していると思われるカスパーゼファミリーやその他の生理活性物質の種類・作用の点において相違するものと考えられ、動物モデルで得られた結果が必ずしもヒトに適用できるものでもない。従って、生きた動物を使用せず、好ましくはヒト細胞から調製した不全角化三次元皮膚モデルや表皮増殖異常モデルの出現が特に所望される。
【0005】
【特許文献1】特開2000−159666
【非特許文献1】J. Invest. Dermatol. Vol.124, No.5, pp.1008-13 (2005)
【非特許文献2】J. Am. Acad. Dermatol. Vol.50, No.1, pp.77-84 (2004)
【発明の開示】
【発明が解決しようとする課題】
【0006】
本発明の課題は、不全角化及び/又は表皮増殖異常三次元皮膚モデル、好ましくはヒト細胞由来の不全角化及び/又は表皮増殖異常三次元皮膚モデルの提供にある。かかる不全角化及び/又は表皮増殖異常三次元皮膚モデルは不全角化及び/又は表皮増殖異常に効果的な薬剤評価方法、不全角化及び/又は表皮増殖異常改善薬剤のスクリーニング方法などに有効である。
【課題を解決するための手段】
【0007】
本発明は、上記課題に着目し、鋭意検討した結果、ケラチノサイト及び繊維芽細胞を含んで成る三次元皮膚モデルに対しUVBを所定の条件下で照射することで、有効な不全角化及び/又は表皮増殖異常三次元皮膚モデルを提供できることを見出し、本発明を完成するに至った。詳しくは、本願は以下の発明を包含する。
(1)ケラチノサイト及び繊維芽細胞を含んで成る三次元皮膚モデルに対しUVBを下記の条件において照射することで不全角化及び/又は表皮増殖異常三次元皮膚モデルを作製する方法:
5≦X×Y/Z≦15
(式中、
XはUVBの強度(mJ)、
YはUVB照射回数、そして
ZはUVB照射時間(日数)を表し、
但し、10≦Xであるか、又は
X≦10のとき、2≦Yである。)。
(2)前記ケラチノサイトがヒト細胞である、(1)の方法。
(3)前記三次元皮膚モデルが、支持体に繊維芽細胞が分散され、その上にケラチノサイトが播種されることで構成される、(1)又は(2)の方法。
(4)前記支持体がコラーゲンゲルである、(3)の方法。
(5)(1)〜(4)のいずれかの方法で作製された不全角化及び/又は表皮増殖異常三次元皮膚モデル。
【発明の効果】
【0008】
本発明に従い提供される不全角化及び/又は表皮増殖異常三次元皮膚モデルにより、不全角化及び/又は表皮増殖異常に有効な薬剤の評価、新規不全角化及び/又は表皮増殖異常改善薬剤のスクリーニングなどが、動物実験に頼ることなく、簡便に行うことが可能となる。
【発明を実施するための最良の形態】
【0009】
三次元皮膚モデル
本発明の方法に使用できる不全角化及び/又は表皮増殖異常三次元皮膚モデルは、ケラチノサイト及び繊維芽細胞を含んで成る三次元皮膚モデルから作製される。かかる三次元皮膚モデルは当業者にとって周知の方法(例えば、Amano S. et al., Exp. Cell Res., Vol.271, pp.249-262, 2001やTsunenga M. et al., Matrix. Biol., Vol.17, pp.603-613, 1998参照のこと)により調製することができ、例えばインサートメッシュ上において繊維芽細胞を支持体、例えばコラーゲンゲルに混ぜ込んだものを播いた後、その上にケラチノサイトを播き、培養することで調製したものであってよい。三次元皮膚モデルは例えば繊維芽細胞を1×104〜108個/cm2、好ましくは0.1〜10×105個/cm2の量で含み、またケラチノサイトを1×102〜106個/cm2、好ましくは1.0〜10×104個/cm2、より好ましくは約4〜8×104個/cm2の量で含むものであってよい。
このような三次元皮膚モデルは市販もされており、特に限定されるわけではないが、例えばEPI−MODEL(J−TEC)、TESTSKIN(商標)(TOYOBO)などが使用できる。
【0010】
三次元皮膚モデルの培養は、例えば培養液として通常のケラチノサイト培養に用いられる培養液、例えばKG培地、EpilifeKG2(クラボウ)、Humedia−KG2(クラボウ)、アッセイ培地(TOYOBO)などを用い、約37℃で0〜14日間かけて行うことができる。培地としては、その他にDMEM培地(GIBCO)又は2−0−a−D−グルコピラノシル−L−アスコルビン酸含有KGMとDMEMを1:11混合した培地などが使用できる。
【0011】
繊維芽細胞及びケラチノサイトは同種系でも異種系であってもよく、あらゆる哺乳動物に由来してよい。しかしながら、限定するわけではないが、ケラチノサイトがヒト由来であることが好ましい。ケラチノサイトがヒト由来である方が、それにより形成される不全角化及び/又は表皮増殖異常三次元皮膚モデルの性状をヒト皮膚のそれに一層近づけることができるからである。また、使用する繊維芽細胞とケラチノサイトの割合は特に限定されるわけではないが、例えばケラチノサイト4〜8×104〜6細胞に対して繊維芽細胞1×105〜7細胞、好ましくはケラチノサイト4〜8×105細胞に対し繊維芽細胞1×106細胞とすることができる。
【0012】
UVB照射
不全角化及び/又は表皮増殖異常形成のためのUVB照射は、上記三次元皮膚モデルに対し以下の条件を満たすようにして行う。
5≦X×Y/Z≦15
(式中、
XはUVBの強度(mJ)、
YはUVB照射回数、そして
ZはUVB照射時間(日数)を表し、
但し、10≦Xであるか、又は
X≦10のとき、2≦Yである。)。
【0013】
なお、UVB照射は例えばTransilluminator(TPREX FL205−E−30/DMR; Toshiba Medical Supply)を用いて行うことができる。また、UVB照射はケラチノサイト培養の0〜14日後に無菌的に行うことが好ましい。上記条件において、「X×Y/Z」(以下、「不全角化作製及び/又は表皮増殖異常誘導指数」を称する場合がある)は5未満であると不全角化の形成及び/又は表皮増殖異常の誘導が認められず、また不全角化作製及び/又は表皮増殖異常誘導指数が15超である場合、棘融解等が生じ、皮膚ダメージが大きすぎてしまい、不全角化の形成及び/又は表皮増殖異常の誘導が困難となる。特に理論に拘束されるものではないが、不全角化及び/又は表皮増殖異常は適切な強度のUVBを連続又は数日置きに照射することで形成されるものと考えられる。
【0014】
本発明に係る不全角化及び/又は表皮増殖異常三次元皮膚モデルは、肌荒れ、例えば紫外線照射を原因とする皮膚老化、皮膚バリアー機能低下に伴う肌保湿力の低下による乾燥肌、乾癬などの炎症性異常角化症やアトピー性皮膚炎を原因とする不全角化及び/又は表皮増殖異常など、さまざまな皮膚性状の治療、改善及び/又は予防を目的とした薬剤の評価、スクリーニングに有効である。かかる不全角化及び/又は表皮増殖異常三次元皮膚モデルはまた、対象の薬剤が不全角化及び/又は表皮増殖異常を惹起するものであるか否かの判定のためにも利用できる。
【0015】
以下、具体例を挙げて、本発明を更に具体的に説明する。なお、本発明はこれにより限定されるものではない。また。%と表示されている場合、特に断りのない限り、質量%を表す。
【実施例】
【0016】
三次元皮膚モデル
三次元皮膚モデルを用い、不全角化及び/又は表皮増殖異常を形成する培養条件、UVB照射条件について検討を行った。三次元皮膚モデルは、(1)インサートメッシュ(大きさ:約2cm)上にケラチノサイトが直接播種され(商品名:EPIMODEL;J−TEC社製;)、培養されたもの又は(2)インサートメッシュ(大きさ:約2cm)上にコラーゲン及び繊維芽細胞を播いた後にケラチノサイトが播種され(商品名:TESTSKIN(TOYOBO))、培養されたものを使用した。培養は、培養液(商品名:アッセイ培地(TOYOBO))を用いて37℃で0〜14日間行った。培養インサートモデルを図1に示す。
【0017】
UVB照射
上記三次元皮膚モデルの各々に対しUVB照射を行った。UVB照射はTransilluminator(TPREX FL205−E−30/DMR; Toshiba Medical Supply)を用い、ケラチノサイト培養0〜14日後に無菌的に行った。
【0018】
組織学的検討
三次元皮膚モデルは、培養後4%パラホルムアルデヒド(PFA)にて4時間固定した後、パラフィンで包埋した。3μmに薄切した切片を、脱パラフィンした後にヘマトキシリン・エオジン染色(HE染色)して不全角化と表皮増殖異常の形成を確認した。
【0019】
生化学的検討
乾癬表皮の上層において発現の亢進が認められるタンパク質として扁平上皮細胞癌関連抗原(SCCA)が知られる(Takeda A.ら、 J. Invest. Dermatol. (2002) 118(1), 147-154)。本発明者は以前、SCCAが関与する表皮の生理学的メカニズムの解明を目的とする研究を行い、SCCAの発現が乾癬などの不全角化の生じた皮膚において特異的に亢進し、SCCAが不全角化を含む皮膚の肌荒れ性状の一因であることを見出し、皮膚角層細胞の扁平上皮細胞癌関連抗原(SCCA)の発現を指標とする皮膚性状の評価方法に係る発明の特許出願を行っている(特願2005−080533)。このように、SCCA、特にSCCA−1は不全角化を原因とする肌荒れなどの皮膚性状の指標となるため、本実験においても角化不全の形成の指標としてSCCA−1の検出を試みた。
【0020】
上記「組織学的検討」と同様に固定し、薄切した切片を、抗SCCA1モノクローナル抗体(Santa Cruz社)を一次抗体に用いて染色し、SCCA1の発現の挙動を確認した。
詳しくは、上記切片をその切片の非特異的結合部位を10%正常ウサギ血清(Histofine, Tokyo, Japan)でブロックした。次にその切片を抗−SCCA−1モノクローナル抗体(1:500に希釈)とインキュベーションし、PBSで洗浄後、核をヘマトキシリンでカウンター染色し、DAKO Envision System(DAKO Corp., CA, USA)で発色して観察を行った。
【0021】
実験結果
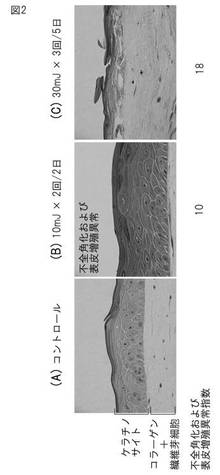
1.UVB照射した三次元皮膚モデルについて組織学的検討したところ、ケラチノサイトと繊維芽細胞の両者を含むモデルのみにおいて、表皮細胞における核の残存、即ち不全角化の形成と、表皮の肥厚化、即ち表皮増殖異常が認められ(図2参照)、ケラチノサイトだけから構成される三次元皮膚モデルでは、不全角化の形成や表皮増殖異常は認められず、しかもUVB 10mJ単回照射で強度の表皮傷害が生じてしまった。(図3参照)。尚、コントロールはUVB照射を行わなかったものである。このことから、ヒト皮膚のUVへの反応を反映した良好な不全角化及び表皮増殖異常モデルを作製するにはケラチノサイトと繊維芽細胞の両者が必要であることが明らかとなった。また、ケラチノサイトと繊維芽細胞の両者を含むモデルでは表皮SCCA−1発現局在が不全角化形成皮膚の表皮上層で確認され、発現が広い範囲で亢進していることが明らかになった(図4)。
【0022】
2.UVB照射条件を検討したところ、下記表1に示すような結果が得られた。
【表1】

【0023】
上記の表に示されている結果を参照すると、不全角化作製及び/又は表皮増殖異常誘導指数が下記の条件:
5≦不全角化作製及び/又は表皮増殖異常誘導指数≦15
条件1:10≦Xであるか、又は
条件2:X≦10のとき、2≦Yである
を満たす場合、不全角化の形成や表皮増殖異常が誘導されることが示された。
【0024】
薬剤評価
1−ピペリジンプロピオン酸(1-PP)は皮膚の不全角化に有効であることが知られ(特開2006−319527)、また本発明者はそれが表皮増殖異常を抑制するという知見も得ている。詳しくは、3%の1−PPを含有する薬剤を一方の頬、及びコントロールを他方の頬に塗布(2ヶ月連用)して、光干渉トモグラフィー(OCT:optical coherence tomography, ISIS optronics社、ドイツ)を用いて表皮厚をそれぞれ測定したとことろ、1−PPの塗布に表皮増殖異常の抑制が認められたとの知見を得ている(データーは示さない)。
【0025】
インサートメッシュ(大きさ:約2cm)上にコラーゲン及び繊維芽細胞の播れた三次元皮膚モデル(商品名:TESTSKIN(TOYOBO))を、1−PPを1%含有する培地(アッセイ培地(TOYOBO))中で37℃にて3日間培養し、しかる後15mJ/cm2にて1回UVB照射を施し(3日目)、さらに翌日同様に15mJ/cm2にて1回UVB照射を施し(4日目)、そして同様の1−PP添加培地中で培養してからPFA固定し、上記のとおりにして組織学的検討を行った。コントロ−ルとして、1−PPの添加されていない同様の培地で皮膚三次元モデルを同様にして培養し、組織学的検討を行った。
【0026】
その結果を図5に示す。1−PPの無添加培地は顕著な表皮異常増殖と、細胞における核の残存により示される不全角化が観察された。一方、1−PP添加培地中で培養された三次元皮膚モデルにおいては、表皮異常増殖の抑制や、表皮細胞中の核の残存で示される不全角化の抑制、即ちUVBによる皮膚障害の抑制が認められた。従って、本発明に係る三次元皮膚モデルは不全角化及び/又は表皮増殖異常改善薬剤のスクリーニングに有効であることがわかる。
【図面の簡単な説明】
【0027】
【図1】培養インサートモデル。(A):ケラチノサイト3次元皮膚モデル。(B):ケラチノサイト+繊維芽細胞3次元皮膚モデル。
【図2】ケラチノサイトと繊維芽細胞の両者を含む三次元皮膚モデルに対しUVB照射した際の組織学的検査結果。(A):照射なし(コントロール)。0日培養開始後、10日目に皮膚を採取して観察。(B):10mJ×2回/2日の条件で照射。不全角化及び表皮増殖異常指数=10.0。0日培養開始後、10日目に皮膚を採取して観察。(C):30mJ×3回/5日の条件で照射。不全角化及び表皮増殖異常指数=18.0。0日培養開始後、10回目に皮膚を採取して観察。
【図3】ケラチノサイトのみを含む三次元皮膚モデルに対しUVB照射した際の組織学的検査結果。(A):照射なし(コントロール)。(B):UVB 10mJ単回照射。
【図4】ケラチノサイトと繊維芽細胞の両者を含む三次元皮膚モデルに対しUVB照射した際のSCCAの発現を示す免疫組織化学的検査結果。(A):照射なし(コントロール)。(B):10mJ×4回/7日の条件で照射。
【図5】1−ピペリジンプロピオン酸の使用により、発明に係る三次元皮膚モデルが不全角化及び/又は表皮増殖異常改善薬剤のスクリーニングに有効であることを示す免疫組織化学的検査結果。(A):コントロール。(B):1%の1−PP塗布。
【符号の説明】
【0028】
1 トランスウェル(インサート)
2 ケラチノサイト
3 微小孔膜
4 培地
5 コラーゲン+繊維芽細胞
【技術分野】
【0001】
本発明は、不全角化及び/又は表皮増殖異常三次元皮膚モデルの作製方法及びその方法により作製された不全角化及び/又は表皮増殖異常三次元皮膚モデルを提供する。
【背景技術】
【0002】
皮膚が正常の角化を行うと顆粒層から角層へと移行する段階で核が消滅する「脱核」が生ずる。表皮細胞は基底層で増殖し、上層に移行して成熟し角層となる。しかしながら、例えば乾癬、炎症性異常角化症、アトピー性皮膚炎といった皮膚病に罹り、正常な角化が行われない肌荒れした皮膚においては、角質細胞に核が未消化のまま残り、角質細胞が核を有した未熟な状態で角層中に存在することがあり、これを「不全角化」又は「錯角化」(parakeratosis)という(J. Am. Acad. Dermatol. Vol.50, No.1, pp.77-84 (2004):非特許文献1)。不全角化の現象は古くから知られているものの、不全角化が生じるメカニズムや生化学的な指標についてはよく知られていなかった。不全角化は肌荒れの顕著な状態であり、その治療・予防に有効な薬剤の評価方法、新規の不全角化改善薬剤の研究・開発が求められ、そのために有効な不全角化モデルの出現が望まれている。
【0003】
紫外線照射、乾燥、界面活性剤など皮膚に有害な外部刺激による皮膚傷害、アトピー性皮膚炎、乾癬、接触性皮膚炎などといった種々の皮膚疾患に見られる肌荒れ症状においては、皮膚バリアー機能が低下し、表皮増殖異常が起こることが報告されている。皮膚の皮膚機能の低下による表皮増殖異常を防止するために有効な新規の皮膚バリアー機能回復促進剤に開発が求められ、そのために有効な表皮増殖異常モデルの出現が望まれている。
【0004】
不全角化モデルの作成方法としては例えばマウスなどの動物モデルの皮膚にオレイン酸溶液を繰り返し塗布することで不全角化を人為的に起こさせる手法がある(非特許文献1)。また、表皮増殖異常モデルの作成方法としては例えばマウスなどの動物モデルに粘着テープを貼り/剥がすといった工程を繰り返す行うことによりの表皮の肥厚化を人為的に起こさせる手法(いわゆるテープストリッピング法[特開2000−159666:非特許文献2])がある。しかしながら、このような方法は動物愛護の観点から敬遠され、またマウスなどの皮膚細胞とヒトの細胞との間には表皮細胞の角質化に関与していると思われるカスパーゼファミリーやその他の生理活性物質の種類・作用の点において相違するものと考えられ、動物モデルで得られた結果が必ずしもヒトに適用できるものでもない。従って、生きた動物を使用せず、好ましくはヒト細胞から調製した不全角化三次元皮膚モデルや表皮増殖異常モデルの出現が特に所望される。
【0005】
【特許文献1】特開2000−159666
【非特許文献1】J. Invest. Dermatol. Vol.124, No.5, pp.1008-13 (2005)
【非特許文献2】J. Am. Acad. Dermatol. Vol.50, No.1, pp.77-84 (2004)
【発明の開示】
【発明が解決しようとする課題】
【0006】
本発明の課題は、不全角化及び/又は表皮増殖異常三次元皮膚モデル、好ましくはヒト細胞由来の不全角化及び/又は表皮増殖異常三次元皮膚モデルの提供にある。かかる不全角化及び/又は表皮増殖異常三次元皮膚モデルは不全角化及び/又は表皮増殖異常に効果的な薬剤評価方法、不全角化及び/又は表皮増殖異常改善薬剤のスクリーニング方法などに有効である。
【課題を解決するための手段】
【0007】
本発明は、上記課題に着目し、鋭意検討した結果、ケラチノサイト及び繊維芽細胞を含んで成る三次元皮膚モデルに対しUVBを所定の条件下で照射することで、有効な不全角化及び/又は表皮増殖異常三次元皮膚モデルを提供できることを見出し、本発明を完成するに至った。詳しくは、本願は以下の発明を包含する。
(1)ケラチノサイト及び繊維芽細胞を含んで成る三次元皮膚モデルに対しUVBを下記の条件において照射することで不全角化及び/又は表皮増殖異常三次元皮膚モデルを作製する方法:
5≦X×Y/Z≦15
(式中、
XはUVBの強度(mJ)、
YはUVB照射回数、そして
ZはUVB照射時間(日数)を表し、
但し、10≦Xであるか、又は
X≦10のとき、2≦Yである。)。
(2)前記ケラチノサイトがヒト細胞である、(1)の方法。
(3)前記三次元皮膚モデルが、支持体に繊維芽細胞が分散され、その上にケラチノサイトが播種されることで構成される、(1)又は(2)の方法。
(4)前記支持体がコラーゲンゲルである、(3)の方法。
(5)(1)〜(4)のいずれかの方法で作製された不全角化及び/又は表皮増殖異常三次元皮膚モデル。
【発明の効果】
【0008】
本発明に従い提供される不全角化及び/又は表皮増殖異常三次元皮膚モデルにより、不全角化及び/又は表皮増殖異常に有効な薬剤の評価、新規不全角化及び/又は表皮増殖異常改善薬剤のスクリーニングなどが、動物実験に頼ることなく、簡便に行うことが可能となる。
【発明を実施するための最良の形態】
【0009】
三次元皮膚モデル
本発明の方法に使用できる不全角化及び/又は表皮増殖異常三次元皮膚モデルは、ケラチノサイト及び繊維芽細胞を含んで成る三次元皮膚モデルから作製される。かかる三次元皮膚モデルは当業者にとって周知の方法(例えば、Amano S. et al., Exp. Cell Res., Vol.271, pp.249-262, 2001やTsunenga M. et al., Matrix. Biol., Vol.17, pp.603-613, 1998参照のこと)により調製することができ、例えばインサートメッシュ上において繊維芽細胞を支持体、例えばコラーゲンゲルに混ぜ込んだものを播いた後、その上にケラチノサイトを播き、培養することで調製したものであってよい。三次元皮膚モデルは例えば繊維芽細胞を1×104〜108個/cm2、好ましくは0.1〜10×105個/cm2の量で含み、またケラチノサイトを1×102〜106個/cm2、好ましくは1.0〜10×104個/cm2、より好ましくは約4〜8×104個/cm2の量で含むものであってよい。
このような三次元皮膚モデルは市販もされており、特に限定されるわけではないが、例えばEPI−MODEL(J−TEC)、TESTSKIN(商標)(TOYOBO)などが使用できる。
【0010】
三次元皮膚モデルの培養は、例えば培養液として通常のケラチノサイト培養に用いられる培養液、例えばKG培地、EpilifeKG2(クラボウ)、Humedia−KG2(クラボウ)、アッセイ培地(TOYOBO)などを用い、約37℃で0〜14日間かけて行うことができる。培地としては、その他にDMEM培地(GIBCO)又は2−0−a−D−グルコピラノシル−L−アスコルビン酸含有KGMとDMEMを1:11混合した培地などが使用できる。
【0011】
繊維芽細胞及びケラチノサイトは同種系でも異種系であってもよく、あらゆる哺乳動物に由来してよい。しかしながら、限定するわけではないが、ケラチノサイトがヒト由来であることが好ましい。ケラチノサイトがヒト由来である方が、それにより形成される不全角化及び/又は表皮増殖異常三次元皮膚モデルの性状をヒト皮膚のそれに一層近づけることができるからである。また、使用する繊維芽細胞とケラチノサイトの割合は特に限定されるわけではないが、例えばケラチノサイト4〜8×104〜6細胞に対して繊維芽細胞1×105〜7細胞、好ましくはケラチノサイト4〜8×105細胞に対し繊維芽細胞1×106細胞とすることができる。
【0012】
UVB照射
不全角化及び/又は表皮増殖異常形成のためのUVB照射は、上記三次元皮膚モデルに対し以下の条件を満たすようにして行う。
5≦X×Y/Z≦15
(式中、
XはUVBの強度(mJ)、
YはUVB照射回数、そして
ZはUVB照射時間(日数)を表し、
但し、10≦Xであるか、又は
X≦10のとき、2≦Yである。)。
【0013】
なお、UVB照射は例えばTransilluminator(TPREX FL205−E−30/DMR; Toshiba Medical Supply)を用いて行うことができる。また、UVB照射はケラチノサイト培養の0〜14日後に無菌的に行うことが好ましい。上記条件において、「X×Y/Z」(以下、「不全角化作製及び/又は表皮増殖異常誘導指数」を称する場合がある)は5未満であると不全角化の形成及び/又は表皮増殖異常の誘導が認められず、また不全角化作製及び/又は表皮増殖異常誘導指数が15超である場合、棘融解等が生じ、皮膚ダメージが大きすぎてしまい、不全角化の形成及び/又は表皮増殖異常の誘導が困難となる。特に理論に拘束されるものではないが、不全角化及び/又は表皮増殖異常は適切な強度のUVBを連続又は数日置きに照射することで形成されるものと考えられる。
【0014】
本発明に係る不全角化及び/又は表皮増殖異常三次元皮膚モデルは、肌荒れ、例えば紫外線照射を原因とする皮膚老化、皮膚バリアー機能低下に伴う肌保湿力の低下による乾燥肌、乾癬などの炎症性異常角化症やアトピー性皮膚炎を原因とする不全角化及び/又は表皮増殖異常など、さまざまな皮膚性状の治療、改善及び/又は予防を目的とした薬剤の評価、スクリーニングに有効である。かかる不全角化及び/又は表皮増殖異常三次元皮膚モデルはまた、対象の薬剤が不全角化及び/又は表皮増殖異常を惹起するものであるか否かの判定のためにも利用できる。
【0015】
以下、具体例を挙げて、本発明を更に具体的に説明する。なお、本発明はこれにより限定されるものではない。また。%と表示されている場合、特に断りのない限り、質量%を表す。
【実施例】
【0016】
三次元皮膚モデル
三次元皮膚モデルを用い、不全角化及び/又は表皮増殖異常を形成する培養条件、UVB照射条件について検討を行った。三次元皮膚モデルは、(1)インサートメッシュ(大きさ:約2cm)上にケラチノサイトが直接播種され(商品名:EPIMODEL;J−TEC社製;)、培養されたもの又は(2)インサートメッシュ(大きさ:約2cm)上にコラーゲン及び繊維芽細胞を播いた後にケラチノサイトが播種され(商品名:TESTSKIN(TOYOBO))、培養されたものを使用した。培養は、培養液(商品名:アッセイ培地(TOYOBO))を用いて37℃で0〜14日間行った。培養インサートモデルを図1に示す。
【0017】
UVB照射
上記三次元皮膚モデルの各々に対しUVB照射を行った。UVB照射はTransilluminator(TPREX FL205−E−30/DMR; Toshiba Medical Supply)を用い、ケラチノサイト培養0〜14日後に無菌的に行った。
【0018】
組織学的検討
三次元皮膚モデルは、培養後4%パラホルムアルデヒド(PFA)にて4時間固定した後、パラフィンで包埋した。3μmに薄切した切片を、脱パラフィンした後にヘマトキシリン・エオジン染色(HE染色)して不全角化と表皮増殖異常の形成を確認した。
【0019】
生化学的検討
乾癬表皮の上層において発現の亢進が認められるタンパク質として扁平上皮細胞癌関連抗原(SCCA)が知られる(Takeda A.ら、 J. Invest. Dermatol. (2002) 118(1), 147-154)。本発明者は以前、SCCAが関与する表皮の生理学的メカニズムの解明を目的とする研究を行い、SCCAの発現が乾癬などの不全角化の生じた皮膚において特異的に亢進し、SCCAが不全角化を含む皮膚の肌荒れ性状の一因であることを見出し、皮膚角層細胞の扁平上皮細胞癌関連抗原(SCCA)の発現を指標とする皮膚性状の評価方法に係る発明の特許出願を行っている(特願2005−080533)。このように、SCCA、特にSCCA−1は不全角化を原因とする肌荒れなどの皮膚性状の指標となるため、本実験においても角化不全の形成の指標としてSCCA−1の検出を試みた。
【0020】
上記「組織学的検討」と同様に固定し、薄切した切片を、抗SCCA1モノクローナル抗体(Santa Cruz社)を一次抗体に用いて染色し、SCCA1の発現の挙動を確認した。
詳しくは、上記切片をその切片の非特異的結合部位を10%正常ウサギ血清(Histofine, Tokyo, Japan)でブロックした。次にその切片を抗−SCCA−1モノクローナル抗体(1:500に希釈)とインキュベーションし、PBSで洗浄後、核をヘマトキシリンでカウンター染色し、DAKO Envision System(DAKO Corp., CA, USA)で発色して観察を行った。
【0021】
実験結果
1.UVB照射した三次元皮膚モデルについて組織学的検討したところ、ケラチノサイトと繊維芽細胞の両者を含むモデルのみにおいて、表皮細胞における核の残存、即ち不全角化の形成と、表皮の肥厚化、即ち表皮増殖異常が認められ(図2参照)、ケラチノサイトだけから構成される三次元皮膚モデルでは、不全角化の形成や表皮増殖異常は認められず、しかもUVB 10mJ単回照射で強度の表皮傷害が生じてしまった。(図3参照)。尚、コントロールはUVB照射を行わなかったものである。このことから、ヒト皮膚のUVへの反応を反映した良好な不全角化及び表皮増殖異常モデルを作製するにはケラチノサイトと繊維芽細胞の両者が必要であることが明らかとなった。また、ケラチノサイトと繊維芽細胞の両者を含むモデルでは表皮SCCA−1発現局在が不全角化形成皮膚の表皮上層で確認され、発現が広い範囲で亢進していることが明らかになった(図4)。
【0022】
2.UVB照射条件を検討したところ、下記表1に示すような結果が得られた。
【表1】

【0023】
上記の表に示されている結果を参照すると、不全角化作製及び/又は表皮増殖異常誘導指数が下記の条件:
5≦不全角化作製及び/又は表皮増殖異常誘導指数≦15
条件1:10≦Xであるか、又は
条件2:X≦10のとき、2≦Yである
を満たす場合、不全角化の形成や表皮増殖異常が誘導されることが示された。
【0024】
薬剤評価
1−ピペリジンプロピオン酸(1-PP)は皮膚の不全角化に有効であることが知られ(特開2006−319527)、また本発明者はそれが表皮増殖異常を抑制するという知見も得ている。詳しくは、3%の1−PPを含有する薬剤を一方の頬、及びコントロールを他方の頬に塗布(2ヶ月連用)して、光干渉トモグラフィー(OCT:optical coherence tomography, ISIS optronics社、ドイツ)を用いて表皮厚をそれぞれ測定したとことろ、1−PPの塗布に表皮増殖異常の抑制が認められたとの知見を得ている(データーは示さない)。
【0025】
インサートメッシュ(大きさ:約2cm)上にコラーゲン及び繊維芽細胞の播れた三次元皮膚モデル(商品名:TESTSKIN(TOYOBO))を、1−PPを1%含有する培地(アッセイ培地(TOYOBO))中で37℃にて3日間培養し、しかる後15mJ/cm2にて1回UVB照射を施し(3日目)、さらに翌日同様に15mJ/cm2にて1回UVB照射を施し(4日目)、そして同様の1−PP添加培地中で培養してからPFA固定し、上記のとおりにして組織学的検討を行った。コントロ−ルとして、1−PPの添加されていない同様の培地で皮膚三次元モデルを同様にして培養し、組織学的検討を行った。
【0026】
その結果を図5に示す。1−PPの無添加培地は顕著な表皮異常増殖と、細胞における核の残存により示される不全角化が観察された。一方、1−PP添加培地中で培養された三次元皮膚モデルにおいては、表皮異常増殖の抑制や、表皮細胞中の核の残存で示される不全角化の抑制、即ちUVBによる皮膚障害の抑制が認められた。従って、本発明に係る三次元皮膚モデルは不全角化及び/又は表皮増殖異常改善薬剤のスクリーニングに有効であることがわかる。
【図面の簡単な説明】
【0027】
【図1】培養インサートモデル。(A):ケラチノサイト3次元皮膚モデル。(B):ケラチノサイト+繊維芽細胞3次元皮膚モデル。
【図2】ケラチノサイトと繊維芽細胞の両者を含む三次元皮膚モデルに対しUVB照射した際の組織学的検査結果。(A):照射なし(コントロール)。0日培養開始後、10日目に皮膚を採取して観察。(B):10mJ×2回/2日の条件で照射。不全角化及び表皮増殖異常指数=10.0。0日培養開始後、10日目に皮膚を採取して観察。(C):30mJ×3回/5日の条件で照射。不全角化及び表皮増殖異常指数=18.0。0日培養開始後、10回目に皮膚を採取して観察。
【図3】ケラチノサイトのみを含む三次元皮膚モデルに対しUVB照射した際の組織学的検査結果。(A):照射なし(コントロール)。(B):UVB 10mJ単回照射。
【図4】ケラチノサイトと繊維芽細胞の両者を含む三次元皮膚モデルに対しUVB照射した際のSCCAの発現を示す免疫組織化学的検査結果。(A):照射なし(コントロール)。(B):10mJ×4回/7日の条件で照射。
【図5】1−ピペリジンプロピオン酸の使用により、発明に係る三次元皮膚モデルが不全角化及び/又は表皮増殖異常改善薬剤のスクリーニングに有効であることを示す免疫組織化学的検査結果。(A):コントロール。(B):1%の1−PP塗布。
【符号の説明】
【0028】
1 トランスウェル(インサート)
2 ケラチノサイト
3 微小孔膜
4 培地
5 コラーゲン+繊維芽細胞
【特許請求の範囲】
【請求項1】
ケラチノサイト及び繊維芽細胞を含んで成る三次元皮膚モデルに対しUVBを下記の条件において照射することで不全角化及び/又は表皮増殖異常三次元皮膚モデルを作製する方法:
5≦X×Y/Z≦15
(式中、
XはUVBの強度(mJ)、
YはUVB照射回数、そして
ZはUVB照射時間(日数)を表し、
但し、10≦Xであるか、又は
X≦10のとき、2≦Yである。)。
【請求項2】
前記ケラチノサイトがヒト細胞である、請求項1記載の方法。
【請求項3】
前記三次元皮膚モデルが、支持体に繊維芽細胞が分散され、その上にケラチノサイトが播種されることで構成される、請求項1又は2記載の方法。
【請求項4】
前記支持体がコラーゲンゲルである、請求項3記載の方法。
【請求項5】
請求項1〜4のいずれか1項記載の方法で作製された不全角化及び/又は表皮増殖異常三次元皮膚モデル。
【請求項1】
ケラチノサイト及び繊維芽細胞を含んで成る三次元皮膚モデルに対しUVBを下記の条件において照射することで不全角化及び/又は表皮増殖異常三次元皮膚モデルを作製する方法:
5≦X×Y/Z≦15
(式中、
XはUVBの強度(mJ)、
YはUVB照射回数、そして
ZはUVB照射時間(日数)を表し、
但し、10≦Xであるか、又は
X≦10のとき、2≦Yである。)。
【請求項2】
前記ケラチノサイトがヒト細胞である、請求項1記載の方法。
【請求項3】
前記三次元皮膚モデルが、支持体に繊維芽細胞が分散され、その上にケラチノサイトが播種されることで構成される、請求項1又は2記載の方法。
【請求項4】
前記支持体がコラーゲンゲルである、請求項3記載の方法。
【請求項5】
請求項1〜4のいずれか1項記載の方法で作製された不全角化及び/又は表皮増殖異常三次元皮膚モデル。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2009−240271(P2009−240271A)
【公開日】平成21年10月22日(2009.10.22)
【国際特許分類】
【出願番号】特願2008−93131(P2008−93131)
【出願日】平成20年3月31日(2008.3.31)
【出願人】(000001959)株式会社資生堂 (1,748)
【Fターム(参考)】
【公開日】平成21年10月22日(2009.10.22)
【国際特許分類】
【出願日】平成20年3月31日(2008.3.31)
【出願人】(000001959)株式会社資生堂 (1,748)
【Fターム(参考)】
[ Back to top ]

