磁気感応性物質、磁気感応性薬剤およびそれらの製造方法
【課題】磁石を用いて、混合物からの機能物質の分離が可能な磁気感応性物質、および磁性を有する微粒子表面に共有結合した有機薄膜を介して薬剤が結合固定されており、磁石を用いて、薬剤の体内動態が制御可能な磁気感応性薬剤、ならびにこれらの製造方法を提供する。
【解決手段】磁気感応性物質10において、磁性を有する微粒子1が、第2の官能基を有する膜化合物の形成する薄膜4によって被覆されており、その表面に、第2の官能基と反応して共有結合を形成する第1の架橋反応基、および機能物質6の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤5が、第2の官能基と第1の架橋反応基との反応により形成された共有結合を介して結合しており、機能物質6の官能基と第2の架橋官能基との反応により形成された結合を介して、機能物質6が微粒子1に結合している。
【解決手段】磁気感応性物質10において、磁性を有する微粒子1が、第2の官能基を有する膜化合物の形成する薄膜4によって被覆されており、その表面に、第2の官能基と反応して共有結合を形成する第1の架橋反応基、および機能物質6の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤5が、第2の官能基と第1の架橋反応基との反応により形成された共有結合を介して結合しており、機能物質6の官能基と第2の架橋官能基との反応により形成された結合を介して、機能物質6が微粒子1に結合している。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、磁気感応性物質、磁気感応性薬剤およびそれらの製造方法に関するものである。さらに詳しくは、磁性を有する微粒子表面に共有結合した有機薄膜を介して機能物質が結合固定されており、磁石を用いて、混合物からの機能物質の分離が可能な磁気感応性物質、および磁性を有する微粒子表面に共有結合した有機薄膜を介して薬剤が結合固定されており、磁石を用いて、薬剤の体内動態が制御可能な磁気感応性薬剤、ならびにこれらの製造方法に関する。
【背景技術】
【0002】
現在、薬剤の副作用を和らげたり、低減させたりする目的で、必要な時間に必要な部位で作用させるための薬物システムが数々研究開発されている。
【0003】
【特許文献1】特表2002−500177号公報
【特許文献2】特表2000−503763号公報
【特許文献3】特開平09−328438号公報
【発明の開示】
【発明が解決しようとする課題】
【0004】
しかしながら、混合物から磁力を用いて分離可能な磁気感応性物質およびその製造方法、さらには磁力を用いて必要な部位に薬剤を集中させるというシステムに用いる薬剤およびその製造方法は、未だ開発、提供されていない。
【0005】
本発明は、磁力を用いて分離あるいは集積が可能な磁気感応性物質を製造し、触媒等に用いた物質の分離を高能率に行うことを目的とする。また、磁力を用いて生体内の必要部位に集中させることができ、且つ、投薬量が極めて少なくて済むDDS用の薬剤を製造し、薬剤による副作用を和らげたり、薬剤の使用量を低減させたりすることを目的とする。
【課題を解決するための手段】
【0006】
前記目的に沿う第1の発明に係る磁気感応性物質は、磁性を有する微粒子に機能物質が結合した磁気感応性物質であって、前記微粒子の表面は、分子の両端に第1および第2の官能基を有する膜化合物の形成する薄膜によって被覆されており、前記膜化合物は、前記第1の官能基と前記微粒子の表面との反応により形成された共有結合を介して前記微粒子の表面に固定されており、前記薄膜の表面には、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記機能物質の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤が、前記第2の官能基と前記第1の架橋反応基との反応により形成された共有結合を介して結合しており、前記機能物質の官能基と前記第2の架橋官能基との反応により形成された結合を介して、前記機能物質が前記微粒子に結合している。
【0007】
第1の発明に係る磁気感応性物質において、前記膜化合物の形成する薄膜が単分子膜であることが好ましい。
【0008】
第1の発明に係る磁気感応性物質において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であってもよい。
【0009】
第2の発明に係る磁気感応性薬剤は、磁性を有する微粒子に薬剤が結合した磁気感応性物質であって、前記微粒子の表面は、分子の両端に第1および第2の官能基を有する膜化合物の形成する薄膜によって被覆されており、前記膜化合物は、前記第1の官能基と前記微粒子の表面との反応により形成された共有結合を介して前記微粒子の表面に固定されており、
前記薄膜の表面には、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記薬剤の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤が、前記第2の官能基と前記第1の架橋反応基との反応により形成された共有結合を介して結合しており、前記薬剤の官能基と前記第2の架橋官能基との反応により形成された結合を介して、前記薬剤が前記微粒子に結合している。
【0010】
第2の発明に係る磁気感応性薬剤において、前記薬剤が、アミノ基、イミノ基、水酸基、およびチオール基のいずれか1を含むタンパク質、アミノ酸、酵素、抗体、抗生物質、抗菌物質、および造影剤のいずれか1であってもよい。
【0011】
第2の発明に係る磁気感応性薬剤において、前記膜化合物の形成する薄膜が単分子膜であることが好ましい。
【0012】
第2の発明に係る磁気感応性薬剤磁気感応性薬剤において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であってもよい。
【0013】
第2の発明に係る磁気感応性薬剤磁気感応性薬剤において、前記薬剤の有する前記官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ前記第2の架橋反応基は、アルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であってもよい。
【0014】
第3の発明に係る磁気感応性物質の製造方法は、磁性を有する微粒子に機能物質が結合した磁気感応性物質の製造方法であって、分子の両端にそれぞれ第1および第2の官能基を有する膜化合物を含む溶液を前記微粒子の表面に接触させ、前記第1の官能基と前記微粒子の表面との間で結合を形成させ、前記膜化合物の形成する薄膜で前記微粒子の表面が被覆された反応性微粒子を調製する工程Aと、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記機能物質の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤を、前記反応性微粒子の表面に接触させ、前記第2の官能基と前記第1の架橋反応基との反応により共有結合を形成させ、前記架橋剤を前記反応性微粒子の表面に固定する工程Bと、前記架橋剤が固定された反応性微粒子の表面に前記機能物質を接触させ、前記機能物質の官能基と前記第2の架橋反応基との反応により結合を形成させ、前記機能物質を前記架橋剤が固定された反応性微粒子に結合させる工程Cとを有する。
【0015】
第3の発明に係る磁気感応性物質の製造方法において、前記工程Aにおける結合の形成後に、未反応の前記膜化合物を除去することが好ましい。
【0016】
第3の発明に係る磁気感応性物質の製造方法において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であってもよい。
【0017】
第3の発明に係る磁気感応性物質の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含んでいてもよい。
【0018】
第3の発明に係る磁気感応性物質の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含んでいてもよい。
【0019】
第3の発明に係る磁気感応性物質の製造方法において、さらに助触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含んでいてもよい。
【0020】
第4の発明に係る磁気感応性薬剤の製造方法は、磁性を有する微粒子に薬剤が結合した磁気感応性薬剤の製造方法であって、分子の両端にそれぞれ第1および第2の官能基を有する膜化合物を含む溶液を前記微粒子の表面に接触させ、前記第1の官能基と前記微粒子の表面との間で結合を形成させ、前記膜化合物の形成する薄膜で前記微粒子の表面が被覆された反応性微粒子を調製する工程Aと、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記薬剤の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤を、前記反応性微粒子の表面に接触させ、前記第2の官能基と前記第1の架橋反応基との反応により共有結合を形成させ、前記架橋剤を前記反応性微粒子の表面に固定する工程Bと、前記架橋剤が固定された反応性微粒子の表面に前記薬剤を接触させ、前記薬剤の官能基と前記第2の架橋反応基との反応により結合を形成させ、前記薬剤を前記架橋剤が固定された反応性微粒子に結合させる工程Cとを有する。
【0021】
第4の発明に係る磁気感応性薬剤の製造方法において、前記工程Aにおける結合の形成後に、未反応の前記膜化合物を除去することが好ましい。
【0022】
第4の発明に係る磁気感応性薬剤の製造方法において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であってもよい。
【0023】
第4の発明に係る磁気感応性薬剤の製造方法において、前記薬剤の有する前記官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ前記第2の架橋反応基は、アルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であってもよい。
【0024】
第4の発明に係る磁気感応性薬剤の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含んでいてもよい。
【0025】
第4の発明に係る磁気感応性薬剤の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含んでいてもよい。
【0026】
第4の発明に係る磁気感応性薬剤の製造方法において、さらに助触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含んでいてもよい。
【発明の効果】
【0027】
請求項1〜3に記載の磁気感応性物質、および請求項9〜14に記載の磁気感応性物質の製造方法は、磁力を用いて分離あるいは集積が可能であり、磁石等の磁気発生手段を用いて、結合した機能物質の分離を高能率に行うことができる磁気感応性物質およびその製造方法を提供できる。
【0028】
特に、請求項2記載の磁気感応性物質においては、第1の膜化合物の形成する薄膜が単分子膜であるため、微粒子本来の物性や機能を保持することができる。
【0029】
請求項3記載の磁気感応性物質においては、第2の官能基がエポキシ基であり、かつ第1の架橋反応基がアミノ基またはイミノ基であるので、加熱により強固な結合を形成できる。
【0030】
請求項10記載の磁気感応性物質の製造方法においては、未反応の膜化合物を除去するので、磁気感応性物質からの膜化合物の溶出を抑制することができる。
【0031】
請求項11記載の磁気感応性物質の製造方法においては、第2の官能基がエポキシ基であり、かつ第1の架橋反応基がアミノ基またはイミノ基であるので、加熱により強固な結合を形成できる。
【0032】
請求項12記載の磁気感応性物質の製造方法においては、膜化合物を含む溶液が、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含むので、反応性微粒子の調製時間を短縮し、磁気感応性物質の製造をより高効率に行うことができる。
【0033】
請求項13および14記載の磁気感応性物質の製造方法においては、膜化合物を含む溶液が、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、アミノアルキルアルコキシシラン化合物からからなる群より選択される1または2以上の化合物をさらに含むので、反応性微粒子の調製時間を短縮し、磁気感応性物質の製造をより高効率に行うことができる。特に、これらの化合物と上述の縮合触媒の両者をともに含む場合には、調製時間をさらに短縮できる。
【0034】
請求項4〜8に記載の磁気感応性薬剤、および請求項15〜21に記載の磁気感応性薬剤の製造方法は、磁石を用いて、薬剤の体内動態が制御可能なであるため、標的部位にのみ選択的に投与することが可能であり、高い効果を有しかつ副作用の少ない磁気感応性薬剤およびその製造方法を提供できる。
【0035】
請求項5記載の磁気感応性薬剤において、薬剤が、アミノ基、イミノ基、水酸基、およびチオール基のいずれか1であるので、エポキシ基との反応により形成された結合により、安定に固定できる。
【0036】
請求項6記載の磁気感応性物質においては、第1の膜化合物の形成する薄膜が単分子膜であるため、微粒子本来の物性や機能を保持することができる。
【0037】
請求項7記載の磁気感応性薬剤においては、第2の官能基がエポキシ基であり、かつ第1の架橋反応基がアミノ基またはイミノ基であるので、加熱により強固な結合を形成できる。
【0038】
請求項8記載の磁気感応性薬剤においては、薬剤の有する官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ第2の架橋反応基はアルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であるので、加熱により形成される結合により薬剤を強固に固定できる。
【0039】
請求項16記載の磁気感応性薬剤の製造方法においては、未反応の膜化合物を除去するので、磁気感応性薬剤からの膜化合物の溶出を抑制することができる。
【0040】
請求項17記載の磁気感応性薬剤の製造方法においては、第2の官能基がエポキシ基であり、かつ第1の架橋反応基がアミノ基またはイミノ基であるので、加熱により強固な結合を形成できる。
【0041】
請求項18記載の磁気感応性薬剤の製造方法においては、薬剤の有する官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ第2の架橋反応基はアルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であるので、反応する官能基を組み合わせれば、加熱により形成される結合により薬剤を強固に固定できる。
【0042】
請求項19記載の磁気感応性薬剤の製造方法においては、膜化合物を含む溶液が、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含むので、反応性微粒子の調製時間を短縮し、磁気感応性物質の製造をより高効率に行うことができる。
【0043】
請求項20および21記載の磁気感応性薬剤の製造方法においては、膜化合物を含む溶液が、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、アミノアルキルアルコキシシラン化合物からからなる群より選択される1または2以上の化合物をさらに含むので、反応性微粒子の調製時間を短縮し、磁気感応性物質の製造をより高効率に行うことができる。特に、これらの化合物と上述の縮合触媒の両者をともに含む場合には、調製時間をさらに短縮できる。
【発明を実施するための最良の形態】
【0044】
以下、図面を参照しながら本発明の一実施の形態に係る磁気感応性薬剤について説明する。
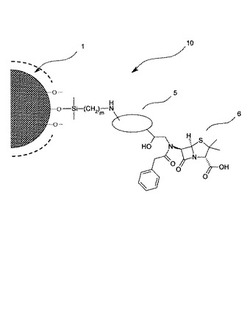
図1に示すように、本発明の一実施の形態に係る磁気感応性薬剤10は、マグネタイト微粒子(磁性を有する微粒子の一例)1の表面が、アミノ基(第2の官能基の一例)を有する膜化合物(第1の膜化合物)の単分子膜3で被覆されたアミノ化マグネタイト微粒子(反応性微粒子の一例)4の表面に、架橋剤5を介してペニシリンG(薬剤の一例)6が結合している。
アミノ基を有する膜化合物は、アルコキシシリル基(第1の官能基の一例)とマグネタイト微粒子1の表面の水酸基2との反応により形成された共有結合を介してマグネタイト微粒子1の表面に固定されている。
架橋剤5は、2個のエポキシ基(第1および第2の架橋反応基の一例)を有するジエポキシ化合物であり、一方のエポキシ基とアミノ化マグネタイト微粒子4の表面のアミノ基との反応により形成される共有結合を介してアミノ化マグネタイト粒子4の表面に固定されている。
ペニシリンG 6は、イミノ基と架橋剤が表面に固定されたアミノ化マグネタイト微粒子7のエポキシ基との反応により形成された共有結合により、架橋剤5を介してアミノ化マグネタイト微粒子4に結合している。
【0045】
磁気感応性薬剤10の製造方法は、図2(a)〜(c)に示すように、アミノ基を有する膜化合物をマグネタイト微粒子1と接触させ、アミノ化マグネタイト微粒子4を製造する工程Aと、アミノ化マグネタイト微粒子4に架橋剤5を接触させ、アミノ基とエポキシ基の反応より形成された共有結合を介して架橋剤5をアミノ化マグネタイト微粒子4の表面に固定する工程Bと、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7とペニシリンG 6とを接触させ、ペニシリンG 6に含まれているイミノ基とエポキシ基との反応により、ペニシリンG 6を、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7の表面に結合させる工程Cとを含んでいる。
【0046】
以下、工程A〜Cについてより詳細に説明する。
工程Aでは、アミノ基を有する膜化合物をマグネタイト微粒子1と接触させ、アミノ化マグネタイト微粒子4を製造する。
【0047】
用いることのできるマグネタイト微粒子1の粒径に特に制限はないが、10nm〜0.1mmの範囲内であることが好ましい。マグネタイト微粒子1の粒径が10nm未満である場合には、磁気特性が大幅に劣化し、粒径が0.1mmを上回る場合には、沈降しやすくなり、溶液中への分散が困難になる。特に、DDS用の磁気感応性薬剤として用いる場合には、マグネタイト微粒子1の粒径は、10〜1μm、好ましくは数十〜数百nmである。粒径が1μmを超すと、血管注射ができなくなるためである。
【0048】
アミノ基を有する膜化合物としては、マグネタイト微粒子1の表面に吸着または水酸基2との反応により結合し、自己組織化により単分子膜を形成することのできる任意の化合物を用いることができるが、直鎖状アルキレン基の一方の末端にアミノ基を、他方の末端にアルコキシシリル基をそれぞれ有し、下記の一般式(化1)で表されるアルコキシシラン化合物が好ましい。
【0049】
【化1】

【0050】
上式において、mは3〜20の整数を、Rは炭素数1〜4のアルキル基をそれぞれ表す。
用いることのできるアミノ基を有する膜化合物の具体例としては、下記(1)〜(8)に示したアルコキシシラン化合物が挙げられる。
【0051】
(1) H2N(CH2)3Si(OCH3)3
(2) H2N(CH2)5Si(OCH3)3
(3) H2N(CH2)7Si(OCH3)3
(4) H2N(CH2)9Si(OCH3)3
(5) H2N(CH2)5Si(OC2H5)3
(6) H2N(CH2)5Si(OC2H5)3
(7) H2N(CH2)7Si(OC2H5)3
(8) H2N(CH2)9Si(OC2H5)3
【0052】
アミノ化マグネタイト微粒子4の製造は、アミノ基を含むアルコキシシラン化合物と、アルコキシシリル基とマグネタイト微粒子1の表面の水酸基2との縮合反応を促進するための縮合触媒と、非水系の有機溶媒とを混合した反応液中にマグネタイト微粒子1を分散させ、室温の空気中で反応させることにより行われる。
【0053】
縮合触媒としては、カルボン酸金属塩、チタン酸エステルおよびチタン酸エステルキレート等の金属塩が利用可能である。
縮合触媒の添加量は、好ましくはアルコキシシラン化合物の0.2〜5質量%であり、より好ましくは0.5〜1質量%である。
【0054】
カルボン酸金属塩の具体例としては、ジブチルスズジラウレート、ジブチルスズジオクテート、ジブチルスズジアセテート、ジオクチルスズジラウレート、ジオクチルスズジオクテート、ジオクチルスズジアセテート、ナフテン酸鉛、ナフテン酸コバルト、2−エチルヘキセン酸鉄が挙げられる。
【0055】
チタン酸エステルの具体例としては、テトラブチルチタネート、テトラノニルチタネートが挙げられる。
チタン酸エステルキレート類の具体例としては、ビス(アセチルアセトニル)ジ−プロピルチタネートが挙げられる。
【0056】
アルコキシシリル基とマグネタイト微粒子1の表面の水酸基2とが縮合反応を起こし、下記の化2で示されるような構造を有するアミノ基を有する膜化合物の単分子膜3を生成する。なお、酸素原子から延びた3本の単結合はマグネタイト微粒子1の表面または隣接するシラン化合物のケイ素(Si)原子と結合しており、そのうち少なくとも1本はマグネタイト微粒子1の表面と結合している。
【0057】
【化2】

【0058】
アルコキシシリル基は、水分の存在下で分解するので、反応は相対湿度45%以下の空気中で行うことが好ましい。なお、縮合反応は、シリカ微粒子21の表面に付着した油脂分や水分により阻害されるので、シリカ微粒子21をよく洗浄して乾燥することにより、これらの不純物を予め除去しておくことが好ましい。
縮合触媒として上述の金属塩のいずれかを用いた場合、縮合反応の完了までに要する時間は2時間程度である。
【0059】
上述の金属塩の代わりに、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、アミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物を縮合触媒として用いた場合、反応時間を1/2〜2/3程度まで短縮できる。
【0060】
あるいは、これらの化合物を助触媒として、上述の金属塩と混合(質量比1:9〜9:1の範囲で使用可能だが、1:1前後が好ましい)して用いると、反応時間をさらに短縮できる。
【0061】
例えば、縮合触媒として、ケチミン化合物であるジャパンエポキシレジン社のH3を用い、その他の条件は同一にしてアミノ化マグネタイト微粒子4の製造を行うと、アミノ化マグネタイト微粒子4の品質を損なうことなく反応時間を1時間程度にまで短縮できる。
【0062】
さらに、縮合触媒として、ジャパンエポキシレジン社のH3とジブチルスズビスアセチルアセトネートとの混合物(混合比は1:1)を用い、その他の条件は同一にしてエポキシ化シリカ微粒子11の製造を行うと、反応時間を20分程度に短縮できる。
【0063】
なお、ここで用いることができるケチミン化合物は特に限定されるものではないが、例えば、2,5,8−トリアザ−1,8−ノナジエン、3,11−ジメチル−4,7,10−トリアザ−3,10−トリデカジエン、2,10−ジメチル−3,6,9−トリアザ−2,9−ウンデカジエン、2,4,12,14−テトラメチル−5,8,11−トリアザ−4,11−ペンタデカジエン、2,4,15,17−テトラメチル−5,8,11,14−テトラアザ−4,14−オクタデカジエン、2,4,20,22−テトラメチル−5,12,19−トリアザ−4,19−トリエイコサジエン等が挙げられる。
【0064】
また、用いることができる有機酸としても特に限定されるものではないが、例えば、ギ酸、酢酸、プロピオン酸、酪酸、マロン酸等が挙げられる。
【0065】
反応液の製造には、有機塩素系溶媒、炭化水素系溶媒、フッ化炭素系溶媒、シリコーン系溶媒、およびこれらの混合溶媒を用いることができる。アルコキシシラン化合物の加水分解を防止するために、乾燥剤または蒸留により使用する溶媒から水分を除去しておくことが好ましい。また、溶媒の沸点は50〜250℃であることが好ましい。
【0066】
具体的に使用可能な溶媒としては、非水系の石油ナフサ、ソルベントナフサ、石油エーテル、石油ベンジン、イソパラフィン、ノルマルパラフィン、デカリン、工業ガソリン、ノナン、デカン、灯油、ジメチルシリコーン、フェニルシリコーン、アルキル変性シリコーン、ポリエーテルシリコーン、ジメチルホルムアミド等を挙げることができる。
さらに、メタノール、エタノール、プロパノール等のアルコール系溶媒、あるいはそれらの混合物を用いることもできる。
【0067】
また、用いることができるフッ化炭素系溶媒としては、フロン系溶媒、フロリナート(米国3M社製)、アフルード(旭硝子株式会社製)等がある。なお、これらは1種単独で用いても良いし、良く混ざるものなら2種以上を組み合わせてもよい。さらに、ジクロロメタン、クロロホルム等の有機塩素系溶媒を添加してもよい。
【0068】
反応液におけるアルコキシシラン化合物の好ましい濃度は、0.5〜3質量%である。
【0069】
反応後、溶媒で洗浄し、未反応物として表面に残った過剰なアルコキシシラン化合物および縮合触媒を除去すると、アミノ基を有する膜化合物の単分子膜3で表面が覆われたアミノ化マグネタイト微粒子4が得られる。このようにして製造されるアミノ化マグネタイト微粒子4の断面構造の模式図を図2(b)に示す。
【0070】
洗浄溶媒としては、アルコキシシラン化合物を溶解できる任意の溶媒を用いることができるが、安価であり、溶解性が高く、風乾により容易に除去することのできるジクロロメタン、クロロホルム、N−メチルピロリドン等が好ましい。
【0071】
反応後、生成したアミノ化マグネタイト微粒子4を溶媒で洗浄せずに空気中に放置すると、表面に残ったアルコキシシラン化合物の一部が空気中の水分により加水分解を受け、生成したシラノール基がアルコキシシリル基と縮合反応を起こす。その結果、アミノ化マグネタイト微粒子4の表面にポリシロキサンよりなる極薄のポリマー膜が形成される。このポリマー膜は、アミノ化マグネタイト微粒子4の表面に共有結合により固定されていないが、エポキシ基を含んでいるため、アミノ化マグネタイト微粒子4に対してアミノ基を有する膜化合物の単分子膜3と同様の反応性を有している。そのため、洗浄を行わなくても、工程B以降の製造工程に特に支障をきたすことはない。
【0072】
なお、本実施の形態においては、アミノ基を有するアルコキシシラン化合物を用いたが、直鎖状アルキレン基の一方の末端にエポキシ基(オキシラン環)を含む官能基を、他方の末端にアルコキシシリル基をそれぞれ有し、下記の一般式(化3)で表されるアルコキシシラン化合物を用いてもよい。
【0073】
【化3】

【0074】
上式において、Eはエポキシ基を有する官能基を、mは3〜20の整数を、Rは炭素数1〜4のアルキル基をそれぞれ表す。
用いることのできるエポキシ基を有する膜化合物の具体例としては、下記(11)〜(22)に示したアルコキシシラン化合物が挙げられる。
【0075】
(11) (CH2OCH)CH2O(CH2)3Si(OCH3)3
(12) (CH2OCH)CH2O(CH2)7Si(OCH3)3
(13) (CH2OCH)CH2O(CH2)11Si(OCH3)3
(14) (CH2CHOCH(CH2)2)CH(CH2)2Si(OCH3)3
(15) (CH2CHOCH(CH2)2)CH(CH2)4Si(OCH3)3
(16) (CH2CHOCH(CH2)2)CH(CH2)6Si(OCH3)3
(17) (CH2OCH)CH2O(CH2)3Si(OC2H5)3
(18) (CH2OCH)CH2O(CH2)7Si(OC2H5)3
(19) (CH2OCH)CH2O(CH2)11Si(OC2H5)3
(20) (CH2CHOCH(CH2)2)CH(CH2)2Si(OC2H5)3
(21) (CH2CHOCH(CH2)2)CH(CH2)4Si(OC2H5)3
(22) (CH2CHOCH(CH2)2)CH(CH2)6Si(OC2H5)3
【0076】
ここで、(CH2OCH)CH2O−基は、化4で表される官能基(グリシドキシ基)を表し、(CH2CHOCH(CH2)2)CH−基は、化5で表される官能基(3,4−エポキシシクロヘキシル基)を表す。
【0077】
【化4】

【0078】
【化5】

【0079】
エポキシ基を有するアルコキシシラン化合物に対しては、上記の縮合触媒に加え、さらに、カルボン酸スズ塩、カルボン酸エステルスズ塩、カルボン酸スズ塩ポリマー、カルボン酸スズ塩キレートを含む化合物を単独でまたは2種類以上を混合して縮合触媒として用いることができる。
用いることのできる助触媒の種類およびそれらの組み合わせ、溶媒の種類、アルコキシシラン化合物、縮合触媒、および助触媒の濃度、反応条件ならびに反応時間についてはエポキシ基を有するアルコキシシラン化合物の場合と同様であるので、説明を省略する。
【0080】
また、本実施の形態においては、微粒子としてマグネタイト微粒子を用いたが、アルコキシシラン化合物と反応する表面基を有する任意の磁性微粒子を用いることもできる。具体的には、鉄、クロム、ニッケルやそれらの合金等よりなる磁性金属微粒子やフェライトやマグネタイト、酸化クロム等よりなる磁性金属酸化物微粒子等が挙げられる。
また、第1の反応基としてアルコキシシリル基以外の官能基を有する膜化合物を用いてもよい。例えば、金メッキ層を有する微粒子の場合には、膜化合物として金原子と強い結合を形成するチオール誘導体またはトリアジンチオール誘導体を用いることができる。
(以上工程A)
【0081】
工程Bでは、アミノ化マグネタイト微粒子4に架橋剤5を接触させ、アミノ基とエポキシ基の反応より形成された共有結合を介して架橋剤5をアミノ化マグネタイト微粒子4の表面に固定し、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7を調製する。
【0082】
架橋剤5として用いることができるジエポキシ化合物には特に制限はなく、各種の公知のジエポキシ化合物を用いることができる。具体的には、エチレングリコールジグリシジルエーテル、ジエチレングリコールジグリシジルエーテル、トリエチレングリコールジグリシジルエーテル、ポリエチレングリコールジグリシジルエーテル、プロピレングリコールジグリシジルエーテル、ジプロピレングリコールジグリシジルエーテル、トリプロピレングリコールジグリシジルエーテル、ポリプロピレングリコールジグリシジルエーテル、ネオペンチルグリコールジグリシジルエーテル、1,6−ヘキサンジオールジグリシジルエーテル等の非環状脂肪族ジグリシジルエーテル類、2,2−ビス(4−ヒドロキシフェニル)プロパンジグリシジルエーテル、ビス(4−ヒドロキシフェニル)メタンジグリシジルエーテル、1,1−ビス(4−ヒドロキシフェニル)エタンジグリシジルエーテル、2,2−ビス(4−ヒドロキシシクロヘキシル)プロパンジグリシジルエーテル、3,3’,5,5’−テトラメチル−4,4’−ヒドロキシビフェニルジグリシジルエーテル、2,2’−ビス(4−(β−ヒドロキシプロポキシ)フェニル)プロパンジグリシジルエーテル等の芳香族または環状脂肪族ジグリシジルエーテル類等が挙げられる。
【0083】
アミノ化マグネタイト微粒子4と架橋剤5とを溶媒中で加熱すると、エポキシ基と網の帰途の間で、下式(化6)のような反応が起こり、共有結合が形成される。溶媒としては、エタノール等のアルコール系溶媒が好ましく、数十分〜数時間程度加熱環流する。
溶媒に添加するアミノ化マグネタイト微粒子4と架橋剤5とのモル比は、導入する薬剤の量等に応じて適宜調節される。
【0084】
【化6】

【0085】
反応終了後、ろ過により溶媒と分離後、溶媒で洗浄し、未反応物として表面に残った過剰な架橋剤5を除去すると、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7が得られる。
洗浄溶媒としては、工程Aと同様の洗浄溶媒を用いることができる。
【0086】
なお、工程Aにおいて、直鎖状アルキレン基の一方の末端にエポキシ基を含む官能基を有するアルコキシシラン化合物を用いた場合には、第1の架橋反応基としてアミノ基またはイミノ基とアルコキシシリル基、あるいは、アミノ基またはイミノ基とチオール基とをそれぞれ分子の両端に含む化合物を架橋剤として用いる。
【0087】
本実施の形態においては、第2の架橋反応基としてエポキシ基を用いたが、生体内で薬剤を放出するために、生分解性を有する官能基を用いてもよい。
(以上工程B)
【0088】
工程Cでは、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7とペニシリンG 6とを接触させ、イミノ基とエポキシ基との反応により、ペニシリンG 6を、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7の表面に結合させ、磁気感応性薬剤10を製造する(図1)。
架橋剤が表面に固定されたアミノ化マグネタイト微粒子7とペニシリンG 6とを溶媒中で加熱すると、ペニシリンG 6がβラクタム環上に有するアミド窒素とエポキシ基との間で、下式(化7)のような反応が起こり、共有結合を形成する。
【0089】
【化7】

【0090】
溶媒としては、エタノール等のアルコール系溶媒が好ましく、数時間程度加熱環流する。
溶媒に添加する架橋剤が表面に固定されたアミノ化マグネタイト微粒子7とペニシリンG 6とのモル比は、導入するペニシリンG 6の量等に応じて適宜調節される。
【0091】
反応終了後、ろ過により溶媒と分離後、溶媒で洗浄し、未反応物として表面に残った過剰なペニシリンG 6を除去すると、磁気感応性薬剤10が得られる。
洗浄溶媒としては、工程Aと同様の洗浄溶媒を用いることができる。
【0092】
本実施の形態においては、薬剤としてペニシリンGを用いたが、アミノ基、イミノ基、水酸基およびチオール基のいずれか1を有し、エポキシ基との反応条件化で分解しない任意の薬剤を用いることができる。例えば、他の抗生物質としては、セファレキシン等が挙げられる。その他にも、タンパク質、アミノ酸、酵素、抗体、ペプチド、抗菌物質、あるいは磁気画像診断用以外の造影剤等を薬剤として用いることができる。
【0093】
薬剤以外の機能物質を同様の方法により磁性を有する微粒子の表面に固定すると、磁気感応性物質が得られる。例えば、機能物質として触媒を用いると、触媒反応終了後、磁石等の磁気発生手段により反応系から容易に回収することができる磁気感応触媒が得られる。
また、特定の生理活性物質に対する親和性を有する抗体やリガンド等を機能物質として用いると、該生理活性物質を含む混合物から、磁石等の磁気発生手段により結合した生理活性物質を分離することができる磁気感応アフィニティ担体が得られる。
あるいは、EDTA、クラウンエーテル、カリックスアレーン、シクロデキストリン等のホスト化合物を機能物質として用いると、混合物から金属イオン、有機化合物等の分離または回収が可能な磁気感応性物質が得られる。
【実施例】
【0094】
以下、本発明の効果を確認するために行った実施例について説明するが、本願発明は、これら実施例によって何ら制限されるものではない。
【0095】
(1)アミノ化マグネタイト微粒子の調製
粒径が数十ナノメートルの無水のマグネタイト微粒子を用意し、よく乾燥した。
3−アミノプロピルトリメトキシシラン(化8)0.99重量部、および酢酸(縮合触媒)0.01重量部を秤量し、これを100重量部のヘキサメチルジシロキサン−ジメチルホルムアミド混合溶媒(1:1v/v)に溶解し、反応液を調製した。
【0096】
【化8】

【0097】
この反応液に乾燥したマグネタイト微粒子を加え、室温の空気中(相対湿度45%)で2時間程度撹拌して反応させた。その後、トリクレンで洗浄し、過剰なアルコキシシラン化合物を除去した。
【0098】
【化2】

【0099】
(2)架橋剤が表面に固定されたアミノ化マグネタイト微粒子の調製
アミノ化マグネタイト微粒子、およびエチレングリコールジグリシジルエーテルをエタノール中で加熱環流した。室温まで放冷後、ろ過し、ろ過物をエタノールで洗浄し、過剰なエチレングリコールジグリシジルエーテルを除去した。
【0100】
(2)磁気感応性薬剤の調製
架橋剤が表面に固定されたアミノ化マグネタイト微粒子の調製、およびペニシリンGをエタノール中で加熱環流した。室温まで放冷後、ろ過し、ろ過物をエタノールで洗浄し、過剰なペニシリンGを除去した。
得られた磁気感応性薬剤は、粒径がたかだか数十ナノメートルなので、純水に分散して血管注射しても、血管が詰まることはない。さらに、この薬剤は、磁石に引き寄せられる機能を持っているため、患部近傍に磁石を設置しておくと血液が一定時間体内を循環する間に磁力で薬剤を患部に集中できる。
したがってトータルの投与鑓が極めて少なくても、患部近傍のみペニシリンGを高濃度にできるため副作用を低減でき、効率の良い治療が可能となった。
【図面の簡単な説明】
【0101】
【図1】本発明の一実施の形態に係る、ペニシリンGが結合固定された磁気感応性薬剤の構造を模式的に表した説明図である。
【図2】(a)は反応前のマグネタイト微粒子表面の構造を模式的に表した説明図、(b)は、エポキシ化マグネタイト微粒子の構造を模式的に表した説明図、(c)は、架橋剤が結合したエポキシ化マグネタイト微粒子の構造を模式的に示す説明図である。
【符号の説明】
【0102】
1:マグネタイト微粒子、2:水酸基、3:アミノ基を有する膜化合物の単分子膜、4:アミノ化マグネタイト微粒子、5:架橋剤、6:ペニシリンG、7:架橋剤が表面に固定されたアミノ化マグネタイト微粒子、10:磁気感応性薬剤
【技術分野】
【0001】
本発明は、磁気感応性物質、磁気感応性薬剤およびそれらの製造方法に関するものである。さらに詳しくは、磁性を有する微粒子表面に共有結合した有機薄膜を介して機能物質が結合固定されており、磁石を用いて、混合物からの機能物質の分離が可能な磁気感応性物質、および磁性を有する微粒子表面に共有結合した有機薄膜を介して薬剤が結合固定されており、磁石を用いて、薬剤の体内動態が制御可能な磁気感応性薬剤、ならびにこれらの製造方法に関する。
【背景技術】
【0002】
現在、薬剤の副作用を和らげたり、低減させたりする目的で、必要な時間に必要な部位で作用させるための薬物システムが数々研究開発されている。
【0003】
【特許文献1】特表2002−500177号公報
【特許文献2】特表2000−503763号公報
【特許文献3】特開平09−328438号公報
【発明の開示】
【発明が解決しようとする課題】
【0004】
しかしながら、混合物から磁力を用いて分離可能な磁気感応性物質およびその製造方法、さらには磁力を用いて必要な部位に薬剤を集中させるというシステムに用いる薬剤およびその製造方法は、未だ開発、提供されていない。
【0005】
本発明は、磁力を用いて分離あるいは集積が可能な磁気感応性物質を製造し、触媒等に用いた物質の分離を高能率に行うことを目的とする。また、磁力を用いて生体内の必要部位に集中させることができ、且つ、投薬量が極めて少なくて済むDDS用の薬剤を製造し、薬剤による副作用を和らげたり、薬剤の使用量を低減させたりすることを目的とする。
【課題を解決するための手段】
【0006】
前記目的に沿う第1の発明に係る磁気感応性物質は、磁性を有する微粒子に機能物質が結合した磁気感応性物質であって、前記微粒子の表面は、分子の両端に第1および第2の官能基を有する膜化合物の形成する薄膜によって被覆されており、前記膜化合物は、前記第1の官能基と前記微粒子の表面との反応により形成された共有結合を介して前記微粒子の表面に固定されており、前記薄膜の表面には、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記機能物質の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤が、前記第2の官能基と前記第1の架橋反応基との反応により形成された共有結合を介して結合しており、前記機能物質の官能基と前記第2の架橋官能基との反応により形成された結合を介して、前記機能物質が前記微粒子に結合している。
【0007】
第1の発明に係る磁気感応性物質において、前記膜化合物の形成する薄膜が単分子膜であることが好ましい。
【0008】
第1の発明に係る磁気感応性物質において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であってもよい。
【0009】
第2の発明に係る磁気感応性薬剤は、磁性を有する微粒子に薬剤が結合した磁気感応性物質であって、前記微粒子の表面は、分子の両端に第1および第2の官能基を有する膜化合物の形成する薄膜によって被覆されており、前記膜化合物は、前記第1の官能基と前記微粒子の表面との反応により形成された共有結合を介して前記微粒子の表面に固定されており、
前記薄膜の表面には、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記薬剤の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤が、前記第2の官能基と前記第1の架橋反応基との反応により形成された共有結合を介して結合しており、前記薬剤の官能基と前記第2の架橋官能基との反応により形成された結合を介して、前記薬剤が前記微粒子に結合している。
【0010】
第2の発明に係る磁気感応性薬剤において、前記薬剤が、アミノ基、イミノ基、水酸基、およびチオール基のいずれか1を含むタンパク質、アミノ酸、酵素、抗体、抗生物質、抗菌物質、および造影剤のいずれか1であってもよい。
【0011】
第2の発明に係る磁気感応性薬剤において、前記膜化合物の形成する薄膜が単分子膜であることが好ましい。
【0012】
第2の発明に係る磁気感応性薬剤磁気感応性薬剤において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であってもよい。
【0013】
第2の発明に係る磁気感応性薬剤磁気感応性薬剤において、前記薬剤の有する前記官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ前記第2の架橋反応基は、アルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であってもよい。
【0014】
第3の発明に係る磁気感応性物質の製造方法は、磁性を有する微粒子に機能物質が結合した磁気感応性物質の製造方法であって、分子の両端にそれぞれ第1および第2の官能基を有する膜化合物を含む溶液を前記微粒子の表面に接触させ、前記第1の官能基と前記微粒子の表面との間で結合を形成させ、前記膜化合物の形成する薄膜で前記微粒子の表面が被覆された反応性微粒子を調製する工程Aと、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記機能物質の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤を、前記反応性微粒子の表面に接触させ、前記第2の官能基と前記第1の架橋反応基との反応により共有結合を形成させ、前記架橋剤を前記反応性微粒子の表面に固定する工程Bと、前記架橋剤が固定された反応性微粒子の表面に前記機能物質を接触させ、前記機能物質の官能基と前記第2の架橋反応基との反応により結合を形成させ、前記機能物質を前記架橋剤が固定された反応性微粒子に結合させる工程Cとを有する。
【0015】
第3の発明に係る磁気感応性物質の製造方法において、前記工程Aにおける結合の形成後に、未反応の前記膜化合物を除去することが好ましい。
【0016】
第3の発明に係る磁気感応性物質の製造方法において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であってもよい。
【0017】
第3の発明に係る磁気感応性物質の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含んでいてもよい。
【0018】
第3の発明に係る磁気感応性物質の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含んでいてもよい。
【0019】
第3の発明に係る磁気感応性物質の製造方法において、さらに助触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含んでいてもよい。
【0020】
第4の発明に係る磁気感応性薬剤の製造方法は、磁性を有する微粒子に薬剤が結合した磁気感応性薬剤の製造方法であって、分子の両端にそれぞれ第1および第2の官能基を有する膜化合物を含む溶液を前記微粒子の表面に接触させ、前記第1の官能基と前記微粒子の表面との間で結合を形成させ、前記膜化合物の形成する薄膜で前記微粒子の表面が被覆された反応性微粒子を調製する工程Aと、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記薬剤の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤を、前記反応性微粒子の表面に接触させ、前記第2の官能基と前記第1の架橋反応基との反応により共有結合を形成させ、前記架橋剤を前記反応性微粒子の表面に固定する工程Bと、前記架橋剤が固定された反応性微粒子の表面に前記薬剤を接触させ、前記薬剤の官能基と前記第2の架橋反応基との反応により結合を形成させ、前記薬剤を前記架橋剤が固定された反応性微粒子に結合させる工程Cとを有する。
【0021】
第4の発明に係る磁気感応性薬剤の製造方法において、前記工程Aにおける結合の形成後に、未反応の前記膜化合物を除去することが好ましい。
【0022】
第4の発明に係る磁気感応性薬剤の製造方法において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であってもよい。
【0023】
第4の発明に係る磁気感応性薬剤の製造方法において、前記薬剤の有する前記官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ前記第2の架橋反応基は、アルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であってもよい。
【0024】
第4の発明に係る磁気感応性薬剤の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含んでいてもよい。
【0025】
第4の発明に係る磁気感応性薬剤の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含んでいてもよい。
【0026】
第4の発明に係る磁気感応性薬剤の製造方法において、さらに助触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含んでいてもよい。
【発明の効果】
【0027】
請求項1〜3に記載の磁気感応性物質、および請求項9〜14に記載の磁気感応性物質の製造方法は、磁力を用いて分離あるいは集積が可能であり、磁石等の磁気発生手段を用いて、結合した機能物質の分離を高能率に行うことができる磁気感応性物質およびその製造方法を提供できる。
【0028】
特に、請求項2記載の磁気感応性物質においては、第1の膜化合物の形成する薄膜が単分子膜であるため、微粒子本来の物性や機能を保持することができる。
【0029】
請求項3記載の磁気感応性物質においては、第2の官能基がエポキシ基であり、かつ第1の架橋反応基がアミノ基またはイミノ基であるので、加熱により強固な結合を形成できる。
【0030】
請求項10記載の磁気感応性物質の製造方法においては、未反応の膜化合物を除去するので、磁気感応性物質からの膜化合物の溶出を抑制することができる。
【0031】
請求項11記載の磁気感応性物質の製造方法においては、第2の官能基がエポキシ基であり、かつ第1の架橋反応基がアミノ基またはイミノ基であるので、加熱により強固な結合を形成できる。
【0032】
請求項12記載の磁気感応性物質の製造方法においては、膜化合物を含む溶液が、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含むので、反応性微粒子の調製時間を短縮し、磁気感応性物質の製造をより高効率に行うことができる。
【0033】
請求項13および14記載の磁気感応性物質の製造方法においては、膜化合物を含む溶液が、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、アミノアルキルアルコキシシラン化合物からからなる群より選択される1または2以上の化合物をさらに含むので、反応性微粒子の調製時間を短縮し、磁気感応性物質の製造をより高効率に行うことができる。特に、これらの化合物と上述の縮合触媒の両者をともに含む場合には、調製時間をさらに短縮できる。
【0034】
請求項4〜8に記載の磁気感応性薬剤、および請求項15〜21に記載の磁気感応性薬剤の製造方法は、磁石を用いて、薬剤の体内動態が制御可能なであるため、標的部位にのみ選択的に投与することが可能であり、高い効果を有しかつ副作用の少ない磁気感応性薬剤およびその製造方法を提供できる。
【0035】
請求項5記載の磁気感応性薬剤において、薬剤が、アミノ基、イミノ基、水酸基、およびチオール基のいずれか1であるので、エポキシ基との反応により形成された結合により、安定に固定できる。
【0036】
請求項6記載の磁気感応性物質においては、第1の膜化合物の形成する薄膜が単分子膜であるため、微粒子本来の物性や機能を保持することができる。
【0037】
請求項7記載の磁気感応性薬剤においては、第2の官能基がエポキシ基であり、かつ第1の架橋反応基がアミノ基またはイミノ基であるので、加熱により強固な結合を形成できる。
【0038】
請求項8記載の磁気感応性薬剤においては、薬剤の有する官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ第2の架橋反応基はアルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であるので、加熱により形成される結合により薬剤を強固に固定できる。
【0039】
請求項16記載の磁気感応性薬剤の製造方法においては、未反応の膜化合物を除去するので、磁気感応性薬剤からの膜化合物の溶出を抑制することができる。
【0040】
請求項17記載の磁気感応性薬剤の製造方法においては、第2の官能基がエポキシ基であり、かつ第1の架橋反応基がアミノ基またはイミノ基であるので、加熱により強固な結合を形成できる。
【0041】
請求項18記載の磁気感応性薬剤の製造方法においては、薬剤の有する官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ第2の架橋反応基はアルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であるので、反応する官能基を組み合わせれば、加熱により形成される結合により薬剤を強固に固定できる。
【0042】
請求項19記載の磁気感応性薬剤の製造方法においては、膜化合物を含む溶液が、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含むので、反応性微粒子の調製時間を短縮し、磁気感応性物質の製造をより高効率に行うことができる。
【0043】
請求項20および21記載の磁気感応性薬剤の製造方法においては、膜化合物を含む溶液が、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、アミノアルキルアルコキシシラン化合物からからなる群より選択される1または2以上の化合物をさらに含むので、反応性微粒子の調製時間を短縮し、磁気感応性物質の製造をより高効率に行うことができる。特に、これらの化合物と上述の縮合触媒の両者をともに含む場合には、調製時間をさらに短縮できる。
【発明を実施するための最良の形態】
【0044】
以下、図面を参照しながら本発明の一実施の形態に係る磁気感応性薬剤について説明する。
図1に示すように、本発明の一実施の形態に係る磁気感応性薬剤10は、マグネタイト微粒子(磁性を有する微粒子の一例)1の表面が、アミノ基(第2の官能基の一例)を有する膜化合物(第1の膜化合物)の単分子膜3で被覆されたアミノ化マグネタイト微粒子(反応性微粒子の一例)4の表面に、架橋剤5を介してペニシリンG(薬剤の一例)6が結合している。
アミノ基を有する膜化合物は、アルコキシシリル基(第1の官能基の一例)とマグネタイト微粒子1の表面の水酸基2との反応により形成された共有結合を介してマグネタイト微粒子1の表面に固定されている。
架橋剤5は、2個のエポキシ基(第1および第2の架橋反応基の一例)を有するジエポキシ化合物であり、一方のエポキシ基とアミノ化マグネタイト微粒子4の表面のアミノ基との反応により形成される共有結合を介してアミノ化マグネタイト粒子4の表面に固定されている。
ペニシリンG 6は、イミノ基と架橋剤が表面に固定されたアミノ化マグネタイト微粒子7のエポキシ基との反応により形成された共有結合により、架橋剤5を介してアミノ化マグネタイト微粒子4に結合している。
【0045】
磁気感応性薬剤10の製造方法は、図2(a)〜(c)に示すように、アミノ基を有する膜化合物をマグネタイト微粒子1と接触させ、アミノ化マグネタイト微粒子4を製造する工程Aと、アミノ化マグネタイト微粒子4に架橋剤5を接触させ、アミノ基とエポキシ基の反応より形成された共有結合を介して架橋剤5をアミノ化マグネタイト微粒子4の表面に固定する工程Bと、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7とペニシリンG 6とを接触させ、ペニシリンG 6に含まれているイミノ基とエポキシ基との反応により、ペニシリンG 6を、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7の表面に結合させる工程Cとを含んでいる。
【0046】
以下、工程A〜Cについてより詳細に説明する。
工程Aでは、アミノ基を有する膜化合物をマグネタイト微粒子1と接触させ、アミノ化マグネタイト微粒子4を製造する。
【0047】
用いることのできるマグネタイト微粒子1の粒径に特に制限はないが、10nm〜0.1mmの範囲内であることが好ましい。マグネタイト微粒子1の粒径が10nm未満である場合には、磁気特性が大幅に劣化し、粒径が0.1mmを上回る場合には、沈降しやすくなり、溶液中への分散が困難になる。特に、DDS用の磁気感応性薬剤として用いる場合には、マグネタイト微粒子1の粒径は、10〜1μm、好ましくは数十〜数百nmである。粒径が1μmを超すと、血管注射ができなくなるためである。
【0048】
アミノ基を有する膜化合物としては、マグネタイト微粒子1の表面に吸着または水酸基2との反応により結合し、自己組織化により単分子膜を形成することのできる任意の化合物を用いることができるが、直鎖状アルキレン基の一方の末端にアミノ基を、他方の末端にアルコキシシリル基をそれぞれ有し、下記の一般式(化1)で表されるアルコキシシラン化合物が好ましい。
【0049】
【化1】

【0050】
上式において、mは3〜20の整数を、Rは炭素数1〜4のアルキル基をそれぞれ表す。
用いることのできるアミノ基を有する膜化合物の具体例としては、下記(1)〜(8)に示したアルコキシシラン化合物が挙げられる。
【0051】
(1) H2N(CH2)3Si(OCH3)3
(2) H2N(CH2)5Si(OCH3)3
(3) H2N(CH2)7Si(OCH3)3
(4) H2N(CH2)9Si(OCH3)3
(5) H2N(CH2)5Si(OC2H5)3
(6) H2N(CH2)5Si(OC2H5)3
(7) H2N(CH2)7Si(OC2H5)3
(8) H2N(CH2)9Si(OC2H5)3
【0052】
アミノ化マグネタイト微粒子4の製造は、アミノ基を含むアルコキシシラン化合物と、アルコキシシリル基とマグネタイト微粒子1の表面の水酸基2との縮合反応を促進するための縮合触媒と、非水系の有機溶媒とを混合した反応液中にマグネタイト微粒子1を分散させ、室温の空気中で反応させることにより行われる。
【0053】
縮合触媒としては、カルボン酸金属塩、チタン酸エステルおよびチタン酸エステルキレート等の金属塩が利用可能である。
縮合触媒の添加量は、好ましくはアルコキシシラン化合物の0.2〜5質量%であり、より好ましくは0.5〜1質量%である。
【0054】
カルボン酸金属塩の具体例としては、ジブチルスズジラウレート、ジブチルスズジオクテート、ジブチルスズジアセテート、ジオクチルスズジラウレート、ジオクチルスズジオクテート、ジオクチルスズジアセテート、ナフテン酸鉛、ナフテン酸コバルト、2−エチルヘキセン酸鉄が挙げられる。
【0055】
チタン酸エステルの具体例としては、テトラブチルチタネート、テトラノニルチタネートが挙げられる。
チタン酸エステルキレート類の具体例としては、ビス(アセチルアセトニル)ジ−プロピルチタネートが挙げられる。
【0056】
アルコキシシリル基とマグネタイト微粒子1の表面の水酸基2とが縮合反応を起こし、下記の化2で示されるような構造を有するアミノ基を有する膜化合物の単分子膜3を生成する。なお、酸素原子から延びた3本の単結合はマグネタイト微粒子1の表面または隣接するシラン化合物のケイ素(Si)原子と結合しており、そのうち少なくとも1本はマグネタイト微粒子1の表面と結合している。
【0057】
【化2】

【0058】
アルコキシシリル基は、水分の存在下で分解するので、反応は相対湿度45%以下の空気中で行うことが好ましい。なお、縮合反応は、シリカ微粒子21の表面に付着した油脂分や水分により阻害されるので、シリカ微粒子21をよく洗浄して乾燥することにより、これらの不純物を予め除去しておくことが好ましい。
縮合触媒として上述の金属塩のいずれかを用いた場合、縮合反応の完了までに要する時間は2時間程度である。
【0059】
上述の金属塩の代わりに、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、アミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物を縮合触媒として用いた場合、反応時間を1/2〜2/3程度まで短縮できる。
【0060】
あるいは、これらの化合物を助触媒として、上述の金属塩と混合(質量比1:9〜9:1の範囲で使用可能だが、1:1前後が好ましい)して用いると、反応時間をさらに短縮できる。
【0061】
例えば、縮合触媒として、ケチミン化合物であるジャパンエポキシレジン社のH3を用い、その他の条件は同一にしてアミノ化マグネタイト微粒子4の製造を行うと、アミノ化マグネタイト微粒子4の品質を損なうことなく反応時間を1時間程度にまで短縮できる。
【0062】
さらに、縮合触媒として、ジャパンエポキシレジン社のH3とジブチルスズビスアセチルアセトネートとの混合物(混合比は1:1)を用い、その他の条件は同一にしてエポキシ化シリカ微粒子11の製造を行うと、反応時間を20分程度に短縮できる。
【0063】
なお、ここで用いることができるケチミン化合物は特に限定されるものではないが、例えば、2,5,8−トリアザ−1,8−ノナジエン、3,11−ジメチル−4,7,10−トリアザ−3,10−トリデカジエン、2,10−ジメチル−3,6,9−トリアザ−2,9−ウンデカジエン、2,4,12,14−テトラメチル−5,8,11−トリアザ−4,11−ペンタデカジエン、2,4,15,17−テトラメチル−5,8,11,14−テトラアザ−4,14−オクタデカジエン、2,4,20,22−テトラメチル−5,12,19−トリアザ−4,19−トリエイコサジエン等が挙げられる。
【0064】
また、用いることができる有機酸としても特に限定されるものではないが、例えば、ギ酸、酢酸、プロピオン酸、酪酸、マロン酸等が挙げられる。
【0065】
反応液の製造には、有機塩素系溶媒、炭化水素系溶媒、フッ化炭素系溶媒、シリコーン系溶媒、およびこれらの混合溶媒を用いることができる。アルコキシシラン化合物の加水分解を防止するために、乾燥剤または蒸留により使用する溶媒から水分を除去しておくことが好ましい。また、溶媒の沸点は50〜250℃であることが好ましい。
【0066】
具体的に使用可能な溶媒としては、非水系の石油ナフサ、ソルベントナフサ、石油エーテル、石油ベンジン、イソパラフィン、ノルマルパラフィン、デカリン、工業ガソリン、ノナン、デカン、灯油、ジメチルシリコーン、フェニルシリコーン、アルキル変性シリコーン、ポリエーテルシリコーン、ジメチルホルムアミド等を挙げることができる。
さらに、メタノール、エタノール、プロパノール等のアルコール系溶媒、あるいはそれらの混合物を用いることもできる。
【0067】
また、用いることができるフッ化炭素系溶媒としては、フロン系溶媒、フロリナート(米国3M社製)、アフルード(旭硝子株式会社製)等がある。なお、これらは1種単独で用いても良いし、良く混ざるものなら2種以上を組み合わせてもよい。さらに、ジクロロメタン、クロロホルム等の有機塩素系溶媒を添加してもよい。
【0068】
反応液におけるアルコキシシラン化合物の好ましい濃度は、0.5〜3質量%である。
【0069】
反応後、溶媒で洗浄し、未反応物として表面に残った過剰なアルコキシシラン化合物および縮合触媒を除去すると、アミノ基を有する膜化合物の単分子膜3で表面が覆われたアミノ化マグネタイト微粒子4が得られる。このようにして製造されるアミノ化マグネタイト微粒子4の断面構造の模式図を図2(b)に示す。
【0070】
洗浄溶媒としては、アルコキシシラン化合物を溶解できる任意の溶媒を用いることができるが、安価であり、溶解性が高く、風乾により容易に除去することのできるジクロロメタン、クロロホルム、N−メチルピロリドン等が好ましい。
【0071】
反応後、生成したアミノ化マグネタイト微粒子4を溶媒で洗浄せずに空気中に放置すると、表面に残ったアルコキシシラン化合物の一部が空気中の水分により加水分解を受け、生成したシラノール基がアルコキシシリル基と縮合反応を起こす。その結果、アミノ化マグネタイト微粒子4の表面にポリシロキサンよりなる極薄のポリマー膜が形成される。このポリマー膜は、アミノ化マグネタイト微粒子4の表面に共有結合により固定されていないが、エポキシ基を含んでいるため、アミノ化マグネタイト微粒子4に対してアミノ基を有する膜化合物の単分子膜3と同様の反応性を有している。そのため、洗浄を行わなくても、工程B以降の製造工程に特に支障をきたすことはない。
【0072】
なお、本実施の形態においては、アミノ基を有するアルコキシシラン化合物を用いたが、直鎖状アルキレン基の一方の末端にエポキシ基(オキシラン環)を含む官能基を、他方の末端にアルコキシシリル基をそれぞれ有し、下記の一般式(化3)で表されるアルコキシシラン化合物を用いてもよい。
【0073】
【化3】

【0074】
上式において、Eはエポキシ基を有する官能基を、mは3〜20の整数を、Rは炭素数1〜4のアルキル基をそれぞれ表す。
用いることのできるエポキシ基を有する膜化合物の具体例としては、下記(11)〜(22)に示したアルコキシシラン化合物が挙げられる。
【0075】
(11) (CH2OCH)CH2O(CH2)3Si(OCH3)3
(12) (CH2OCH)CH2O(CH2)7Si(OCH3)3
(13) (CH2OCH)CH2O(CH2)11Si(OCH3)3
(14) (CH2CHOCH(CH2)2)CH(CH2)2Si(OCH3)3
(15) (CH2CHOCH(CH2)2)CH(CH2)4Si(OCH3)3
(16) (CH2CHOCH(CH2)2)CH(CH2)6Si(OCH3)3
(17) (CH2OCH)CH2O(CH2)3Si(OC2H5)3
(18) (CH2OCH)CH2O(CH2)7Si(OC2H5)3
(19) (CH2OCH)CH2O(CH2)11Si(OC2H5)3
(20) (CH2CHOCH(CH2)2)CH(CH2)2Si(OC2H5)3
(21) (CH2CHOCH(CH2)2)CH(CH2)4Si(OC2H5)3
(22) (CH2CHOCH(CH2)2)CH(CH2)6Si(OC2H5)3
【0076】
ここで、(CH2OCH)CH2O−基は、化4で表される官能基(グリシドキシ基)を表し、(CH2CHOCH(CH2)2)CH−基は、化5で表される官能基(3,4−エポキシシクロヘキシル基)を表す。
【0077】
【化4】

【0078】
【化5】

【0079】
エポキシ基を有するアルコキシシラン化合物に対しては、上記の縮合触媒に加え、さらに、カルボン酸スズ塩、カルボン酸エステルスズ塩、カルボン酸スズ塩ポリマー、カルボン酸スズ塩キレートを含む化合物を単独でまたは2種類以上を混合して縮合触媒として用いることができる。
用いることのできる助触媒の種類およびそれらの組み合わせ、溶媒の種類、アルコキシシラン化合物、縮合触媒、および助触媒の濃度、反応条件ならびに反応時間についてはエポキシ基を有するアルコキシシラン化合物の場合と同様であるので、説明を省略する。
【0080】
また、本実施の形態においては、微粒子としてマグネタイト微粒子を用いたが、アルコキシシラン化合物と反応する表面基を有する任意の磁性微粒子を用いることもできる。具体的には、鉄、クロム、ニッケルやそれらの合金等よりなる磁性金属微粒子やフェライトやマグネタイト、酸化クロム等よりなる磁性金属酸化物微粒子等が挙げられる。
また、第1の反応基としてアルコキシシリル基以外の官能基を有する膜化合物を用いてもよい。例えば、金メッキ層を有する微粒子の場合には、膜化合物として金原子と強い結合を形成するチオール誘導体またはトリアジンチオール誘導体を用いることができる。
(以上工程A)
【0081】
工程Bでは、アミノ化マグネタイト微粒子4に架橋剤5を接触させ、アミノ基とエポキシ基の反応より形成された共有結合を介して架橋剤5をアミノ化マグネタイト微粒子4の表面に固定し、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7を調製する。
【0082】
架橋剤5として用いることができるジエポキシ化合物には特に制限はなく、各種の公知のジエポキシ化合物を用いることができる。具体的には、エチレングリコールジグリシジルエーテル、ジエチレングリコールジグリシジルエーテル、トリエチレングリコールジグリシジルエーテル、ポリエチレングリコールジグリシジルエーテル、プロピレングリコールジグリシジルエーテル、ジプロピレングリコールジグリシジルエーテル、トリプロピレングリコールジグリシジルエーテル、ポリプロピレングリコールジグリシジルエーテル、ネオペンチルグリコールジグリシジルエーテル、1,6−ヘキサンジオールジグリシジルエーテル等の非環状脂肪族ジグリシジルエーテル類、2,2−ビス(4−ヒドロキシフェニル)プロパンジグリシジルエーテル、ビス(4−ヒドロキシフェニル)メタンジグリシジルエーテル、1,1−ビス(4−ヒドロキシフェニル)エタンジグリシジルエーテル、2,2−ビス(4−ヒドロキシシクロヘキシル)プロパンジグリシジルエーテル、3,3’,5,5’−テトラメチル−4,4’−ヒドロキシビフェニルジグリシジルエーテル、2,2’−ビス(4−(β−ヒドロキシプロポキシ)フェニル)プロパンジグリシジルエーテル等の芳香族または環状脂肪族ジグリシジルエーテル類等が挙げられる。
【0083】
アミノ化マグネタイト微粒子4と架橋剤5とを溶媒中で加熱すると、エポキシ基と網の帰途の間で、下式(化6)のような反応が起こり、共有結合が形成される。溶媒としては、エタノール等のアルコール系溶媒が好ましく、数十分〜数時間程度加熱環流する。
溶媒に添加するアミノ化マグネタイト微粒子4と架橋剤5とのモル比は、導入する薬剤の量等に応じて適宜調節される。
【0084】
【化6】

【0085】
反応終了後、ろ過により溶媒と分離後、溶媒で洗浄し、未反応物として表面に残った過剰な架橋剤5を除去すると、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7が得られる。
洗浄溶媒としては、工程Aと同様の洗浄溶媒を用いることができる。
【0086】
なお、工程Aにおいて、直鎖状アルキレン基の一方の末端にエポキシ基を含む官能基を有するアルコキシシラン化合物を用いた場合には、第1の架橋反応基としてアミノ基またはイミノ基とアルコキシシリル基、あるいは、アミノ基またはイミノ基とチオール基とをそれぞれ分子の両端に含む化合物を架橋剤として用いる。
【0087】
本実施の形態においては、第2の架橋反応基としてエポキシ基を用いたが、生体内で薬剤を放出するために、生分解性を有する官能基を用いてもよい。
(以上工程B)
【0088】
工程Cでは、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7とペニシリンG 6とを接触させ、イミノ基とエポキシ基との反応により、ペニシリンG 6を、架橋剤が表面に固定されたアミノ化マグネタイト微粒子7の表面に結合させ、磁気感応性薬剤10を製造する(図1)。
架橋剤が表面に固定されたアミノ化マグネタイト微粒子7とペニシリンG 6とを溶媒中で加熱すると、ペニシリンG 6がβラクタム環上に有するアミド窒素とエポキシ基との間で、下式(化7)のような反応が起こり、共有結合を形成する。
【0089】
【化7】

【0090】
溶媒としては、エタノール等のアルコール系溶媒が好ましく、数時間程度加熱環流する。
溶媒に添加する架橋剤が表面に固定されたアミノ化マグネタイト微粒子7とペニシリンG 6とのモル比は、導入するペニシリンG 6の量等に応じて適宜調節される。
【0091】
反応終了後、ろ過により溶媒と分離後、溶媒で洗浄し、未反応物として表面に残った過剰なペニシリンG 6を除去すると、磁気感応性薬剤10が得られる。
洗浄溶媒としては、工程Aと同様の洗浄溶媒を用いることができる。
【0092】
本実施の形態においては、薬剤としてペニシリンGを用いたが、アミノ基、イミノ基、水酸基およびチオール基のいずれか1を有し、エポキシ基との反応条件化で分解しない任意の薬剤を用いることができる。例えば、他の抗生物質としては、セファレキシン等が挙げられる。その他にも、タンパク質、アミノ酸、酵素、抗体、ペプチド、抗菌物質、あるいは磁気画像診断用以外の造影剤等を薬剤として用いることができる。
【0093】
薬剤以外の機能物質を同様の方法により磁性を有する微粒子の表面に固定すると、磁気感応性物質が得られる。例えば、機能物質として触媒を用いると、触媒反応終了後、磁石等の磁気発生手段により反応系から容易に回収することができる磁気感応触媒が得られる。
また、特定の生理活性物質に対する親和性を有する抗体やリガンド等を機能物質として用いると、該生理活性物質を含む混合物から、磁石等の磁気発生手段により結合した生理活性物質を分離することができる磁気感応アフィニティ担体が得られる。
あるいは、EDTA、クラウンエーテル、カリックスアレーン、シクロデキストリン等のホスト化合物を機能物質として用いると、混合物から金属イオン、有機化合物等の分離または回収が可能な磁気感応性物質が得られる。
【実施例】
【0094】
以下、本発明の効果を確認するために行った実施例について説明するが、本願発明は、これら実施例によって何ら制限されるものではない。
【0095】
(1)アミノ化マグネタイト微粒子の調製
粒径が数十ナノメートルの無水のマグネタイト微粒子を用意し、よく乾燥した。
3−アミノプロピルトリメトキシシラン(化8)0.99重量部、および酢酸(縮合触媒)0.01重量部を秤量し、これを100重量部のヘキサメチルジシロキサン−ジメチルホルムアミド混合溶媒(1:1v/v)に溶解し、反応液を調製した。
【0096】
【化8】

【0097】
この反応液に乾燥したマグネタイト微粒子を加え、室温の空気中(相対湿度45%)で2時間程度撹拌して反応させた。その後、トリクレンで洗浄し、過剰なアルコキシシラン化合物を除去した。
【0098】
【化2】

【0099】
(2)架橋剤が表面に固定されたアミノ化マグネタイト微粒子の調製
アミノ化マグネタイト微粒子、およびエチレングリコールジグリシジルエーテルをエタノール中で加熱環流した。室温まで放冷後、ろ過し、ろ過物をエタノールで洗浄し、過剰なエチレングリコールジグリシジルエーテルを除去した。
【0100】
(2)磁気感応性薬剤の調製
架橋剤が表面に固定されたアミノ化マグネタイト微粒子の調製、およびペニシリンGをエタノール中で加熱環流した。室温まで放冷後、ろ過し、ろ過物をエタノールで洗浄し、過剰なペニシリンGを除去した。
得られた磁気感応性薬剤は、粒径がたかだか数十ナノメートルなので、純水に分散して血管注射しても、血管が詰まることはない。さらに、この薬剤は、磁石に引き寄せられる機能を持っているため、患部近傍に磁石を設置しておくと血液が一定時間体内を循環する間に磁力で薬剤を患部に集中できる。
したがってトータルの投与鑓が極めて少なくても、患部近傍のみペニシリンGを高濃度にできるため副作用を低減でき、効率の良い治療が可能となった。
【図面の簡単な説明】
【0101】
【図1】本発明の一実施の形態に係る、ペニシリンGが結合固定された磁気感応性薬剤の構造を模式的に表した説明図である。
【図2】(a)は反応前のマグネタイト微粒子表面の構造を模式的に表した説明図、(b)は、エポキシ化マグネタイト微粒子の構造を模式的に表した説明図、(c)は、架橋剤が結合したエポキシ化マグネタイト微粒子の構造を模式的に示す説明図である。
【符号の説明】
【0102】
1:マグネタイト微粒子、2:水酸基、3:アミノ基を有する膜化合物の単分子膜、4:アミノ化マグネタイト微粒子、5:架橋剤、6:ペニシリンG、7:架橋剤が表面に固定されたアミノ化マグネタイト微粒子、10:磁気感応性薬剤
【特許請求の範囲】
【請求項1】
磁性を有する微粒子に機能物質が結合した磁気感応性物質であって、
前記微粒子の表面は、分子の両端に第1および第2の官能基を有する膜化合物の形成する薄膜によって被覆されており、
前記膜化合物は、前記第1の官能基と前記微粒子の表面との反応により形成された共有結合を介して前記微粒子の表面に固定されており、
前記薄膜の表面には、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記機能物質の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤が、前記第2の官能基と前記第1の架橋反応基との反応により形成された共有結合を介して結合しており、
前記機能物質の官能基と前記第2の架橋官能基との反応により形成された結合を介して、前記機能物質が前記微粒子に結合していることを特徴とする磁気感応性物質。
【請求項2】
請求項1記載の磁気感応性物質において、前記膜化合物の形成する薄膜が単分子膜であることを特徴とする磁気感応性物質。
【請求項3】
請求項1および2のいずれか1項に記載の磁気感応性物質において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であることを特徴とする磁気感応性物質。
【請求項4】
磁性を有する微粒子に薬剤が結合した磁気感応性薬剤であって、
前記微粒子の表面は、分子の両端に第1および第2の官能基を有する膜化合物の形成する薄膜によって被覆されており、
前記膜化合物は、前記第1の官能基と前記微粒子の表面との反応により形成された共有結合を介して前記微粒子の表面に固定されており、
前記薄膜の表面には、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記薬剤の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤が、前記第2の官能基と前記第1の架橋反応基との反応により形成された共有結合を介して結合しており、
前記薬剤の官能基と前記第2の架橋官能基との反応により形成された結合を介して、前記薬剤が前記微粒子に結合していることを特徴とする磁気感応性薬剤。
【請求項5】
請求項4記載の磁気官能性薬剤において、前記薬剤が、アミノ基、イミノ基、水酸基、およびチオール基のいずれか1を含むタンパク質、アミノ酸、酵素、抗体、抗生物質、抗菌物質、および造影剤のいずれか1であることを特徴とする磁気官能性薬剤。
【請求項6】
請求項4および5のいずれか1項に記載の磁気感応性薬剤において、前記膜化合物の形成する薄膜が単分子膜であることを特徴とする磁気感応性薬剤。
【請求項7】
請求項4〜6のいずれか1項に記載の磁気感応性薬剤において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であることを特徴とする磁気感応性薬剤。
【請求項8】
請求項4〜7のいずれか1項に記載の磁気感応性薬剤において、前記薬剤の有する前記官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ前記第2の架橋反応基は、アルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であることを特徴とする磁気感応性薬剤。
【請求項9】
磁性を有する微粒子に機能物質が結合した磁気感応性物質の製造方法であって、
分子の両端にそれぞれ第1および第2の官能基を有する膜化合物を含む溶液を前記微粒子の表面に接触させ、前記第1の官能基と前記微粒子の表面との間で結合を形成させ、前記膜化合物の形成する薄膜で前記微粒子の表面が被覆された反応性微粒子を調製する工程Aと、
前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記機能物質の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤を、前記反応性微粒子の表面に接触させ、前記第2の官能基と前記第1の架橋反応基との反応により共有結合を形成させ、前記架橋剤を前記反応性微粒子の表面に固定する工程Bと、
前記架橋剤が固定された反応性微粒子の表面に前記機能物質を接触させ、前記機能物質の官能基と前記第2の架橋反応基との反応により結合を形成させ、前記機能物質を前記架橋剤が固定された反応性微粒子に結合させる工程Cとを有することを特徴とする磁気感応性物質の製造方法。
【請求項10】
請求項9記載の磁気感応性物質の製造方法において、前記工程Aにおける結合の形成後に、未反応の前記膜化合物を除去することを特徴とする磁気感応性物質の製造方法。
【請求項11】
請求項9および10のいずれか1項に記載の磁気感応性物質の製造方法において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であることを特徴とする磁気感応性物質の製造方法。
【請求項12】
請求項11記載の磁気感応性物質の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含むことを特徴とする磁気感応性物質の製造方法。
【請求項13】
請求項11記載の磁気感応性物質の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含むことを特徴とする磁気感応性物質の製造方法。
【請求項14】
請求項13記載の磁気感応性物質の製造方法において、さらに助触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含むことを特徴とする磁気感応性物質の製造方法。
【請求項15】
磁性を有する微粒子に薬剤が結合した磁気感応性薬剤の製造方法であって、
分子の両端にそれぞれ第1および第2の官能基を有する膜化合物を含む溶液を前記微粒子の表面に接触させ、前記第1の官能基と前記微粒子の表面との間で結合を形成させ、前記膜化合物の形成する薄膜で前記微粒子の表面が被覆された反応性微粒子を調製する工程Aと、
前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記薬剤の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤を、前記反応性微粒子の表面に接触させ、前記第2の官能基と前記第1の架橋反応基との反応により共有結合を形成させ、前記架橋剤を前記反応性微粒子の表面に固定する工程Bと、
前記架橋剤が固定された反応性微粒子の表面に前記薬剤を接触させ、前記薬剤の官能基と前記第2の架橋反応基との反応により結合を形成させ、前記薬剤を前記架橋剤が固定された反応性微粒子に結合させる工程Cとを有することを特徴とする磁気感応性薬剤の製造方法。
【請求項16】
請求項15記載の磁気感応性物質の製造方法において、前記工程Aにおける結合の形成後に、未反応の前記膜化合物を除去することを特徴とする磁気感応性薬剤の製造方法。
【請求項17】
請求項15および16のいずれか1項に記載の磁気感応性薬剤の製造方法において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であることを特徴とする磁気感応性薬剤の製造方法。
【請求項18】
請求項15〜17のいずれか1項に記載の磁気感応性薬剤の製造方法において、前記薬剤の有する前記官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ前記第2の架橋反応基は、アルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であることを特徴とする磁気感応性薬剤の製造方法。
【請求項19】
請求項18記載の磁気感応性薬剤の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含むことを特徴とする磁気感応性薬剤の製造方法。
【請求項20】
請求項18記載の磁気感応性薬剤の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含むことを特徴とする磁気感応性薬剤の製造方法。
【請求項21】
請求項20記載の磁気感応性薬剤の製造方法において、さらに助触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含むことを特徴とする磁気感応性薬剤の製造方法。
【請求項1】
磁性を有する微粒子に機能物質が結合した磁気感応性物質であって、
前記微粒子の表面は、分子の両端に第1および第2の官能基を有する膜化合物の形成する薄膜によって被覆されており、
前記膜化合物は、前記第1の官能基と前記微粒子の表面との反応により形成された共有結合を介して前記微粒子の表面に固定されており、
前記薄膜の表面には、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記機能物質の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤が、前記第2の官能基と前記第1の架橋反応基との反応により形成された共有結合を介して結合しており、
前記機能物質の官能基と前記第2の架橋官能基との反応により形成された結合を介して、前記機能物質が前記微粒子に結合していることを特徴とする磁気感応性物質。
【請求項2】
請求項1記載の磁気感応性物質において、前記膜化合物の形成する薄膜が単分子膜であることを特徴とする磁気感応性物質。
【請求項3】
請求項1および2のいずれか1項に記載の磁気感応性物質において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であることを特徴とする磁気感応性物質。
【請求項4】
磁性を有する微粒子に薬剤が結合した磁気感応性薬剤であって、
前記微粒子の表面は、分子の両端に第1および第2の官能基を有する膜化合物の形成する薄膜によって被覆されており、
前記膜化合物は、前記第1の官能基と前記微粒子の表面との反応により形成された共有結合を介して前記微粒子の表面に固定されており、
前記薄膜の表面には、前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記薬剤の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤が、前記第2の官能基と前記第1の架橋反応基との反応により形成された共有結合を介して結合しており、
前記薬剤の官能基と前記第2の架橋官能基との反応により形成された結合を介して、前記薬剤が前記微粒子に結合していることを特徴とする磁気感応性薬剤。
【請求項5】
請求項4記載の磁気官能性薬剤において、前記薬剤が、アミノ基、イミノ基、水酸基、およびチオール基のいずれか1を含むタンパク質、アミノ酸、酵素、抗体、抗生物質、抗菌物質、および造影剤のいずれか1であることを特徴とする磁気官能性薬剤。
【請求項6】
請求項4および5のいずれか1項に記載の磁気感応性薬剤において、前記膜化合物の形成する薄膜が単分子膜であることを特徴とする磁気感応性薬剤。
【請求項7】
請求項4〜6のいずれか1項に記載の磁気感応性薬剤において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であることを特徴とする磁気感応性薬剤。
【請求項8】
請求項4〜7のいずれか1項に記載の磁気感応性薬剤において、前記薬剤の有する前記官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ前記第2の架橋反応基は、アルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であることを特徴とする磁気感応性薬剤。
【請求項9】
磁性を有する微粒子に機能物質が結合した磁気感応性物質の製造方法であって、
分子の両端にそれぞれ第1および第2の官能基を有する膜化合物を含む溶液を前記微粒子の表面に接触させ、前記第1の官能基と前記微粒子の表面との間で結合を形成させ、前記膜化合物の形成する薄膜で前記微粒子の表面が被覆された反応性微粒子を調製する工程Aと、
前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記機能物質の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤を、前記反応性微粒子の表面に接触させ、前記第2の官能基と前記第1の架橋反応基との反応により共有結合を形成させ、前記架橋剤を前記反応性微粒子の表面に固定する工程Bと、
前記架橋剤が固定された反応性微粒子の表面に前記機能物質を接触させ、前記機能物質の官能基と前記第2の架橋反応基との反応により結合を形成させ、前記機能物質を前記架橋剤が固定された反応性微粒子に結合させる工程Cとを有することを特徴とする磁気感応性物質の製造方法。
【請求項10】
請求項9記載の磁気感応性物質の製造方法において、前記工程Aにおける結合の形成後に、未反応の前記膜化合物を除去することを特徴とする磁気感応性物質の製造方法。
【請求項11】
請求項9および10のいずれか1項に記載の磁気感応性物質の製造方法において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であることを特徴とする磁気感応性物質の製造方法。
【請求項12】
請求項11記載の磁気感応性物質の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含むことを特徴とする磁気感応性物質の製造方法。
【請求項13】
請求項11記載の磁気感応性物質の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含むことを特徴とする磁気感応性物質の製造方法。
【請求項14】
請求項13記載の磁気感応性物質の製造方法において、さらに助触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含むことを特徴とする磁気感応性物質の製造方法。
【請求項15】
磁性を有する微粒子に薬剤が結合した磁気感応性薬剤の製造方法であって、
分子の両端にそれぞれ第1および第2の官能基を有する膜化合物を含む溶液を前記微粒子の表面に接触させ、前記第1の官能基と前記微粒子の表面との間で結合を形成させ、前記膜化合物の形成する薄膜で前記微粒子の表面が被覆された反応性微粒子を調製する工程Aと、
前記第2の官能基と反応して共有結合を形成する第1の架橋反応基、および前記薬剤の官能基と反応して結合を形成する第2の架橋反応基とを有する架橋剤を、前記反応性微粒子の表面に接触させ、前記第2の官能基と前記第1の架橋反応基との反応により共有結合を形成させ、前記架橋剤を前記反応性微粒子の表面に固定する工程Bと、
前記架橋剤が固定された反応性微粒子の表面に前記薬剤を接触させ、前記薬剤の官能基と前記第2の架橋反応基との反応により結合を形成させ、前記薬剤を前記架橋剤が固定された反応性微粒子に結合させる工程Cとを有することを特徴とする磁気感応性薬剤の製造方法。
【請求項16】
請求項15記載の磁気感応性物質の製造方法において、前記工程Aにおける結合の形成後に、未反応の前記膜化合物を除去することを特徴とする磁気感応性薬剤の製造方法。
【請求項17】
請求項15および16のいずれか1項に記載の磁気感応性薬剤の製造方法において、前記第1の官能基がアルコキシシリル基であり、前記第2の官能基がエポキシ基であり、かつ前記第1の架橋反応基がアミノ基またはイミノ基であることを特徴とする磁気感応性薬剤の製造方法。
【請求項18】
請求項15〜17のいずれか1項に記載の磁気感応性薬剤の製造方法において、前記薬剤の有する前記官能基はアミノ基、イミノ基、水酸基およびチオール基のいずれか1であり、かつ前記第2の架橋反応基は、アルコキシシリル基、エポキシ基、イソシアネート基、およびチオール基のいずれか1であることを特徴とする磁気感応性薬剤の製造方法。
【請求項19】
請求項18記載の磁気感応性薬剤の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、カルボン酸金属塩、カルボン酸エステル金属塩、カルボン酸金属塩ポリマー、カルボン酸金属塩キレート、チタン酸エステル、およびチタン酸エステルキレートからなる群から選択される1または2以上の化合物を含むことを特徴とする磁気感応性薬剤の製造方法。
【請求項20】
請求項18記載の磁気感応性薬剤の製造方法において、前記膜化合物を含む溶液は、さらに縮合触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含むことを特徴とする磁気感応性薬剤の製造方法。
【請求項21】
請求項20記載の磁気感応性薬剤の製造方法において、さらに助触媒として、ケチミン化合物、有機酸、アルジミン化合物、エナミン化合物、オキサゾリジン化合物、およびアミノアルキルアルコキシシラン化合物からなる群より選択される1または2以上の化合物をさらに含むことを特徴とする磁気感応性薬剤の製造方法。
【図1】


【図2】




【図2】


【公開番号】特開2008−222595(P2008−222595A)
【公開日】平成20年9月25日(2008.9.25)
【国際特許分類】
【出願番号】特願2007−60317(P2007−60317)
【出願日】平成19年3月9日(2007.3.9)
【出願人】(304028346)国立大学法人 香川大学 (285)
【出願人】(503027931)学校法人同志社 (346)
【Fターム(参考)】
【公開日】平成20年9月25日(2008.9.25)
【国際特許分類】
【出願日】平成19年3月9日(2007.3.9)
【出願人】(304028346)国立大学法人 香川大学 (285)
【出願人】(503027931)学校法人同志社 (346)
【Fターム(参考)】
[ Back to top ]

