蛍光分析による抗原抗体反応検出方法
【課題】 多項目又は多検体の抗原抗体反応を簡便かつ迅速に検出する方法を提供すること。
【解決手段】 本発明は、互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体を、被検試料溶液に混合し、その溶液中の少なくとも一つの蛍光色素の蛍光強度を測定して、その蛍光強度の時間変化に基づいて、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かを判定する。蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合していると判定された場合、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子と結合し抗原抗体反応を生じたと判定する。また、この方法に適したマイクロプレートが提供される。
【解決手段】 本発明は、互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体を、被検試料溶液に混合し、その溶液中の少なくとも一つの蛍光色素の蛍光強度を測定して、その蛍光強度の時間変化に基づいて、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かを判定する。蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合していると判定された場合、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子と結合し抗原抗体反応を生じたと判定する。また、この方法に適したマイクロプレートが提供される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、抗原抗体反応を検出する方法に係り、より詳細には、一分子蛍光分析技術により抗原抗体反応を検出する方法及びその方法に有利に利用可能なマイクロプレートに係る。
【背景技術】
【0002】
生物科学、医学又は薬学の分野に於いて、周知の如く、抗原抗体反応は、生体内外の種々の生体分子を検出することができるので、従来より、生体内の種々の病気の診断や生理活性物質のスクリーニングに応用されている。例えば、細菌、ウィルス、病原性タンパク質、腫瘍などの種々の疾患の原因物質又はその原因物質に由来する物質に特異的に反応する抗体を用い、その抗体が(生体から得られた体液等に於いて)抗原抗体反応を起こしたか否かを検出することで、生体内に於ける原因物質又はそれに由来する物質の有無が検査される。また、逆に、生体内に上記の如き疾患の原因物質又はそれに由来する物質に対する抗体が存在するか否かを、その抗体に対する抗原(又はエピトープ)により(生体から得られた体液等に於いて)抗原抗体反応が起きたか否かを検出することにより、生体内に疾患の原因物質が存在するか否かを検査する場合もある。更に、アレルギーや自己免疫疾患などの一部の疾患の場合には、生体内に特定の物質(食物、花粉、ハウスダスト、カビ、ダニ等)を抗原とする抗体が存在するか否かが、その特定の物質により(生体から得られた体液等に於いて)抗原抗体反応が起きたか否かを検出することにより検査される。
【0003】
抗原抗体反応の検出方法としては、ELISA法、ウェスタンブロット法といった生化学的な方法が一般的であるが、これらの伝統的な方法は、検出に要する処理操作が多く、時間がかかり、また、多量の試料を要する。そこで、近年、より少量の試料にて且より短時間にて抗原抗体反応の検出を可能にする方法又は装置の開発が進められている。例えば、特許文献1に於いては、表面プラズモン共鳴を利用して抗原抗体反応の検出を行う特殊な測定用チップが提案されている。また、特許文献2に於いては、細胞フローメトリーと蛍光測定とを組み合わせた装置を用いて抗原抗体反応を検出するための特殊な試料などが開示されている。
【0004】
また、近年、光学顕微鏡の光学系を用いた光計測技術の進歩により、一光子又は蛍光一分子の蛍光等の微弱光の検出・測定が可能となってきたことから、そのような微弱光の計測技術を用いて、抗原抗体反応を検出する試みが為されつつある。そのような例として、例えば、特許文献3に於いて、レーザー共焦点顕微鏡の光学系を用いた蛍光相関分光法又は蛍光偏光解析法により抗原抗体反応が検出されることが示されている。かかる方法によれば、測定に必要な試料は、従前に比して極めて低濃度且微量でよく(一回の測定で使用される量は、たかだか数十μl程度)、測定時間も大幅に短縮される(一回の測定は10秒程度)。従って、上記の如き微弱光の計測技術を用いて抗原抗体反応を検出する方法又は装置は、病気の診断や生理活性物質のスクリーニングなど、検体数が多い場合にも、従前に比して、速やかに検査が実行できる強力なツールとなることが期待されている。
【特許文献1】特開2006−250668
【特許文献2】特開2005−098877
【特許文献3】特開2005−337805
【発明の開示】
【発明が解決しようとする課題】
【0005】
ところで、抗原抗体反応の検出方法を疾患又はその原因物質等の有無の診断やその他の抗体又は抗原のスクリーニングに応用する場合、しばしば、検査されるべき試料(被検試料)中に複数の種類の抗体又は抗原(疾患の原因物質又はそれに由来する物質)の存否の確認が望まれる場合がある(例えば、アレルギーの診断など)。例えば、上記の特許文献3に記載の蛍光相関分光法又は蛍光偏光解析法を用いた抗原抗体反応検出法によれば、個々の抗体又は抗原の確認検査は、微量の被検試料にて短時間で済むが、それでも、特に、臨床の現場など、被検試料が多数であり、且、検査されるべき抗体の数が多い場合には、全ての検査を完了するためには、それなりの被検試料量と検査時間を要する。従って、もしそのような多項目又は多検体の抗原抗体反応を確認する必要がある場合であっても、微量の被検試料にて迅速に検査が実行できる方法又は装置があれば有利である。また、抗原抗体反応の検査に於ける準備又は処理操作は、できるだけ簡便であることが望ましい。
【0006】
かくして、本発明の一つの目的は、多項目又は多検体の抗原抗体反応を簡便かつ迅速に検出する方法を提供することである。
【課題を解決するための手段】
【0007】
本発明の一つの態様によれば、本発明の抗原抗体反応を検出する方法は、互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体を、それらの複数の種類の抗原又は抗体のいずれかに対する抗体又は抗原が含まれているか否かが検査される被検試料溶液に混合して混合試料溶液を調製する過程と、混合試料溶液中の少なくとも一つの蛍光色素の蛍光強度を測定する過程と、測定された蛍光強度の時間変化に基づいて、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かを判定する過程とを含み、測定された蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合していると判定された場合には、その蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子と結合し抗原抗体反応を生じたと判定し、その蛍光強度に対応する蛍光色素で標識された抗原又は抗体に対する抗体又は抗原が被検試料溶液中に存在すると判定することを特徴とする。なお、当業者にとって理解される如く、被検試料溶液へ混合される蛍光色素で標識した「複数の種類の抗原又は抗体」が抗原(即ち、任意の生体に於いて抗原となり得る物質)であれば、被検試料溶液中に含まれているか否かが検出される物質は、抗体であり、被検試料溶液へ混合される蛍光色素で標識した「複数の種類の抗原又は抗体」が抗体であれば、被検試料溶液中に含まれているか否かが検出される物質は抗原である。
【0008】
上記の構成によれば、抗原抗体反応の検出が、蛍光色素の蛍光強度を測定し、その蛍光時間の変化に基づいて、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かを判定する蛍光分析により行われるので、ELISA等の伝統的な手法に比べ、被検試料量と処理操作時間が大幅に低減されるだけでなく、被検試料溶液へ互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体を混合するという手法により、検査されるべき項目又は存否が確認されるべき物質が複数在っても、被検試料量は、一回の検査に必要な試料量分のみでよくなる。被検試料溶液へ混合される抗原又は抗体、即ち、被検試料溶液中の物質を探索するための「プローブ」試料は、互いに異なる蛍光色素で標識されるので、個々のプローブ試料が抗原抗体反応を起こすか否かは、それぞれの蛍光色素の蛍光強度を別々に測定する必要があるが(検出する色素の吸収波長又は発光波長特性に応じて蛍光検出装置に於いて励起波長又は受光波長の選択が為される。)、被検試料溶液自体は交換する必要はない。複数の種類の蛍光色素が一波長の励起光で励起できる場合には、蛍光測定装置の光検出器に於いて適宜波長を弁別する装置(フィルター、回折格子等)が用いられてよい。
【0009】
また、上記の構成に於いて、複数の種類の抗原又は抗体に標識された蛍光色素の全てについて各々の蛍光強度を測定し、測定された蛍光強度の各々の時間変化に基づいて、蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かを判定し、蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合していると判定されたときに、蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子と結合し抗原抗体反応を生じたと判定するようになっていてよい。しかしながら、被検試料溶液へ混合された蛍光色素の各々の蛍光強度の測定・分析を順々に行う間に、検出されるべき結果が判明したときには、全ての色素の蛍光測定を行わなくてもよいことは理解されるべきである。なお、使用する蛍光測定装置において、複数の種類の互いに吸収・発光波長特性の異なる蛍光色素の励起及び蛍光の検出が同時にできるときには、蛍光色素の蛍光測定は、同時に実行されてよく、その場合、更に測定時間が短縮される。
【0010】
上記の本発明の方法に於いては、蛍光強度の測定は、蛍光一分子からの蛍光を測定し、その時間変化又は揺らぎを解析して蛍光一分子の状態又は運動を観測する蛍光分析法(一分子蛍光分析技術)により為される。例えば、蛍光強度の測定は「蛍光相関分光法」により行われてよく、その場合には、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かは、蛍光強度の時間変化に基づいて蛍光相関分光法により算出された並進拡散時間に基づいて判定されてよい。また、蛍光強度の測定は「蛍光強度分布解析法」により行われてよく、その場合には、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かが、蛍光強度の時間変化に基づいて蛍光強度分布解析法により算出された一蛍光発光体当たりの蛍光強度に基づいて判定されてよい(この場合、後述の如く、複数の種類の蛍光標識された抗原又は抗体が被検試料溶液中の一つの分子に同時に結合している必要がある。「一蛍光発光体」とは、蛍光一分子ではなく、溶液中で一体的に運動する蛍光を発する物体を意味する。)また、蛍光強度の測定が「蛍光偏光解消法」により行われてよく、その場合には、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かが蛍光強度の時間変化に基づいて蛍光偏光解消法により算出された蛍光偏光度により判定されてよい(この場合、一分子蛍光分析を実行する装置ではなく、通常の蛍光偏光解消測定装置であってもよい。)。
【0011】
上記の本発明は、特に疾患又はその原因物質等の有無の診断やその他の抗体のスクリーニングなど、検査されるべき抗原抗体反応が複数ある場合に有利に用いられる。従って、例えば、本発明の抗原抗体検出方法が食物によるアレルギー性疾患の診断に使用される場合には、本発明に於いて使用されるプローブ試料(互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体)は、抗原抗体反応が発生した場合に抗原となる食物に含まれるタンパク質であってよい。また、プローブ試料は、アレルギー性疾患患者の体液中に含まれる抗体に対する抗原であってもよい。これらの場合、本発明によれば、複数の食物若しくはその中に含まれるタンパク質又はその他のアレルゲンのうち、いずれのものがアレルギー反応を示す原因となっているかを迅速に且複数のものについて、同時に検査・診断することが可能となる。更に、プローブ試料は、自己免疫疾患患者の体液中に含まれる抗体に対する抗原であってもよく、これにより、自己免疫疾患の種類の特定を迅速に実施できることとなる。本発明を上記の如き、疾患の検査・診断に用いる場合には、被検試料溶液が血清又は血漿又はその他の生体から得られた体液試料が用いられてよい。理解されるべきことは、この場合、本発明の特徴によれば、複数の疾患に関わる抗原又は抗体の存否を検査するために必要な被検試料溶液となる体液試料は、微量でよいということである。なお、被検試料溶液が、血清など自家蛍光を持つ可能性がある場合には、自家蛍光が測定に乗らないように、できる限り長波長、短くとも540nm以上で励起できる蛍光色素を使用することが好ましい。
【0012】
上記の方法を実施するに当たり、蛍光測定は、複数のウェルを有し抗原抗体反応を蛍光測定分析により検出するのに適したマイクロプレートであって、複数のウェルの各々に予め少なくとも一つの蛍光標識された抗原又は抗体が分注されていることを特徴とするマイクロプレートにより有利に実行することができる。かかるマイクロプレートの態様に於いて、予め互いに異なる蛍光色素にて標識された複数の種類の抗原又は抗体が同一のウェルに分注されていてよい。即ち、複数のウェルのそれぞれに、互いに異なる蛍光色素にて標識された複数の種類の抗原又は抗体から成るプローブ試料が分注される。この場合、複数の被検試料溶液を別々のウェルに分注することにより、系統的に多数の被検試料溶液について、複数の種類の抗原抗体反応の検出が可能となる。また、マイクロプレートのもう一つの態様に於いて、複数のウェルに別々の予め互いに異なる蛍光色素にて標識された複数の種類の抗原又は抗体が分注されていてよい。この場合、一つの被検試料溶液を別々の抗原又は抗体が分注されたウェルに分注することにより、一つの被検試料溶液について多種類の抗原抗体反応の確認が為される。いずれの場合に於いても、一枚のプレートで多数の検査が実施されることとなるので、蛍光測定分析装置に於いて被検試料溶液を変更する操作が一段と簡単化される。かかる特徴は、疾患又はその原因物質等の有無の診断やその他の抗体又は生理活性物質等のスクリーニングを行う際、非常に有利である。
【0013】
なお、上記のマイクロプレートは、複数のウェルに分注された蛍光標識抗原又は抗体を乾燥させた状態に保持されていてよい。これにより、プローブ試料の長期保存が可能となり、蛍光標識抗原又は抗体を検査の度に調製する必要がなくなる。使用者は、検査の実行に当たり、単に被検試料溶液をウェルに添加するだけで、蛍光測定・分析を行うことができ、非常に便利である。被検試料溶液が血清など自家蛍光を持つ可能性がある場合には、540nm以上で励起できる蛍光色素を使用することが好ましい。
【発明の効果】
【0014】
本発明によれば、上記の説明から理解される如く、蛍光測定分析、特に、一分子蛍光測定分析を用いて、多種類の抗原抗体反応の検出が、微量の被検試料にて迅速に実行できる。従前の多種類の抗原抗体反応の検出方法に於いては、抗原抗体反応の種類を識別するために、マイクロビーズや基板等に抗原又は抗体を固定するなどの処理が必要であった。しかしながら、本発明によれば、多種類の抗原抗体反応の区別は、蛍光色素の波長によりなされるので、試料の蛍光標識操作が必要とはなるものの、蛍光測定及び分析するための試料標本である混合試料溶液の調製操作は、被検試料溶液とプローブ試料とを殆どそのまま混合するだけでよく、従って、試料の固定等の操作に於ける試料の損失はなく、また、プローブ試料を基板等に固定する必要がないことから、試料の変性の可能性も低減され、測定結果の信頼性も高くなる。
【0015】
かくして、本発明の方法は、病気又は各種疾患の診断や生理活性物質のスクリーニングなど、検体数が多い場合にも、微量な試料にて且短時間にて、そして、高い信頼性にて、検査が実行できる多種類の抗原抗体反応検出及び識別方法としての利用が期待される。
【0016】
本発明のその他の目的及び利点は、以下の本発明の好ましい実施形態の説明により明らかになるであろう。
【発明を実施するための最良の形態】
【0017】
以下に添付の図を参照しつつ、本発明を幾つかの好ましい実施形態について詳細に説明する。
【0018】
抗原抗体反応の検出の手順
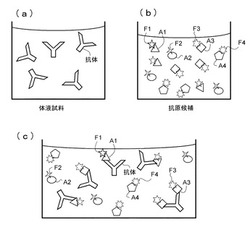
図1は、抗原抗体反応により、例えば、血清、血漿、尿、鼻汁、涙液、糞便、組織抽出液などの生体から得られた体液試料又は培養液等の被検試料溶液中に含まれている抗体を検出する本発明の方法の好ましい実施形態に於ける処理過程に於ける試料中の分子の状態を示す模式図である。
【0019】
同図を参照して、図1(a)に示されている如く、例えば、或る疾患の患者の体液試料中には、その疾患に罹患すると、その原因物質(細菌、ウイルス、病原性タンパク質、腫瘍)又はそれに由来する物質に対する抗体が含有される。また、アレルギー性疾患の場合であれば、患者の体液試料中には、そのアレルギー性疾患に特有の(食物、花粉、ハウスダスト、カビ、ダニ等のアレルゲンに対する)抗体が含まれる。或いは、任意の培養細胞からも抗体が産生される。疾患の種類は、それらの抗体と特異的に結合する、即ち、抗原抗体反応を引き起こす物質を特定することにより特定される。しかしながら、疾患の種類が特定されるまでは、いずれの物質と抗原抗体反応を起こすか(又は抗原抗体反応自体を起こすか否か)は分からず、従って、複数の種類の物質について抗原抗体反応を起こすか否かを検査することが必要な場合がある。そこで、本実施形態では、抗体検出のためのプローブ試料として、被検試料溶液中の存否が確認されるべき抗体の候補に対応する複数の種類の抗原候補A1−A4にそれぞれ別々の蛍光色素F1−F4を付加したもの(蛍光標識したもの)をプローブ試料として調製し(図1(b))、これらを体液試料と混合する。
【0020】
存否が確認されるべき抗体の候補に対応する複数の種類の抗原候補は、当業者にとって任意の生理活性物質、例えば、タンパク質、核酸、脂質、糖類その他の生体分子等又は化学物質であってよい。これらの抗原候補の蛍光標識は、抗原候補となる物質の種類及び特性に応じて当業者にとって任意の手法により為されてよい。例えば、タンパク質であれば、蛍光標識は、タンパク質中の特定の基を標的にしたケミカルラベリング法により為されてよい。また、その他の物質については、任意の方法で蛍光標識された物質が化学合成されてもよい。蛍光色素としては、この分野で通常使われる任意の蛍光色素、例えば、TAMRA(carboxymethylrhodamine)、TMR(tetramethylrhodamine)、Alexa647、Rhodamine
Green、Alexa488などであってよいが、これらに限定されない。重要なことは、一つの被検試料溶液へ混合される複数種の抗原候補の物質に付加される蛍光色素の発光波長のスペクトルが異なり、これらの蛍光の各々が、後述の蛍光測定の際、受光波長の選択により識別できる態様になっている必要がある。なお、受光波長に於いて識別できない場合、励起波長で識別できればよい(ただし、蛍光測定装置の光源に於いて、それぞれの励起波長の励起光を供給できるようになっている必要がある。)。
【0021】
かくして、抗原候補A1−A4は、被検試料溶液に混合されると(図1(c))、もし対応する抗体が存在する場合には、抗体に特異的に結合する(抗原抗体反応。A1、A3)。一方、特異的に結合できる抗体が存在しない場合には、抗原候補は、溶液中に単独で浮遊することとなる(A2、A4)。従って、抗体に結合した抗原の色素F1、F3と抗体に結合していない色素F2、F4とでは、溶液中のブラウン運動の態様が異なることとなる。かかる運動性の違いは、蛍光色素F1−F4の蛍光強度の時間変化(揺らぎ)に反映されるので、抗原候補が抗体に結合したか否かが蛍光強度の時間変化に基づいて判定できることとなる。
【0022】
蛍光測定は、典型的には、1分子蛍光分析システム MF20(オリンパス)が用いられてよい。かかるシステムに於いては、蛍光相関分光法、蛍光偏光解消法、蛍光強度分布解析法のいずれかにより、蛍光色素Fの運動状態が判定される。以下、各分析方法に於いて、抗原候補が抗体に結合しているか否かが計測結果に如何に反映されるかについて説明する。
【0023】
蛍光相関分光法では、微小の蛍光観察領域をブラウン運動により通過する分子の移動(並進運動)の速さが観測される。分子の並進運動の速さは、測定された蛍光強度の時間を変数とした自己相関関数の形状に反映される。分子の並進運動の速さの指標としては、測定開始時から自己相関関数の値が半分になるまでの時間の長さ(並進拡散時間)が用いられる。分子の移動は、分子の大きさが大きいほど、遅くなるので、並進拡散時間が長くなる。本発明の場合、図1(c)のA1、A3の如く、抗原が抗体に結合すると、蛍光色素Fは、抗原及び抗体と一体的に運動し、従って、図1(c)のA2、A4に比して、蛍光色素Fの運動の速さが顕著に低減し、並進拡散時間が長くなる。従って、並進拡散時間により、或る抗原について、抗原抗体反応が起きた否かが分かり、抗原A1、A3に対する抗体が被検試料溶液中に存在することが確認される。
【0024】
蛍光偏光解消法では、この分野に於いて知られている如く、分子の回転ブラウン運動(自転)の速さが観測される。分子の回転運動の速さは、測定された蛍光の縦偏光と横偏光の強度の割合又は偏光度に反映される。分子の回転は、分子の大きさが大きいほど、遅くなるので、偏光度が大きくなる。本発明の場合、抗体に結合した抗原上の蛍光色素の回転ブラウン運動は遅くなるので、偏光度が大きくなり、これにより、或る抗原について、抗原抗体反応が起きた否かが分かり、抗原A1、A3に対する抗体が被検試料溶液中に存在することが確認される。
【0025】
蛍光強度分布解析法では、微小の蛍光観察領域内から発せられる光子の検出(フォトンカウンティング)を行い、単位時間当たりの光子が検出された頻度を統計的に処理することによって、微小の蛍光観察領域内の蛍光発光体の数密度と、一蛍光発光体当たりの蛍光強度が算出される。本発明の場合、抗原A3の如く、蛍光標識された抗原が一つの抗体に複数結合すると、結合前各々が一つの蛍光発光体として独立に運動していた個々の蛍光色素分子は、抗体に拘束され一つの蛍光発光体として運動することになるので、蛍光発光体の数密度が低減する一方、抗体に複数の蛍光色素分子が存在することにより一蛍光発光体当たりの蛍光強度が増大する。かくして、抗原A3については、蛍光発光体の数密度の低減と一蛍光発光体当たりの蛍光強度の増大から抗原抗体反応が起きたことが検出される。抗体に一つしか結合しない抗原A1の場合であっても、もし抗原A1の蛍光色素の蛍光強度が抗体に結合することにより変化する場合には、そのことにより、結合の有無が検出できる可能性がある。
【0026】
実際の測定では、一つの被検試料溶液について、蛍光色素F1−F4の蛍光が識別できる態様にて、蛍光強度が測定され、その時間変化が解析される。波長の弁別は、蛍光の光検出器の受光面までの光路にハイパスフィルター又はバンドパスフィルターを挿入するか或いは回折格子等を用いて特定の波長の光のみ光検出器に受光されるようになっていてよい。かかる波長弁別の構成は、当業者にとって任意の構成によりなされてよい。また、種々の波長の光で色素を励起し、色素の吸収(励起)波長特性の違いにより複数の種類の色素の蛍光を識別してもよい。
【0027】
かくして、蛍光測定・分析による蛍光色素の運動状態から抗原候補が抗体に結合しているか否かが判定され、即ち、抗原抗体反応の有無が検出される。なお、上記の方法に於いて、抗原候補と被検試料溶液を混合した段階でのみ蛍光測定・分析を実行しても、その結果の数値から蛍光色素が抗体と一体的に運動しているか否かを推定することができるが、抗原候補を被検試料溶液と混合する前の段階で、比較のために蛍光測定・解析を実行してもよい。また、上記の実施形態に於いては、被検試料が抗体であり、プローブ試料が抗原であったが、被検試料が抗原であり、プローブ試料が抗体であってもよい。ただし、その場合、抗原抗体反応により、プローブ試料である抗体の運動状態が顕著に変化するほど大きな抗原である必要がある。
【0028】
抗原抗体反応検出用マイクロプレート
ところで、上記の蛍光測定・分析に於いて、図2(A)に模式的に示されているマイクロプレートを用いると、より効率的に種々の被検試料溶液についての測定・分析を行うことができる。同図を参照して、本発明に有利に使用されるマイクロプレート10は、上面が開孔した複数のウェル12と、ガラス又は光を透過するプラスチック等のプレートの底面部材14とを有する。マイクロプレートの全体の寸法は、平面に於いて約10cm程度であり、一つのウェルの容量は、100μl程度であり、測定に於いては、数十μl程度の試料が注入される。マイクロプレートが蛍光測定装置に配置されると、図2(B)に示されている如く、装置の励起光は、底面を透過して、ウェル内で集光され、そこで、励起された色素の蛍光は、底面を透過して、光検出器(図示せず)へ導かれる。
【0029】
本発明に於いて、蛍光測定の際にマイクロプレートを使用する場合、マイクロプレートの各ウェルには、それぞれ別の被検試料溶液が注入されてよい。また、好適には、予め検出されるべき抗体の種類が特定されている場合、例えば、自己免疫疾患或いはアレルギー性疾患の患者の体液試料中の抗体を検出することが目的とされる場合には、測定に先立って、蛍光標識された抗原候補を各ウェルへ分注した状態に調製される。
【0030】
かかるマイクロプレートの抗原候補の分注の一つの態様としては、複数のウェルの各々に互いに異なる蛍光色素にて標識された複数の種類の抗原候補が予め分注される(図2(C))。この場合、各ウェルへそれぞれ異なる被検試料溶液が注入され、一つのマイクロプレートで多数の被検試料溶液の検査が実行できることとなる。また、別の態様としては、複数のウェルの各々に別々の種類の抗原候補が分注されてもよい。それぞれのウェルについては、一種類の抗原候補が分注されてもよいが(図2(D))、複数の種類の抗原候補が分注されてもよい図2(E)。一度の蛍光測定に於いて同じ溶液で識別可能な蛍光色素の数は、色素の発光波長の範囲(のスペクトル)の幅によって制限される(発光波長のスペクトルの重なりが大きい色素同士は、同じ溶液中で計測は困難である。)。従って、或る一つの被検試料溶液に於いて、同一の溶液中で利用可能な色素の種類を越える数の抗原抗体反応を検出したいときは、複数のウェルのそれぞれに別々の抗原候補又は別々の抗原候補の組み合わせを分注するようになっていてよい。
【0031】
そのような予め抗原候補を分注したマイクロプレートを準備しておけば、検査の度に抗原候補を調製する必要がなく便利である。また、抗原候補が、乾燥しても抗原としての活性を失わない場合には、各ウェルへ複数の種類の抗原候補(例えば、良く使用する抗原候補)を分注した後、乾燥され、保存できるようになっていてよい。
【0032】
かかるマイクロプレートの調製は、例えば、以下の如く為されてよい(図2(F))。
1.反応を検出したい抗原を蛍光標識し精製する。
2.マイクロプレートの各ウェルに10nMの蛍光標識された抗原を5μlずつ入れ、自然乾燥、滅圧乾燥又は凍結乾燥などにより乾燥する。
なお、抗原候補が分注されたマイクロプレートを長期保存する場合には、抗原候補及び蛍光色素の変性を回避するべく遮光冷蔵保存される。使用時には室温に戻され、各ウェルに被検試料溶液を注入し、適当な反応時間の後、蛍光測定が行われる。
【0033】
上記に説明した本発明の有効性を検証するために、以下の実験を行った。なお、以下の実施例は、本発明の有効性を例示するものであって、本発明の範囲を限定するものではないことは理解されるべきである。
【実施例1】
【0034】
抗原抗体反応の典型的な例であるアレルギー性疾患に関与する二つの抗原抗体反応が、本発明の方法により一つの被検試料溶液に於いて検出されることを確認した。アレルギー性疾患とは、端的に述べれば、体内に入ってきた抗原(アレルゲン)がマスト細胞の表面にあるIgE抗体と結合することによって、マスト細胞からヒスタミンなどの化学伝達物質が放出され、これらの化学伝達物質の作用によって現れる症状である。或る物質に対してアレルギー症状を起こす患者は、その物質を抗原とする抗体を有している。従って、そのような患者の体液中に如何なる物質に対する抗体が存在するかを検出できれば、アレルゲンが特定され、アレルギーの予防や治療のために非常に有用な情報となる。下記の実験では、そのようなアレルギー性疾患のうち、食物アレルギー症状を引き起こすことが知られている卵白に含まれるオボアルブミンと、牛乳に含まれるβラクトグロブリンの2種類を蛍光標識し、それぞれを抗原とする抗原抗体反応を検出する実験を行った。
【0035】
測定の処理操作は、以下の通りとした。
1.オボアルブミン(製造元MP Biomedicals,Inc.)は、TAMRA NHS−ester(オリンパス)を用いて、βラクトグロブリン(製造元ICN BIOMEDICALS)は、ATTO633 NHS−ester(ATTO-TEC)を用いて、それぞれ蛍光標識し精製した。TAMRA[5-(and-6)-Carboxytetramethylrhodamine]の吸収・蛍光波長のピークは、それぞれ541nm及び565nmであり、ATTO633の吸収・蛍光波長のピークは、それぞれ629nm及び657nmである。
2.かくして蛍光標識された抗原をリン酸バッファ+0.05%Tween20中に溶解し、両方の抗原を含むプローブ溶液を、それぞれの抗原の終濃度数nMとなるように調製した。そこへ、抗オボアルブミン抗体(製造元MP Biomedicals,Inc.)のみ、抗βラクトグロブリン抗体(製造元BETHYL LABORATORIES)のみ、両方の抗体を含む溶液(被検試料溶液)をそれぞれ混合し、合計の溶液量が50μLとなるよう調製し、37℃で30分間放置した。なお、対照用として、プローブ溶液へ抗体を含まない溶液を混合したものも用意した。
3.かくして調製した(対照用を含む)4種類の被検溶液について、1分子蛍光分析システムMF20(オリンパス)を使用し、蛍光相関分光法により蛍光分子の並進拡散時間を測定した。測定では、(i)波長543nmで励起した場合、(ii)波長633nmで励起した場合及び(iii)波長543nmと波長633nmとの二重励起した場合の三通りにて行った。測定時の光検出器で受光させた波長範囲は以下の通りである。
(i)励起波長543nmのとき …560−620nm
(ii)励起波長633nmのとき …660−710nm
(iii)励起波長543nm及び633nm(二重励起)…565−595nm及び650−690nm
なお、(iii)の場合、光検出器を二つ用い、その一方に565−595nmの範囲の波長の光、他方に650−690nmの範囲の波長の光が入射されるようにした。レーザー強度は、100μWとし、一つの試料につき、10秒間計測を5回ずつ行い、各々について、MF20に準備された蛍光相関分光分析法用のプログラムにより、蛍光強度の自己相関関数を演算し、並進拡散時間の平均を算出した。
【0036】
図3は、上記(i)−(iii)のそれぞれの場合に於ける4種類の被検溶液の並進拡散時間の結果をグラフで示したものである。同図を参照して、並進拡散時間は、(i)励起波長543nmのときの蛍光強度(図3(A))及び(iii)の受光波長が565−595nmの光検出器の蛍光強度(図3(C))から測定・算出されたものについては、抗オボアルブミン抗体のみ含む溶液、両方の抗体を含む溶液に於いてのみ増大し、(ii)励起波長633nmのときの蛍光強度(図3(C))及び(iii)の受光波長が650−690nmの光検出器の蛍光強度(図3(D))から測定・算出されたものについては、抗βラクトグロブリン抗体のみ含む溶液、両方の抗体を含む溶液に於いてのみ増大した。オボアルブミンに付加された蛍光色素TAMRAは、発光波長(のピーク)が565nmであり、βラクトグロブリンに付加された蛍光色素ATTO633の発光波長(のピーク)が657nmであることから、図3(A)及び(C)の結果は、オボアルブミン分子の運動状態を表しているものであると考えられ、抗オボアルブミン抗体の存在下では、その他の抗体が存在していても、オボアルブミン分子は、抗オボアルブミン抗体と結合することを示している。また、同様に、図3(B)及び(D)の結果は、βラクトグロブリン分子の運動状態を表しているものであると考えられ、抗βラクトグロブリン抗体の存在下では、その他の抗体が存在していても、βラクトグロブリン分子は、抗βラクトグロブリン抗体と結合することを示している。
【0037】
これらの結果は、被検試料溶液中に複数種類の抗体が混合され、複数種類の抗原抗体反応が発生している状態でも励起・発光波長を適当に選択することにより、特定の抗原抗体反応が確認できることを示している。また、上記(iii)の色素の同時励起の条件に於ける測定による結果(図3(C)及び(D))に示されている如く、抗原の蛍光標識を同時に励起する場合であっても、発光波長を適当に選択することにより、複数種類の抗原抗体反応のうち、特定の抗原抗体反応を選択的に確認できることを示している。
【0038】
かくして、上記の実施例に於いて例示されている如く、本発明によれば、アレルギーを引き起こす可能性のある抗原と抗体との反応を検出し、原因となっている抗原の特定が、被検試料溶液中に複数種類の抗原抗体反応が発生している場合でも、微量の試料にて且ハイスループットにて実行されることが理解されるべきである。
【図面の簡単な説明】
【0039】
【図1】図1は、実施形態の処理過程中に於ける試料中の分子の状態を模式的に表したものである。
【図2】図2(A)は、本発明の方法の好ましい実施形態に有利に用いられるマイクロプレートの模式図である。図2(B)は、蛍光測定中のウェルの状態を模式的に表した図である。図2(C)−(E)は、抗原候補の分注の種々の態様を説明する図である。図2(F)−(G)は、予め分注された抗原候補の乾燥の過程を模式的に示したものである。
【図3】図3は、実施例に於ける試料の蛍光相関分光法により得られた蛍光強度の自己相関関数より算出される並進拡散時間の結果を示すグラフ図である。図中、抗A抗体は、抗オボアルブミン抗体、抗B抗体は、抗βラクトグロブリン抗体を表す。(A)は、励起波長543nm、受光波長560−620nmとした場合、(B)は、励起波長633nm、受光波長660−710nmとした場合、(C)は、励起波長543nm及び633nm、受光波長565−595nmとした場合、(D)は、励起波長543nm及び633nm、受光波長650−690nmとした場合である。
【符号の説明】
【0040】
10…マイクロプレート
12…ウェル
14…マイクロプレートの底面
【技術分野】
【0001】
本発明は、抗原抗体反応を検出する方法に係り、より詳細には、一分子蛍光分析技術により抗原抗体反応を検出する方法及びその方法に有利に利用可能なマイクロプレートに係る。
【背景技術】
【0002】
生物科学、医学又は薬学の分野に於いて、周知の如く、抗原抗体反応は、生体内外の種々の生体分子を検出することができるので、従来より、生体内の種々の病気の診断や生理活性物質のスクリーニングに応用されている。例えば、細菌、ウィルス、病原性タンパク質、腫瘍などの種々の疾患の原因物質又はその原因物質に由来する物質に特異的に反応する抗体を用い、その抗体が(生体から得られた体液等に於いて)抗原抗体反応を起こしたか否かを検出することで、生体内に於ける原因物質又はそれに由来する物質の有無が検査される。また、逆に、生体内に上記の如き疾患の原因物質又はそれに由来する物質に対する抗体が存在するか否かを、その抗体に対する抗原(又はエピトープ)により(生体から得られた体液等に於いて)抗原抗体反応が起きたか否かを検出することにより、生体内に疾患の原因物質が存在するか否かを検査する場合もある。更に、アレルギーや自己免疫疾患などの一部の疾患の場合には、生体内に特定の物質(食物、花粉、ハウスダスト、カビ、ダニ等)を抗原とする抗体が存在するか否かが、その特定の物質により(生体から得られた体液等に於いて)抗原抗体反応が起きたか否かを検出することにより検査される。
【0003】
抗原抗体反応の検出方法としては、ELISA法、ウェスタンブロット法といった生化学的な方法が一般的であるが、これらの伝統的な方法は、検出に要する処理操作が多く、時間がかかり、また、多量の試料を要する。そこで、近年、より少量の試料にて且より短時間にて抗原抗体反応の検出を可能にする方法又は装置の開発が進められている。例えば、特許文献1に於いては、表面プラズモン共鳴を利用して抗原抗体反応の検出を行う特殊な測定用チップが提案されている。また、特許文献2に於いては、細胞フローメトリーと蛍光測定とを組み合わせた装置を用いて抗原抗体反応を検出するための特殊な試料などが開示されている。
【0004】
また、近年、光学顕微鏡の光学系を用いた光計測技術の進歩により、一光子又は蛍光一分子の蛍光等の微弱光の検出・測定が可能となってきたことから、そのような微弱光の計測技術を用いて、抗原抗体反応を検出する試みが為されつつある。そのような例として、例えば、特許文献3に於いて、レーザー共焦点顕微鏡の光学系を用いた蛍光相関分光法又は蛍光偏光解析法により抗原抗体反応が検出されることが示されている。かかる方法によれば、測定に必要な試料は、従前に比して極めて低濃度且微量でよく(一回の測定で使用される量は、たかだか数十μl程度)、測定時間も大幅に短縮される(一回の測定は10秒程度)。従って、上記の如き微弱光の計測技術を用いて抗原抗体反応を検出する方法又は装置は、病気の診断や生理活性物質のスクリーニングなど、検体数が多い場合にも、従前に比して、速やかに検査が実行できる強力なツールとなることが期待されている。
【特許文献1】特開2006−250668
【特許文献2】特開2005−098877
【特許文献3】特開2005−337805
【発明の開示】
【発明が解決しようとする課題】
【0005】
ところで、抗原抗体反応の検出方法を疾患又はその原因物質等の有無の診断やその他の抗体又は抗原のスクリーニングに応用する場合、しばしば、検査されるべき試料(被検試料)中に複数の種類の抗体又は抗原(疾患の原因物質又はそれに由来する物質)の存否の確認が望まれる場合がある(例えば、アレルギーの診断など)。例えば、上記の特許文献3に記載の蛍光相関分光法又は蛍光偏光解析法を用いた抗原抗体反応検出法によれば、個々の抗体又は抗原の確認検査は、微量の被検試料にて短時間で済むが、それでも、特に、臨床の現場など、被検試料が多数であり、且、検査されるべき抗体の数が多い場合には、全ての検査を完了するためには、それなりの被検試料量と検査時間を要する。従って、もしそのような多項目又は多検体の抗原抗体反応を確認する必要がある場合であっても、微量の被検試料にて迅速に検査が実行できる方法又は装置があれば有利である。また、抗原抗体反応の検査に於ける準備又は処理操作は、できるだけ簡便であることが望ましい。
【0006】
かくして、本発明の一つの目的は、多項目又は多検体の抗原抗体反応を簡便かつ迅速に検出する方法を提供することである。
【課題を解決するための手段】
【0007】
本発明の一つの態様によれば、本発明の抗原抗体反応を検出する方法は、互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体を、それらの複数の種類の抗原又は抗体のいずれかに対する抗体又は抗原が含まれているか否かが検査される被検試料溶液に混合して混合試料溶液を調製する過程と、混合試料溶液中の少なくとも一つの蛍光色素の蛍光強度を測定する過程と、測定された蛍光強度の時間変化に基づいて、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かを判定する過程とを含み、測定された蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合していると判定された場合には、その蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子と結合し抗原抗体反応を生じたと判定し、その蛍光強度に対応する蛍光色素で標識された抗原又は抗体に対する抗体又は抗原が被検試料溶液中に存在すると判定することを特徴とする。なお、当業者にとって理解される如く、被検試料溶液へ混合される蛍光色素で標識した「複数の種類の抗原又は抗体」が抗原(即ち、任意の生体に於いて抗原となり得る物質)であれば、被検試料溶液中に含まれているか否かが検出される物質は、抗体であり、被検試料溶液へ混合される蛍光色素で標識した「複数の種類の抗原又は抗体」が抗体であれば、被検試料溶液中に含まれているか否かが検出される物質は抗原である。
【0008】
上記の構成によれば、抗原抗体反応の検出が、蛍光色素の蛍光強度を測定し、その蛍光時間の変化に基づいて、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かを判定する蛍光分析により行われるので、ELISA等の伝統的な手法に比べ、被検試料量と処理操作時間が大幅に低減されるだけでなく、被検試料溶液へ互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体を混合するという手法により、検査されるべき項目又は存否が確認されるべき物質が複数在っても、被検試料量は、一回の検査に必要な試料量分のみでよくなる。被検試料溶液へ混合される抗原又は抗体、即ち、被検試料溶液中の物質を探索するための「プローブ」試料は、互いに異なる蛍光色素で標識されるので、個々のプローブ試料が抗原抗体反応を起こすか否かは、それぞれの蛍光色素の蛍光強度を別々に測定する必要があるが(検出する色素の吸収波長又は発光波長特性に応じて蛍光検出装置に於いて励起波長又は受光波長の選択が為される。)、被検試料溶液自体は交換する必要はない。複数の種類の蛍光色素が一波長の励起光で励起できる場合には、蛍光測定装置の光検出器に於いて適宜波長を弁別する装置(フィルター、回折格子等)が用いられてよい。
【0009】
また、上記の構成に於いて、複数の種類の抗原又は抗体に標識された蛍光色素の全てについて各々の蛍光強度を測定し、測定された蛍光強度の各々の時間変化に基づいて、蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かを判定し、蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合していると判定されたときに、蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子と結合し抗原抗体反応を生じたと判定するようになっていてよい。しかしながら、被検試料溶液へ混合された蛍光色素の各々の蛍光強度の測定・分析を順々に行う間に、検出されるべき結果が判明したときには、全ての色素の蛍光測定を行わなくてもよいことは理解されるべきである。なお、使用する蛍光測定装置において、複数の種類の互いに吸収・発光波長特性の異なる蛍光色素の励起及び蛍光の検出が同時にできるときには、蛍光色素の蛍光測定は、同時に実行されてよく、その場合、更に測定時間が短縮される。
【0010】
上記の本発明の方法に於いては、蛍光強度の測定は、蛍光一分子からの蛍光を測定し、その時間変化又は揺らぎを解析して蛍光一分子の状態又は運動を観測する蛍光分析法(一分子蛍光分析技術)により為される。例えば、蛍光強度の測定は「蛍光相関分光法」により行われてよく、その場合には、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かは、蛍光強度の時間変化に基づいて蛍光相関分光法により算出された並進拡散時間に基づいて判定されてよい。また、蛍光強度の測定は「蛍光強度分布解析法」により行われてよく、その場合には、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かが、蛍光強度の時間変化に基づいて蛍光強度分布解析法により算出された一蛍光発光体当たりの蛍光強度に基づいて判定されてよい(この場合、後述の如く、複数の種類の蛍光標識された抗原又は抗体が被検試料溶液中の一つの分子に同時に結合している必要がある。「一蛍光発光体」とは、蛍光一分子ではなく、溶液中で一体的に運動する蛍光を発する物体を意味する。)また、蛍光強度の測定が「蛍光偏光解消法」により行われてよく、その場合には、蛍光強度に対応する蛍光色素で標識された抗原又は抗体が被検試料溶液中の分子に結合しているか否かが蛍光強度の時間変化に基づいて蛍光偏光解消法により算出された蛍光偏光度により判定されてよい(この場合、一分子蛍光分析を実行する装置ではなく、通常の蛍光偏光解消測定装置であってもよい。)。
【0011】
上記の本発明は、特に疾患又はその原因物質等の有無の診断やその他の抗体のスクリーニングなど、検査されるべき抗原抗体反応が複数ある場合に有利に用いられる。従って、例えば、本発明の抗原抗体検出方法が食物によるアレルギー性疾患の診断に使用される場合には、本発明に於いて使用されるプローブ試料(互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体)は、抗原抗体反応が発生した場合に抗原となる食物に含まれるタンパク質であってよい。また、プローブ試料は、アレルギー性疾患患者の体液中に含まれる抗体に対する抗原であってもよい。これらの場合、本発明によれば、複数の食物若しくはその中に含まれるタンパク質又はその他のアレルゲンのうち、いずれのものがアレルギー反応を示す原因となっているかを迅速に且複数のものについて、同時に検査・診断することが可能となる。更に、プローブ試料は、自己免疫疾患患者の体液中に含まれる抗体に対する抗原であってもよく、これにより、自己免疫疾患の種類の特定を迅速に実施できることとなる。本発明を上記の如き、疾患の検査・診断に用いる場合には、被検試料溶液が血清又は血漿又はその他の生体から得られた体液試料が用いられてよい。理解されるべきことは、この場合、本発明の特徴によれば、複数の疾患に関わる抗原又は抗体の存否を検査するために必要な被検試料溶液となる体液試料は、微量でよいということである。なお、被検試料溶液が、血清など自家蛍光を持つ可能性がある場合には、自家蛍光が測定に乗らないように、できる限り長波長、短くとも540nm以上で励起できる蛍光色素を使用することが好ましい。
【0012】
上記の方法を実施するに当たり、蛍光測定は、複数のウェルを有し抗原抗体反応を蛍光測定分析により検出するのに適したマイクロプレートであって、複数のウェルの各々に予め少なくとも一つの蛍光標識された抗原又は抗体が分注されていることを特徴とするマイクロプレートにより有利に実行することができる。かかるマイクロプレートの態様に於いて、予め互いに異なる蛍光色素にて標識された複数の種類の抗原又は抗体が同一のウェルに分注されていてよい。即ち、複数のウェルのそれぞれに、互いに異なる蛍光色素にて標識された複数の種類の抗原又は抗体から成るプローブ試料が分注される。この場合、複数の被検試料溶液を別々のウェルに分注することにより、系統的に多数の被検試料溶液について、複数の種類の抗原抗体反応の検出が可能となる。また、マイクロプレートのもう一つの態様に於いて、複数のウェルに別々の予め互いに異なる蛍光色素にて標識された複数の種類の抗原又は抗体が分注されていてよい。この場合、一つの被検試料溶液を別々の抗原又は抗体が分注されたウェルに分注することにより、一つの被検試料溶液について多種類の抗原抗体反応の確認が為される。いずれの場合に於いても、一枚のプレートで多数の検査が実施されることとなるので、蛍光測定分析装置に於いて被検試料溶液を変更する操作が一段と簡単化される。かかる特徴は、疾患又はその原因物質等の有無の診断やその他の抗体又は生理活性物質等のスクリーニングを行う際、非常に有利である。
【0013】
なお、上記のマイクロプレートは、複数のウェルに分注された蛍光標識抗原又は抗体を乾燥させた状態に保持されていてよい。これにより、プローブ試料の長期保存が可能となり、蛍光標識抗原又は抗体を検査の度に調製する必要がなくなる。使用者は、検査の実行に当たり、単に被検試料溶液をウェルに添加するだけで、蛍光測定・分析を行うことができ、非常に便利である。被検試料溶液が血清など自家蛍光を持つ可能性がある場合には、540nm以上で励起できる蛍光色素を使用することが好ましい。
【発明の効果】
【0014】
本発明によれば、上記の説明から理解される如く、蛍光測定分析、特に、一分子蛍光測定分析を用いて、多種類の抗原抗体反応の検出が、微量の被検試料にて迅速に実行できる。従前の多種類の抗原抗体反応の検出方法に於いては、抗原抗体反応の種類を識別するために、マイクロビーズや基板等に抗原又は抗体を固定するなどの処理が必要であった。しかしながら、本発明によれば、多種類の抗原抗体反応の区別は、蛍光色素の波長によりなされるので、試料の蛍光標識操作が必要とはなるものの、蛍光測定及び分析するための試料標本である混合試料溶液の調製操作は、被検試料溶液とプローブ試料とを殆どそのまま混合するだけでよく、従って、試料の固定等の操作に於ける試料の損失はなく、また、プローブ試料を基板等に固定する必要がないことから、試料の変性の可能性も低減され、測定結果の信頼性も高くなる。
【0015】
かくして、本発明の方法は、病気又は各種疾患の診断や生理活性物質のスクリーニングなど、検体数が多い場合にも、微量な試料にて且短時間にて、そして、高い信頼性にて、検査が実行できる多種類の抗原抗体反応検出及び識別方法としての利用が期待される。
【0016】
本発明のその他の目的及び利点は、以下の本発明の好ましい実施形態の説明により明らかになるであろう。
【発明を実施するための最良の形態】
【0017】
以下に添付の図を参照しつつ、本発明を幾つかの好ましい実施形態について詳細に説明する。
【0018】
抗原抗体反応の検出の手順
図1は、抗原抗体反応により、例えば、血清、血漿、尿、鼻汁、涙液、糞便、組織抽出液などの生体から得られた体液試料又は培養液等の被検試料溶液中に含まれている抗体を検出する本発明の方法の好ましい実施形態に於ける処理過程に於ける試料中の分子の状態を示す模式図である。
【0019】
同図を参照して、図1(a)に示されている如く、例えば、或る疾患の患者の体液試料中には、その疾患に罹患すると、その原因物質(細菌、ウイルス、病原性タンパク質、腫瘍)又はそれに由来する物質に対する抗体が含有される。また、アレルギー性疾患の場合であれば、患者の体液試料中には、そのアレルギー性疾患に特有の(食物、花粉、ハウスダスト、カビ、ダニ等のアレルゲンに対する)抗体が含まれる。或いは、任意の培養細胞からも抗体が産生される。疾患の種類は、それらの抗体と特異的に結合する、即ち、抗原抗体反応を引き起こす物質を特定することにより特定される。しかしながら、疾患の種類が特定されるまでは、いずれの物質と抗原抗体反応を起こすか(又は抗原抗体反応自体を起こすか否か)は分からず、従って、複数の種類の物質について抗原抗体反応を起こすか否かを検査することが必要な場合がある。そこで、本実施形態では、抗体検出のためのプローブ試料として、被検試料溶液中の存否が確認されるべき抗体の候補に対応する複数の種類の抗原候補A1−A4にそれぞれ別々の蛍光色素F1−F4を付加したもの(蛍光標識したもの)をプローブ試料として調製し(図1(b))、これらを体液試料と混合する。
【0020】
存否が確認されるべき抗体の候補に対応する複数の種類の抗原候補は、当業者にとって任意の生理活性物質、例えば、タンパク質、核酸、脂質、糖類その他の生体分子等又は化学物質であってよい。これらの抗原候補の蛍光標識は、抗原候補となる物質の種類及び特性に応じて当業者にとって任意の手法により為されてよい。例えば、タンパク質であれば、蛍光標識は、タンパク質中の特定の基を標的にしたケミカルラベリング法により為されてよい。また、その他の物質については、任意の方法で蛍光標識された物質が化学合成されてもよい。蛍光色素としては、この分野で通常使われる任意の蛍光色素、例えば、TAMRA(carboxymethylrhodamine)、TMR(tetramethylrhodamine)、Alexa647、Rhodamine
Green、Alexa488などであってよいが、これらに限定されない。重要なことは、一つの被検試料溶液へ混合される複数種の抗原候補の物質に付加される蛍光色素の発光波長のスペクトルが異なり、これらの蛍光の各々が、後述の蛍光測定の際、受光波長の選択により識別できる態様になっている必要がある。なお、受光波長に於いて識別できない場合、励起波長で識別できればよい(ただし、蛍光測定装置の光源に於いて、それぞれの励起波長の励起光を供給できるようになっている必要がある。)。
【0021】
かくして、抗原候補A1−A4は、被検試料溶液に混合されると(図1(c))、もし対応する抗体が存在する場合には、抗体に特異的に結合する(抗原抗体反応。A1、A3)。一方、特異的に結合できる抗体が存在しない場合には、抗原候補は、溶液中に単独で浮遊することとなる(A2、A4)。従って、抗体に結合した抗原の色素F1、F3と抗体に結合していない色素F2、F4とでは、溶液中のブラウン運動の態様が異なることとなる。かかる運動性の違いは、蛍光色素F1−F4の蛍光強度の時間変化(揺らぎ)に反映されるので、抗原候補が抗体に結合したか否かが蛍光強度の時間変化に基づいて判定できることとなる。
【0022】
蛍光測定は、典型的には、1分子蛍光分析システム MF20(オリンパス)が用いられてよい。かかるシステムに於いては、蛍光相関分光法、蛍光偏光解消法、蛍光強度分布解析法のいずれかにより、蛍光色素Fの運動状態が判定される。以下、各分析方法に於いて、抗原候補が抗体に結合しているか否かが計測結果に如何に反映されるかについて説明する。
【0023】
蛍光相関分光法では、微小の蛍光観察領域をブラウン運動により通過する分子の移動(並進運動)の速さが観測される。分子の並進運動の速さは、測定された蛍光強度の時間を変数とした自己相関関数の形状に反映される。分子の並進運動の速さの指標としては、測定開始時から自己相関関数の値が半分になるまでの時間の長さ(並進拡散時間)が用いられる。分子の移動は、分子の大きさが大きいほど、遅くなるので、並進拡散時間が長くなる。本発明の場合、図1(c)のA1、A3の如く、抗原が抗体に結合すると、蛍光色素Fは、抗原及び抗体と一体的に運動し、従って、図1(c)のA2、A4に比して、蛍光色素Fの運動の速さが顕著に低減し、並進拡散時間が長くなる。従って、並進拡散時間により、或る抗原について、抗原抗体反応が起きた否かが分かり、抗原A1、A3に対する抗体が被検試料溶液中に存在することが確認される。
【0024】
蛍光偏光解消法では、この分野に於いて知られている如く、分子の回転ブラウン運動(自転)の速さが観測される。分子の回転運動の速さは、測定された蛍光の縦偏光と横偏光の強度の割合又は偏光度に反映される。分子の回転は、分子の大きさが大きいほど、遅くなるので、偏光度が大きくなる。本発明の場合、抗体に結合した抗原上の蛍光色素の回転ブラウン運動は遅くなるので、偏光度が大きくなり、これにより、或る抗原について、抗原抗体反応が起きた否かが分かり、抗原A1、A3に対する抗体が被検試料溶液中に存在することが確認される。
【0025】
蛍光強度分布解析法では、微小の蛍光観察領域内から発せられる光子の検出(フォトンカウンティング)を行い、単位時間当たりの光子が検出された頻度を統計的に処理することによって、微小の蛍光観察領域内の蛍光発光体の数密度と、一蛍光発光体当たりの蛍光強度が算出される。本発明の場合、抗原A3の如く、蛍光標識された抗原が一つの抗体に複数結合すると、結合前各々が一つの蛍光発光体として独立に運動していた個々の蛍光色素分子は、抗体に拘束され一つの蛍光発光体として運動することになるので、蛍光発光体の数密度が低減する一方、抗体に複数の蛍光色素分子が存在することにより一蛍光発光体当たりの蛍光強度が増大する。かくして、抗原A3については、蛍光発光体の数密度の低減と一蛍光発光体当たりの蛍光強度の増大から抗原抗体反応が起きたことが検出される。抗体に一つしか結合しない抗原A1の場合であっても、もし抗原A1の蛍光色素の蛍光強度が抗体に結合することにより変化する場合には、そのことにより、結合の有無が検出できる可能性がある。
【0026】
実際の測定では、一つの被検試料溶液について、蛍光色素F1−F4の蛍光が識別できる態様にて、蛍光強度が測定され、その時間変化が解析される。波長の弁別は、蛍光の光検出器の受光面までの光路にハイパスフィルター又はバンドパスフィルターを挿入するか或いは回折格子等を用いて特定の波長の光のみ光検出器に受光されるようになっていてよい。かかる波長弁別の構成は、当業者にとって任意の構成によりなされてよい。また、種々の波長の光で色素を励起し、色素の吸収(励起)波長特性の違いにより複数の種類の色素の蛍光を識別してもよい。
【0027】
かくして、蛍光測定・分析による蛍光色素の運動状態から抗原候補が抗体に結合しているか否かが判定され、即ち、抗原抗体反応の有無が検出される。なお、上記の方法に於いて、抗原候補と被検試料溶液を混合した段階でのみ蛍光測定・分析を実行しても、その結果の数値から蛍光色素が抗体と一体的に運動しているか否かを推定することができるが、抗原候補を被検試料溶液と混合する前の段階で、比較のために蛍光測定・解析を実行してもよい。また、上記の実施形態に於いては、被検試料が抗体であり、プローブ試料が抗原であったが、被検試料が抗原であり、プローブ試料が抗体であってもよい。ただし、その場合、抗原抗体反応により、プローブ試料である抗体の運動状態が顕著に変化するほど大きな抗原である必要がある。
【0028】
抗原抗体反応検出用マイクロプレート
ところで、上記の蛍光測定・分析に於いて、図2(A)に模式的に示されているマイクロプレートを用いると、より効率的に種々の被検試料溶液についての測定・分析を行うことができる。同図を参照して、本発明に有利に使用されるマイクロプレート10は、上面が開孔した複数のウェル12と、ガラス又は光を透過するプラスチック等のプレートの底面部材14とを有する。マイクロプレートの全体の寸法は、平面に於いて約10cm程度であり、一つのウェルの容量は、100μl程度であり、測定に於いては、数十μl程度の試料が注入される。マイクロプレートが蛍光測定装置に配置されると、図2(B)に示されている如く、装置の励起光は、底面を透過して、ウェル内で集光され、そこで、励起された色素の蛍光は、底面を透過して、光検出器(図示せず)へ導かれる。
【0029】
本発明に於いて、蛍光測定の際にマイクロプレートを使用する場合、マイクロプレートの各ウェルには、それぞれ別の被検試料溶液が注入されてよい。また、好適には、予め検出されるべき抗体の種類が特定されている場合、例えば、自己免疫疾患或いはアレルギー性疾患の患者の体液試料中の抗体を検出することが目的とされる場合には、測定に先立って、蛍光標識された抗原候補を各ウェルへ分注した状態に調製される。
【0030】
かかるマイクロプレートの抗原候補の分注の一つの態様としては、複数のウェルの各々に互いに異なる蛍光色素にて標識された複数の種類の抗原候補が予め分注される(図2(C))。この場合、各ウェルへそれぞれ異なる被検試料溶液が注入され、一つのマイクロプレートで多数の被検試料溶液の検査が実行できることとなる。また、別の態様としては、複数のウェルの各々に別々の種類の抗原候補が分注されてもよい。それぞれのウェルについては、一種類の抗原候補が分注されてもよいが(図2(D))、複数の種類の抗原候補が分注されてもよい図2(E)。一度の蛍光測定に於いて同じ溶液で識別可能な蛍光色素の数は、色素の発光波長の範囲(のスペクトル)の幅によって制限される(発光波長のスペクトルの重なりが大きい色素同士は、同じ溶液中で計測は困難である。)。従って、或る一つの被検試料溶液に於いて、同一の溶液中で利用可能な色素の種類を越える数の抗原抗体反応を検出したいときは、複数のウェルのそれぞれに別々の抗原候補又は別々の抗原候補の組み合わせを分注するようになっていてよい。
【0031】
そのような予め抗原候補を分注したマイクロプレートを準備しておけば、検査の度に抗原候補を調製する必要がなく便利である。また、抗原候補が、乾燥しても抗原としての活性を失わない場合には、各ウェルへ複数の種類の抗原候補(例えば、良く使用する抗原候補)を分注した後、乾燥され、保存できるようになっていてよい。
【0032】
かかるマイクロプレートの調製は、例えば、以下の如く為されてよい(図2(F))。
1.反応を検出したい抗原を蛍光標識し精製する。
2.マイクロプレートの各ウェルに10nMの蛍光標識された抗原を5μlずつ入れ、自然乾燥、滅圧乾燥又は凍結乾燥などにより乾燥する。
なお、抗原候補が分注されたマイクロプレートを長期保存する場合には、抗原候補及び蛍光色素の変性を回避するべく遮光冷蔵保存される。使用時には室温に戻され、各ウェルに被検試料溶液を注入し、適当な反応時間の後、蛍光測定が行われる。
【0033】
上記に説明した本発明の有効性を検証するために、以下の実験を行った。なお、以下の実施例は、本発明の有効性を例示するものであって、本発明の範囲を限定するものではないことは理解されるべきである。
【実施例1】
【0034】
抗原抗体反応の典型的な例であるアレルギー性疾患に関与する二つの抗原抗体反応が、本発明の方法により一つの被検試料溶液に於いて検出されることを確認した。アレルギー性疾患とは、端的に述べれば、体内に入ってきた抗原(アレルゲン)がマスト細胞の表面にあるIgE抗体と結合することによって、マスト細胞からヒスタミンなどの化学伝達物質が放出され、これらの化学伝達物質の作用によって現れる症状である。或る物質に対してアレルギー症状を起こす患者は、その物質を抗原とする抗体を有している。従って、そのような患者の体液中に如何なる物質に対する抗体が存在するかを検出できれば、アレルゲンが特定され、アレルギーの予防や治療のために非常に有用な情報となる。下記の実験では、そのようなアレルギー性疾患のうち、食物アレルギー症状を引き起こすことが知られている卵白に含まれるオボアルブミンと、牛乳に含まれるβラクトグロブリンの2種類を蛍光標識し、それぞれを抗原とする抗原抗体反応を検出する実験を行った。
【0035】
測定の処理操作は、以下の通りとした。
1.オボアルブミン(製造元MP Biomedicals,Inc.)は、TAMRA NHS−ester(オリンパス)を用いて、βラクトグロブリン(製造元ICN BIOMEDICALS)は、ATTO633 NHS−ester(ATTO-TEC)を用いて、それぞれ蛍光標識し精製した。TAMRA[5-(and-6)-Carboxytetramethylrhodamine]の吸収・蛍光波長のピークは、それぞれ541nm及び565nmであり、ATTO633の吸収・蛍光波長のピークは、それぞれ629nm及び657nmである。
2.かくして蛍光標識された抗原をリン酸バッファ+0.05%Tween20中に溶解し、両方の抗原を含むプローブ溶液を、それぞれの抗原の終濃度数nMとなるように調製した。そこへ、抗オボアルブミン抗体(製造元MP Biomedicals,Inc.)のみ、抗βラクトグロブリン抗体(製造元BETHYL LABORATORIES)のみ、両方の抗体を含む溶液(被検試料溶液)をそれぞれ混合し、合計の溶液量が50μLとなるよう調製し、37℃で30分間放置した。なお、対照用として、プローブ溶液へ抗体を含まない溶液を混合したものも用意した。
3.かくして調製した(対照用を含む)4種類の被検溶液について、1分子蛍光分析システムMF20(オリンパス)を使用し、蛍光相関分光法により蛍光分子の並進拡散時間を測定した。測定では、(i)波長543nmで励起した場合、(ii)波長633nmで励起した場合及び(iii)波長543nmと波長633nmとの二重励起した場合の三通りにて行った。測定時の光検出器で受光させた波長範囲は以下の通りである。
(i)励起波長543nmのとき …560−620nm
(ii)励起波長633nmのとき …660−710nm
(iii)励起波長543nm及び633nm(二重励起)…565−595nm及び650−690nm
なお、(iii)の場合、光検出器を二つ用い、その一方に565−595nmの範囲の波長の光、他方に650−690nmの範囲の波長の光が入射されるようにした。レーザー強度は、100μWとし、一つの試料につき、10秒間計測を5回ずつ行い、各々について、MF20に準備された蛍光相関分光分析法用のプログラムにより、蛍光強度の自己相関関数を演算し、並進拡散時間の平均を算出した。
【0036】
図3は、上記(i)−(iii)のそれぞれの場合に於ける4種類の被検溶液の並進拡散時間の結果をグラフで示したものである。同図を参照して、並進拡散時間は、(i)励起波長543nmのときの蛍光強度(図3(A))及び(iii)の受光波長が565−595nmの光検出器の蛍光強度(図3(C))から測定・算出されたものについては、抗オボアルブミン抗体のみ含む溶液、両方の抗体を含む溶液に於いてのみ増大し、(ii)励起波長633nmのときの蛍光強度(図3(C))及び(iii)の受光波長が650−690nmの光検出器の蛍光強度(図3(D))から測定・算出されたものについては、抗βラクトグロブリン抗体のみ含む溶液、両方の抗体を含む溶液に於いてのみ増大した。オボアルブミンに付加された蛍光色素TAMRAは、発光波長(のピーク)が565nmであり、βラクトグロブリンに付加された蛍光色素ATTO633の発光波長(のピーク)が657nmであることから、図3(A)及び(C)の結果は、オボアルブミン分子の運動状態を表しているものであると考えられ、抗オボアルブミン抗体の存在下では、その他の抗体が存在していても、オボアルブミン分子は、抗オボアルブミン抗体と結合することを示している。また、同様に、図3(B)及び(D)の結果は、βラクトグロブリン分子の運動状態を表しているものであると考えられ、抗βラクトグロブリン抗体の存在下では、その他の抗体が存在していても、βラクトグロブリン分子は、抗βラクトグロブリン抗体と結合することを示している。
【0037】
これらの結果は、被検試料溶液中に複数種類の抗体が混合され、複数種類の抗原抗体反応が発生している状態でも励起・発光波長を適当に選択することにより、特定の抗原抗体反応が確認できることを示している。また、上記(iii)の色素の同時励起の条件に於ける測定による結果(図3(C)及び(D))に示されている如く、抗原の蛍光標識を同時に励起する場合であっても、発光波長を適当に選択することにより、複数種類の抗原抗体反応のうち、特定の抗原抗体反応を選択的に確認できることを示している。
【0038】
かくして、上記の実施例に於いて例示されている如く、本発明によれば、アレルギーを引き起こす可能性のある抗原と抗体との反応を検出し、原因となっている抗原の特定が、被検試料溶液中に複数種類の抗原抗体反応が発生している場合でも、微量の試料にて且ハイスループットにて実行されることが理解されるべきである。
【図面の簡単な説明】
【0039】
【図1】図1は、実施形態の処理過程中に於ける試料中の分子の状態を模式的に表したものである。
【図2】図2(A)は、本発明の方法の好ましい実施形態に有利に用いられるマイクロプレートの模式図である。図2(B)は、蛍光測定中のウェルの状態を模式的に表した図である。図2(C)−(E)は、抗原候補の分注の種々の態様を説明する図である。図2(F)−(G)は、予め分注された抗原候補の乾燥の過程を模式的に示したものである。
【図3】図3は、実施例に於ける試料の蛍光相関分光法により得られた蛍光強度の自己相関関数より算出される並進拡散時間の結果を示すグラフ図である。図中、抗A抗体は、抗オボアルブミン抗体、抗B抗体は、抗βラクトグロブリン抗体を表す。(A)は、励起波長543nm、受光波長560−620nmとした場合、(B)は、励起波長633nm、受光波長660−710nmとした場合、(C)は、励起波長543nm及び633nm、受光波長565−595nmとした場合、(D)は、励起波長543nm及び633nm、受光波長650−690nmとした場合である。
【符号の説明】
【0040】
10…マイクロプレート
12…ウェル
14…マイクロプレートの底面
【特許請求の範囲】
【請求項1】
抗原抗体反応を検出する方法であって、
互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体を、前記複数の抗原又は抗体のいずれかに対する抗体又は抗原が含まれているか否かが検査される被検試料溶液に混合し混合試料溶液を調製する過程と、
前記混合試料溶液中の少なくとも一つの前記蛍光色素の蛍光強度を測定する過程と、
前記測定された蛍光強度の時間変化に基づいて、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合しているか否かを判定する過程と
を含み、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合していると判定された場合には、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子と結合し抗原抗体反応を生じたと判定し、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体に対する抗体又は抗原が前記被検試料溶液に含まれていると判定することを特徴とする方法。
【請求項2】
請求項1の方法であって、前記複数の種類の抗原又は抗体に標識された蛍光色素の全てについて各々の蛍光強度を測定し、前記測定された蛍光強度の各々の時間変化に基づいて、前記蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合しているか否かを判定し、前記蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合していると判定されたときに、前記蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子と結合し抗原抗体反応を生じたと判定することを特徴とする方法。
【請求項3】
請求項1又は2の方法であって、前記蛍光強度の測定が蛍光相関分光法により行われ、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合しているか否かが前記蛍光強度の時間変化に基づいて前記蛍光相関分光法により算出された並進拡散時間に基づいて判定されることを特徴とする方法。
【請求項4】
請求項1又は2の方法であって、前記蛍光強度の測定が蛍光偏光解消法により行われ、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合しているか否かが前記蛍光強度の時間変化に基づいて前記蛍光偏光解消法により算出された蛍光偏光度に基づいて判定されることを特徴とする方法。
【請求項5】
請求項1又は2の方法であって、前記蛍光強度の測定が蛍光強度分布解析法により行われ、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合しているか否かが前記蛍光強度の時間変化に基づいて前記蛍光強度分布解析法により算出された一蛍光発光体当たりの蛍光強度に基づいて判定されることを特徴とする方法。
【請求項6】
請求項1又は2の方法であって、前記被検試料溶液に混合される前記互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体が前記抗原抗体反応が発生した場合に抗原となる食物に含まれるタンパク質であることを特徴とする方法。
【請求項7】
請求項1又は2の方法であって、前記被検試料溶液に混合される前記互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体がアレルギー性疾患患者の体液中に含まれる抗体に対する抗原であることを特徴とする方法。
【請求項8】
請求項1又は2の方法であって、前記被検試料溶液に混合される前記互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体が自己免疫疾患患者の体液中に含まれる抗体に対する抗原であることを特徴とする方法。
【請求項9】
請求項1又は2の方法であって、前記被検試料溶液が血清又は血漿又は生体から得られた体液試料であることを特徴とする方法。
【請求項10】
請求項1又は2の方法であって、前記蛍光標識が540nm以上の波長の光で励起可能であることを特徴とする方法。
【請求項11】
複数のウェルを有し抗原抗体反応を蛍光測定分析により検出するのに適したマイクロプレートであって、前記複数のウェルの各々に予め少なくとも一つの蛍光標識された抗原又は抗体が分注されていることを特徴とするマイクロプレート。
【請求項12】
請求項11のマイクロプレートであって、予め互いに異なる蛍光色素にて標識された複数の種類の抗原又は抗体が同一のウェルに分注されていることを特徴とするマイクロプレート。
【請求項13】
請求項11のマイクロプレートであって、前記複数のウェルに別々の予め互いに異なる蛍光色素にて標識された少なくとも一種類の抗原又は抗体が分注されていることを特徴とするマイクロプレート。
【請求項14】
請求項11乃至13のマイクロプレートであって、前記複数のウェルに分注された前記蛍光標識された抗原又は抗体が乾燥された状態に保持されていることを特徴とするマイクロプレート。
【請求項15】
請求項11乃至13のマイクロプレートであって、前記蛍光標識が540nm以上の波長の光で励起可能であることを特徴とするマイクロプレート。
【請求項1】
抗原抗体反応を検出する方法であって、
互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体を、前記複数の抗原又は抗体のいずれかに対する抗体又は抗原が含まれているか否かが検査される被検試料溶液に混合し混合試料溶液を調製する過程と、
前記混合試料溶液中の少なくとも一つの前記蛍光色素の蛍光強度を測定する過程と、
前記測定された蛍光強度の時間変化に基づいて、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合しているか否かを判定する過程と
を含み、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合していると判定された場合には、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子と結合し抗原抗体反応を生じたと判定し、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体に対する抗体又は抗原が前記被検試料溶液に含まれていると判定することを特徴とする方法。
【請求項2】
請求項1の方法であって、前記複数の種類の抗原又は抗体に標識された蛍光色素の全てについて各々の蛍光強度を測定し、前記測定された蛍光強度の各々の時間変化に基づいて、前記蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合しているか否かを判定し、前記蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合していると判定されたときに、前記蛍光強度の各々に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子と結合し抗原抗体反応を生じたと判定することを特徴とする方法。
【請求項3】
請求項1又は2の方法であって、前記蛍光強度の測定が蛍光相関分光法により行われ、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合しているか否かが前記蛍光強度の時間変化に基づいて前記蛍光相関分光法により算出された並進拡散時間に基づいて判定されることを特徴とする方法。
【請求項4】
請求項1又は2の方法であって、前記蛍光強度の測定が蛍光偏光解消法により行われ、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合しているか否かが前記蛍光強度の時間変化に基づいて前記蛍光偏光解消法により算出された蛍光偏光度に基づいて判定されることを特徴とする方法。
【請求項5】
請求項1又は2の方法であって、前記蛍光強度の測定が蛍光強度分布解析法により行われ、前記蛍光強度に対応する蛍光色素で標識された抗原又は抗体が前記被検試料溶液中の分子に結合しているか否かが前記蛍光強度の時間変化に基づいて前記蛍光強度分布解析法により算出された一蛍光発光体当たりの蛍光強度に基づいて判定されることを特徴とする方法。
【請求項6】
請求項1又は2の方法であって、前記被検試料溶液に混合される前記互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体が前記抗原抗体反応が発生した場合に抗原となる食物に含まれるタンパク質であることを特徴とする方法。
【請求項7】
請求項1又は2の方法であって、前記被検試料溶液に混合される前記互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体がアレルギー性疾患患者の体液中に含まれる抗体に対する抗原であることを特徴とする方法。
【請求項8】
請求項1又は2の方法であって、前記被検試料溶液に混合される前記互いに異なる蛍光色素で標識した複数の種類の抗原又は抗体が自己免疫疾患患者の体液中に含まれる抗体に対する抗原であることを特徴とする方法。
【請求項9】
請求項1又は2の方法であって、前記被検試料溶液が血清又は血漿又は生体から得られた体液試料であることを特徴とする方法。
【請求項10】
請求項1又は2の方法であって、前記蛍光標識が540nm以上の波長の光で励起可能であることを特徴とする方法。
【請求項11】
複数のウェルを有し抗原抗体反応を蛍光測定分析により検出するのに適したマイクロプレートであって、前記複数のウェルの各々に予め少なくとも一つの蛍光標識された抗原又は抗体が分注されていることを特徴とするマイクロプレート。
【請求項12】
請求項11のマイクロプレートであって、予め互いに異なる蛍光色素にて標識された複数の種類の抗原又は抗体が同一のウェルに分注されていることを特徴とするマイクロプレート。
【請求項13】
請求項11のマイクロプレートであって、前記複数のウェルに別々の予め互いに異なる蛍光色素にて標識された少なくとも一種類の抗原又は抗体が分注されていることを特徴とするマイクロプレート。
【請求項14】
請求項11乃至13のマイクロプレートであって、前記複数のウェルに分注された前記蛍光標識された抗原又は抗体が乾燥された状態に保持されていることを特徴とするマイクロプレート。
【請求項15】
請求項11乃至13のマイクロプレートであって、前記蛍光標識が540nm以上の波長の光で励起可能であることを特徴とするマイクロプレート。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2010−256010(P2010−256010A)
【公開日】平成22年11月11日(2010.11.11)
【国際特許分類】
【出願番号】特願2006−299697(P2006−299697)
【出願日】平成18年11月2日(2006.11.2)
【出願人】(000000376)オリンパス株式会社 (11,466)
【Fターム(参考)】
【公開日】平成22年11月11日(2010.11.11)
【国際特許分類】
【出願日】平成18年11月2日(2006.11.2)
【出願人】(000000376)オリンパス株式会社 (11,466)
【Fターム(参考)】
[ Back to top ]

