アルキミカ、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツングにより出願された特許
1 - 8 / 8
脱離反応によるニトリルの製造方法
R−C≡N(式II)で表されるニトリルを製造するための、N−アルキルカルボキサミド(RCO−NHR1)またはカルボン酸のアンモニウム塩(RCOO−NH3R1+)、またはアルキルアミンまたはアンモニウム塩(RCOOH+NH2R1、RCOOH+NH3R1+)(式中、Rは、任意に置換された直鎖状または分岐鎖状のC1〜C12アルキル基、C3〜C12シクロアルキル基、アルケニル基、アルキニル基またはアリール基もしくはヘテロアリール基であり、R1は、任意に置換された直鎖状または分岐鎖状のC2〜C12アルキル基、C3〜C12シクロアルキル基、アルケニル基またはアルキニル基である。)の存在下にあるカルボン酸を、無水ホスホン酸と、所望により塩基の存在下で、有機溶剤中、−30〜180℃の温度で反応させる、方法。使用する無水ホスホン酸は、特に式(I)で表される2,4,6−置換された1,3,5,2,4,6−トリオキサチアホスフィナン2,4,6−トリオキシドである。
 (もっと読む)
(もっと読む)
アリールアミン、アリールエーテルおよびアリールチオエーテルの製造方法
本発明は、第1級または第2級アミン、アルコールまたはチオアルコール(II)を、ブレンステッド塩基の存在下で、かつa)V、Mn、Fe、Co、Ni、Rh、Pd、Ir、Ptの群から選択された遷移金属、該遷移金属の錯体、塩または化合物、およびb)少なくとも一種のスルホン化されたホスフィン配位子を含む触媒または予備触媒の存在下で、置換されたアリールまたはヘテロアリール化合物(I)と、溶剤または溶剤混合物中でスキーム1にしたがって、クロス−カップリングさせることにより、アリール−またはヘテロアリールアミン、エーテルまたはチオエーテル(III)を製造する方法に関する。スキーム1中、Halはフッ素、塩素、臭素、ヨウ素、アルコキシ、トリフルオロメタンスルホネート、ノナフルオロトリメチル−メタンスルホネート、メタンスルホネート、4−トルエンスルホネート、ベンゼンスルホネート、2−ナフタレンスルホネート、3−ニトロベンゼンスルホネート、4−ニトロベンゼンスルホネート、4−クロロベンゼンスルホネート、2,4,6−トリイソプロピルベンゼンスルホネートまたは他のいずれかのスルホネートを表し、XはO、S、またはNR”を表す。本発明は、新規なホスフィン配位子にも関する。 (もっと読む)
α−脱離基で置換されたケトンのADH還元および環化による単一の鏡像異性体エポキシドの製造方法
本方法は、単一の鏡像異性体エポキシドの製造方法であって、α−脱離基で置換されたケトンを、補因子の存在下、および所望により、酸化された補因子を再生するための好適な系の存在下、(R)−または(S)−選択性アルコールデヒドロゲナーゼで還元して、対応する単一の鏡像異性体アルコールを製造し、続いて塩基誘発される環化により、対応する単一の鏡像異性体エポキシドを製造する(式1)、方法
(式1中、LGは、F、Cl、Br、I、OSO2Ar、OSO2CH3、OSO2R、もしくはOP(O)OR2を表すことができ、R1、R2、およびR3は、それぞれ独立して、水素、分岐鎖状または非分岐鎖状の、所望により置換されたC1〜C20アルキル基、所望により不規則に置換されたC3〜C10シクロアルキル基もしくはアルケニル基または不規則に置換された炭素環式もしくは複素環式アリール基を表すか、またはCO2R、CONR2、COSR、CS2R、C(NH)NR2、CN、CHal3、ArO、ArS、RO、RS、CHO、OH、NHR、NR2、Cl、F、Br、I、またはSiR3の群から選択された基に対応する)に関する。  (もっと読む)
(もっと読む)
無水環状ホスホン酸の製造法
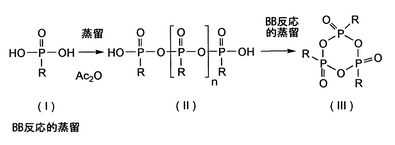
式(III)の無水環状ホスホン酸を、a)式(I)のホスホン酸誘導体を無水酢酸と30〜150℃で、酢酸と無水酢酸の混合物を蒸留により除去しながら反応させ、b)次いで、工程a)で得られた式(II)のオリゴマー状無水ホスホン酸を反応的蒸留にかけ、対応する式(III)の環状三量体状無水ホスホン酸に転化することにより、製造する方法を開示する。ここで、nは0〜300の数であり、Rは、アリル、アリール、または開鎖、環状、または分岐したC1〜C8アルキル基、アリールオキシ、アリルオキシ、または開鎖、環状、または分岐したC1〜C8アルキル基を含んでなるアルコキシである。好ましくは、工程b)で形成された環状三量体状無水ホスホン酸を、環状三量体状無水ホスホン酸に対して不活性な挙動を示す有機溶剤に直ちに溶解させる。 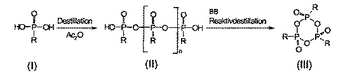 (もっと読む)
(もっと読む)
無水アルキルホスホン酸類を用いた、アルコール類から水の脱離によるアルケン類の製造方法
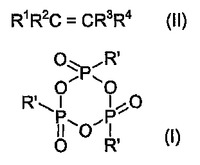
本発明は、a)一級アルコール類(R1R2CHCH2‐OH)またはb)二級アルコール類(R1R2CHCHR3‐OH)またはc)三級アルコール類(R1R2CH‐CR3R4OH)と環状無水アルキルホスホン酸類との−100〜+120℃の範囲内の温度における反応による、式(II)のアルケン類の製造方法に関し、ここでRおよび/またはR1および/またはR2および/またはR3および/またはR4はH、直鎖または分岐C1‐C12アルキル基、C3‐C10シクロアルキル基、アルケニル基、アリール基またはヘテロアリール基を表わす。好ましくは、式(I)の2,4,6‐置換1,3,5,2,4,6‐トリオキサトリホスフィナン 2,4,6‐トリオキシドが環状無水ホスホン酸として用いられ、ここでR′は(互いに独立して)アリル、アリールまたは開鎖もしくは分岐C1‐C12アルキル基を表わす。場合により反応は三級アミン塩基NR53の存在下で行われる。
R1R2C=CR3R4 (II)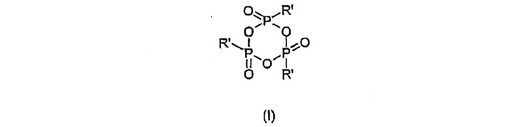
 (もっと読む)
(もっと読む)
無水アルキルホスホン酸類でのアルデヒドオキシム類から水の脱離によるニトリル類の製造方法
本発明は、アルデヒドオキシム類(R1CH=N‐OH)を環状無水アルキルホスホン酸類と−100〜+120℃の範囲内の温度で反応させることによる、式(II)R1‐CNのニトリル類の製造方法に関し、ここでR1はH、直鎖または分岐C1‐C12アルキル基、C3‐C10シクロアルキル、アルケニル、アリールまたはヘテロアリール基を表わす。好ましく用いられる環状無水アルキルホスホン酸は式(I)の2,4,6‐置換1,3,5,2,4,6‐トリオキサトリホスフィナン 2,4,6‐トリオキシドであり、ここでR′は独立してアリル、アリールまたは開鎖もしくは分岐C1‐C12アルキル基を表わす。場合により、反応は三級アミン塩基NR23の存在下で行われる。
 (もっと読む)
(もっと読む)
第一級および第二級アルコールをアルキルホスホン酸無水物で酸化することによる、アルデヒド類およびケトン類の製造方法
本発明は、a.)式(II)のアルデヒド類:R1−CHOおよびb.)式(III)のケトン類:R1−C(O)−R2を、a.)第一級アルコール(R1CH2−OH)またはb.)第二級アルコール(R1−CH(OH)−R2)と、環状ホスホン酸無水物とを、ジアルキル−、ジアリール−および/またはアルキルアリールスルホキシドの存在下で、−100〜+120℃の温度で反応させることにより製造する方法であって、式中、R1および/またはR2は、それぞれ、H、置換された線状または分枝状C1〜C12−アルキルラジカル、置換されたC3〜C10−シクロアルキル、−アルケニル、−アリール、または−ヘテロアリールラジカルである。環状ホスホン酸無水物が、好ましくは式(I)の2,4,6−置換された1,3,5,2,4,6−トリオキサトリホスフィナーネ(式中、R’は、独立してアリル、アリールまたは開鎖もしくは分枝のC1〜C12−アルキルラジカルである)として用いられる。所望により、反応は、3級アミン塩基NR53の存在下で行うことができる。
 (もっと読む)
(もっと読む)
無水プロパンホスホン酸の脱水反応によるニトリルおよびイソニトリルの製造法
本発明は、a)式(II)のニトリルおよびb)式(III)のイソニトリルを製造する方法であって、a)カルボン酸アミド(RCO−NH2)、カルボン酸のアンモニウム塩(RCOO−NH4+)またはカルボン酸を、アンモニアまたはアンモニウム塩の存在下(RCOOH+NH3、RCOOH+NH4+)で、またはb)ホルムアミド(H−CO−NHR)またはアミンとギ酸の混合物を、無水環状ホスホン酸と、水を除去しながら、温度−30〜+120℃で反応させる、方法に関し、ここでRは、任意に置換された直鎖状または分岐鎖状のC1〜C8アルキル基、C3〜C10シクロアルキル、アルケニル基、アルキニル基またはアリール基またはヘテロアリール基である。無水環状ホスホン酸としては、式(I)の2,4,6−置換された1,3,5,2,4,6−トリオキサトリホスフィナン2,4,6−トリオキシドを使用し、式中、x=3、4または5であり、R’は、それぞれ独立して、開鎖の、または分岐した、飽和または不飽和の直鎖状C1〜C16アルキル基、あるいは環状C3〜C16アルキル基、またはアリールもしくはヘテロアリールである。  (もっと読む)
(もっと読む)
1 - 8 / 8
[ Back to top ]

