干渉物質の存在下でサンプルを分析する方法及び装置
【課題】干渉物質の存在下でサンプルを迅速で正確に分析する方法及び装置を提供すること。
【解決手段】本方法は、生理学的サンプルを電気化学セルに導入し、第1過渡電流及び第2過渡電流を測定する。第1ピーク電流値及び第2ピーク電流値からピーク電流値を取得して、このピーク電流値を用いて電流値から干渉物質の影響を低減する。この「補正」電流値に基づき、正確な検体濃度を決定できる。
【解決手段】本方法は、生理学的サンプルを電気化学セルに導入し、第1過渡電流及び第2過渡電流を測定する。第1ピーク電流値及び第2ピーク電流値からピーク電流値を取得して、このピーク電流値を用いて電流値から干渉物質の影響を低減する。この「補正」電流値に基づき、正確な検体濃度を決定できる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、干渉物質の存在下でサンプルを迅速で正確に分析する方法及び装置に関する。
【背景技術】
【0002】
LifeScan社から入手可能なOneTouch(登録商標)Ultra(登録商標)全血試験キットなどで使用される電気化学的グルコース試験片は、糖尿病患者から採取した血液サンプル中のグルコース濃度を測定するように設計されている。グルコースの測定は、フラボ酵素グルコースオキシダーゼ(GOx(ox))による特異的酸化に基づく。この反応の間、酵素は還元され、(GOx(red))となる。酵素は、酸化された媒介物質フェリシアニド(Fe(CN)63−)と反応して再酸化され、フェリシアニド(Fe(CN)63−)自体はこの工程、即ち反応時に還元される。これらの反応の概要は以下の通りである。

【0003】
2本の電極の間に試験電位を印加して上記の反応が行われると、電極面で還元された媒介物質(フェロシアニド、即ちFe(CN)64−)が電気化学的に再酸化することにより電流が流れる可能性がある。理想的な環境では、上記の化学反応時に生成されるフェロシアニドの量は、電極間に存在するサンプル中のグルコースの量と正比例するため、生成された電流は、サンプルのグルコース含有量と比例することになる。フェリシアニドなどの媒介物質とは、グルコースオキシダーゼなどのレドックス酵素と電極間で電子を交換する化合物である。他の種類のグルコース試験片では、ピロロキノリンキノン(PQQ)補助因子を用いた酵素グルコースデヒドロゲナーゼをグルコースオキシダーゼの代わりに使用することができる。グルコース濃度が増加すると、生成される還元された媒介物質の量も増加することから、グルコース濃度と還元された媒介物質の再酸化により発生する電流の間には直接の因果関係がある。特に、電気的境界面(electrical interface)を越えた電子の移動が電流の流れとなる(1モルのグルコースが酸化されるごとに2モルの電子が移動する)。このことから、グルコースの導入により生じた電流を、検体電流、より具体的には、グルコース電流と呼ぶことがある。
【0004】
血液中のグルコースレベルを監視することは、糖尿病などの疾病を管理する上で重要な手段となることから、上述の原理を用いた、試験用計量器が普及している。試験時に生成されるグルコース電流は、試験用計量器により記録され、簡単な数式に基づいて電流をグルコース濃度に対応させる所定のアルゴリズムを用いて、グルコース濃度表示値に変換される。一般的に、試験用計量器は、電極と試薬を含むサンプル反応チャンバを有した使い捨ての試験片と共に動作する。使用時、使用者が、サンプル反応チャンバに少量の血液を注入すると試験用計量器が分析を行い、使用者に血糖値を知らせるようになっている。
【0005】
電気化学的な意味において、試験用計量器は二重の機能を有している。第1は、分極試験電位(0.4V)を印加して、電気的境界面を分極させ、2つの作用電極面の間にセル電流が流れるようにすることである。第2は、試験用計量器がセル電流を計測できることである。したがって、試験用計量器は、実際には、グルコースの測定を容易にし、および/または試験用計量器のその他の機能を実行するために、3本目、場合によっては4本目の電極を用いることがあるが、2本の電極モードで動作する簡単な電気化学的システムとして考えることができる。
【0006】
多くの場合、上記の化学反応式は、試験片に発生する化学反応を十分に近似しており、相当に正確なグルコース濃度の表示値を得ることができると考えられる。しかしながら、特定の状況で特定の目的の下において、例えば、電極で測定される電流の一部にサンプル内のその他の薬物または化合物の存在によるものが含まれる場合などでは、測定精度の向上が有利である場合がある。このような薬物または化合物が存在する場合、それらを干渉物質と呼び、この結果生じる追加的な電流を干渉電流(interferent current)と呼ぶことができる。
【0007】
考えられる干渉物質(即ち、試験電位が印加された際に干渉電流を生成する可能性のある血液などの生理学的流体に存在する化合物)の例として、アスコルビン酸塩、尿酸塩、アセトアミノフェン(Tylenol(登録商標)またはパラセタモール)などがあげられる。試験用計量器に干渉電流が生成される第1のメカニズムは、媒介物質(例えば、フェリシアニド)の還元により一つ以上の干渉の原因となる化合物が酸化されることである。更に、こうして還元された媒介物質は作用電極で酸化され得る。この第1のメカニズムは、間接干渉電流と呼ぶこともできる。試験用計量器に干渉電流が生成される第2のメカニズムは、作用電極において一つ以上の干渉物質が酸化されることである。第2のメカニズムは、直接干渉電流と呼ぶことができる。こうして、測定されるセル電流に、干渉物質から生じる望まない電流成分が含まれる。
【発明の開示】
【発明が解決しようとする課題】
【0008】
干渉物質の影響を削減するために使用可能な方法は、第1作用電極と基準電極と共に第2作用電極を使用することである。第2作用電極が剥き出しの状態であれば、第2作用電極は直接干渉電流を測定することができる。第1作用電極は、グルコース電流、直接干渉電流及び間接干渉電流の合計を含む電流を測定するため、酵素と媒介物質を含むようにする。第2作用電極で測定した直接干渉電流を第1作用電極で測定した電流から引くと、干渉物質の影響を削減できる。
【0009】
代替或いは追加的として、第2(又は第3)作用電極を媒介物質(しかし酵素ではない)で被覆して、第2作用電極が直接及び間接干渉電流の合計(しかしグルコースは入らない)を含む電流を測定できるようにする。この場合、第2作用電極で測定した直接及び間接干渉電流を第1作用電極で測定した電流から引くと干渉物質の影響を削減できる。
【0010】
ユーザが提供する血液サンプルを少量で済ませるため、サンプル反応チャンバは小型の方が好ましい。干渉物質の影響を補償するために第2(または第3)作用電極を用いる欠点は、第2作用電極は、サンプル反応チャンバの容積を相応に増加することである。更に、第2作用電極を用いると、構造が複雑となり、製造コストの増加を招くという欠点がある。したがって、2本の電極のみを用いて干渉物質の影響を受けずにグルコースを測定する方法の開発が必要とされている。
【課題を解決するための手段】
【0011】
本発明は広義には、生理学的サンプル中の検体濃度を電気化学的に決定する方法及び装置を提供する。一態様において、本明細書中に記載の方法は、電気を印加し、電流を測定する試験片を用いる。本方法は、こうして測定した電流値に基づいて、干渉物質の影響を最小限にしながら、迅速に検体濃度を測定できる。
【0012】
一実施の形態において、本方法は、生理学的サンプルを電気化学セルに導入するステップを含んでなる。例えば、相互に離間した第1及び第2電極と試薬とを備えたセルなど、様々な電気化学的セルを使用できる。一旦サンプルが付着すると、本方法は、第1の極性を有する第1試験電位を反応セルに印加し、セル電流を時間関数として測定し、第1過渡電流を得る。第1の極性とは反対の第2の極性を有する第2試験電位をセルに印加し、セル電流を時間関数として測定することによって、第2過渡電流を得る。
【0013】
次に第1及び第2過渡電流を分析し、第1過渡電流から第1ピーク電流値を決定し、第2過渡電流から第2ピーク電流値を決定する。第1ピーク電流値及び第2ピーク電流値に基づいて、サンプル中の干渉物質の影響を決定できる。
【0014】
一実施の形態において、干渉物質の影響は、第1ピーク電流値及び第2ピーク電流値を用いて電流値を補正することによって減少する。例えば、補正電流値は、第2過渡電流から導出した第1電流値を修正することによって決定できる。こうして得られた補正電流値は、干渉物質に起因する電流成分を除去した第1電流値を表せる。
【0015】
一態様において、干渉物質からの第1電流値への寄与は、第1電流値と干渉物質補正係数とを積算することによって、(少なくとも部分的に)除去する。干渉物質補正数式は、

であり、ipbは第1ピーク電流値、ipaは第2ピーク電流値、issは定常電流値である。
【0016】
補正電流値を用いて検体濃度を決定できる。例えば、本方法は、第2過渡電流から第2電流値を算出し、第1過渡電流から第3電流値を算出するステップを含むことができる。検体濃度は、数式

から得ることができる。[C]が検体濃度、i4が第1補正電流値、i2が第2電流値、i3が第3電流値、a、p及びZが補正係数である。
【0017】
本明細書に開示される他の実施の形態において、検体濃度は数式

に基づいて決定され、[C]が検体濃度、ippが第1過渡電流から導出される電流値、Coがグルコース濃度概算値、Zが較正係数、ipaが第1ピーク電流値、ipbが第2ピーク電流値、issが定常電流値である。一代替態様において、ippは、第1過渡電流終端近傍の短時間期間にわたる電流の平均値である。
【0018】
本明細書に開示された他の実施の形態は、検体と干渉物質の両方を含有した生理学的サンプルにおける検体濃度を決定する方法である。当該方法は、電気化学的セルに生理学的サンプルを導入し、第1の極性を有する第1試験電位を反応セルに印加する。セル電流値を時間関数として測定し、第1過渡電流を得る。次に、開回路電位時間期間を経過させる。開回路電位時間期間が経過した後、第2の極性を有する第2試験電位を印加することによって、第2過渡電流を測定する。
【0019】
第1過渡電流及び第2過渡電流に基づいて、第1ピーク電流値及び第2ピーク電流値が得られる。第2ピーク電流値から第1ピーク電流値を減算して、サンプル内の検体濃度と比例する補正電流を決定する。補正電流を用いて検体濃度を算出する。
【0020】
例えば、検体濃度は、数式

に基づいて算出できる。[C]が検体濃度、ipaが第1ピーク電流値、ipbが第2ピーク電流値、slope及びinterceptが較正係数である。他の態様において、数式は、反応キネティクスを考慮して、以下の数式に修正できる。

[C]が検体濃度、ipaが第1ピーク電流値、ipbが第2ピーク電流値、i2が第2過渡電流から導出される電流値、i3が第1過渡電流から導出される電流値、slope及びinterceptが較正係数である、
【0021】
更に他の実施の形態は、検体と干渉物質の両方を含有した生理学的サンプルにおけるヘモグロビン濃度を決定する方法である。当該方法は、電気化学的セルに生理学的サンプルを導入し、第1の極性を有する第1試験電位を前記セルに印加するステップを含んでなる。セル電流値を時間関数として測定し、第1過渡電流を得る。次に、第2の極性を有する第2試験電位を印加し、セル電流値を時間関数として測定することによって、第2過渡電流を測定する。
【0022】
第1過渡電流に基づいて、第1定常電流を決定し、第2過渡電流に基づいて第2定常電流を決定する。第2定常電流値から第1定常電流値を減算し、ヘモグロビン濃度に比例する電流値を得る。
【0023】
一態様において、ヘモグロビン濃度は
数式

に基づいて算出される。
[H]が、検体濃度、issaが前記第1過渡電流からの定常電流、issbが前記第2過渡電流からの定常電流、slope及びinterceptが較正係数、Fがファラデー定数、Aが第1電極の面積、Dがレドックス活性分子の拡散係数、Lが電極の間隔である。
【発明を実施するための最良の形態】
【0024】
本発明の方法および装置は、種々多様なサンプル中の種々多様な検体の測定に使用するのに適しており、特に対象となる検体がグルコースである場合に、全血またはその誘導物中の検体を測定するのに特に適している。本発明は、迅速な方法で正確な測定結果を得ることができる生理学的サンプル中の検体濃度値を測定する方法を提供する。本明細書では、検体濃度値の測定に使用できる代表的な実施の形態の試験片の構造について説明する。さらに、本明細書では、試験片に発生する過渡電流を試験片と電気的に接続した計量器によって測定し収集する、試験片を用いた方法について説明する。さらに、本明細書では、迅速な方法で過渡電流を処理するために用いられ、正確な検体濃度を出力するアルゴリズムについて説明する。さらなる態様において、干渉物質の影響を削減するように検体濃度を測定する方法について説明する。
【0025】
本発明の方法は、原理的には、離間した第1及び第2電極を有する如何なる種類の電気化学セルと共に用いることができる。本明細書では、本発明を例示するため、対向する電極を用いた特定の実施の形態について説明する。しかしながら、本発明は、同一平面上の電極を用いたセルなど、他の構成の電極を用いたセルにも同様に適用可能であることが理解される。適用しなくてはならない唯一の構成上の制限は、干渉電流の測定が検体(例えばグルコース)の反応により生成される電気活性種からの影響をほとんど受けることのないように電極は配置される必要があるという点である。これは通常、検体の反応により生成される電気活性種が、干渉電流を測定する電極に、干渉電流の測定前または測定時中に到達する時間のないように電極を十分に離間することにより達成される。
【0026】
以下、図1A〜図4Bを参照して、様々な実施の形態の、近端部80から遠端部82へ長手方向軸Lに沿って延在し、側縁部56、58を含む伸長体59を有する試験片62の形状のかかる装置について説明する。伸長体59は、電極164、166と試薬72を含有する電極近端側サンプル反応チャンバ61を含むことができる。試験片伸長体59は遠端側にさらに、試験用計量器(図示されてない)と電気的に接続する電気的接点63、67を含むことができる。
【0027】
一態様において、試験片62は、第1導電層66、スペーサ層60、第2導電層64を含む多層から形成される。第1導電層66及び/又は第2導電層64は、一実施の形態では、絶縁シート(図示されてない)に配置された様々な導電性材料から形成できる。スペーサ層60は、様々な電気絶縁性材料から形成でき、接着剤を含む、又は接着剤から形成されてもよい。三層の試験片が図示されているが、追加の導電層または絶縁層を用いて、試験片伸長体59を形成できることは当業者には明らかである。
【0028】
図1A〜図1Cに示すように、近端側サンプル反応チャンバ61は、第1導電層66、第2導電層64及びスペーサ層60により画定できる。以下により詳細に説明するように、反応チャンバ61はまた、試薬72、第1及び第2電極166、164を含むことができる。例えば、スペーサ層60の切り欠き領域68は、第2導電層64と第1導電層66の一部を露出させることにより、第1電極166と第2電極164をそれぞれ形成できる。一形態として、試薬72は第1電極166上に形成した層でもよい。
【0029】
一実施の形態において、反応チャンバ61は少量のサンプルを分析するようになっている。例えば、サンプル反応チャンバ61の容量は、約0.1μl(microliter)乃至約5μlの範囲、好ましくは、約0.2μl乃至約3μlの範囲、より好ましくは、約0.3μl乃至約1μlの範囲とできる。少量のサンプルを収容するため、電極は近接していることが好ましい。例えば、スペーサ層60は、第1電極166と第2電極164間の距離を画定する場合、スペーサ層60の高さが約1ミクロン(micron)乃至約500ミクロンの範囲、好ましくは、約10ミクロン乃至約400ミクロンの範囲、より好ましくは、約40ミクロン乃至約200ミクロンの範囲とできる。
【0030】
反応チャンバ61の一層の容積削減を支援するため、切り欠き領域68及び/又は伸長体59の長手方向及び/又は側方向の寸法を調節することができる。例えば、試験片伸長体59は、反応チャンバ61の側方向の幅が試験片伸長体59の全幅(最大幅)より小さくなるように、切り取り部51、52を有することができる。切り取り部51、52はまた、反応チャンバ61へのサンプルの送入を容易できる。例えば、切り取り部51、52は、使用者の指の一部に対応した形状を有することができる。使用者が指を刺して絞り出した血液を採取する際、切り取り部51、52は、使用者が自身の指に付着した血液サンプルを伸長体59の側縁部56、58のサンプル注入口(例えば、開口部70)の位置に合わせやすくできる。2つの切り取り部が図示されているが、当業者には、試験片伸長体59は、切り取り部を一つのみ有してもよいし、或いは切り取り部を有さなくてもよいことは明らかである。
【0031】
上述したように、試験片伸長体59の近端部は、サンプルを反応チャンバ61に注入するための少なくとも一つのサンプル注入口を有することができる。例えば、切り欠き領域68は、試験片伸長体59の側縁部56、58から横方向に延在し、生物学的流体をサンプル反応チャンバ61へ注入する二つの開口部70を形成できる。二つの開口部70が存在すると、一方を、サンプルをサンプル反応チャンバ61に注入するサンプル注入口として機能させながら、他方を通気口として機能させることができる。当業者には、例えば、第1及び/又は第2導電層66、64にサンプル注入口および/または通気口を設けるなど、試験片伸長体59内の上記とは異なる場所にサンプル注入口及び/又は通気口を設けた代替の構造体を用いてサンプルをサンプル反応チャンバ61へ注入することが可能であることは明らかである。
【0032】
一実施の形態において、試験片62は、毛細管現象によりサンプルを反応チャンバ61へ引き入れるようになっている。例えば、反応チャンバ61と開口部70の寸法と表面の特性は、液体サンプル(例えば、全血)が開口部70の一つと接触する際に毛細管力を生成するようにできる。当業者には、反応チャンバ61には、例えば、ビーズ、多孔性膜及び/又はその他の充填物など、毛細管力を補助/生成するための構造体を含められることは明らかである。
【0033】
上述のようにして、試薬72などの試薬を反応チャンバ61内に付着できる。試薬72の組成は、目的とする検体及び希望するサンプルの形態に応じて変更できる。一態様において、試薬72は、少なくとも一つの媒介物質及び酵素を含み、第1電極166に付着する。適当な媒介物質の例として、フェリシアニド、フェロセン、フェロセン誘導物、オスミウムビピリジル錯体及びキノン誘導物が挙げられる。適当な酵素の例として、グルコースオキシダーゼ、ピロロキノリンキノン(PQQ)補助因子をベースとしたグルコースデヒドロゲナーゼ(GDH)、ニコチンアミドアデニンジヌクレオチド補助因子をベースとしたGDHが挙げられる。試薬層72を生成するために適した代表的な試薬配合物については、参照によりその全開示内容が本明細書に援用される、「滅菌され、較正されたバイオセンサーベースの医療デバイスの製造方法」と題した係属中の米国特許出願第10/242,951号、米国特許公開番号第2004/0120848号に記載している。
【0034】
近端側サンプルチャンバ61に対して遠端側に位置する伸長体59は、第1及び第2電極166、164を遠端側電気的接点63、67と電気的に接続する接続トラックを有することができる。一態様において、第1導電層66は、第1電極166を第1電気的接点67と電気的に接続する第1接続トラック76を有する。同様に、第2導電層64は、第2電極164を第2電気的接点63と電気的に接続する第2接続トラック78を有する(図1B)。
【0035】
第1及び第2導電層はまた、試験片62と試験用計量器との電気的接触を容易にする第1及び第2電気的接点67、63を画成できる。一実施の形態では、第1導電層66の一部は、スペーサ層60及び第2導電層64の遠端部から更に遠端側へ延在し、第1電気的接点67を画成する。第2電気的接点は63、第2導電層64の一部を露出する第1導電層66に形成されたU字形状切り込み部65により画成できる。当業者には、試験片62は、試験用計量器と電気的に接続する他の様々な代替可能な電気的接点構成を有することができることは明らかである。例えば、参照によりその全開示内容が本明細書に援用される、米国特許第6,379,513号には、電気化学セル接続構造体が開示されている。
【0036】
図5は、試験片62の第1電極166及び第2電極164とそれぞれ電気的に接続する、第1電気的接点67及び第2電気的接点63と接する試験用計量器100の簡略図である。試験用計量器100は、第1電極166及び第2電極164と、それぞれ第1電気的接点67及び第2電気的接点63を介して電気的に接続するようになっている(図2および図5を参照)。一態様において、試験用計量器100は、第2電気的接点63とU字形状切り込み部65を介して接触する。
【0037】
図5に示すように、電気的接点67は、67a及び67bと付された2本のプロング(prong)を有することができる。代表的な一実施の形態では、試験用計量器100が試験片62と接すると回路が完結するように、試験用計量器100はプロング67a、67bと別々に接続する。試験用計量器100は、プロング67a及び67b間の抵抗又は電気的導通を測定して、試験片62が試験用計量器100と電気的に接続しているか否かを判断できる。当業者には、試験用計量器100は、様々な代替可能なセンサ及び/又は回路を用いて、試験片62が試験用計量器100に対して適切に配置されているか否かを判断できることは明らかである。
【0038】
試験用計量器100はまた、反応チャンバ61内の流体の存在を検出するように構成することもできる。例えば、試験用計量器100が試験片62が挿入されたことを認識すると、試験用計量器100は、第1電極166と第2電極164間に定電流(例えば、1μAの電流)を流すことができる。開始時に反応チャンバ61は乾燥しているため、試験用計量器100は最大電圧を印加して、所望の電流を得るようにしてもよい。しかしながら、一旦生理学的サンプルが使用者により注入口70に投与されると、サンプル反応チャンバ61は満たされる。生理学的サンプルが第1電極166と第2電極164間の間隙を満たすと、試験用計量器100は、所定の閾値を下回る測定電圧の低下を検出する(米国特許第6,193,873号参照)。
【0039】
幾つかかのケースにおいて、生理学的流体が付着したことを認識したとしても、サンプル反応チャンバ61が完全に満たされたことを示すとは限らず、サンプル反応チャンバ61内における生理学的流体の一部の存在の確認のみを意味する場合もある。試験用計量器100が、生物学的流体が試験片62に付着されたと判断すると、生理学的流体がサンプル反応チャンバ61を完全に満たすように短い時間であるが、限られた時間待機することができる。
【0040】
一旦生理学的サンプルが試験片62に投与されると、試験用計量器100は、開回路電位と複数の試験電位をそれぞれ所定の時間期間印加することにより、グルコース試験を実行できる。例えば、グルコース試験はグルコース試験時間期間TGにわたり実行でき、グルコース試験時間期間TGは、開回路時間期間TOC、第1電位時間期間T1及び第2試験電位時間期間T2を連続して含むことができる。図6は、3つの時間期間を含む代表的な試験を表すグラフである。
【0041】
以下の本発明の実施の形態において、一連の時間期間は全体で、5秒間のグルコース試験時間期間TGを表す。しかしながら、グルコース試験時間期間は変更可能であり、例えば、5秒間を上回る、或いは下回る時間期間も含む。一態様において、グルコース試験時間期間TGは、約1秒乃至約10秒の範囲とすることができ、好ましくは約2秒乃至約8秒の範囲とすることができ、より好ましくは約3秒乃至約6秒の範囲とできる。グルコース試験は、開回路時間期間TOCでサンプル反応チャンバ61を充填できる。開回路時間期間TOCは、サンプルの性質(例えば、粘性、組成など)、サンプル反応チャンバの寸法及び物理的特性、及び/又は充填方法の違い(例えば、毛細管現象の強さ)に応じて変更できる。例えば、周囲温度が低く(例えば、約5℃)及び/又はヘマトクリット値が高い(例えば60%を超える)ため、血液サンプルが粘性の可能性のある場合、追加の開回路時間を要することがある。本発明の一実施の形態では、開回路時間期間TOCは、約0.1秒乃至約2秒の範囲でよく、好ましくは約0.3秒乃至約1.5秒の範囲でよく、より好ましくは約0.5秒乃至約1秒の範囲でよい。
【0042】
一旦開回路時間期間TOCが経過すると、試験用計量器100は、第1電極166と第2電極164の間に第1試験電位E1を第1試験電位時間期間T1の間印加できる。第1試験電位時間期間T1が経過すると、試験用計量器100は、第1電極166と第2電極164の間に第2試験電位E2を第2試験電位時間期間T2の間印加できる。T1及びT2の間、試験用計量器100はセル電流を第1試験電位時間期間T1の間ia(t)で、第2試験電位時間期間T2の間ib(t)で表される時間関数として測定することができ、これらを時間−過渡電流又は過渡電流と呼ぶ。
【0043】
一実施の形態において、第1試験電位E1は第1の極性を有し、第2試験電位E2は第2の極性を有し、第1の極性は第2の極性の反対である。更に、第1試験電位E1は、限界酸化電流が測定される作用電極として第2電極164が機能するように、第2電極164に対して十分に負の大きさを持つことができる。酸化可能な種は作用電極面で局所的に枯渇し、酸化電流の測定値はバルク溶液から作用電極面の方向へ拡散する酸化可能な種の流れに比例するようになる。ここで「バルク溶液」とは、酸化可能な種が枯渇ゾーン内に存在しなくなった作用電極から十分に離れた溶液の一部を意味する。同様に、第2試験電位E2は、限界酸化電流が測定される作用電極として第1電極166が機能するように、第2電極164に対して十分に正の大きさを持つことができる。一実施の形態では、第1試験電位E1及び第2試験電位E2は、約−0.6ボルト乃至約+0.6ボルトの範囲とできる。第1試験電位E1が負である場合、試薬72は第1電極166に設けることができる。
【0044】
図6に、代表的な一グルコース試験時間期間TGをグラフで示す。ここで第1試験電位E1には−0.3ボルトを印加し、第2試験電位E2には+0.3ボルトを印加できる。第1試験電位時間期間T1は3秒であり、第2試験電位時間期間T2は1秒であった。第2試験電位E2は第1試験電位E1を印加した直後に印加する。
【0045】
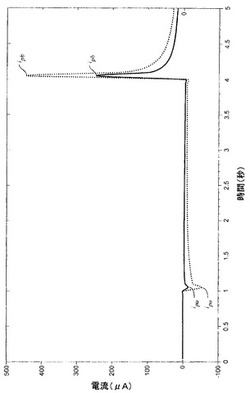
図7に、干渉物質を添加していないグルコース濃度62mg/dLの生理学的サンプル(実線)とアスコルビン酸塩濃度20mg/dLの生理学的サンプル(点線)について、図6のグルコース試験時間期間TGに基づく試験を実行して生成された第1及び第2過渡電流をグラフで示す。図8に、図7の第1過渡電流の拡大図をグラフで示す。
【0046】
試験片が、図1A〜図4Bに示す面が対向する構成を有するとした場合、グルコース濃度は、以下の数式1に示す第1グルコースアルゴリズムを用いて算出できる。
【数1】

【0047】
上記の数式1において、[G]はグルコース濃度を表し、i1は第1電流値、i2は第2電流値、i3は第3電流値、p、Z及びaは実験により得られた較正定数を表す。数式1の導出方法については、参照によりその全開示内容が本明細書に援用される、2005年9月30日に出願された「迅速な電気化学的分析方法及び装置」と題した係属中の米国特許出願第11/240,797号に記載している。
【0048】
第1電流値i1及び第2電流値i2は第2電流過度から算出することができ、第3電流値i3は第1電流過度から算出される。便宜上、「第1」、「第2」及び「第3」という名称を用いたが、当業者にはこれが電流値を算出する順番を反映すると限らないことは明らかである。数式1及び後述する数式に記載する全ての電流値(例えば、i1、i2及びi3)には、電流の絶対値を使用できる。
【0049】
第1電流値i1及び第2電流値i2は、一態様では、第2電流過度の時間期間における電流値の積分、第2電流過度の時間期間における電流値の合計、或いは第2電流過度の電流値の平均又は一つと第2電流過度の時間期間との積とできる。同様に、第3電流値i3は、一態様では、第1電流過度の時間期間における電流値の積分、第1電流過度の時間期間における電流値の合計、或いは第1電流過度の電流値の平均又は一つと第1電流過度の時間期間との積を用いることができる。電流値の合計については、所定範囲の連続した電流測定値から2つのみ、或いは電流測定値の全てを加算して求めることができる。
【0050】
他の実施の形態において、第1電流値i1、第2電流値i2及び第3電流値i3は、クーロン値で置換できる。電流を測定する代わりに、通過した電荷を測定できる。通過した電荷の合計は、電流過度の積分と同一の情報となる。例えば、通過電荷は、所定の時間期間にわたって測定でき、第1、第2及び/又は第3電流値として使用できる。
【0051】
本明細書で開示する一実施の形態の方法において、グルコース反応キネティクスは電流値(例えば、i1、i2及び/又はi3)を用いて求められる。この結果は、ヘマトクリット濃度と温度の影響を受けにくいため、高い正確さと精度でグルコース濃度を測定できる。
【0052】
一態様において、試薬層72は第1電極166上に設ける。これにより生理学的サンプルと溶解後、試薬のほとんどは第1電極166の近傍に残留する。この結果、少なくとも初期において、還元された媒介物質の多くの部分は第1電極166近傍に存在する。所定の時間期間が経過した後、グルコースとの反応により試薬層72で生成された還元された媒介物質は、第1電極166から受動的に拡散する。このプロセスの間、第1電極166と第2電極164間の媒介物質濃度の大きさは、還元された媒介物質の濃度が第1電極166でより高く、第2電極164でより低くなる勾配を形成する。第1電極166側の還元された媒介物質の濃度が大きくなる程、大きさの勾配は急になる。第1電流過度の大きさは、この勾配の大きさと比例する。したがって、試薬層72で生成された還元された媒介物質の量は、還元された媒介物質の第2電極164への拡散を促進する。電極で測定される電流の変化速度は、試薬層72における還元された媒介物質濃度の変化速度及びグルコース反応キネティクス(即ち、還元された媒介物質を生成するグルコースの反応速度)を示す。
【0053】
グルコース反応キネティクスは、電極間隔(グルコースが試薬層72へ拡散するために要する最大距離に関係する)、生理学的サンプルの粘性、ヘマトクリット濃度及び温度を含む複数の因子に左右される。
【0054】
生理学的サンプルの粘性は、ヘマトクリット値、タンパク質、脂質含有量又はそれらの組み合わせの増加とともに増加する可能性がある。ヘマトクリット値は、血液サンプル中の赤血球の比率を示す。通常、赤血球の比率が高いと、血液の粘性が高くなり、結果として赤血球中の全グルコースの比率は大きくなる。赤血球中のグルコースが試薬層72と反応するためには、グルコースは、赤血球膜を越えて移動する必要がある。特定の条件の下では、この移動は比較的緩やかであり、グルコース反応キネティクスを制限することがある。したがって、ヘマトクリット値が高くなるとグルコース反応キネティクスは遅くなる。粘性は通常、サンプル反応チャンバ61内の全体的な拡散プロセスを緩やかにする。温度が高くなると通常、関連する移動プロセスは迅速になり、サンプル反応チャンバ61内のグルコースと試薬層72との反応速度は増加する。
【0055】
電流値(i1、i2及び/又はi3)、特に電流値の比率を用いて、グルコース反応キネティクスのばらつきを補正できる。例えば、第2電流過度の大きさは一般的に第1電流過度の大きさの絶対値より大きくなる。このため、i2/i3の比率は一般的に、サンプル反応チャンバ61内でグルコース反応が進行している間は1より大きくなり、グルコース反応が完了すると1になる。i2/i3値の1との乖離は、反応完了の度合いを示す係数となる。i2/i3値が比較的大きい場合は、グルコース反応が完了までほど遠く、i2/i3値が1に近い場合は、グルコース反応は完了に近いことを意味する。したがって、i2/i3の比率は一般的にグルコース反応の進捗情報を示し、グルコース濃度の測定におけるヘマトクリット値、粘性及び温度の影響を除去するために使用できる。
【0056】
さらに計算の精度を高めるため、一以上の較正係数を使用できる。例えば、数式1に示す、i2/i3の比率をべき指数pで累乗する。ここでpは、特定のロットの試験片に使用できる較正係数である。べき指数pを用いることは、精度を向上し、試験時間を短縮するための経験的な手法から発見された。本発明の一実施の形態において、pは約0.2乃至約4の範囲、好ましくは、約0.1乃至約1の範囲とできる。
【0057】
数式1に示すように、切り欠き領域68及びスペーサ層60の高さのばらつきの可能性を表す較正係数aを使用できる。切り欠き領域68のばらつきは、測定電流の大きさを相応にシフトする原因となり得る。特定の状況では、製造工程で試験片のロット毎に電流面積のばらつきが生じることがある。同様に、スペーサ層60の高さもロット毎にばらつきが生じることがある。スペーサ層60の高さのばらつきは、試験電流に相応の影響を与える。例えば、スペーサ層60の高さが増加すると、試験電流は低下する。ロット毎に試験片の較正係数aを算出することは、電極面積及びスペーサ層60の高さのばらつきの補償に有益である。較正係数aを算出すると、因子aは、試験片のロットの較正工程で算出できる。
【0058】
一実施の形態では、数式1に示すように、バックグラウンドのばらつきを表すために較正係数Zを用いる。生理学的流体を試験片62に付加する前の試薬層72内における酸化可能な種の存在がバックグラウンド信号に寄与することがある。例えば、生理学的流体が試験片に注入される前に試薬層72が少量のフェロシアニド(例えば、還元された媒介物質)を含有していた場合、測定される試験電流はグルコース濃度とは無関係に増加する。これは、特定のロットの試験片について測定される試験電流全体の恒常的なバイアスとなる。このバイアスを補正するために較正係数Zを用いることができる。因子pと同様に、Zもまた、較正工程で算出できる。
【0059】
本明細書では較正係数p、a及びZを用いた方法について開示するが、当業者には、これらを用いることが必須でないことは明らかである。例えば、一実施の形態では、グルコース濃度は、p、a及び/又はZを用いずに算出できる(数式1において、p及び/又はaを1と等価に設定し、Zをゼロと等価に設定できる)。
【0060】
i1、i2及びi3を算出する時間期間の選択は、個別の種類の試験片毎に学習アルゴリズムに従って決定(即ち経験的に決定)できる。学習アルゴリズムを実行する際、複数の試験片について、試験時に使用者が遭遇する可能性のある範囲の条件で試験を行う。かかる条件は、20mg/dL乃至600mg/dLの範囲のグルコース濃度、0%乃至70%の範囲のヘマトクリット値、5℃乃至45℃の範囲の温度、相対湿度5%(5%RH)乃至95%RHの範囲の湿度、及び内因性及び外因性干渉物質を含んでもよい。内因性及び外因性干渉物質、及びそれらの生理学的濃度範囲の例については、参照によりその全開示内容が本明細書に援用される、Wayne著、PA.:NCCLS、1986年刊行の「National Committee for Clinical Laboratory Standards: Interferent Testing in Clinical Chemistry; proposed guideline EP7−P.」と題した刊行物に記載している。数式1を用いて算出したグルコース濃度が正確で(即ち、基準測定値の+/−10%内)、ばらつきが少なく(即ち、1σにおける試験片間のばらつきが約2%以下)なるように、標準的な最小化技術又は誤差処理技術を用いた時間期間、即ちi1、i2及びi3の選択の最適化を定義している。当業者には第1電流値、第2電流値及び第3電流値に選択した時間期間は同一でもよく、或いは異なってもよいことは明らかであり、一実施の形態では、二つの電流値のみを算出する。例えば、第2電流値i2は、第1電流値i1と同一となるように定義してもよい。
【0061】
時間期間i1、i2及びi3を選択後、試験片ロットを較正できる。試験片ロットを較正する代表的な方法については、参照によりその全開示内容が本明細書に援用される、米国特許第6,780,645号に記載している。より具体的には、較正係数a、p及び/又はZは、試験片のロット毎に算出できる。通常、複数の供与者から採血した血液中のグルコースの濃度範囲をグルコース試験片で試験し、正確で精度の高いことが知られている基準装置でも試験する。本発明の試験片により得た結果と基準法により得た結果の結果との誤差を、a、p及び/又はZの最適な組み合わせを求めて最小化する。一実施の形態では、試験片ロットから試験片を用いる前に、この較正情報を試験用計量器100へ送信し、及び/又は試験用計量器100に保存できる。
【0062】
サンプル中の干渉物質の存在を示すことができる検体濃度を算出する更なる方法について説明する。例えば、通風などの特定の疾病は人体の尿酸濃度を上昇させ、グルコース測定の精度に影響を与えることがある。尿酸塩は、作用電極面、及び/又は酸化された媒介物質により酸化されやすいため、多くの電気化学的測定において、潜在的な干渉物質となる。本発明の一実施の形態では、数式1を修正して尿酸塩などの干渉物質の存在下におけるグルコース測定精度を高めている。修正アルゴリズムを開発するため、第1過渡電流及び第2電流過度時における干渉物質の酸化に対応する数学的関係式を求めた。
【0063】
還元された媒介物質全体の濃度がグルコース試験時間期間TGの間サンプル反応チャンバ61内で変化しないと仮定した場合、第1過渡電流の電流の大きさは時間関数として以下の数式2で表すことができる。
【数2】

【0064】
issは、第1試験電位E1印加後の定常電流であり、Dは、媒介物質の拡散係数であり、Lは、スペーサ層60の厚みである。数式2においてtは第1試験電位E1を印加してから経過した時間を表す。図7の場合を例にとると、数式2で用いたtの値は、実時間から1秒引くことになる。第2電流過度の電流の大きさは時間関数として以下の数式3で表すことができる。
【数3】

第1試験電位E1と極性が反対の第2試験電位E2を第1試験電位E1の直後に印加しており、この第2試験電位E2から第2電流過度が生成されるため、数式3の指数項には数式2の指数項と異なる係数が2つある。数式3において、tは第2試験電位E2を印加してから経過した時間を表す。図7の場合を例にとると、数式3で用いたtの値は、実時間から4秒引くことになる。―0.3Vの第1試験電位E1を印加している間、第2電極164では干渉物質が酸化され、これにより、第1電極166では還元された媒介物質が生成される。還元された媒介物質が第1電極166で蓄積されるため、第2試験電位E2印加時の初期電流が指数項で2倍の大きさになる。
【0065】
図9に、サンプル反応チャンバ61内の濃度勾配をグラフで示し、数式2の指数項と数式3の指数項を比較した場合の2つの係数の違いを説明する。還元された媒介物質全体の濃度がグルコース試験時間期間TGの間サンプル反応チャンバ61内で変化しないと仮定した場合、酸化可能な種の濃度は、第1試験電位E1が試験片62に印加される前にサンプル反応チャンバ61内全体で均一になる必要がある。図9上で円で描いた複数の点は、濃度が1であることを示し、酸化可能な種の正規化濃度が一定であったことを表す。この初期濃度をバルク濃度と呼ぶことができる。第1試験電位E1が一旦印加されると、第2電極164における酸化可能な種の正規化濃度は直ちに枯渇し、濃度は0となる。図9において、第2電極164の表面はX軸上でゼロとして表され、第2電極164から第1電極66への正規化距離はX軸上で1として表されることに留意されたい。
【0066】
第1試験電位E1の印加後、酸化可能な種の正規化濃度は、第1電極166でバルク濃度の2倍となり、この場合では2となる。図9上で四角で描いた複数の点は、サンプル反応チャンバ61内の濃度勾配が線形であることを示し、酸化可能な種の正規化濃度は第1電極166で最大で、第2電極164で最小である。サンプル反応チャンバ61内における電荷保存則により、第2電極164で酸化可能な種が消費される毎に、第1電極166では酸化可能な種が生成される。このため、第1電極166における酸化可能な種の正規化濃度は、第1試験電位E1の印加後、2となる。
【0067】
第2試験電位E2を印加すると短時間後に電流は、E1を印加してから同様の時間が経過した時点の電流から定常電流を引いた値の2倍となる。2倍となる理由は、第1電極166の酸化可能な種の初期濃度がバルク濃度の2倍となるためである。反対に、第1試験電位E1を印加する前の第2電極164における酸化された種の初期の正規化濃度は半分に過ぎず、この場合、バルク濃度であった。定常電流を引く理由は、2本の電極間に存在する酸化可能な種の勾配により第1電極166から離間する電子の流れがあるためである。
【0068】
図7に示すように、第1試験電位時間期間T1にはipaで示すピーク電流があり、第2試験電位時間期間T2にはipbで示すピーク電流がある。第1ピーク電流ipa及び第2ピーク電流ipbは共に、第1試験電位E1及び第2試験電位E2を印加した後短時間後、例えば、0.1秒後にそれぞれ測定された。数式3から数式2を引いて数式4を導くことができる。
【数4】

【0069】
数式2に2を乗じて、加算の項を相殺したことに留意されたい。数式4は、試験片62を干渉物質を含むがグルコースを含まないサンプルで試験した場合の第1過渡電流と第2過渡電流との関係を示す。サンプル中にグルコースが含まれない場合、試薬層72はグルコース試験時間期間TG時に還元された媒介物質を生成しない。従って、第1及び第2過渡電流は両方とも干渉物質の酸化のみを反映することになる。上述の説明から、第1及び第2ピーク電流と定常電流の関係は、基本的な電気化学的数式に基づいて、或いは口頭/図形の発見的な議論により導出できることは明らかである。数式4は両方の方法から導き出せる。
【0070】
開回路時時間期間TOCを用いて、ピークが第1試験電位E1を印加した直後に形成されるよう第1ピーク電流値ipaの先鋭度を高めてもよい。公称開回路時間期間TOCはサンプル反応チャンバを完全に充填可能な時間である。更に、公称開回路時間期間TOCは、試薬層72が溶解され、酸化された媒介物質が第1電極166により還元され、限界酸化電流が第2電極164で測定できる時間である。
【0071】
第1及び第2過渡電流の大きさは、試薬層72がグルコース試験時間期間TG時に還元された媒介物質を生成する場合、より複雑な関係を有する。約1.1秒後の早い時期には、試薬層72がグルコース反応による還元された媒介物質を大量に生成しないと仮定する。更に、生成された還元された媒介物質のほとんどは、最初に試薬層72が付着していた第1電極166の近傍に残り、第2電極164へ拡散するものはわずかである仮定する。したがって、ipaの大きさの大部分は、第2電極164における干渉物質の酸化に起因する直接的な干渉電流である。
【0072】
約4.1秒後の遅い時期には、試薬層72がグルコースの存在する第1電極166においてグルコース反応によって還元された媒介物質を大量に生成すると仮定する。また、酸化された媒介物質により干渉物質が酸化される可能性があるため、大量の還元された媒介物質が生成される可能性はある。上述のように、酸化された媒介物質を還元する干渉物質は電流に寄与し、こうして生じる電流は間接電流と呼ぶことができる。更に、干渉物質はまた、第1電極164で直接酸化される可能性があり、こうして生じる電流は直接電流と呼ぶことができる。媒介物質が作用電極で酸化される可能性のある状況では、直接酸化と間接酸化の合計は、酸化された媒介物質が作用電極に付着しなかった場合に測定された直接酸化電流とほぼ等しいと仮定できる。要約すると、ipbの大きさは、間接的及び直接的な干渉物質の酸化、及び第2電極164におけるグルコース反応に起因する。ipaは、主に干渉物質により制御されると判断されるため、ipbをipaと共に用いて、補正係数を決定できる。例えば、以下に示すように、ipbをipaと共に用いた数学的関数により、グルコースと比例するが干渉物質の影響を受けにくい補正電流を決定できる。
【0073】
グルコースに比例するが、干渉物質に起因する電流の相当成分を除去した電流i4を算出するため、数式5を実験により導き出した。
【数5】

【0074】
issを分子及び分母の両方に加算し、グルコースが存在しない場合でも分子がゼロに近づくようにした。issは、最小時間を上回る時間の電流について、数式5Bを用いて概算でき、適当な最小時間は数式5Cから概算できる。
【数5B】

【数5C】

【0075】
issは第2電位を印加後の定常電流である。iは電流の測定値で時間関数である。Dはレドックス活性分子の拡散係数であり、この係数は、Fickの第1法則、即ち、J(x,t)=−D dC(x,t)/dxから決定できる。Lはスペーサの厚さである。tは第2電位の印加時間であり、t=0を第2時間期間の開始とする。
【0076】
数式1においてi1をi4で置き換えると、数式6に示す第2グルコースアルゴリズムが得られる。
【数6】

このように、数式6は、干渉物質の存在下で2本の電極のみを用いて正確なグルコースの測定を可能にする。
【0077】
本発明の他の実施の形態において、数式7に示すグルコースアルゴリズムを用いて、グルコースを干渉物質の存在下で測定できる。数式7では、初期濃度Coを補正係数で乗じている。生成物は、反応したグルコースの濃度とバックグラウンドの還元された媒介物質の和に比例する。したがって、Zを減算し、その結果を(iss/ipp)pで乗じ、サンプル中の全グルコースを測定する。
【数7】

【0078】
ippは、第1過渡電流から導かれる電流値である。一態様において、ippは、第1過渡電流の終端近傍の短時間期間にわたる電流の平均値である。例えば、電流の平均値は、3.8乃至4.0秒内に測定できる。Coは、グルコース濃度の概算値で、数式8によって定義される。
【数8】

【0079】
Fはファラデー定数、すなわち96,485C/moleである。Aは作用電極の面積である。
【0080】
特定の干渉物質は電極面で容易に直接酸化されることはない。例えば、アセトアミノフェンは、第1電極を−0.3Vに保持しても、金をスパッタリングして形成した第2電極164では容易に酸化しない可能性がある。第2電極164で直接干渉電流を測定できない場合、干渉物質によるipa及びipbの関係は、グルコースの存在しない数式4で表せなくなる。同様に、数式6及び数式7も、干渉物質の存在下におけるグルコースの正確な測定値を表さなくなる。第2電極164で干渉電流が測定されない問題を解決するため、酸化された媒介物質を含むが、酵素をほとんど含まない第2試薬層を、第2電極164に設けることができる。例えば、フェリシアニドなどの酸化された媒介物質は容易にアセトアミノフェンを酸化して、間接干渉電流を第2電極164で測定可能にできる。干渉物質の酸化を第2電極164で測定できるようにすることにより、数式6及ぶ数式7は干渉物質の存在下でグルコース濃度を正確に算出できるようになる。
【0081】
この問題を解決する他の実施の形態において、十分な量の酸化された媒介物質を第1電極上に、及び/又は、第1電極内に乾燥させて、セルを充填する際に酸化された媒介物質の一部がサンプルのバルクと混合しても大量の酵素がサンプルのバルクと混合することのないようにできる。これは、例えば、配合物中に十分な量の酸化された媒介物質を含有させ、酸化された媒介物質の少なくとも一部がほとんど酵素を含まずに結晶化するように十分にゆっくりと乾燥することによって実現できる。この結晶は溶解し、媒介物質は酵素よりも大きさがほぼ小さいことから、酵素よりも広範にサンプルと混合する。このようにして、潜在的な干渉物質を酸化された媒介物質により酸化できるので、干渉電流の一部として測定可能な還元された媒介物質を生成でき、第2試薬層を不要にできる。
【0082】
他の実施の形態においては、開回路電位を第1試験電位E1と第2試験電位E2の間に印加する。この開回路電位を「第2」開回路電位と呼ぶが、「第2」という言葉は便宜上用いたものであり、「第1」開回路電位を必要とするという意味ではない。第2開回路電位は電気化学的勾配を崩壊し、非摂動状態(即ち、第1試験電位E1の印加により、第1電極166に蓄積した酸化された媒介物質がバルク溶液に拡散して戻れる状態)に戻すことができる。このような条件の下、干渉物質の影響は、第2過渡電流から第1過渡電流を直接引くことにより、除去できる。上述したように、第1試験電位E1の直後に第2試験電位E2を印加した際、初期電流は、数式3の項に示すように、大きくなる。しかしながら、第2開回路電位を、第1電極166の還元された媒介物質の蓄積を散逸してバルク溶液に戻る程度に長く印加した場合、第2試験電位E2の初期電流は、第1試験電位E1の初期電流と等しくなる。このため、試験時間期間時に還元された媒介物質が生成されず、第2開回路電位を十分に長く印加した場合、第1及び第2試験電位の過渡電流は同一となる。
【0083】
還元された媒介物質が第1電極166から散逸するために要する時間は、標準的な拡散に関する数式を用いて予測できる。一般的に、第1電極166の表面で散逸する還元された媒介物質のフラクションは時間関数として、

に比例する。一例として、Lを95ミクロン、Dを4.5 x 10−6 cm2/sと仮定してもよい。図10に、還元された媒介物質の勾配の摂動の百分率を第2開回路時間期間の関数としてグラフで示す。この場合、摂動は、還元された媒介物質の濃度がバルク濃度に近づく前に既に散逸する必要のある還元された媒介物質の量を表す。上記の仮定の値をパラメータL及びDに用いると、第2開回路電位に要する十分に長い時間は約2.5秒間(即ち、5xL2/(4π2D))となる。本発明の一実施の形態において、第2開回路電位時間期間は、約1秒乃至約5秒の範囲、好ましくは約2秒乃至約4秒の範囲とできる。当業者は、所定の試験片のパラメータに応じて、グルコース反応のない条件で第1及び第2試験電位の過渡電流が同一となる十分に長い開回路電位時間期間を容易に決定できる。
【0084】
数式9に示す十分に長い開回路電位時間期間を用いた場合、簡易なアルゴリズムを用いて干渉物質の存在下のグルコース濃度を算出できる。
【数9】

【0085】
数式9で、切片(intercept)及び傾き(slope)は較正係数である。この場合、ipbはグルコース濃度及び干渉物質濃度と比例し、ipaは干渉物質濃度のみに比例する。ipbとipaの差異は、干渉物質成分を補正したグルコースに比例する電流となる。試験を実行するために使用する電気化学セルが同一平面上に電極を有する場合は数式9を用いることができる。
【0086】
数式10に、十分に長い開回路電位時間期間において干渉物質の存在下でグルコース濃度を算出する別の簡略化したアルゴリズムを示す。
【数10】

【0087】
数式10は、グルコース反応キネティクスを表す補正係数

を有する点以外は数式9と同様である。
【0088】
本明細書で開示する他の実施の形態において、血液中のヘモグロビン測定用の試験片を準備してもよい。この実施の形態では、試験片62の試薬層72を、フェリシアニドとデオキシコール酸ナトリウムなどの溶血試薬を含有する新試薬層に置き換える。血液を新試薬層に投与すると、赤血球は溶血し、フェリシアニドがヘモグロビンを酸化するようになる。ヘモグロビンセンサについては、参照によりその全開示内容が本明細書に援用される、米国特許第6,632,349号に記載している。続いて生成されたフェロシアニドを次にヘモグロビン電流として測定できる。グルコースと同様に、フェロシアニドはアッセイの初期段階時に第2電極164に到達しないものと仮定する。試験用計量器によって試験片内の血液が検出されると、試験用計量器は1秒間開回路電位を、3秒間第1試験電位−0.3Vを、5秒間試験電位+0.3Vを連続して印加できる。
【0089】
ヘモグロビン濃度Hは、以下の数式11に示す第1ヘモグロビンアルゴリズムを用いて測定できる。
【数11】

【0090】
この場合、Coはヘモグロビン濃度に比例し、標準的な回帰分析(傾き(slope)及び切片(intercept))を用いた基準技術で較正できる。しかしながら数式11は、干渉物質の存在下でヘモグロビンアッセイを正確に実行できるように修正できる。数式12は、ヘモグロビンセンサの精度を改善した第2ヘモグロビンアルゴリズムを示す。
【数12】

【0091】
ここで、issa及びissbは、それぞれ第1過渡電流及び第2過渡電流からの定常電流である。
【実施例1】
【0092】
シトラコン酸塩をpH6.8において67mM、0.1%の消泡剤(2部のプルロニック(Pluronic)P103と1部のプルロニックF87)、60mMのサッカロース及び1.7mMのCaCl2を含有する緩衝剤を調合した。次に、PQQ補助因子を用いたGDHを緩衝液に添加し、15mg/mLとした。その後PQQを緩衝液に添加し、GHDを活性化した。PQQの添加後、配合物を約1時間インキュベートさせた。次に、フェリシアン化カリウムを混合物に添加し、600mMとした。配合物は、参照によりその全開示内容が本明細書に援用される、米国特許第6,749,887号、6,689,411号及び6,676,995号に記載したスロットコーティング処理により図1に示す第1導電層66上にストライプした。配合物をコーティングし、乾燥させ、試薬層72、スペーサ層60及び第2電極164をその上に組立て、試験片62を形成する。
【実施例2】
【0093】
複数の試験片62を約83乃至88mg/dLの範囲の濃度のグルコースを含有する血液で試験した。血液サンプルには干渉物質を混入した。試験片62は試験用計量器100を用いて5秒間のグルコース試験時間期間TG試験した。試験用計量器100には図6に示す電位波形を印加した。試験片毎に試験電流を測定し、数式1に示す第1グルコースアルゴリズム及び数式6に示す第2グルコースアルゴリズムを用いてグルコース濃度に変換した。試験片毎にmg/dLの単位で基準法に対する平均バイアスを算出した結果を図11に示す。図11から、第1グルコースアルゴリズムを用いた場合と比較して第2グルコースアルゴリズムを用いた場合、アスコルビン酸塩及び尿酸塩などの干渉物質の存在下における全体的なバイアスが削減されたことがわかる。
【実施例3】
【0094】
異なる試験片62のセットを用いて同様の方法で本実施例3の実験を繰り返した。この実験では、試験片毎に試験電流を測定し、数式1に示す第1グルコースアルゴリズム及び数式7に示す第3グルコースアルゴリズムを用いてグルコース濃度に変換した。試験片毎にmg/dLの単位で基準法に対する平均バイアスを算出した結果を図12に示す。図12から、第1グルコースアルゴリズムを用いた場合に対して第3グルコースアルゴリズムを用いた場合、干渉物質の存在下における全体的なバイアスが削減されたことがわかる。簡単な電流の合計値の代わりに、Coを用いることにより、干渉物質の存在下におけるより正確な測定を可能にできる。
【実施例4】
【0095】
ヘモグロビン測定用の試験片62を複数用意した。複数の試験片62を16.3g/dLの濃度のヘモグロビンを含有する血液で試験した。血液サンプルには干渉物質を混入した。試験片毎に試験電流を測定し、数式9に示す第1ヘモグロビン数式及び数式10に示す第2ヘモグロビン数式を用いてヘモグロビン濃度に変換した。試験片毎にmg/dLの単位で基準法に対する平均バイアスを算出した結果を図13に示す。図13から、第1ヘモグロビン数式を用いた場合に対して第2グルコース数式を用いた場合、アスコルビン酸塩(AA=10 mg/dL)、尿酸塩(UA=10mg/dL)及びアセトアミノフェン(Acet=20mg/dL)などの干渉物質の存在下における全体的なバイアスが削減されたことがわかる。
【0096】
当業者であれば、上記の実施態様に基づき、本発明の更なる特徴及び利点を想起することができるであろう。したがって、本発明は、添付された請求項により示された内容以外の、具体的に示されまた記載された内容に限定されることはない。本明細書において記載された全ての刊行物及び参考文献は、ここに本明細書の一部を構成するものとしてその内容を援用する。
【0097】
本発明の新規な特長について、添付の特許請求の範囲に詳細に記載する。本発明の特長及び利点は、本発明の原理を用いた例示された実施の形態に記載される詳細な説明及び添付の図面を参照してより理解される。
【図面の簡単な説明】
【0098】
【図1A】本発明の方法の使用に好適な組立済み試験片の斜視図。
【図1B】本発明の方法の使用に好適な試験片の分解斜視図。
【図1C】本発明の方法の使用に好適な試験片近端部分の拡大斜視図。
【図2】本発明の一実施の形態の試験片の底面図。
【図3】図2に示した試験片の側面図。
【図4A】図3に示した試験片の上面図。
【図4B】図4Aに示した試験片における近端部分の4A−4A矢視拡大側面図。
【図5】本発明の試験片の一部と電気的に接続する試験用計器の簡略図。
【図6】試験用計器が所定の時間期間で連続して印加する開回路電位と試験電位の電位波形の例。
【図7】干渉物質を添加していない濃度62mg/dLのグルコースを含有した生理学的サンプル(実線)と濃度20mg/dLのアスコルビン酸塩を含有した生理学的サンプル(点線)を試験して生成した第1過渡電流及び第2過渡電流を示すグラフ。
【図8】第1過渡電流を示す図7の拡大図。
【図9】サンプル反応チャンバ内の還元された媒介物質の濃度勾配を示すグラフ。
【図10】第1電極における還元された媒介物質の勾配の摂動百分率を第2開回路時間期間の関数として示すグラフ。
【図11】第1グルコースアルゴリズムと第2グルコースアルゴリズムを用いた場合におけるグルコース濃度測定結果のバイアスの絶対値を示すグラフ。
【図12】第1グルコースアルゴリズムと第3グルコースアルゴリズムを用いた場合におけるグルコース濃度測定結果のバイアスの絶対値を示すグラフ。
【図13】第1ヘモグロビンルゴリズムと第2ヘモグロビンアルゴリズムを用いて特定の干渉物質の存在下でヘモグロビン濃度を測定した場合におけるバイアスの絶対値を示すグラフ。
【符号の説明】
【0099】
61 反応チャンバ
62 試験片
100 試験用計量器
166 第1電極
164 第2電極
【技術分野】
【0001】
本発明は、干渉物質の存在下でサンプルを迅速で正確に分析する方法及び装置に関する。
【背景技術】
【0002】
LifeScan社から入手可能なOneTouch(登録商標)Ultra(登録商標)全血試験キットなどで使用される電気化学的グルコース試験片は、糖尿病患者から採取した血液サンプル中のグルコース濃度を測定するように設計されている。グルコースの測定は、フラボ酵素グルコースオキシダーゼ(GOx(ox))による特異的酸化に基づく。この反応の間、酵素は還元され、(GOx(red))となる。酵素は、酸化された媒介物質フェリシアニド(Fe(CN)63−)と反応して再酸化され、フェリシアニド(Fe(CN)63−)自体はこの工程、即ち反応時に還元される。これらの反応の概要は以下の通りである。

【0003】
2本の電極の間に試験電位を印加して上記の反応が行われると、電極面で還元された媒介物質(フェロシアニド、即ちFe(CN)64−)が電気化学的に再酸化することにより電流が流れる可能性がある。理想的な環境では、上記の化学反応時に生成されるフェロシアニドの量は、電極間に存在するサンプル中のグルコースの量と正比例するため、生成された電流は、サンプルのグルコース含有量と比例することになる。フェリシアニドなどの媒介物質とは、グルコースオキシダーゼなどのレドックス酵素と電極間で電子を交換する化合物である。他の種類のグルコース試験片では、ピロロキノリンキノン(PQQ)補助因子を用いた酵素グルコースデヒドロゲナーゼをグルコースオキシダーゼの代わりに使用することができる。グルコース濃度が増加すると、生成される還元された媒介物質の量も増加することから、グルコース濃度と還元された媒介物質の再酸化により発生する電流の間には直接の因果関係がある。特に、電気的境界面(electrical interface)を越えた電子の移動が電流の流れとなる(1モルのグルコースが酸化されるごとに2モルの電子が移動する)。このことから、グルコースの導入により生じた電流を、検体電流、より具体的には、グルコース電流と呼ぶことがある。
【0004】
血液中のグルコースレベルを監視することは、糖尿病などの疾病を管理する上で重要な手段となることから、上述の原理を用いた、試験用計量器が普及している。試験時に生成されるグルコース電流は、試験用計量器により記録され、簡単な数式に基づいて電流をグルコース濃度に対応させる所定のアルゴリズムを用いて、グルコース濃度表示値に変換される。一般的に、試験用計量器は、電極と試薬を含むサンプル反応チャンバを有した使い捨ての試験片と共に動作する。使用時、使用者が、サンプル反応チャンバに少量の血液を注入すると試験用計量器が分析を行い、使用者に血糖値を知らせるようになっている。
【0005】
電気化学的な意味において、試験用計量器は二重の機能を有している。第1は、分極試験電位(0.4V)を印加して、電気的境界面を分極させ、2つの作用電極面の間にセル電流が流れるようにすることである。第2は、試験用計量器がセル電流を計測できることである。したがって、試験用計量器は、実際には、グルコースの測定を容易にし、および/または試験用計量器のその他の機能を実行するために、3本目、場合によっては4本目の電極を用いることがあるが、2本の電極モードで動作する簡単な電気化学的システムとして考えることができる。
【0006】
多くの場合、上記の化学反応式は、試験片に発生する化学反応を十分に近似しており、相当に正確なグルコース濃度の表示値を得ることができると考えられる。しかしながら、特定の状況で特定の目的の下において、例えば、電極で測定される電流の一部にサンプル内のその他の薬物または化合物の存在によるものが含まれる場合などでは、測定精度の向上が有利である場合がある。このような薬物または化合物が存在する場合、それらを干渉物質と呼び、この結果生じる追加的な電流を干渉電流(interferent current)と呼ぶことができる。
【0007】
考えられる干渉物質(即ち、試験電位が印加された際に干渉電流を生成する可能性のある血液などの生理学的流体に存在する化合物)の例として、アスコルビン酸塩、尿酸塩、アセトアミノフェン(Tylenol(登録商標)またはパラセタモール)などがあげられる。試験用計量器に干渉電流が生成される第1のメカニズムは、媒介物質(例えば、フェリシアニド)の還元により一つ以上の干渉の原因となる化合物が酸化されることである。更に、こうして還元された媒介物質は作用電極で酸化され得る。この第1のメカニズムは、間接干渉電流と呼ぶこともできる。試験用計量器に干渉電流が生成される第2のメカニズムは、作用電極において一つ以上の干渉物質が酸化されることである。第2のメカニズムは、直接干渉電流と呼ぶことができる。こうして、測定されるセル電流に、干渉物質から生じる望まない電流成分が含まれる。
【発明の開示】
【発明が解決しようとする課題】
【0008】
干渉物質の影響を削減するために使用可能な方法は、第1作用電極と基準電極と共に第2作用電極を使用することである。第2作用電極が剥き出しの状態であれば、第2作用電極は直接干渉電流を測定することができる。第1作用電極は、グルコース電流、直接干渉電流及び間接干渉電流の合計を含む電流を測定するため、酵素と媒介物質を含むようにする。第2作用電極で測定した直接干渉電流を第1作用電極で測定した電流から引くと、干渉物質の影響を削減できる。
【0009】
代替或いは追加的として、第2(又は第3)作用電極を媒介物質(しかし酵素ではない)で被覆して、第2作用電極が直接及び間接干渉電流の合計(しかしグルコースは入らない)を含む電流を測定できるようにする。この場合、第2作用電極で測定した直接及び間接干渉電流を第1作用電極で測定した電流から引くと干渉物質の影響を削減できる。
【0010】
ユーザが提供する血液サンプルを少量で済ませるため、サンプル反応チャンバは小型の方が好ましい。干渉物質の影響を補償するために第2(または第3)作用電極を用いる欠点は、第2作用電極は、サンプル反応チャンバの容積を相応に増加することである。更に、第2作用電極を用いると、構造が複雑となり、製造コストの増加を招くという欠点がある。したがって、2本の電極のみを用いて干渉物質の影響を受けずにグルコースを測定する方法の開発が必要とされている。
【課題を解決するための手段】
【0011】
本発明は広義には、生理学的サンプル中の検体濃度を電気化学的に決定する方法及び装置を提供する。一態様において、本明細書中に記載の方法は、電気を印加し、電流を測定する試験片を用いる。本方法は、こうして測定した電流値に基づいて、干渉物質の影響を最小限にしながら、迅速に検体濃度を測定できる。
【0012】
一実施の形態において、本方法は、生理学的サンプルを電気化学セルに導入するステップを含んでなる。例えば、相互に離間した第1及び第2電極と試薬とを備えたセルなど、様々な電気化学的セルを使用できる。一旦サンプルが付着すると、本方法は、第1の極性を有する第1試験電位を反応セルに印加し、セル電流を時間関数として測定し、第1過渡電流を得る。第1の極性とは反対の第2の極性を有する第2試験電位をセルに印加し、セル電流を時間関数として測定することによって、第2過渡電流を得る。
【0013】
次に第1及び第2過渡電流を分析し、第1過渡電流から第1ピーク電流値を決定し、第2過渡電流から第2ピーク電流値を決定する。第1ピーク電流値及び第2ピーク電流値に基づいて、サンプル中の干渉物質の影響を決定できる。
【0014】
一実施の形態において、干渉物質の影響は、第1ピーク電流値及び第2ピーク電流値を用いて電流値を補正することによって減少する。例えば、補正電流値は、第2過渡電流から導出した第1電流値を修正することによって決定できる。こうして得られた補正電流値は、干渉物質に起因する電流成分を除去した第1電流値を表せる。
【0015】
一態様において、干渉物質からの第1電流値への寄与は、第1電流値と干渉物質補正係数とを積算することによって、(少なくとも部分的に)除去する。干渉物質補正数式は、

であり、ipbは第1ピーク電流値、ipaは第2ピーク電流値、issは定常電流値である。
【0016】
補正電流値を用いて検体濃度を決定できる。例えば、本方法は、第2過渡電流から第2電流値を算出し、第1過渡電流から第3電流値を算出するステップを含むことができる。検体濃度は、数式

から得ることができる。[C]が検体濃度、i4が第1補正電流値、i2が第2電流値、i3が第3電流値、a、p及びZが補正係数である。
【0017】
本明細書に開示される他の実施の形態において、検体濃度は数式

に基づいて決定され、[C]が検体濃度、ippが第1過渡電流から導出される電流値、Coがグルコース濃度概算値、Zが較正係数、ipaが第1ピーク電流値、ipbが第2ピーク電流値、issが定常電流値である。一代替態様において、ippは、第1過渡電流終端近傍の短時間期間にわたる電流の平均値である。
【0018】
本明細書に開示された他の実施の形態は、検体と干渉物質の両方を含有した生理学的サンプルにおける検体濃度を決定する方法である。当該方法は、電気化学的セルに生理学的サンプルを導入し、第1の極性を有する第1試験電位を反応セルに印加する。セル電流値を時間関数として測定し、第1過渡電流を得る。次に、開回路電位時間期間を経過させる。開回路電位時間期間が経過した後、第2の極性を有する第2試験電位を印加することによって、第2過渡電流を測定する。
【0019】
第1過渡電流及び第2過渡電流に基づいて、第1ピーク電流値及び第2ピーク電流値が得られる。第2ピーク電流値から第1ピーク電流値を減算して、サンプル内の検体濃度と比例する補正電流を決定する。補正電流を用いて検体濃度を算出する。
【0020】
例えば、検体濃度は、数式

に基づいて算出できる。[C]が検体濃度、ipaが第1ピーク電流値、ipbが第2ピーク電流値、slope及びinterceptが較正係数である。他の態様において、数式は、反応キネティクスを考慮して、以下の数式に修正できる。

[C]が検体濃度、ipaが第1ピーク電流値、ipbが第2ピーク電流値、i2が第2過渡電流から導出される電流値、i3が第1過渡電流から導出される電流値、slope及びinterceptが較正係数である、
【0021】
更に他の実施の形態は、検体と干渉物質の両方を含有した生理学的サンプルにおけるヘモグロビン濃度を決定する方法である。当該方法は、電気化学的セルに生理学的サンプルを導入し、第1の極性を有する第1試験電位を前記セルに印加するステップを含んでなる。セル電流値を時間関数として測定し、第1過渡電流を得る。次に、第2の極性を有する第2試験電位を印加し、セル電流値を時間関数として測定することによって、第2過渡電流を測定する。
【0022】
第1過渡電流に基づいて、第1定常電流を決定し、第2過渡電流に基づいて第2定常電流を決定する。第2定常電流値から第1定常電流値を減算し、ヘモグロビン濃度に比例する電流値を得る。
【0023】
一態様において、ヘモグロビン濃度は
数式

に基づいて算出される。
[H]が、検体濃度、issaが前記第1過渡電流からの定常電流、issbが前記第2過渡電流からの定常電流、slope及びinterceptが較正係数、Fがファラデー定数、Aが第1電極の面積、Dがレドックス活性分子の拡散係数、Lが電極の間隔である。
【発明を実施するための最良の形態】
【0024】
本発明の方法および装置は、種々多様なサンプル中の種々多様な検体の測定に使用するのに適しており、特に対象となる検体がグルコースである場合に、全血またはその誘導物中の検体を測定するのに特に適している。本発明は、迅速な方法で正確な測定結果を得ることができる生理学的サンプル中の検体濃度値を測定する方法を提供する。本明細書では、検体濃度値の測定に使用できる代表的な実施の形態の試験片の構造について説明する。さらに、本明細書では、試験片に発生する過渡電流を試験片と電気的に接続した計量器によって測定し収集する、試験片を用いた方法について説明する。さらに、本明細書では、迅速な方法で過渡電流を処理するために用いられ、正確な検体濃度を出力するアルゴリズムについて説明する。さらなる態様において、干渉物質の影響を削減するように検体濃度を測定する方法について説明する。
【0025】
本発明の方法は、原理的には、離間した第1及び第2電極を有する如何なる種類の電気化学セルと共に用いることができる。本明細書では、本発明を例示するため、対向する電極を用いた特定の実施の形態について説明する。しかしながら、本発明は、同一平面上の電極を用いたセルなど、他の構成の電極を用いたセルにも同様に適用可能であることが理解される。適用しなくてはならない唯一の構成上の制限は、干渉電流の測定が検体(例えばグルコース)の反応により生成される電気活性種からの影響をほとんど受けることのないように電極は配置される必要があるという点である。これは通常、検体の反応により生成される電気活性種が、干渉電流を測定する電極に、干渉電流の測定前または測定時中に到達する時間のないように電極を十分に離間することにより達成される。
【0026】
以下、図1A〜図4Bを参照して、様々な実施の形態の、近端部80から遠端部82へ長手方向軸Lに沿って延在し、側縁部56、58を含む伸長体59を有する試験片62の形状のかかる装置について説明する。伸長体59は、電極164、166と試薬72を含有する電極近端側サンプル反応チャンバ61を含むことができる。試験片伸長体59は遠端側にさらに、試験用計量器(図示されてない)と電気的に接続する電気的接点63、67を含むことができる。
【0027】
一態様において、試験片62は、第1導電層66、スペーサ層60、第2導電層64を含む多層から形成される。第1導電層66及び/又は第2導電層64は、一実施の形態では、絶縁シート(図示されてない)に配置された様々な導電性材料から形成できる。スペーサ層60は、様々な電気絶縁性材料から形成でき、接着剤を含む、又は接着剤から形成されてもよい。三層の試験片が図示されているが、追加の導電層または絶縁層を用いて、試験片伸長体59を形成できることは当業者には明らかである。
【0028】
図1A〜図1Cに示すように、近端側サンプル反応チャンバ61は、第1導電層66、第2導電層64及びスペーサ層60により画定できる。以下により詳細に説明するように、反応チャンバ61はまた、試薬72、第1及び第2電極166、164を含むことができる。例えば、スペーサ層60の切り欠き領域68は、第2導電層64と第1導電層66の一部を露出させることにより、第1電極166と第2電極164をそれぞれ形成できる。一形態として、試薬72は第1電極166上に形成した層でもよい。
【0029】
一実施の形態において、反応チャンバ61は少量のサンプルを分析するようになっている。例えば、サンプル反応チャンバ61の容量は、約0.1μl(microliter)乃至約5μlの範囲、好ましくは、約0.2μl乃至約3μlの範囲、より好ましくは、約0.3μl乃至約1μlの範囲とできる。少量のサンプルを収容するため、電極は近接していることが好ましい。例えば、スペーサ層60は、第1電極166と第2電極164間の距離を画定する場合、スペーサ層60の高さが約1ミクロン(micron)乃至約500ミクロンの範囲、好ましくは、約10ミクロン乃至約400ミクロンの範囲、より好ましくは、約40ミクロン乃至約200ミクロンの範囲とできる。
【0030】
反応チャンバ61の一層の容積削減を支援するため、切り欠き領域68及び/又は伸長体59の長手方向及び/又は側方向の寸法を調節することができる。例えば、試験片伸長体59は、反応チャンバ61の側方向の幅が試験片伸長体59の全幅(最大幅)より小さくなるように、切り取り部51、52を有することができる。切り取り部51、52はまた、反応チャンバ61へのサンプルの送入を容易できる。例えば、切り取り部51、52は、使用者の指の一部に対応した形状を有することができる。使用者が指を刺して絞り出した血液を採取する際、切り取り部51、52は、使用者が自身の指に付着した血液サンプルを伸長体59の側縁部56、58のサンプル注入口(例えば、開口部70)の位置に合わせやすくできる。2つの切り取り部が図示されているが、当業者には、試験片伸長体59は、切り取り部を一つのみ有してもよいし、或いは切り取り部を有さなくてもよいことは明らかである。
【0031】
上述したように、試験片伸長体59の近端部は、サンプルを反応チャンバ61に注入するための少なくとも一つのサンプル注入口を有することができる。例えば、切り欠き領域68は、試験片伸長体59の側縁部56、58から横方向に延在し、生物学的流体をサンプル反応チャンバ61へ注入する二つの開口部70を形成できる。二つの開口部70が存在すると、一方を、サンプルをサンプル反応チャンバ61に注入するサンプル注入口として機能させながら、他方を通気口として機能させることができる。当業者には、例えば、第1及び/又は第2導電層66、64にサンプル注入口および/または通気口を設けるなど、試験片伸長体59内の上記とは異なる場所にサンプル注入口及び/又は通気口を設けた代替の構造体を用いてサンプルをサンプル反応チャンバ61へ注入することが可能であることは明らかである。
【0032】
一実施の形態において、試験片62は、毛細管現象によりサンプルを反応チャンバ61へ引き入れるようになっている。例えば、反応チャンバ61と開口部70の寸法と表面の特性は、液体サンプル(例えば、全血)が開口部70の一つと接触する際に毛細管力を生成するようにできる。当業者には、反応チャンバ61には、例えば、ビーズ、多孔性膜及び/又はその他の充填物など、毛細管力を補助/生成するための構造体を含められることは明らかである。
【0033】
上述のようにして、試薬72などの試薬を反応チャンバ61内に付着できる。試薬72の組成は、目的とする検体及び希望するサンプルの形態に応じて変更できる。一態様において、試薬72は、少なくとも一つの媒介物質及び酵素を含み、第1電極166に付着する。適当な媒介物質の例として、フェリシアニド、フェロセン、フェロセン誘導物、オスミウムビピリジル錯体及びキノン誘導物が挙げられる。適当な酵素の例として、グルコースオキシダーゼ、ピロロキノリンキノン(PQQ)補助因子をベースとしたグルコースデヒドロゲナーゼ(GDH)、ニコチンアミドアデニンジヌクレオチド補助因子をベースとしたGDHが挙げられる。試薬層72を生成するために適した代表的な試薬配合物については、参照によりその全開示内容が本明細書に援用される、「滅菌され、較正されたバイオセンサーベースの医療デバイスの製造方法」と題した係属中の米国特許出願第10/242,951号、米国特許公開番号第2004/0120848号に記載している。
【0034】
近端側サンプルチャンバ61に対して遠端側に位置する伸長体59は、第1及び第2電極166、164を遠端側電気的接点63、67と電気的に接続する接続トラックを有することができる。一態様において、第1導電層66は、第1電極166を第1電気的接点67と電気的に接続する第1接続トラック76を有する。同様に、第2導電層64は、第2電極164を第2電気的接点63と電気的に接続する第2接続トラック78を有する(図1B)。
【0035】
第1及び第2導電層はまた、試験片62と試験用計量器との電気的接触を容易にする第1及び第2電気的接点67、63を画成できる。一実施の形態では、第1導電層66の一部は、スペーサ層60及び第2導電層64の遠端部から更に遠端側へ延在し、第1電気的接点67を画成する。第2電気的接点は63、第2導電層64の一部を露出する第1導電層66に形成されたU字形状切り込み部65により画成できる。当業者には、試験片62は、試験用計量器と電気的に接続する他の様々な代替可能な電気的接点構成を有することができることは明らかである。例えば、参照によりその全開示内容が本明細書に援用される、米国特許第6,379,513号には、電気化学セル接続構造体が開示されている。
【0036】
図5は、試験片62の第1電極166及び第2電極164とそれぞれ電気的に接続する、第1電気的接点67及び第2電気的接点63と接する試験用計量器100の簡略図である。試験用計量器100は、第1電極166及び第2電極164と、それぞれ第1電気的接点67及び第2電気的接点63を介して電気的に接続するようになっている(図2および図5を参照)。一態様において、試験用計量器100は、第2電気的接点63とU字形状切り込み部65を介して接触する。
【0037】
図5に示すように、電気的接点67は、67a及び67bと付された2本のプロング(prong)を有することができる。代表的な一実施の形態では、試験用計量器100が試験片62と接すると回路が完結するように、試験用計量器100はプロング67a、67bと別々に接続する。試験用計量器100は、プロング67a及び67b間の抵抗又は電気的導通を測定して、試験片62が試験用計量器100と電気的に接続しているか否かを判断できる。当業者には、試験用計量器100は、様々な代替可能なセンサ及び/又は回路を用いて、試験片62が試験用計量器100に対して適切に配置されているか否かを判断できることは明らかである。
【0038】
試験用計量器100はまた、反応チャンバ61内の流体の存在を検出するように構成することもできる。例えば、試験用計量器100が試験片62が挿入されたことを認識すると、試験用計量器100は、第1電極166と第2電極164間に定電流(例えば、1μAの電流)を流すことができる。開始時に反応チャンバ61は乾燥しているため、試験用計量器100は最大電圧を印加して、所望の電流を得るようにしてもよい。しかしながら、一旦生理学的サンプルが使用者により注入口70に投与されると、サンプル反応チャンバ61は満たされる。生理学的サンプルが第1電極166と第2電極164間の間隙を満たすと、試験用計量器100は、所定の閾値を下回る測定電圧の低下を検出する(米国特許第6,193,873号参照)。
【0039】
幾つかかのケースにおいて、生理学的流体が付着したことを認識したとしても、サンプル反応チャンバ61が完全に満たされたことを示すとは限らず、サンプル反応チャンバ61内における生理学的流体の一部の存在の確認のみを意味する場合もある。試験用計量器100が、生物学的流体が試験片62に付着されたと判断すると、生理学的流体がサンプル反応チャンバ61を完全に満たすように短い時間であるが、限られた時間待機することができる。
【0040】
一旦生理学的サンプルが試験片62に投与されると、試験用計量器100は、開回路電位と複数の試験電位をそれぞれ所定の時間期間印加することにより、グルコース試験を実行できる。例えば、グルコース試験はグルコース試験時間期間TGにわたり実行でき、グルコース試験時間期間TGは、開回路時間期間TOC、第1電位時間期間T1及び第2試験電位時間期間T2を連続して含むことができる。図6は、3つの時間期間を含む代表的な試験を表すグラフである。
【0041】
以下の本発明の実施の形態において、一連の時間期間は全体で、5秒間のグルコース試験時間期間TGを表す。しかしながら、グルコース試験時間期間は変更可能であり、例えば、5秒間を上回る、或いは下回る時間期間も含む。一態様において、グルコース試験時間期間TGは、約1秒乃至約10秒の範囲とすることができ、好ましくは約2秒乃至約8秒の範囲とすることができ、より好ましくは約3秒乃至約6秒の範囲とできる。グルコース試験は、開回路時間期間TOCでサンプル反応チャンバ61を充填できる。開回路時間期間TOCは、サンプルの性質(例えば、粘性、組成など)、サンプル反応チャンバの寸法及び物理的特性、及び/又は充填方法の違い(例えば、毛細管現象の強さ)に応じて変更できる。例えば、周囲温度が低く(例えば、約5℃)及び/又はヘマトクリット値が高い(例えば60%を超える)ため、血液サンプルが粘性の可能性のある場合、追加の開回路時間を要することがある。本発明の一実施の形態では、開回路時間期間TOCは、約0.1秒乃至約2秒の範囲でよく、好ましくは約0.3秒乃至約1.5秒の範囲でよく、より好ましくは約0.5秒乃至約1秒の範囲でよい。
【0042】
一旦開回路時間期間TOCが経過すると、試験用計量器100は、第1電極166と第2電極164の間に第1試験電位E1を第1試験電位時間期間T1の間印加できる。第1試験電位時間期間T1が経過すると、試験用計量器100は、第1電極166と第2電極164の間に第2試験電位E2を第2試験電位時間期間T2の間印加できる。T1及びT2の間、試験用計量器100はセル電流を第1試験電位時間期間T1の間ia(t)で、第2試験電位時間期間T2の間ib(t)で表される時間関数として測定することができ、これらを時間−過渡電流又は過渡電流と呼ぶ。
【0043】
一実施の形態において、第1試験電位E1は第1の極性を有し、第2試験電位E2は第2の極性を有し、第1の極性は第2の極性の反対である。更に、第1試験電位E1は、限界酸化電流が測定される作用電極として第2電極164が機能するように、第2電極164に対して十分に負の大きさを持つことができる。酸化可能な種は作用電極面で局所的に枯渇し、酸化電流の測定値はバルク溶液から作用電極面の方向へ拡散する酸化可能な種の流れに比例するようになる。ここで「バルク溶液」とは、酸化可能な種が枯渇ゾーン内に存在しなくなった作用電極から十分に離れた溶液の一部を意味する。同様に、第2試験電位E2は、限界酸化電流が測定される作用電極として第1電極166が機能するように、第2電極164に対して十分に正の大きさを持つことができる。一実施の形態では、第1試験電位E1及び第2試験電位E2は、約−0.6ボルト乃至約+0.6ボルトの範囲とできる。第1試験電位E1が負である場合、試薬72は第1電極166に設けることができる。
【0044】
図6に、代表的な一グルコース試験時間期間TGをグラフで示す。ここで第1試験電位E1には−0.3ボルトを印加し、第2試験電位E2には+0.3ボルトを印加できる。第1試験電位時間期間T1は3秒であり、第2試験電位時間期間T2は1秒であった。第2試験電位E2は第1試験電位E1を印加した直後に印加する。
【0045】
図7に、干渉物質を添加していないグルコース濃度62mg/dLの生理学的サンプル(実線)とアスコルビン酸塩濃度20mg/dLの生理学的サンプル(点線)について、図6のグルコース試験時間期間TGに基づく試験を実行して生成された第1及び第2過渡電流をグラフで示す。図8に、図7の第1過渡電流の拡大図をグラフで示す。
【0046】
試験片が、図1A〜図4Bに示す面が対向する構成を有するとした場合、グルコース濃度は、以下の数式1に示す第1グルコースアルゴリズムを用いて算出できる。
【数1】

【0047】
上記の数式1において、[G]はグルコース濃度を表し、i1は第1電流値、i2は第2電流値、i3は第3電流値、p、Z及びaは実験により得られた較正定数を表す。数式1の導出方法については、参照によりその全開示内容が本明細書に援用される、2005年9月30日に出願された「迅速な電気化学的分析方法及び装置」と題した係属中の米国特許出願第11/240,797号に記載している。
【0048】
第1電流値i1及び第2電流値i2は第2電流過度から算出することができ、第3電流値i3は第1電流過度から算出される。便宜上、「第1」、「第2」及び「第3」という名称を用いたが、当業者にはこれが電流値を算出する順番を反映すると限らないことは明らかである。数式1及び後述する数式に記載する全ての電流値(例えば、i1、i2及びi3)には、電流の絶対値を使用できる。
【0049】
第1電流値i1及び第2電流値i2は、一態様では、第2電流過度の時間期間における電流値の積分、第2電流過度の時間期間における電流値の合計、或いは第2電流過度の電流値の平均又は一つと第2電流過度の時間期間との積とできる。同様に、第3電流値i3は、一態様では、第1電流過度の時間期間における電流値の積分、第1電流過度の時間期間における電流値の合計、或いは第1電流過度の電流値の平均又は一つと第1電流過度の時間期間との積を用いることができる。電流値の合計については、所定範囲の連続した電流測定値から2つのみ、或いは電流測定値の全てを加算して求めることができる。
【0050】
他の実施の形態において、第1電流値i1、第2電流値i2及び第3電流値i3は、クーロン値で置換できる。電流を測定する代わりに、通過した電荷を測定できる。通過した電荷の合計は、電流過度の積分と同一の情報となる。例えば、通過電荷は、所定の時間期間にわたって測定でき、第1、第2及び/又は第3電流値として使用できる。
【0051】
本明細書で開示する一実施の形態の方法において、グルコース反応キネティクスは電流値(例えば、i1、i2及び/又はi3)を用いて求められる。この結果は、ヘマトクリット濃度と温度の影響を受けにくいため、高い正確さと精度でグルコース濃度を測定できる。
【0052】
一態様において、試薬層72は第1電極166上に設ける。これにより生理学的サンプルと溶解後、試薬のほとんどは第1電極166の近傍に残留する。この結果、少なくとも初期において、還元された媒介物質の多くの部分は第1電極166近傍に存在する。所定の時間期間が経過した後、グルコースとの反応により試薬層72で生成された還元された媒介物質は、第1電極166から受動的に拡散する。このプロセスの間、第1電極166と第2電極164間の媒介物質濃度の大きさは、還元された媒介物質の濃度が第1電極166でより高く、第2電極164でより低くなる勾配を形成する。第1電極166側の還元された媒介物質の濃度が大きくなる程、大きさの勾配は急になる。第1電流過度の大きさは、この勾配の大きさと比例する。したがって、試薬層72で生成された還元された媒介物質の量は、還元された媒介物質の第2電極164への拡散を促進する。電極で測定される電流の変化速度は、試薬層72における還元された媒介物質濃度の変化速度及びグルコース反応キネティクス(即ち、還元された媒介物質を生成するグルコースの反応速度)を示す。
【0053】
グルコース反応キネティクスは、電極間隔(グルコースが試薬層72へ拡散するために要する最大距離に関係する)、生理学的サンプルの粘性、ヘマトクリット濃度及び温度を含む複数の因子に左右される。
【0054】
生理学的サンプルの粘性は、ヘマトクリット値、タンパク質、脂質含有量又はそれらの組み合わせの増加とともに増加する可能性がある。ヘマトクリット値は、血液サンプル中の赤血球の比率を示す。通常、赤血球の比率が高いと、血液の粘性が高くなり、結果として赤血球中の全グルコースの比率は大きくなる。赤血球中のグルコースが試薬層72と反応するためには、グルコースは、赤血球膜を越えて移動する必要がある。特定の条件の下では、この移動は比較的緩やかであり、グルコース反応キネティクスを制限することがある。したがって、ヘマトクリット値が高くなるとグルコース反応キネティクスは遅くなる。粘性は通常、サンプル反応チャンバ61内の全体的な拡散プロセスを緩やかにする。温度が高くなると通常、関連する移動プロセスは迅速になり、サンプル反応チャンバ61内のグルコースと試薬層72との反応速度は増加する。
【0055】
電流値(i1、i2及び/又はi3)、特に電流値の比率を用いて、グルコース反応キネティクスのばらつきを補正できる。例えば、第2電流過度の大きさは一般的に第1電流過度の大きさの絶対値より大きくなる。このため、i2/i3の比率は一般的に、サンプル反応チャンバ61内でグルコース反応が進行している間は1より大きくなり、グルコース反応が完了すると1になる。i2/i3値の1との乖離は、反応完了の度合いを示す係数となる。i2/i3値が比較的大きい場合は、グルコース反応が完了までほど遠く、i2/i3値が1に近い場合は、グルコース反応は完了に近いことを意味する。したがって、i2/i3の比率は一般的にグルコース反応の進捗情報を示し、グルコース濃度の測定におけるヘマトクリット値、粘性及び温度の影響を除去するために使用できる。
【0056】
さらに計算の精度を高めるため、一以上の較正係数を使用できる。例えば、数式1に示す、i2/i3の比率をべき指数pで累乗する。ここでpは、特定のロットの試験片に使用できる較正係数である。べき指数pを用いることは、精度を向上し、試験時間を短縮するための経験的な手法から発見された。本発明の一実施の形態において、pは約0.2乃至約4の範囲、好ましくは、約0.1乃至約1の範囲とできる。
【0057】
数式1に示すように、切り欠き領域68及びスペーサ層60の高さのばらつきの可能性を表す較正係数aを使用できる。切り欠き領域68のばらつきは、測定電流の大きさを相応にシフトする原因となり得る。特定の状況では、製造工程で試験片のロット毎に電流面積のばらつきが生じることがある。同様に、スペーサ層60の高さもロット毎にばらつきが生じることがある。スペーサ層60の高さのばらつきは、試験電流に相応の影響を与える。例えば、スペーサ層60の高さが増加すると、試験電流は低下する。ロット毎に試験片の較正係数aを算出することは、電極面積及びスペーサ層60の高さのばらつきの補償に有益である。較正係数aを算出すると、因子aは、試験片のロットの較正工程で算出できる。
【0058】
一実施の形態では、数式1に示すように、バックグラウンドのばらつきを表すために較正係数Zを用いる。生理学的流体を試験片62に付加する前の試薬層72内における酸化可能な種の存在がバックグラウンド信号に寄与することがある。例えば、生理学的流体が試験片に注入される前に試薬層72が少量のフェロシアニド(例えば、還元された媒介物質)を含有していた場合、測定される試験電流はグルコース濃度とは無関係に増加する。これは、特定のロットの試験片について測定される試験電流全体の恒常的なバイアスとなる。このバイアスを補正するために較正係数Zを用いることができる。因子pと同様に、Zもまた、較正工程で算出できる。
【0059】
本明細書では較正係数p、a及びZを用いた方法について開示するが、当業者には、これらを用いることが必須でないことは明らかである。例えば、一実施の形態では、グルコース濃度は、p、a及び/又はZを用いずに算出できる(数式1において、p及び/又はaを1と等価に設定し、Zをゼロと等価に設定できる)。
【0060】
i1、i2及びi3を算出する時間期間の選択は、個別の種類の試験片毎に学習アルゴリズムに従って決定(即ち経験的に決定)できる。学習アルゴリズムを実行する際、複数の試験片について、試験時に使用者が遭遇する可能性のある範囲の条件で試験を行う。かかる条件は、20mg/dL乃至600mg/dLの範囲のグルコース濃度、0%乃至70%の範囲のヘマトクリット値、5℃乃至45℃の範囲の温度、相対湿度5%(5%RH)乃至95%RHの範囲の湿度、及び内因性及び外因性干渉物質を含んでもよい。内因性及び外因性干渉物質、及びそれらの生理学的濃度範囲の例については、参照によりその全開示内容が本明細書に援用される、Wayne著、PA.:NCCLS、1986年刊行の「National Committee for Clinical Laboratory Standards: Interferent Testing in Clinical Chemistry; proposed guideline EP7−P.」と題した刊行物に記載している。数式1を用いて算出したグルコース濃度が正確で(即ち、基準測定値の+/−10%内)、ばらつきが少なく(即ち、1σにおける試験片間のばらつきが約2%以下)なるように、標準的な最小化技術又は誤差処理技術を用いた時間期間、即ちi1、i2及びi3の選択の最適化を定義している。当業者には第1電流値、第2電流値及び第3電流値に選択した時間期間は同一でもよく、或いは異なってもよいことは明らかであり、一実施の形態では、二つの電流値のみを算出する。例えば、第2電流値i2は、第1電流値i1と同一となるように定義してもよい。
【0061】
時間期間i1、i2及びi3を選択後、試験片ロットを較正できる。試験片ロットを較正する代表的な方法については、参照によりその全開示内容が本明細書に援用される、米国特許第6,780,645号に記載している。より具体的には、較正係数a、p及び/又はZは、試験片のロット毎に算出できる。通常、複数の供与者から採血した血液中のグルコースの濃度範囲をグルコース試験片で試験し、正確で精度の高いことが知られている基準装置でも試験する。本発明の試験片により得た結果と基準法により得た結果の結果との誤差を、a、p及び/又はZの最適な組み合わせを求めて最小化する。一実施の形態では、試験片ロットから試験片を用いる前に、この較正情報を試験用計量器100へ送信し、及び/又は試験用計量器100に保存できる。
【0062】
サンプル中の干渉物質の存在を示すことができる検体濃度を算出する更なる方法について説明する。例えば、通風などの特定の疾病は人体の尿酸濃度を上昇させ、グルコース測定の精度に影響を与えることがある。尿酸塩は、作用電極面、及び/又は酸化された媒介物質により酸化されやすいため、多くの電気化学的測定において、潜在的な干渉物質となる。本発明の一実施の形態では、数式1を修正して尿酸塩などの干渉物質の存在下におけるグルコース測定精度を高めている。修正アルゴリズムを開発するため、第1過渡電流及び第2電流過度時における干渉物質の酸化に対応する数学的関係式を求めた。
【0063】
還元された媒介物質全体の濃度がグルコース試験時間期間TGの間サンプル反応チャンバ61内で変化しないと仮定した場合、第1過渡電流の電流の大きさは時間関数として以下の数式2で表すことができる。
【数2】

【0064】
issは、第1試験電位E1印加後の定常電流であり、Dは、媒介物質の拡散係数であり、Lは、スペーサ層60の厚みである。数式2においてtは第1試験電位E1を印加してから経過した時間を表す。図7の場合を例にとると、数式2で用いたtの値は、実時間から1秒引くことになる。第2電流過度の電流の大きさは時間関数として以下の数式3で表すことができる。
【数3】

第1試験電位E1と極性が反対の第2試験電位E2を第1試験電位E1の直後に印加しており、この第2試験電位E2から第2電流過度が生成されるため、数式3の指数項には数式2の指数項と異なる係数が2つある。数式3において、tは第2試験電位E2を印加してから経過した時間を表す。図7の場合を例にとると、数式3で用いたtの値は、実時間から4秒引くことになる。―0.3Vの第1試験電位E1を印加している間、第2電極164では干渉物質が酸化され、これにより、第1電極166では還元された媒介物質が生成される。還元された媒介物質が第1電極166で蓄積されるため、第2試験電位E2印加時の初期電流が指数項で2倍の大きさになる。
【0065】
図9に、サンプル反応チャンバ61内の濃度勾配をグラフで示し、数式2の指数項と数式3の指数項を比較した場合の2つの係数の違いを説明する。還元された媒介物質全体の濃度がグルコース試験時間期間TGの間サンプル反応チャンバ61内で変化しないと仮定した場合、酸化可能な種の濃度は、第1試験電位E1が試験片62に印加される前にサンプル反応チャンバ61内全体で均一になる必要がある。図9上で円で描いた複数の点は、濃度が1であることを示し、酸化可能な種の正規化濃度が一定であったことを表す。この初期濃度をバルク濃度と呼ぶことができる。第1試験電位E1が一旦印加されると、第2電極164における酸化可能な種の正規化濃度は直ちに枯渇し、濃度は0となる。図9において、第2電極164の表面はX軸上でゼロとして表され、第2電極164から第1電極66への正規化距離はX軸上で1として表されることに留意されたい。
【0066】
第1試験電位E1の印加後、酸化可能な種の正規化濃度は、第1電極166でバルク濃度の2倍となり、この場合では2となる。図9上で四角で描いた複数の点は、サンプル反応チャンバ61内の濃度勾配が線形であることを示し、酸化可能な種の正規化濃度は第1電極166で最大で、第2電極164で最小である。サンプル反応チャンバ61内における電荷保存則により、第2電極164で酸化可能な種が消費される毎に、第1電極166では酸化可能な種が生成される。このため、第1電極166における酸化可能な種の正規化濃度は、第1試験電位E1の印加後、2となる。
【0067】
第2試験電位E2を印加すると短時間後に電流は、E1を印加してから同様の時間が経過した時点の電流から定常電流を引いた値の2倍となる。2倍となる理由は、第1電極166の酸化可能な種の初期濃度がバルク濃度の2倍となるためである。反対に、第1試験電位E1を印加する前の第2電極164における酸化された種の初期の正規化濃度は半分に過ぎず、この場合、バルク濃度であった。定常電流を引く理由は、2本の電極間に存在する酸化可能な種の勾配により第1電極166から離間する電子の流れがあるためである。
【0068】
図7に示すように、第1試験電位時間期間T1にはipaで示すピーク電流があり、第2試験電位時間期間T2にはipbで示すピーク電流がある。第1ピーク電流ipa及び第2ピーク電流ipbは共に、第1試験電位E1及び第2試験電位E2を印加した後短時間後、例えば、0.1秒後にそれぞれ測定された。数式3から数式2を引いて数式4を導くことができる。
【数4】

【0069】
数式2に2を乗じて、加算の項を相殺したことに留意されたい。数式4は、試験片62を干渉物質を含むがグルコースを含まないサンプルで試験した場合の第1過渡電流と第2過渡電流との関係を示す。サンプル中にグルコースが含まれない場合、試薬層72はグルコース試験時間期間TG時に還元された媒介物質を生成しない。従って、第1及び第2過渡電流は両方とも干渉物質の酸化のみを反映することになる。上述の説明から、第1及び第2ピーク電流と定常電流の関係は、基本的な電気化学的数式に基づいて、或いは口頭/図形の発見的な議論により導出できることは明らかである。数式4は両方の方法から導き出せる。
【0070】
開回路時時間期間TOCを用いて、ピークが第1試験電位E1を印加した直後に形成されるよう第1ピーク電流値ipaの先鋭度を高めてもよい。公称開回路時間期間TOCはサンプル反応チャンバを完全に充填可能な時間である。更に、公称開回路時間期間TOCは、試薬層72が溶解され、酸化された媒介物質が第1電極166により還元され、限界酸化電流が第2電極164で測定できる時間である。
【0071】
第1及び第2過渡電流の大きさは、試薬層72がグルコース試験時間期間TG時に還元された媒介物質を生成する場合、より複雑な関係を有する。約1.1秒後の早い時期には、試薬層72がグルコース反応による還元された媒介物質を大量に生成しないと仮定する。更に、生成された還元された媒介物質のほとんどは、最初に試薬層72が付着していた第1電極166の近傍に残り、第2電極164へ拡散するものはわずかである仮定する。したがって、ipaの大きさの大部分は、第2電極164における干渉物質の酸化に起因する直接的な干渉電流である。
【0072】
約4.1秒後の遅い時期には、試薬層72がグルコースの存在する第1電極166においてグルコース反応によって還元された媒介物質を大量に生成すると仮定する。また、酸化された媒介物質により干渉物質が酸化される可能性があるため、大量の還元された媒介物質が生成される可能性はある。上述のように、酸化された媒介物質を還元する干渉物質は電流に寄与し、こうして生じる電流は間接電流と呼ぶことができる。更に、干渉物質はまた、第1電極164で直接酸化される可能性があり、こうして生じる電流は直接電流と呼ぶことができる。媒介物質が作用電極で酸化される可能性のある状況では、直接酸化と間接酸化の合計は、酸化された媒介物質が作用電極に付着しなかった場合に測定された直接酸化電流とほぼ等しいと仮定できる。要約すると、ipbの大きさは、間接的及び直接的な干渉物質の酸化、及び第2電極164におけるグルコース反応に起因する。ipaは、主に干渉物質により制御されると判断されるため、ipbをipaと共に用いて、補正係数を決定できる。例えば、以下に示すように、ipbをipaと共に用いた数学的関数により、グルコースと比例するが干渉物質の影響を受けにくい補正電流を決定できる。
【0073】
グルコースに比例するが、干渉物質に起因する電流の相当成分を除去した電流i4を算出するため、数式5を実験により導き出した。
【数5】

【0074】
issを分子及び分母の両方に加算し、グルコースが存在しない場合でも分子がゼロに近づくようにした。issは、最小時間を上回る時間の電流について、数式5Bを用いて概算でき、適当な最小時間は数式5Cから概算できる。
【数5B】

【数5C】

【0075】
issは第2電位を印加後の定常電流である。iは電流の測定値で時間関数である。Dはレドックス活性分子の拡散係数であり、この係数は、Fickの第1法則、即ち、J(x,t)=−D dC(x,t)/dxから決定できる。Lはスペーサの厚さである。tは第2電位の印加時間であり、t=0を第2時間期間の開始とする。
【0076】
数式1においてi1をi4で置き換えると、数式6に示す第2グルコースアルゴリズムが得られる。
【数6】

このように、数式6は、干渉物質の存在下で2本の電極のみを用いて正確なグルコースの測定を可能にする。
【0077】
本発明の他の実施の形態において、数式7に示すグルコースアルゴリズムを用いて、グルコースを干渉物質の存在下で測定できる。数式7では、初期濃度Coを補正係数で乗じている。生成物は、反応したグルコースの濃度とバックグラウンドの還元された媒介物質の和に比例する。したがって、Zを減算し、その結果を(iss/ipp)pで乗じ、サンプル中の全グルコースを測定する。
【数7】

【0078】
ippは、第1過渡電流から導かれる電流値である。一態様において、ippは、第1過渡電流の終端近傍の短時間期間にわたる電流の平均値である。例えば、電流の平均値は、3.8乃至4.0秒内に測定できる。Coは、グルコース濃度の概算値で、数式8によって定義される。
【数8】

【0079】
Fはファラデー定数、すなわち96,485C/moleである。Aは作用電極の面積である。
【0080】
特定の干渉物質は電極面で容易に直接酸化されることはない。例えば、アセトアミノフェンは、第1電極を−0.3Vに保持しても、金をスパッタリングして形成した第2電極164では容易に酸化しない可能性がある。第2電極164で直接干渉電流を測定できない場合、干渉物質によるipa及びipbの関係は、グルコースの存在しない数式4で表せなくなる。同様に、数式6及び数式7も、干渉物質の存在下におけるグルコースの正確な測定値を表さなくなる。第2電極164で干渉電流が測定されない問題を解決するため、酸化された媒介物質を含むが、酵素をほとんど含まない第2試薬層を、第2電極164に設けることができる。例えば、フェリシアニドなどの酸化された媒介物質は容易にアセトアミノフェンを酸化して、間接干渉電流を第2電極164で測定可能にできる。干渉物質の酸化を第2電極164で測定できるようにすることにより、数式6及ぶ数式7は干渉物質の存在下でグルコース濃度を正確に算出できるようになる。
【0081】
この問題を解決する他の実施の形態において、十分な量の酸化された媒介物質を第1電極上に、及び/又は、第1電極内に乾燥させて、セルを充填する際に酸化された媒介物質の一部がサンプルのバルクと混合しても大量の酵素がサンプルのバルクと混合することのないようにできる。これは、例えば、配合物中に十分な量の酸化された媒介物質を含有させ、酸化された媒介物質の少なくとも一部がほとんど酵素を含まずに結晶化するように十分にゆっくりと乾燥することによって実現できる。この結晶は溶解し、媒介物質は酵素よりも大きさがほぼ小さいことから、酵素よりも広範にサンプルと混合する。このようにして、潜在的な干渉物質を酸化された媒介物質により酸化できるので、干渉電流の一部として測定可能な還元された媒介物質を生成でき、第2試薬層を不要にできる。
【0082】
他の実施の形態においては、開回路電位を第1試験電位E1と第2試験電位E2の間に印加する。この開回路電位を「第2」開回路電位と呼ぶが、「第2」という言葉は便宜上用いたものであり、「第1」開回路電位を必要とするという意味ではない。第2開回路電位は電気化学的勾配を崩壊し、非摂動状態(即ち、第1試験電位E1の印加により、第1電極166に蓄積した酸化された媒介物質がバルク溶液に拡散して戻れる状態)に戻すことができる。このような条件の下、干渉物質の影響は、第2過渡電流から第1過渡電流を直接引くことにより、除去できる。上述したように、第1試験電位E1の直後に第2試験電位E2を印加した際、初期電流は、数式3の項に示すように、大きくなる。しかしながら、第2開回路電位を、第1電極166の還元された媒介物質の蓄積を散逸してバルク溶液に戻る程度に長く印加した場合、第2試験電位E2の初期電流は、第1試験電位E1の初期電流と等しくなる。このため、試験時間期間時に還元された媒介物質が生成されず、第2開回路電位を十分に長く印加した場合、第1及び第2試験電位の過渡電流は同一となる。
【0083】
還元された媒介物質が第1電極166から散逸するために要する時間は、標準的な拡散に関する数式を用いて予測できる。一般的に、第1電極166の表面で散逸する還元された媒介物質のフラクションは時間関数として、

に比例する。一例として、Lを95ミクロン、Dを4.5 x 10−6 cm2/sと仮定してもよい。図10に、還元された媒介物質の勾配の摂動の百分率を第2開回路時間期間の関数としてグラフで示す。この場合、摂動は、還元された媒介物質の濃度がバルク濃度に近づく前に既に散逸する必要のある還元された媒介物質の量を表す。上記の仮定の値をパラメータL及びDに用いると、第2開回路電位に要する十分に長い時間は約2.5秒間(即ち、5xL2/(4π2D))となる。本発明の一実施の形態において、第2開回路電位時間期間は、約1秒乃至約5秒の範囲、好ましくは約2秒乃至約4秒の範囲とできる。当業者は、所定の試験片のパラメータに応じて、グルコース反応のない条件で第1及び第2試験電位の過渡電流が同一となる十分に長い開回路電位時間期間を容易に決定できる。
【0084】
数式9に示す十分に長い開回路電位時間期間を用いた場合、簡易なアルゴリズムを用いて干渉物質の存在下のグルコース濃度を算出できる。
【数9】

【0085】
数式9で、切片(intercept)及び傾き(slope)は較正係数である。この場合、ipbはグルコース濃度及び干渉物質濃度と比例し、ipaは干渉物質濃度のみに比例する。ipbとipaの差異は、干渉物質成分を補正したグルコースに比例する電流となる。試験を実行するために使用する電気化学セルが同一平面上に電極を有する場合は数式9を用いることができる。
【0086】
数式10に、十分に長い開回路電位時間期間において干渉物質の存在下でグルコース濃度を算出する別の簡略化したアルゴリズムを示す。
【数10】

【0087】
数式10は、グルコース反応キネティクスを表す補正係数

を有する点以外は数式9と同様である。
【0088】
本明細書で開示する他の実施の形態において、血液中のヘモグロビン測定用の試験片を準備してもよい。この実施の形態では、試験片62の試薬層72を、フェリシアニドとデオキシコール酸ナトリウムなどの溶血試薬を含有する新試薬層に置き換える。血液を新試薬層に投与すると、赤血球は溶血し、フェリシアニドがヘモグロビンを酸化するようになる。ヘモグロビンセンサについては、参照によりその全開示内容が本明細書に援用される、米国特許第6,632,349号に記載している。続いて生成されたフェロシアニドを次にヘモグロビン電流として測定できる。グルコースと同様に、フェロシアニドはアッセイの初期段階時に第2電極164に到達しないものと仮定する。試験用計量器によって試験片内の血液が検出されると、試験用計量器は1秒間開回路電位を、3秒間第1試験電位−0.3Vを、5秒間試験電位+0.3Vを連続して印加できる。
【0089】
ヘモグロビン濃度Hは、以下の数式11に示す第1ヘモグロビンアルゴリズムを用いて測定できる。
【数11】

【0090】
この場合、Coはヘモグロビン濃度に比例し、標準的な回帰分析(傾き(slope)及び切片(intercept))を用いた基準技術で較正できる。しかしながら数式11は、干渉物質の存在下でヘモグロビンアッセイを正確に実行できるように修正できる。数式12は、ヘモグロビンセンサの精度を改善した第2ヘモグロビンアルゴリズムを示す。
【数12】

【0091】
ここで、issa及びissbは、それぞれ第1過渡電流及び第2過渡電流からの定常電流である。
【実施例1】
【0092】
シトラコン酸塩をpH6.8において67mM、0.1%の消泡剤(2部のプルロニック(Pluronic)P103と1部のプルロニックF87)、60mMのサッカロース及び1.7mMのCaCl2を含有する緩衝剤を調合した。次に、PQQ補助因子を用いたGDHを緩衝液に添加し、15mg/mLとした。その後PQQを緩衝液に添加し、GHDを活性化した。PQQの添加後、配合物を約1時間インキュベートさせた。次に、フェリシアン化カリウムを混合物に添加し、600mMとした。配合物は、参照によりその全開示内容が本明細書に援用される、米国特許第6,749,887号、6,689,411号及び6,676,995号に記載したスロットコーティング処理により図1に示す第1導電層66上にストライプした。配合物をコーティングし、乾燥させ、試薬層72、スペーサ層60及び第2電極164をその上に組立て、試験片62を形成する。
【実施例2】
【0093】
複数の試験片62を約83乃至88mg/dLの範囲の濃度のグルコースを含有する血液で試験した。血液サンプルには干渉物質を混入した。試験片62は試験用計量器100を用いて5秒間のグルコース試験時間期間TG試験した。試験用計量器100には図6に示す電位波形を印加した。試験片毎に試験電流を測定し、数式1に示す第1グルコースアルゴリズム及び数式6に示す第2グルコースアルゴリズムを用いてグルコース濃度に変換した。試験片毎にmg/dLの単位で基準法に対する平均バイアスを算出した結果を図11に示す。図11から、第1グルコースアルゴリズムを用いた場合と比較して第2グルコースアルゴリズムを用いた場合、アスコルビン酸塩及び尿酸塩などの干渉物質の存在下における全体的なバイアスが削減されたことがわかる。
【実施例3】
【0094】
異なる試験片62のセットを用いて同様の方法で本実施例3の実験を繰り返した。この実験では、試験片毎に試験電流を測定し、数式1に示す第1グルコースアルゴリズム及び数式7に示す第3グルコースアルゴリズムを用いてグルコース濃度に変換した。試験片毎にmg/dLの単位で基準法に対する平均バイアスを算出した結果を図12に示す。図12から、第1グルコースアルゴリズムを用いた場合に対して第3グルコースアルゴリズムを用いた場合、干渉物質の存在下における全体的なバイアスが削減されたことがわかる。簡単な電流の合計値の代わりに、Coを用いることにより、干渉物質の存在下におけるより正確な測定を可能にできる。
【実施例4】
【0095】
ヘモグロビン測定用の試験片62を複数用意した。複数の試験片62を16.3g/dLの濃度のヘモグロビンを含有する血液で試験した。血液サンプルには干渉物質を混入した。試験片毎に試験電流を測定し、数式9に示す第1ヘモグロビン数式及び数式10に示す第2ヘモグロビン数式を用いてヘモグロビン濃度に変換した。試験片毎にmg/dLの単位で基準法に対する平均バイアスを算出した結果を図13に示す。図13から、第1ヘモグロビン数式を用いた場合に対して第2グルコース数式を用いた場合、アスコルビン酸塩(AA=10 mg/dL)、尿酸塩(UA=10mg/dL)及びアセトアミノフェン(Acet=20mg/dL)などの干渉物質の存在下における全体的なバイアスが削減されたことがわかる。
【0096】
当業者であれば、上記の実施態様に基づき、本発明の更なる特徴及び利点を想起することができるであろう。したがって、本発明は、添付された請求項により示された内容以外の、具体的に示されまた記載された内容に限定されることはない。本明細書において記載された全ての刊行物及び参考文献は、ここに本明細書の一部を構成するものとしてその内容を援用する。
【0097】
本発明の新規な特長について、添付の特許請求の範囲に詳細に記載する。本発明の特長及び利点は、本発明の原理を用いた例示された実施の形態に記載される詳細な説明及び添付の図面を参照してより理解される。
【図面の簡単な説明】
【0098】
【図1A】本発明の方法の使用に好適な組立済み試験片の斜視図。
【図1B】本発明の方法の使用に好適な試験片の分解斜視図。
【図1C】本発明の方法の使用に好適な試験片近端部分の拡大斜視図。
【図2】本発明の一実施の形態の試験片の底面図。
【図3】図2に示した試験片の側面図。
【図4A】図3に示した試験片の上面図。
【図4B】図4Aに示した試験片における近端部分の4A−4A矢視拡大側面図。
【図5】本発明の試験片の一部と電気的に接続する試験用計器の簡略図。
【図6】試験用計器が所定の時間期間で連続して印加する開回路電位と試験電位の電位波形の例。
【図7】干渉物質を添加していない濃度62mg/dLのグルコースを含有した生理学的サンプル(実線)と濃度20mg/dLのアスコルビン酸塩を含有した生理学的サンプル(点線)を試験して生成した第1過渡電流及び第2過渡電流を示すグラフ。
【図8】第1過渡電流を示す図7の拡大図。
【図9】サンプル反応チャンバ内の還元された媒介物質の濃度勾配を示すグラフ。
【図10】第1電極における還元された媒介物質の勾配の摂動百分率を第2開回路時間期間の関数として示すグラフ。
【図11】第1グルコースアルゴリズムと第2グルコースアルゴリズムを用いた場合におけるグルコース濃度測定結果のバイアスの絶対値を示すグラフ。
【図12】第1グルコースアルゴリズムと第3グルコースアルゴリズムを用いた場合におけるグルコース濃度測定結果のバイアスの絶対値を示すグラフ。
【図13】第1ヘモグロビンルゴリズムと第2ヘモグロビンアルゴリズムを用いて特定の干渉物質の存在下でヘモグロビン濃度を測定した場合におけるバイアスの絶対値を示すグラフ。
【符号の説明】
【0099】
61 反応チャンバ
62 試験片
100 試験用計量器
166 第1電極
164 第2電極
【特許請求の範囲】
【請求項1】
検体濃度試験における干渉物質の影響を低減する方法であって、当該方法は、
(a)(i)相互に離間した第1電極及び第2電極と、(ii)第1試薬層とを備えた電気化学的セルに生理学的サンプルを導入するステップと、
(b)第1の極性を有する第1試験電位を前記セルに印加し、セル電流を測定し、第1ピーク電流値を得るステップと、
(c)第2試験電位を印加し、セル電流を測定し、第2ピーク電流値を得るステップと、
(d)前記第1ピーク電流値及び前記第2ピーク電流値に基づいて、グルコース濃度算出における干渉物質の影響を低減するために用いることができる干渉補正係数を算出するステップとを含んでなる方法。
【請求項2】
前記ステップ(c)が更に、セル電流を時間関数として測定し、第2過渡電流を得て、前記第2過渡電流に基づいて第1電流値を算出するステップを含む、請求項1記載の方法。
【請求項3】
更に、前記第1電流値から干渉電流値を除去することによって、第1補正電流値を算出するステップを含む、請求項2記載の方法。
【請求項4】
前記第1補正電流値を算出するステップが、干渉物質補正数式によって前記第1電流値を積算するステップを含み、
前記干渉物質補正数式は、

であり、
ipbは前記第1ピーク電流値、ipaは前記第2ピーク電流値、issは定常電流値である、請求項3記載の方法。
【請求項5】
前記方法は更に、前記第2過渡電流に基づいて第2電流値を算出するステップと、前記ステップ(b)において、セル電流を時間関数として測定し、第1過渡電流を得て、前記第1過渡電流に基づいて第3電流値を算出するステップを含む、請求項4記載の方法。
【請求項6】
更に、数式

に基づいて検体濃度を算出するステップを含み、[C]が検体濃度、i4が前記第1補正電流値、i2が前記第2電流値、i3が前記第3電流値、a、p及びZは補正係数である、請求項5記載の方法。
【請求項7】
前記第1試薬層が前記第1電極上に配設される、請求項1記載の方法。
【請求項8】
前記第1の極性が前記第2電極に対して負であり、前記第2の極性が前記第2の電極に対して正である、請求項7記載の方法。
【請求項9】
レドックス媒介物質を含むが、ほとんど酵素を含まない第2試薬層が前記第2電極上に配設され、前記レドックス媒介物質は、生理学的サンプル内に存在する干渉物質を酸化できる、請求項8記載の方法。
【請求項10】
前記ステップ(c)が、更に、セル電流を時間関数として測定し、第2過渡電流を得る、請求項1記載の方法。
【請求項11】
検体濃度が数式

に基づいて算出され、[C]が検体濃度、ippが前記第2過渡電流から導出される電流値、Coがグルコース濃度概算値、ipaが前記第1ピーク電流値、ipbが前記第2ピーク電流値、issが定常電流値、Zが較正係数である、請求項1記載の方法。
【請求項12】
ippが、第2過渡電流終端近傍の短時間期間にわたる電流の平均値である、請求項11記載の方法。
【請求項13】
検体と干渉物質の両方を含有した生理学的サンプルにおける検体濃度を決定する方法であって、当該方法は、
(a)(i)相互に離間した第1電極及び第2電極と、(ii)酵素及び媒介物質を含有する第1試薬層とを備えた電気化学的セルに生理学的サンプルを導入するステップと、
(b)第1の極性を有する第1試験電位を前記セルに印加し、セル電流を測定し、第1ピーク電流値を決定するステップと、
(c)開回路電位時間期間を経過させるステップと、
(d)開回路電位時間期間の後、第2の極性を有する第2試験電位を印加し、セル電流を測定し、第2ピーク電流値を決定するステップと、
(e)前記第2ピーク電流値から前記第1ピーク電流値を減算して、前記サンプル内の前記検体濃度と比例する補正電流値を決定するステップと、
(f)前記補正電流を用いて検体濃度を算出するステップとを含んでなる方法。
【請求項14】
前記開回路電位時間期間が、約1秒乃至5秒の範囲である、請求項13記載の方法。
【請求項15】
前記開回路電位時間期間が、約2秒乃至3秒の範囲である、請求項13記載の方法。
【請求項16】
前記検体濃度が、数式

に基づいて算出され、[C]が検体濃度、ipaが前記第1ピーク電流値、ipbが前記第2ピーク電流値、slope及びinterceptが較正係数である、請求項13記載の方法。
【請求項17】
更に、前記ステップ(b)において第1過渡電流を測定し、前記ステップ(c)において第2過渡電流を測定するステップを含む、請求項13記載の方法。
【請求項18】
前記検体濃度が、数式

に基づいて算出され、
[C]が検体濃度、ipaが前記第1ピーク電流値、ipbが前記第2ピーク電流値、i2が前記第2過渡電流から導出される電流値、i3が前記第1過渡電流から導出される電流値、slope及びinterceptが較正係数である、請求項17記載の方法。
【請求項19】
検体と干渉物質の両方を含有した生理学的サンプルにおける検体濃度を決定する方法であって、当該方法は、
(a)(i)相互に離間した第1電極及び第2電極と、(ii)試薬層とを備えた電気化学的セルに生理学的サンプルを導入するステップと、
(b)第1の極性を有する第1試験電位を前記セルに印加し、セル電流を測定するステップと、
(c)第2の極性を有する第2試験電位を印加し、セル電流を測定するステップと、
(d)前記(b)の前記電流測定から第1定常電流値を決定するステップと、
(e)前記(c)の前記電流測定から第2定常電流値を決定するステップと、
(f)前記第2定常電流値から前記第1定常電流値を減算し、検体濃度に比例するが、干渉物質の影響の少ない値を決定するステップとを含んでなる方法。
【請求項20】
前記検体濃度は、数式

に基づいて算出され、
[H]が、検体濃度、issaが前記第1過渡電流からの定常電流、issbが前記第2過渡電流からの定常電流、slope及びinterceptが較正係数、Fがファラデー定数、Aが第1電極の面積、Dがレドックス活性分子の拡散係数、Lが電極の間隔である、請求項19記載の方法。
【請求項21】
前記検体がヘモグロビンである、請求項18記載の方法。
【請求項1】
検体濃度試験における干渉物質の影響を低減する方法であって、当該方法は、
(a)(i)相互に離間した第1電極及び第2電極と、(ii)第1試薬層とを備えた電気化学的セルに生理学的サンプルを導入するステップと、
(b)第1の極性を有する第1試験電位を前記セルに印加し、セル電流を測定し、第1ピーク電流値を得るステップと、
(c)第2試験電位を印加し、セル電流を測定し、第2ピーク電流値を得るステップと、
(d)前記第1ピーク電流値及び前記第2ピーク電流値に基づいて、グルコース濃度算出における干渉物質の影響を低減するために用いることができる干渉補正係数を算出するステップとを含んでなる方法。
【請求項2】
前記ステップ(c)が更に、セル電流を時間関数として測定し、第2過渡電流を得て、前記第2過渡電流に基づいて第1電流値を算出するステップを含む、請求項1記載の方法。
【請求項3】
更に、前記第1電流値から干渉電流値を除去することによって、第1補正電流値を算出するステップを含む、請求項2記載の方法。
【請求項4】
前記第1補正電流値を算出するステップが、干渉物質補正数式によって前記第1電流値を積算するステップを含み、
前記干渉物質補正数式は、

であり、
ipbは前記第1ピーク電流値、ipaは前記第2ピーク電流値、issは定常電流値である、請求項3記載の方法。
【請求項5】
前記方法は更に、前記第2過渡電流に基づいて第2電流値を算出するステップと、前記ステップ(b)において、セル電流を時間関数として測定し、第1過渡電流を得て、前記第1過渡電流に基づいて第3電流値を算出するステップを含む、請求項4記載の方法。
【請求項6】
更に、数式

に基づいて検体濃度を算出するステップを含み、[C]が検体濃度、i4が前記第1補正電流値、i2が前記第2電流値、i3が前記第3電流値、a、p及びZは補正係数である、請求項5記載の方法。
【請求項7】
前記第1試薬層が前記第1電極上に配設される、請求項1記載の方法。
【請求項8】
前記第1の極性が前記第2電極に対して負であり、前記第2の極性が前記第2の電極に対して正である、請求項7記載の方法。
【請求項9】
レドックス媒介物質を含むが、ほとんど酵素を含まない第2試薬層が前記第2電極上に配設され、前記レドックス媒介物質は、生理学的サンプル内に存在する干渉物質を酸化できる、請求項8記載の方法。
【請求項10】
前記ステップ(c)が、更に、セル電流を時間関数として測定し、第2過渡電流を得る、請求項1記載の方法。
【請求項11】
検体濃度が数式

に基づいて算出され、[C]が検体濃度、ippが前記第2過渡電流から導出される電流値、Coがグルコース濃度概算値、ipaが前記第1ピーク電流値、ipbが前記第2ピーク電流値、issが定常電流値、Zが較正係数である、請求項1記載の方法。
【請求項12】
ippが、第2過渡電流終端近傍の短時間期間にわたる電流の平均値である、請求項11記載の方法。
【請求項13】
検体と干渉物質の両方を含有した生理学的サンプルにおける検体濃度を決定する方法であって、当該方法は、
(a)(i)相互に離間した第1電極及び第2電極と、(ii)酵素及び媒介物質を含有する第1試薬層とを備えた電気化学的セルに生理学的サンプルを導入するステップと、
(b)第1の極性を有する第1試験電位を前記セルに印加し、セル電流を測定し、第1ピーク電流値を決定するステップと、
(c)開回路電位時間期間を経過させるステップと、
(d)開回路電位時間期間の後、第2の極性を有する第2試験電位を印加し、セル電流を測定し、第2ピーク電流値を決定するステップと、
(e)前記第2ピーク電流値から前記第1ピーク電流値を減算して、前記サンプル内の前記検体濃度と比例する補正電流値を決定するステップと、
(f)前記補正電流を用いて検体濃度を算出するステップとを含んでなる方法。
【請求項14】
前記開回路電位時間期間が、約1秒乃至5秒の範囲である、請求項13記載の方法。
【請求項15】
前記開回路電位時間期間が、約2秒乃至3秒の範囲である、請求項13記載の方法。
【請求項16】
前記検体濃度が、数式

に基づいて算出され、[C]が検体濃度、ipaが前記第1ピーク電流値、ipbが前記第2ピーク電流値、slope及びinterceptが較正係数である、請求項13記載の方法。
【請求項17】
更に、前記ステップ(b)において第1過渡電流を測定し、前記ステップ(c)において第2過渡電流を測定するステップを含む、請求項13記載の方法。
【請求項18】
前記検体濃度が、数式

に基づいて算出され、
[C]が検体濃度、ipaが前記第1ピーク電流値、ipbが前記第2ピーク電流値、i2が前記第2過渡電流から導出される電流値、i3が前記第1過渡電流から導出される電流値、slope及びinterceptが較正係数である、請求項17記載の方法。
【請求項19】
検体と干渉物質の両方を含有した生理学的サンプルにおける検体濃度を決定する方法であって、当該方法は、
(a)(i)相互に離間した第1電極及び第2電極と、(ii)試薬層とを備えた電気化学的セルに生理学的サンプルを導入するステップと、
(b)第1の極性を有する第1試験電位を前記セルに印加し、セル電流を測定するステップと、
(c)第2の極性を有する第2試験電位を印加し、セル電流を測定するステップと、
(d)前記(b)の前記電流測定から第1定常電流値を決定するステップと、
(e)前記(c)の前記電流測定から第2定常電流値を決定するステップと、
(f)前記第2定常電流値から前記第1定常電流値を減算し、検体濃度に比例するが、干渉物質の影響の少ない値を決定するステップとを含んでなる方法。
【請求項20】
前記検体濃度は、数式

に基づいて算出され、
[H]が、検体濃度、issaが前記第1過渡電流からの定常電流、issbが前記第2過渡電流からの定常電流、slope及びinterceptが較正係数、Fがファラデー定数、Aが第1電極の面積、Dがレドックス活性分子の拡散係数、Lが電極の間隔である、請求項19記載の方法。
【請求項21】
前記検体がヘモグロビンである、請求項18記載の方法。
【図1A】


【図1B】


【図1C】


【図2】


【図3】


【図4A】


【図4B】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】




【図1B】


【図1C】


【図2】


【図3】


【図4A】


【図4B】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【公開番号】特開2007−271622(P2007−271622A)
【公開日】平成19年10月18日(2007.10.18)
【国際特許分類】
【外国語出願】
【出願番号】特願2007−87635(P2007−87635)
【出願日】平成19年3月29日(2007.3.29)
【出願人】(596159500)ライフスキャン・インコーポレイテッド (100)
【氏名又は名称原語表記】Lifescan,Inc.
【住所又は居所原語表記】1000 Gibraltar Drive,Milpitas,California 95035,United States of America
【公開日】平成19年10月18日(2007.10.18)
【国際特許分類】
【出願番号】特願2007−87635(P2007−87635)
【出願日】平成19年3月29日(2007.3.29)
【出願人】(596159500)ライフスキャン・インコーポレイテッド (100)
【氏名又は名称原語表記】Lifescan,Inc.
【住所又は居所原語表記】1000 Gibraltar Drive,Milpitas,California 95035,United States of America
[ Back to top ]

