核酸増幅反応装置、核酸増幅反応装置に用いる基板、及び核酸増幅反応方法
【課題】より高い検出感度が得られる核酸増幅反応装置を提供すること。
【解決手段】光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、反応領域の水平断面積が小さくなるようにテーパウェル形状に形成された、核酸増幅反応の反応場となる反応領域と、前記反応領域を加熱する温度制御手段と、前記反応領域に光を照射する照射手段と、前記反応領域からの前記析出する物質による光の散乱光量を検出する検出手段と、を備える、核酸増幅反応装置。
【解決手段】光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、反応領域の水平断面積が小さくなるようにテーパウェル形状に形成された、核酸増幅反応の反応場となる反応領域と、前記反応領域を加熱する温度制御手段と、前記反応領域に光を照射する照射手段と、前記反応領域からの前記析出する物質による光の散乱光量を検出する検出手段と、を備える、核酸増幅反応装置。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、核酸増幅反応装置、核酸増幅反応装置に用いる基板、及び核酸増幅反応方法に関する。より詳細には、核酸増幅反応の反応場となる反応領域をテーパウェル形状に形成し、これを備える核酸増幅反応装置等に関する。
【背景技術】
【0002】
近年、PCR法(Polymerase Chain Reaction;ポリメラーゼ連鎖反応)やLAMP法(Loop-Mediated Isothermal Amplification)等による遺伝子増幅反応を行って検証することが微量核酸の定量分析の標準的手法となっている。このような手法によって、遺伝子発現解析、遺伝的疾患、癌化、微生物やウイルス等の感染症の検査、またSNP解析等の遺伝子解析が進められている。
ここで、核酸の増幅産物を検出する方法において、インターカレーター法や蛍光標識プローブ法等のように蛍光物質を用いる蛍光検出方法、また増幅過程での副産物のピロリン酸にマグネシウムイオン等の金属イオンで水に不溶又は難溶性の塩を形成した濁度物質を用いる濁度検出法等が主として用いられている(特許文献1〜3)。
上述のような核酸の増幅産物を検出する方法を用いて、遺伝子発現解析、感染症検査、またSNP解析等の遺伝子解析が行える核酸増幅反応装置が広く市販されている。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特開2008−237207号公報
【特許文献2】国際公開第01/83817号パンフレット
【特許文献3】特許413347号公報
【発明の概要】
【発明が解決しようとする課題】
【0004】
そして、これら核酸増幅反応装置において、円筒状ウェルプレートを一般的に用いているが、更なる検出感度の向上が求められている。
【0005】
そこで、本発明は、より高い検出感度が得られる核酸増幅反応装置、核酸増幅反応装置に用いる基板、及び核酸増幅反応方法を提供することを主目的とする。
【課題を解決するための手段】
【0006】
上記課題解決のために、本発明は、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、反応領域の水平断面積が小さくなるようにテーパウェル形状に形成された、核酸増幅反応の反応場となる反応領域と、前記反応領域を加熱する温度制御手段と、前記反応領域に光を照射する照射手段と、前記反応領域からの前記析出する物質による光の散乱光量を検出する検出手段と、を備える、核酸増幅反応装置を提供する。
また、前記反応領域の内面の傾斜面が、滑面処理されたものが好適である。
【0007】
また、本発明は、核酸増幅反応の反応場となる反応領域が形成され、該反応領域は、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、領域断面積が小さくなるように形成されたテーパウェルである核酸増幅反応用マイクロチップを提供する。
【0008】
また、本発明は、核酸増幅反応の反応場となる反応領域に光を照射して、増幅反応の進行に伴って析出する物質による前記光の散乱光量を検出する手順を含み、前記反応領域として、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、領域断面積が小さくなるように形成されたテーパウェルを用いる核酸増幅反応方法を提供する。
【発明の効果】
【0009】
本発明によれば、より高い検出感度が得られる核酸増幅反応装置、基板及び核酸増幅反応方法が提供される。
【図面の簡単な説明】
【0010】
【図1】本発明に係わる核酸増幅反応装置における概念図を示す。
【図2】本発明に係わる核酸増幅反応用マイクロチップにおける反応領域の光軸方向に沿った垂直断面図を示す。
【発明を実施するための形態】
【0011】
以下、本発明を実施するための好適な形態について図面を参照しながら説明する。なお、以下に説明する実施形態は、本発明の代表的な実施形態の一例を示したものであり、これにより本発明の範囲が狭く解釈されることはない。
【0012】
1.核酸増幅反応装置
(1)反応領域
(a)基板(核酸増幅反応用マイクロチップ)
(b)核酸増幅反応
(c)核酸増幅(産物)の検出方法
(2)温度制御手段
(3)照射手段
(4)検出手段
2.核酸増幅反応装置の動作
(1)変形例
(a)RT−LAMP装置の動作
(b)RT−PCR装置の動作
【0013】
<1.核酸増幅反応装置>
図1は、本発明に係わる核酸増幅反応装置における概念図である。また、図2は、本発明に係わる核酸増幅反応用マイクロチップにおける反応領域の光軸方向に沿った垂直断面図である。
なお、以下に説明する図面では、説明の便宜上、装置の構成等を簡略化して示している。
【0014】
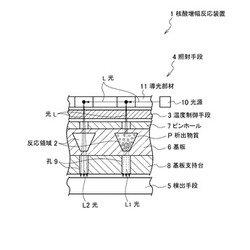
本発明に係わる核酸増幅反応装置1は、核酸増幅反応を制御して、核酸を増幅させ、定量するための、反応領域2、温度制御手段3、照射手段4及び検出手段5から構成されている。
本発明の核酸増幅反応装置1は、照射手段4と検出手段5との間に温度制御手段3及び脱着可能な反応領域2(基板6)が配置されている。
更に、反応領域2と照射手段4の間には、光量や光成分等を調整するために、適宜、ピンホール7、フィルタ(図示せず)、集光レンズ(図示せず)を配設してもよい。また、反応領域2と検出手段5の間には、光量や光成分等を調整するためや反応領域2を支持するために、適宜、基板支持台8、フィルタ(図示せず)、集光レンズ(図示せず)を配設してもよい。
尚、本発明の核酸増幅反応装置1には、本発明の装置に関しての各種動作(例えば、光制御、温度制御、核酸増幅反応、検出制御、検出光量算出やモニタリング等)を制御する制御部(図示せず)が備えられている。
以下に各構成について詳細に説明する。
【0015】
(1)反応領域
前記反応領域2は、核酸の増幅反応の反応場となるエリアであり、テーパウェル形状に形成されている。
前記テーパウェルは、光軸方向で核酸増幅反応の進行に伴って析出する物質Pが沈降する方向に従って、反応領域の水平断面積が小さくなるように形成されているものである。
【0016】
ところで、一般的なウェル、例えば円筒状ウェルでは、反応初期時の低散乱状態において検出感度や検出精度を向上させるためには、反応場中の光線透過距離を長くする、すなわち、光軸方向に従ってウェルを伸長させる必要がある。しかし、ウェルを伸長させることにより核酸増幅反応の温度制御をする熱源からの距離が拡大するためウェル内部で温度差が拡大するので、核酸増幅の反応効率が低下したり、反応にむらができ検出が不安定になり易い。
ところが、本発明の如く反応領域をテーパウェル形状とすることにより、反応場中の析出・沈降する物質が、ウェル底面側でより高濃度となり、散乱の度合いが増す。すなわち、テーパウェル形状として光線透過領域の散乱断面積を制御することで、反応領域の水平断面積において局所的に析出物質の凝集度が高まることとなる。よって、光線通過距離を長くしなくとも、反応領域中の微量な核酸でも検出することが可能となり、また初期反応時(低散乱)での検出感度が向上し、また、モニタリングも良好となる。
このように反応領域をテーパウェル形状にすることにより、核酸増幅反応による濁度検出における検出感度や検出精度が良好となる。また、本発明のテーパウェル形状を有する核酸増幅反応用マイクロチップを用いることによって、高効率な濁度検出を実現することも可能となる。更に散乱距離を拡大しなくとも、装置の性能や信頼性を確保できるので、核酸増幅反応装置全体の小型化、特に薄型化も行い易い。
【0017】
図2は、反応領域2の底面21の中心を通る垂直平面で切断した反応領域2の断面形状の例示である。また、破線の2Cは円筒状ウェルの垂直断面形状を示す。
前記反応領域2は、底面21及び上面22を有し、この何れの面にも同一光軸方向で光を通過させることが可能な平面を有するのが好適である。また、これら両面は互いに平行する対向面であるのが好適である。
更に、底面21及び上面22を設ける反応領域2は、前記析出物質Pが沈降しやすいように傾斜面23を有する。そして、光軸方向で垂直断面した際の前記反応領域2の傾斜面23,23は、底面21方向に従って反応領域2の幅が小さくなるような形状とするのが好適である。当該形状としては、例えば、角錐台形状2Aや凹型放物面形状2B等が挙げられる。
また、前記反応領域2の内面(傾斜面23)の立体形状は、例えば、円錐台や多角錐台の錐台形状や光軸を中心とした回転放物面形状等が挙げられる。このうち、形成が容易なので、円錐台形状が好適である。円筒状ウェル2Cの容量と同じ容量でかつ同じ光線透過距離である場合でも、テーパ型の傾斜面23として光線透過領域の散乱断面積を制御することによって、検出感度及び検出精度の向上が可能となる。具体的には、前記反応領域2の底面21の面積が、この上面22の面積を1としたとき、1/2〜1/5、より1/3〜1/4とするのが好適である。この範囲内の面積比に底面21の面積をすることによって、前記析出物質Pが傾斜面23に吸着せずに沈降し易い傾斜を形成することが可能となる。よって、底面側で局所的に析出物質の凝集度を効率よく上げることも可能となるので、核酸増幅反応の濁度検出における検出感度や検出精度が良好となる。
【0018】
更に、前記反応領域2は、傾斜面23の内面に滑面処理されたものが好適である。これにより、前記析出物質(粒子)Pの当該傾斜面への表面付着が更に軽減され、かつこの傾斜により、より前記析出物質Pがウェル底面側で高濃度になり易い。よって、更に濁度検出における検出感度や検出精度が良好となる。
前記滑面処理としては、研磨処理、コーティング処理等が挙げられる。研磨処理としては、研磨剤を用いて行う化学機械研磨処理等が挙げられる。当該研磨剤としては、無機充填剤(粒子)を含む、プラスチック基板やガラス基板等を研磨するためのスラリー状のものが挙げられる。当該無機充填剤としては、例えば炭酸カルシウム、水酸化アルミニウム、水酸化カルシウム、水酸化マグネシウム、酸化チタン、無水珪酸、珪石等から選ばれる1種又は2種以上のものが挙げられる。
またコーティング処理に用いるコーティング剤としては、シリコン等が挙げられ、好ましくは透過性の高いシリコンが有利である。透過性の高いシリコンを用いることにより反応領域2内面の全面に塗布することも可能となるので核酸増幅反応用マイクロチップ等の反応領域2を有する基板の作製効率が良好となる。
【0019】
(a)基板(核酸増幅反応用マイクロチップ)
前記反応領域2は、例えば、核酸増幅反応用マイクロチップ等の反応容器(例えば、基板)内に単数又は複数形成されているのが好適である。このような反応容器であれば、上述のようなテーパウェル形状を形成し易い。
前記反応領域2を備える核酸増幅反応用マイクロチップ(基板6)は、単数又は複数の基板から形成することができる。
前記基板6の両端面のうち、一端の面は光が照射される面(上面22方向)であり、他端の面は反応領域(反応場中の光線通路)を通過した光が出射される面(底面21方向)であり、これらは互いに平行する対向面であるのが好適である。
これにより、光を反応領域2の上面22に照射して、反応領域2を通過させ、底面21から出射して光の散乱光量や透過光量を検出手段5にて測定する。尚、前記核酸増幅反応用マイクロチップの反応領域2の底面側に、反応領域2の側方から光を照射して光の散乱光量や透過光量を測定することも可能である。
【0020】
前記反応領域2の基板6への形成方法は、特に限定されないが、例えば、ガラス製基板層のウェットエッチングやドライエッチングによって、又はプラスチック製基板層のナノインプリントや射出形成、切削加工によって行うことが好適である。
例えば、前記反応領域2の形成方法としては、角錐台形状2Aや凹型放物面形状2B等のような反応領域2を研磨切削加工や鋳型成形等にて1つの基板上に単数又は複数形成し、この基板の上面に他の基板を配置すること等が挙げられる。
また、前記基板6の材料は、特に限定されず、検出方法や加工容易性、耐久性等を考慮して適宜選択するのが好適である。当該材料としては、光透過性のある素材で所望の検出方法に応じて適宜選択すればよく、例えば、ガラスや各種プラスチック(ポリプロピレン、ポリカーボネイト、シクロオレフィンポリマー、ポリジメチルシロキサン等)が挙げられる。
このようにして形成された反応領域2には、核酸増幅反応に必要な試薬類を予め充填していてもよい。
【0021】
(b)核酸増幅反応
本発明において、「核酸増幅反応」には、温度サイクルを実施する従来のPCR(polymerase chain reaction)法や、温度サイクルを伴わない各種等温増幅法が含まれる。等温増幅法としては、例えば、LAMP(Loop-Mediated Isothermal Amplification)法やSMAP(SMartAmplification Process)法、NASBA(Nucleic Acid Sequence-Based Amplification)法、ICAN(Isothermal and Chimeric primer-initiated Amplification of Nucleic acids)法(登録商標)、TRC(transcription-reverse transcription concerted)法、SDA(strand displacement amplification)法、TMA(transcription-mediated amplification)法、RCA(rolling circle amplification)法等が挙げられる。
この他、「核酸増幅反応」には、核酸の増幅を目的とする変温あるいは等温による核酸増幅反応が広く包含されるものとする。また、これらの核酸増幅反応には、リアルタイムPCR(RT−PCR)法やRT−LAMP法などの増幅核酸鎖の定量を伴う反応も包含される。
【0022】
また、「試薬」には、上記の核酸増幅反応において、増幅核酸鎖を得るために必要な試
薬であって、具体的には、標的核酸鎖に相補的な塩基配列とされたオリゴヌクレオチドプ
ライマー、核酸モノマー(dNTP)、酵素、反応緩衝液(バッファー)溶質などが含ま
れる。
【0023】
前記PCR法は、「熱変性(約95℃)→プライマーのアニーリング(約55〜60℃)→伸長反応(約72℃)」という増幅サイクルを連続的に行う。
また、前記LAMP法とは、DNAのループ形成を利用して、一定温度でDNAやRNAからdsDNAを増幅産物として得る方法である。一例として、成分(i)、(ii)(iii)を加え、インナープライマーが鋳型核酸上の相補的配列に対して安定的な塩基対結合を形成することができ、かつ鎖置換型ポリメラーゼが酵素活性を維持しうる温度でインキュベートすることにより進行する。このときのインキュベート温度は50〜70℃、時間は1分〜10時間程度が好適である。
成分(i)インナープラマー2種、又は更にアウタープライマー2種、又は更にループプライマー2種;成分(ii)鎖置換型ポリメラーゼ;成分(iii)基質ヌクレオチド。
【0024】
(c)核酸増幅(産物)の検出方法
前記核酸増幅の検出方法としては、例えば、濁度物質、蛍光物質や化学発光物質等を用いる方法が挙げられる。
【0025】
また、前記濁度物質を用いる方法としては、例えば核酸増幅反応の結果生じるピロリン酸とこれに結合可能な金属イオンにより生じた析出物質を用いる方法等が挙げられる。当該金属イオンは、一価又は二価の金属イオンであり、ピロリン酸と結合すると水に不溶又は難溶性の塩を形成して濁度物質となる。
当該金属イオンとしては、具体的には、アルカリ金属イオン、アルカリ土類金属イオン及び二価遷移金属イオン等が挙げられる。このうち、例えば、マグネシウム(II)、カルシウム(II)及びバリウム(II)等のアルカリ土類金属イオン;亜鉛(II)、鉛(II)、マンガン(II)、ニッケル(II)及び鉄(II)等の二価遷移金属イオン等から選ばれる1種又は2以上が好ましい。更に好ましくは、マグネシウム(II)、マンガン(II)、ニッケル(II)及び鉄(II)である。
当該金属イオンを添加するときの濃度は、0.01〜100mMの範囲であれば好適である。検出波長は、300〜800nmとするのが好適である。
【0026】
また、前記蛍光物質や化学発光物質を用いる方法としては、例えば、二本鎖核酸に特異的に挿入されて蛍光を発する蛍光色素(誘導体)を用いるインターカレート方法、増幅する核酸配列に特異的なオリゴヌクレオチドに蛍光色素を結合させたプローブを用いる標識プローブ方法等が挙げられる。
前記標識プローブ法としては、例えばハイブリダイゼーション(Hyb)プローブ法、加水分解(TaqMan)プローブ法等が挙げられる。
前記Hybプローブ法は、予め2種のプローブが近接するようにデザインされたドナー色素でラベルされたプローブとアクセプター色素でラベルされたプローブという2種のプローブを用いる方法である。そして、当該2種のプローブが標的核酸にハイブリダイズするとドナー色素により励起されたアクセプター色素が蛍光を発する。
また、前記TaqManプローブ法は、レポーター色素とクエンチャー色素の2つが近接するようにラベルされているプローブを用いる方法である。そして、当該プローブが核酸伸長の際に加水分解され、このときクエンチャー色素とレポーター色素とが離れ、レポーター色素が励起されると蛍光を発する。
【0027】
前記蛍光物質を用いる方法に使用する蛍光色素(誘導体)としては、SYBR(登録商標) Green I、SYBR(登録商標) Green II、SYBR(登録商標)Gold、YO (Oxazole Yellow)、TO (Thiazole Orange)、PG (Pico(登録商標)Green)、臭化エチジウム等が挙げられる。
前記化学発光物質を用いる方法に使用する有機化合物としては、ルミノール、ロフィン、ルシゲニン、シュウ酸エステル等が挙げられる。
【0028】
(2)温度制御手段
前記温度制御手段3は、前記反応領域2を加熱するためのものである。前記温度制御手段3としては、特に限定されないが、例えば、ペルチェ等のヒータや光透過性のあるITOヒータ等が挙げられる。
また、前記温度制御手段3の形状としては、例えば薄膜状や平板状等が挙げられる。
また、前記温度制御手段3は、前記反応領域2に熱が伝わりやすい位置に配設されるのが好適である。例えば近接するように配設されるのが好適であり、具体的には、前記反応領域2の上部、下部、側部や外周部等の何れの位置に配設してもよい。また、他の部材、例えばピンホール7等を介してもよい。
このうち、前記温度制御手段3は、薄膜状や平板状の形状で、前記反応領域2の上部及び/又は下部に配設するのが、好適である。このとき、基板支持台8として前記温度制御手段3を配置してもよく、また光軸上に孔9を設けて光を通過させてもよい。これにより、前記反応領域2の光線通過距離を長くしなくともよいことから、熱源からの距離を拡大する必要がなく、結果反応領域2内部の温度制御が容易であるので、濁度検出による検出感度や検出精度が向上する。
【0029】
(3)照射手段
前記照射手段4は、光源10を備え、当該光源10から出射される光Lが前記反応領域2に照射される構成であればよい。具体的には、前記照射手段4は、光源10から出射された光Lを、核酸増幅反応の進行に伴って析出する物質Pによる光の散乱光量を検出するために、前記反応領域2の上面22に照射できるものであればよい。例えば、前記光源10を、前記反応領域2の上面22の上方に配置してもよいし、また、前記光源10から出射された光Lを前記反応領域2に導光する導光部材11を配置してもよい。
このうち、前記照射手段4に、前記光源10から発せられた光を反応領域2に照射する導光部材11を備えるのが好適である。当該導光部材11には、光入射端部が設けられており、当該光入射端部に、前記光源10の単数又は複数から出射された光が入射される。当該入射された光Lを各反応領域に導光させるように部材(例えばプリズム、反射板や凹凸等)が、前記導光部材11の内部には設けられている。
前記導光部材11を配設することにより、光源の数を減らすことができ、かつ基板6上の単数又は複数の反応領域2に均一な光の照射を行うことができ、濁度検出における検出感度や検出精度も良好である。しかも、光源数を減らすことによって、装置全体の小型化、特に薄型化も可能となり、また低消費電力化も可能となる。
【0030】
尚、前記光源10は、特に限定されないが、目的とする核酸増幅物を良好に検出することができる所望の光を出射するものが好適である。前記光源10としては、例えば、レーザー光源、白色又は単色の発光ダイオード(LED)、水銀灯、タングステンランプ等が挙げられる。このうち、LEDが、低消費電力化や低コスト化が可能となるので、好適である。また、当該LEDは、各種フィルタを用いれば所望の光成分を得ることも可能であるので有利である。
尚、前記レーザー光源としては、レーザー光の種類によっては特に限定されないが、アルゴンイオン(Ar)レーザー、ヘリウム−ネオン(He-Ne)レーザー、ダイ(dye)レーザー、クリプトン(Cr)レーザー等を出射する光源であればよい。当該レーザー光源は、1種又は2種以上、自由に組み合わせて用いることができる。
【0031】
尚、図1に示すように、前記照射手段4からの光Lは反応領域2に到達し、反応領域内での増幅反応の進行に伴って析出する物質(生成される濁度物質)Pによって反射される或いは吸収される。そして、当該濁度物質Pによる光の散乱光量又は透過光量(光L1,L2)を、適宜絞り(孔9)、集光レンズ及び蛍光フィルタ等を通過して、検出手段5(光学検出器)にて検出する。
ここでの散乱光としては、例えば、前方散乱光、後方散乱光や側方散乱光等が挙げられるが、本装置において前方散乱光が容易に検出しやすく、検出感度もよいので、有利である。
【0032】
(4)検出手段
前記検出手段5は、反応領域2の他端(具体的には底面21)から出射する光L1,L2の光量を検出することが可能な機構であればよい。当該検出手段5には、光学検出器が少なくとも備えられている。
前記光学検出器としては、特に限定されず、例えば、フォトダイオード(PD)アレイ、CCDイメージセンサやCMOSイメージセンサ等のエリア撮像素子、小型光センサ、ラインセンサースキャン、PMT(光電子倍増管)等が挙げられ、これらを適宜組み合わせてもよい。当該光学検出器で、核酸増幅反応によって生じる濁度物質P等を検出する。
【0033】
尚、本発明の核酸増幅反応装置1内に、励起フィルタや蛍光フィルタを適宜配設してもよい。例えば、照射手段4と反応領域2との間に励起フィルタを配設してもよく、また反応領域2と検出手段5との間に蛍光フィルタを配設してもよい。
前記励起フィルタ(図示せず)により、核酸増幅反応の検出方法に応じて所望の特定波長の光成分とする、また不要な光成分を除去できる。また、前記蛍光フィルタ(図示せず)により、検出に必要な光成分(散乱光、透過光や蛍光)にすることができる。これにより、検出感度や検出精度が向上する。
【0034】
<2.核酸増幅反応装置1の動作>
以下に、上述した核酸増幅反応装置1の動作及び濁度物質Pによる散乱光量を検出する核酸増幅反応方法について、説明する。
前記光源10から、光Lが出射される。当該光Lは、前記光入射端部から導光部材11に入射される。入射された光Lは、導光部材11内部のプリズム等の部材によって、反応領域2の入端面(上面22)に到達するように照射される。
照射された光Lは、核酸の増幅反応の反応場となるテーパウェル形状に形成された反応領域2の一端(上面22)に照射され、テーパ型のウェル内に入射される。このとき、核酸増幅反応において析出する物質Pが、傾斜面23によりウェル底面側でより高濃度となり、これにより光散乱の度合いが増す。そして、当該光Lは、反応領域2内で核酸増幅反応の進行に伴って生じる析出物質Pに照射される。この照射された光Lは、反応領域2内の析出物質Pの表面で反射されるか或いは吸収され、光L1(散乱光及び透過光)となる。また、析出物質Pが少ない時には光L2となる。これら光L1,L2は、反応領域2の他端(底面21)から出射される。このとき、出射された光L1,L2は、適宜、蛍光フィルタによって所望の光成分(例えば散乱光成分或いは透過光成分)にしてもよい。出射された光L1,L2は、検出手段5(光学検出器)にて、出射された前記光の光量を検出する。すなわち、増幅反応の進行に伴って生じる析出物質Pによる前記光の散乱光量を検出する。
【0035】
斯様に、濁度検出による核酸増幅反応において、テーパウェル形状に形成された反応領域に光を照射して、反応の進行に伴って析出する物質による前記光の散乱光量を検出する手順を含むが好適である。
そして、上述のように、反応領域として、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、領域断面積が小さくなるように形成されたテーパウェル形状を用いるのが好適である。
このように用いることにより、光線通過距離を長くしなくとも、前述のウェル底面側に、核酸増幅の結果生じるピロリン酸とこれと結合する金属イオンとにより生成される析出する物質の凝集度が高まることとなる。そして、この析出物質における散乱光量(或いは透過光量)が減少しやすくなるので、検出感度や検出精度が向上する。
【0036】
また、前記反応領域の内面の傾斜面が、滑面処理されたものが好適である。また、前記反応領域の内面が、円若しくは角の錐台面形状又は凹回転放物面形状であるのが好適である。また、前記反応領域の底面面積が、当該上面面積の1/2〜1/5であるのが好適である。また、前記核酸増幅反応の検出が、LAMP法又はPCR法による濁度検出であるのが好適である。これにより、析出物質がウェル底面側で高濃度になり易くなるので、検出感度及び検出精度が良好となる。
【0037】
(1)変形例
本発明の核酸増幅反応装置は、反応終了後の反応領域2を、前記温度制御手段3等に設置して、核酸増幅検出装置としても使用可能である。
また、LAMP装置やPCR装置として用い、濁度物質検出にて核酸を定量することも可能である。
(a)RT−LAMP装置の動作
以下に、RT−LAMP装置において、ステップSl1の手順での核酸の検出方法について説明する。
温度制御ステップ(ステップSl1)にて、反応領域2内が一定温度(60〜65℃)になるように設定することで、各反応領域2内の核酸が増幅されてゆく。尚、このLAMP法では、一本鎖から二本鎖への熱変性が必要なく、この等温条件下、プライマーのアニーリングと核酸伸長とが繰り返り行われる。
この核酸増幅反応の結果、ピロリン酸が生成され、このピロリン酸に金属イオンが結合して不溶性又は難溶性の塩が形成され、この塩が濁度物質となる(測定波長300〜800nm)。この濁度物質に入射光(光L)が照射されることで、散乱光(光L1,L2)となる。この散乱光の散乱光量をリアルタイムに検出手段5で測定し、定量化する。また、透過光量からも定量化することは可能である。
【0038】
(b)RT−PCR装置の動作
ここで、RT―PCR装置において、ステップSp1(熱変性)、ステップSp2(プライマーのアニーリング)、ステップSp3(DNA伸長)の手順での核酸の検出方法について説明する。
熱変性ステップ(ステップSp1)では、反応領域2内が95℃になるように前記温度制御手段にて制御し、二本鎖DNAを変性させ一本鎖DNAとする。
続くアニーリングステップ(ステップSp2)では、反応領域2内が55℃となるように設定することで、プライマーが当該一本鎖DNAと相補的な塩基配列と結合させる。
次のDNA伸長ステップ(ステップSp3)では、反応領域2内が72℃となるように制御することで、プライマーをDNA合成の開始点として、ポリメラーゼ反応を進行させてcDNAを伸長させる。
このようなステップSp1〜Sp3の温度サイクルを繰り返すことによって、各反応領域2内のDNAは増幅されてゆく。この核酸増幅反応の結果、ピロリン酸が生成され、上述のようにして濁度物質を検出し、核酸量を定量化する。
【産業上の利用可能性】
【0039】
本発明に係わる核酸増幅反応装置は、テーパウェル形状を採用して反応領域の水平断面積が小さくなるようにしてウェル底面側の局所的に析出物質の凝集度を高めるので、高い検出感度の測定が可能である。また、光線通過距離を長くしなくともよいことから、装置全体の小型化、特に薄型のハンディタイプ化も可能である。また、適宜蛍光検出も可能である。
【符号の説明】
【0040】
1 核酸増幅反応装置;2 反応領域;3 温度制御手段;4 照射手段;5 検出手段;6 基板;7 ピンホール;8 基板支持台;9 孔;10 光源;11 導光部材;L,L1,L2 光;P 析出物質;2A 角錐台形状;2B 凹型放物面形状;2C 円筒状ウェル;21 底面;22 上面;23 傾斜面
【技術分野】
【0001】
本発明は、核酸増幅反応装置、核酸増幅反応装置に用いる基板、及び核酸増幅反応方法に関する。より詳細には、核酸増幅反応の反応場となる反応領域をテーパウェル形状に形成し、これを備える核酸増幅反応装置等に関する。
【背景技術】
【0002】
近年、PCR法(Polymerase Chain Reaction;ポリメラーゼ連鎖反応)やLAMP法(Loop-Mediated Isothermal Amplification)等による遺伝子増幅反応を行って検証することが微量核酸の定量分析の標準的手法となっている。このような手法によって、遺伝子発現解析、遺伝的疾患、癌化、微生物やウイルス等の感染症の検査、またSNP解析等の遺伝子解析が進められている。
ここで、核酸の増幅産物を検出する方法において、インターカレーター法や蛍光標識プローブ法等のように蛍光物質を用いる蛍光検出方法、また増幅過程での副産物のピロリン酸にマグネシウムイオン等の金属イオンで水に不溶又は難溶性の塩を形成した濁度物質を用いる濁度検出法等が主として用いられている(特許文献1〜3)。
上述のような核酸の増幅産物を検出する方法を用いて、遺伝子発現解析、感染症検査、またSNP解析等の遺伝子解析が行える核酸増幅反応装置が広く市販されている。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特開2008−237207号公報
【特許文献2】国際公開第01/83817号パンフレット
【特許文献3】特許413347号公報
【発明の概要】
【発明が解決しようとする課題】
【0004】
そして、これら核酸増幅反応装置において、円筒状ウェルプレートを一般的に用いているが、更なる検出感度の向上が求められている。
【0005】
そこで、本発明は、より高い検出感度が得られる核酸増幅反応装置、核酸増幅反応装置に用いる基板、及び核酸増幅反応方法を提供することを主目的とする。
【課題を解決するための手段】
【0006】
上記課題解決のために、本発明は、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、反応領域の水平断面積が小さくなるようにテーパウェル形状に形成された、核酸増幅反応の反応場となる反応領域と、前記反応領域を加熱する温度制御手段と、前記反応領域に光を照射する照射手段と、前記反応領域からの前記析出する物質による光の散乱光量を検出する検出手段と、を備える、核酸増幅反応装置を提供する。
また、前記反応領域の内面の傾斜面が、滑面処理されたものが好適である。
【0007】
また、本発明は、核酸増幅反応の反応場となる反応領域が形成され、該反応領域は、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、領域断面積が小さくなるように形成されたテーパウェルである核酸増幅反応用マイクロチップを提供する。
【0008】
また、本発明は、核酸増幅反応の反応場となる反応領域に光を照射して、増幅反応の進行に伴って析出する物質による前記光の散乱光量を検出する手順を含み、前記反応領域として、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、領域断面積が小さくなるように形成されたテーパウェルを用いる核酸増幅反応方法を提供する。
【発明の効果】
【0009】
本発明によれば、より高い検出感度が得られる核酸増幅反応装置、基板及び核酸増幅反応方法が提供される。
【図面の簡単な説明】
【0010】
【図1】本発明に係わる核酸増幅反応装置における概念図を示す。
【図2】本発明に係わる核酸増幅反応用マイクロチップにおける反応領域の光軸方向に沿った垂直断面図を示す。
【発明を実施するための形態】
【0011】
以下、本発明を実施するための好適な形態について図面を参照しながら説明する。なお、以下に説明する実施形態は、本発明の代表的な実施形態の一例を示したものであり、これにより本発明の範囲が狭く解釈されることはない。
【0012】
1.核酸増幅反応装置
(1)反応領域
(a)基板(核酸増幅反応用マイクロチップ)
(b)核酸増幅反応
(c)核酸増幅(産物)の検出方法
(2)温度制御手段
(3)照射手段
(4)検出手段
2.核酸増幅反応装置の動作
(1)変形例
(a)RT−LAMP装置の動作
(b)RT−PCR装置の動作
【0013】
<1.核酸増幅反応装置>
図1は、本発明に係わる核酸増幅反応装置における概念図である。また、図2は、本発明に係わる核酸増幅反応用マイクロチップにおける反応領域の光軸方向に沿った垂直断面図である。
なお、以下に説明する図面では、説明の便宜上、装置の構成等を簡略化して示している。
【0014】
本発明に係わる核酸増幅反応装置1は、核酸増幅反応を制御して、核酸を増幅させ、定量するための、反応領域2、温度制御手段3、照射手段4及び検出手段5から構成されている。
本発明の核酸増幅反応装置1は、照射手段4と検出手段5との間に温度制御手段3及び脱着可能な反応領域2(基板6)が配置されている。
更に、反応領域2と照射手段4の間には、光量や光成分等を調整するために、適宜、ピンホール7、フィルタ(図示せず)、集光レンズ(図示せず)を配設してもよい。また、反応領域2と検出手段5の間には、光量や光成分等を調整するためや反応領域2を支持するために、適宜、基板支持台8、フィルタ(図示せず)、集光レンズ(図示せず)を配設してもよい。
尚、本発明の核酸増幅反応装置1には、本発明の装置に関しての各種動作(例えば、光制御、温度制御、核酸増幅反応、検出制御、検出光量算出やモニタリング等)を制御する制御部(図示せず)が備えられている。
以下に各構成について詳細に説明する。
【0015】
(1)反応領域
前記反応領域2は、核酸の増幅反応の反応場となるエリアであり、テーパウェル形状に形成されている。
前記テーパウェルは、光軸方向で核酸増幅反応の進行に伴って析出する物質Pが沈降する方向に従って、反応領域の水平断面積が小さくなるように形成されているものである。
【0016】
ところで、一般的なウェル、例えば円筒状ウェルでは、反応初期時の低散乱状態において検出感度や検出精度を向上させるためには、反応場中の光線透過距離を長くする、すなわち、光軸方向に従ってウェルを伸長させる必要がある。しかし、ウェルを伸長させることにより核酸増幅反応の温度制御をする熱源からの距離が拡大するためウェル内部で温度差が拡大するので、核酸増幅の反応効率が低下したり、反応にむらができ検出が不安定になり易い。
ところが、本発明の如く反応領域をテーパウェル形状とすることにより、反応場中の析出・沈降する物質が、ウェル底面側でより高濃度となり、散乱の度合いが増す。すなわち、テーパウェル形状として光線透過領域の散乱断面積を制御することで、反応領域の水平断面積において局所的に析出物質の凝集度が高まることとなる。よって、光線通過距離を長くしなくとも、反応領域中の微量な核酸でも検出することが可能となり、また初期反応時(低散乱)での検出感度が向上し、また、モニタリングも良好となる。
このように反応領域をテーパウェル形状にすることにより、核酸増幅反応による濁度検出における検出感度や検出精度が良好となる。また、本発明のテーパウェル形状を有する核酸増幅反応用マイクロチップを用いることによって、高効率な濁度検出を実現することも可能となる。更に散乱距離を拡大しなくとも、装置の性能や信頼性を確保できるので、核酸増幅反応装置全体の小型化、特に薄型化も行い易い。
【0017】
図2は、反応領域2の底面21の中心を通る垂直平面で切断した反応領域2の断面形状の例示である。また、破線の2Cは円筒状ウェルの垂直断面形状を示す。
前記反応領域2は、底面21及び上面22を有し、この何れの面にも同一光軸方向で光を通過させることが可能な平面を有するのが好適である。また、これら両面は互いに平行する対向面であるのが好適である。
更に、底面21及び上面22を設ける反応領域2は、前記析出物質Pが沈降しやすいように傾斜面23を有する。そして、光軸方向で垂直断面した際の前記反応領域2の傾斜面23,23は、底面21方向に従って反応領域2の幅が小さくなるような形状とするのが好適である。当該形状としては、例えば、角錐台形状2Aや凹型放物面形状2B等が挙げられる。
また、前記反応領域2の内面(傾斜面23)の立体形状は、例えば、円錐台や多角錐台の錐台形状や光軸を中心とした回転放物面形状等が挙げられる。このうち、形成が容易なので、円錐台形状が好適である。円筒状ウェル2Cの容量と同じ容量でかつ同じ光線透過距離である場合でも、テーパ型の傾斜面23として光線透過領域の散乱断面積を制御することによって、検出感度及び検出精度の向上が可能となる。具体的には、前記反応領域2の底面21の面積が、この上面22の面積を1としたとき、1/2〜1/5、より1/3〜1/4とするのが好適である。この範囲内の面積比に底面21の面積をすることによって、前記析出物質Pが傾斜面23に吸着せずに沈降し易い傾斜を形成することが可能となる。よって、底面側で局所的に析出物質の凝集度を効率よく上げることも可能となるので、核酸増幅反応の濁度検出における検出感度や検出精度が良好となる。
【0018】
更に、前記反応領域2は、傾斜面23の内面に滑面処理されたものが好適である。これにより、前記析出物質(粒子)Pの当該傾斜面への表面付着が更に軽減され、かつこの傾斜により、より前記析出物質Pがウェル底面側で高濃度になり易い。よって、更に濁度検出における検出感度や検出精度が良好となる。
前記滑面処理としては、研磨処理、コーティング処理等が挙げられる。研磨処理としては、研磨剤を用いて行う化学機械研磨処理等が挙げられる。当該研磨剤としては、無機充填剤(粒子)を含む、プラスチック基板やガラス基板等を研磨するためのスラリー状のものが挙げられる。当該無機充填剤としては、例えば炭酸カルシウム、水酸化アルミニウム、水酸化カルシウム、水酸化マグネシウム、酸化チタン、無水珪酸、珪石等から選ばれる1種又は2種以上のものが挙げられる。
またコーティング処理に用いるコーティング剤としては、シリコン等が挙げられ、好ましくは透過性の高いシリコンが有利である。透過性の高いシリコンを用いることにより反応領域2内面の全面に塗布することも可能となるので核酸増幅反応用マイクロチップ等の反応領域2を有する基板の作製効率が良好となる。
【0019】
(a)基板(核酸増幅反応用マイクロチップ)
前記反応領域2は、例えば、核酸増幅反応用マイクロチップ等の反応容器(例えば、基板)内に単数又は複数形成されているのが好適である。このような反応容器であれば、上述のようなテーパウェル形状を形成し易い。
前記反応領域2を備える核酸増幅反応用マイクロチップ(基板6)は、単数又は複数の基板から形成することができる。
前記基板6の両端面のうち、一端の面は光が照射される面(上面22方向)であり、他端の面は反応領域(反応場中の光線通路)を通過した光が出射される面(底面21方向)であり、これらは互いに平行する対向面であるのが好適である。
これにより、光を反応領域2の上面22に照射して、反応領域2を通過させ、底面21から出射して光の散乱光量や透過光量を検出手段5にて測定する。尚、前記核酸増幅反応用マイクロチップの反応領域2の底面側に、反応領域2の側方から光を照射して光の散乱光量や透過光量を測定することも可能である。
【0020】
前記反応領域2の基板6への形成方法は、特に限定されないが、例えば、ガラス製基板層のウェットエッチングやドライエッチングによって、又はプラスチック製基板層のナノインプリントや射出形成、切削加工によって行うことが好適である。
例えば、前記反応領域2の形成方法としては、角錐台形状2Aや凹型放物面形状2B等のような反応領域2を研磨切削加工や鋳型成形等にて1つの基板上に単数又は複数形成し、この基板の上面に他の基板を配置すること等が挙げられる。
また、前記基板6の材料は、特に限定されず、検出方法や加工容易性、耐久性等を考慮して適宜選択するのが好適である。当該材料としては、光透過性のある素材で所望の検出方法に応じて適宜選択すればよく、例えば、ガラスや各種プラスチック(ポリプロピレン、ポリカーボネイト、シクロオレフィンポリマー、ポリジメチルシロキサン等)が挙げられる。
このようにして形成された反応領域2には、核酸増幅反応に必要な試薬類を予め充填していてもよい。
【0021】
(b)核酸増幅反応
本発明において、「核酸増幅反応」には、温度サイクルを実施する従来のPCR(polymerase chain reaction)法や、温度サイクルを伴わない各種等温増幅法が含まれる。等温増幅法としては、例えば、LAMP(Loop-Mediated Isothermal Amplification)法やSMAP(SMartAmplification Process)法、NASBA(Nucleic Acid Sequence-Based Amplification)法、ICAN(Isothermal and Chimeric primer-initiated Amplification of Nucleic acids)法(登録商標)、TRC(transcription-reverse transcription concerted)法、SDA(strand displacement amplification)法、TMA(transcription-mediated amplification)法、RCA(rolling circle amplification)法等が挙げられる。
この他、「核酸増幅反応」には、核酸の増幅を目的とする変温あるいは等温による核酸増幅反応が広く包含されるものとする。また、これらの核酸増幅反応には、リアルタイムPCR(RT−PCR)法やRT−LAMP法などの増幅核酸鎖の定量を伴う反応も包含される。
【0022】
また、「試薬」には、上記の核酸増幅反応において、増幅核酸鎖を得るために必要な試
薬であって、具体的には、標的核酸鎖に相補的な塩基配列とされたオリゴヌクレオチドプ
ライマー、核酸モノマー(dNTP)、酵素、反応緩衝液(バッファー)溶質などが含ま
れる。
【0023】
前記PCR法は、「熱変性(約95℃)→プライマーのアニーリング(約55〜60℃)→伸長反応(約72℃)」という増幅サイクルを連続的に行う。
また、前記LAMP法とは、DNAのループ形成を利用して、一定温度でDNAやRNAからdsDNAを増幅産物として得る方法である。一例として、成分(i)、(ii)(iii)を加え、インナープライマーが鋳型核酸上の相補的配列に対して安定的な塩基対結合を形成することができ、かつ鎖置換型ポリメラーゼが酵素活性を維持しうる温度でインキュベートすることにより進行する。このときのインキュベート温度は50〜70℃、時間は1分〜10時間程度が好適である。
成分(i)インナープラマー2種、又は更にアウタープライマー2種、又は更にループプライマー2種;成分(ii)鎖置換型ポリメラーゼ;成分(iii)基質ヌクレオチド。
【0024】
(c)核酸増幅(産物)の検出方法
前記核酸増幅の検出方法としては、例えば、濁度物質、蛍光物質や化学発光物質等を用いる方法が挙げられる。
【0025】
また、前記濁度物質を用いる方法としては、例えば核酸増幅反応の結果生じるピロリン酸とこれに結合可能な金属イオンにより生じた析出物質を用いる方法等が挙げられる。当該金属イオンは、一価又は二価の金属イオンであり、ピロリン酸と結合すると水に不溶又は難溶性の塩を形成して濁度物質となる。
当該金属イオンとしては、具体的には、アルカリ金属イオン、アルカリ土類金属イオン及び二価遷移金属イオン等が挙げられる。このうち、例えば、マグネシウム(II)、カルシウム(II)及びバリウム(II)等のアルカリ土類金属イオン;亜鉛(II)、鉛(II)、マンガン(II)、ニッケル(II)及び鉄(II)等の二価遷移金属イオン等から選ばれる1種又は2以上が好ましい。更に好ましくは、マグネシウム(II)、マンガン(II)、ニッケル(II)及び鉄(II)である。
当該金属イオンを添加するときの濃度は、0.01〜100mMの範囲であれば好適である。検出波長は、300〜800nmとするのが好適である。
【0026】
また、前記蛍光物質や化学発光物質を用いる方法としては、例えば、二本鎖核酸に特異的に挿入されて蛍光を発する蛍光色素(誘導体)を用いるインターカレート方法、増幅する核酸配列に特異的なオリゴヌクレオチドに蛍光色素を結合させたプローブを用いる標識プローブ方法等が挙げられる。
前記標識プローブ法としては、例えばハイブリダイゼーション(Hyb)プローブ法、加水分解(TaqMan)プローブ法等が挙げられる。
前記Hybプローブ法は、予め2種のプローブが近接するようにデザインされたドナー色素でラベルされたプローブとアクセプター色素でラベルされたプローブという2種のプローブを用いる方法である。そして、当該2種のプローブが標的核酸にハイブリダイズするとドナー色素により励起されたアクセプター色素が蛍光を発する。
また、前記TaqManプローブ法は、レポーター色素とクエンチャー色素の2つが近接するようにラベルされているプローブを用いる方法である。そして、当該プローブが核酸伸長の際に加水分解され、このときクエンチャー色素とレポーター色素とが離れ、レポーター色素が励起されると蛍光を発する。
【0027】
前記蛍光物質を用いる方法に使用する蛍光色素(誘導体)としては、SYBR(登録商標) Green I、SYBR(登録商標) Green II、SYBR(登録商標)Gold、YO (Oxazole Yellow)、TO (Thiazole Orange)、PG (Pico(登録商標)Green)、臭化エチジウム等が挙げられる。
前記化学発光物質を用いる方法に使用する有機化合物としては、ルミノール、ロフィン、ルシゲニン、シュウ酸エステル等が挙げられる。
【0028】
(2)温度制御手段
前記温度制御手段3は、前記反応領域2を加熱するためのものである。前記温度制御手段3としては、特に限定されないが、例えば、ペルチェ等のヒータや光透過性のあるITOヒータ等が挙げられる。
また、前記温度制御手段3の形状としては、例えば薄膜状や平板状等が挙げられる。
また、前記温度制御手段3は、前記反応領域2に熱が伝わりやすい位置に配設されるのが好適である。例えば近接するように配設されるのが好適であり、具体的には、前記反応領域2の上部、下部、側部や外周部等の何れの位置に配設してもよい。また、他の部材、例えばピンホール7等を介してもよい。
このうち、前記温度制御手段3は、薄膜状や平板状の形状で、前記反応領域2の上部及び/又は下部に配設するのが、好適である。このとき、基板支持台8として前記温度制御手段3を配置してもよく、また光軸上に孔9を設けて光を通過させてもよい。これにより、前記反応領域2の光線通過距離を長くしなくともよいことから、熱源からの距離を拡大する必要がなく、結果反応領域2内部の温度制御が容易であるので、濁度検出による検出感度や検出精度が向上する。
【0029】
(3)照射手段
前記照射手段4は、光源10を備え、当該光源10から出射される光Lが前記反応領域2に照射される構成であればよい。具体的には、前記照射手段4は、光源10から出射された光Lを、核酸増幅反応の進行に伴って析出する物質Pによる光の散乱光量を検出するために、前記反応領域2の上面22に照射できるものであればよい。例えば、前記光源10を、前記反応領域2の上面22の上方に配置してもよいし、また、前記光源10から出射された光Lを前記反応領域2に導光する導光部材11を配置してもよい。
このうち、前記照射手段4に、前記光源10から発せられた光を反応領域2に照射する導光部材11を備えるのが好適である。当該導光部材11には、光入射端部が設けられており、当該光入射端部に、前記光源10の単数又は複数から出射された光が入射される。当該入射された光Lを各反応領域に導光させるように部材(例えばプリズム、反射板や凹凸等)が、前記導光部材11の内部には設けられている。
前記導光部材11を配設することにより、光源の数を減らすことができ、かつ基板6上の単数又は複数の反応領域2に均一な光の照射を行うことができ、濁度検出における検出感度や検出精度も良好である。しかも、光源数を減らすことによって、装置全体の小型化、特に薄型化も可能となり、また低消費電力化も可能となる。
【0030】
尚、前記光源10は、特に限定されないが、目的とする核酸増幅物を良好に検出することができる所望の光を出射するものが好適である。前記光源10としては、例えば、レーザー光源、白色又は単色の発光ダイオード(LED)、水銀灯、タングステンランプ等が挙げられる。このうち、LEDが、低消費電力化や低コスト化が可能となるので、好適である。また、当該LEDは、各種フィルタを用いれば所望の光成分を得ることも可能であるので有利である。
尚、前記レーザー光源としては、レーザー光の種類によっては特に限定されないが、アルゴンイオン(Ar)レーザー、ヘリウム−ネオン(He-Ne)レーザー、ダイ(dye)レーザー、クリプトン(Cr)レーザー等を出射する光源であればよい。当該レーザー光源は、1種又は2種以上、自由に組み合わせて用いることができる。
【0031】
尚、図1に示すように、前記照射手段4からの光Lは反応領域2に到達し、反応領域内での増幅反応の進行に伴って析出する物質(生成される濁度物質)Pによって反射される或いは吸収される。そして、当該濁度物質Pによる光の散乱光量又は透過光量(光L1,L2)を、適宜絞り(孔9)、集光レンズ及び蛍光フィルタ等を通過して、検出手段5(光学検出器)にて検出する。
ここでの散乱光としては、例えば、前方散乱光、後方散乱光や側方散乱光等が挙げられるが、本装置において前方散乱光が容易に検出しやすく、検出感度もよいので、有利である。
【0032】
(4)検出手段
前記検出手段5は、反応領域2の他端(具体的には底面21)から出射する光L1,L2の光量を検出することが可能な機構であればよい。当該検出手段5には、光学検出器が少なくとも備えられている。
前記光学検出器としては、特に限定されず、例えば、フォトダイオード(PD)アレイ、CCDイメージセンサやCMOSイメージセンサ等のエリア撮像素子、小型光センサ、ラインセンサースキャン、PMT(光電子倍増管)等が挙げられ、これらを適宜組み合わせてもよい。当該光学検出器で、核酸増幅反応によって生じる濁度物質P等を検出する。
【0033】
尚、本発明の核酸増幅反応装置1内に、励起フィルタや蛍光フィルタを適宜配設してもよい。例えば、照射手段4と反応領域2との間に励起フィルタを配設してもよく、また反応領域2と検出手段5との間に蛍光フィルタを配設してもよい。
前記励起フィルタ(図示せず)により、核酸増幅反応の検出方法に応じて所望の特定波長の光成分とする、また不要な光成分を除去できる。また、前記蛍光フィルタ(図示せず)により、検出に必要な光成分(散乱光、透過光や蛍光)にすることができる。これにより、検出感度や検出精度が向上する。
【0034】
<2.核酸増幅反応装置1の動作>
以下に、上述した核酸増幅反応装置1の動作及び濁度物質Pによる散乱光量を検出する核酸増幅反応方法について、説明する。
前記光源10から、光Lが出射される。当該光Lは、前記光入射端部から導光部材11に入射される。入射された光Lは、導光部材11内部のプリズム等の部材によって、反応領域2の入端面(上面22)に到達するように照射される。
照射された光Lは、核酸の増幅反応の反応場となるテーパウェル形状に形成された反応領域2の一端(上面22)に照射され、テーパ型のウェル内に入射される。このとき、核酸増幅反応において析出する物質Pが、傾斜面23によりウェル底面側でより高濃度となり、これにより光散乱の度合いが増す。そして、当該光Lは、反応領域2内で核酸増幅反応の進行に伴って生じる析出物質Pに照射される。この照射された光Lは、反応領域2内の析出物質Pの表面で反射されるか或いは吸収され、光L1(散乱光及び透過光)となる。また、析出物質Pが少ない時には光L2となる。これら光L1,L2は、反応領域2の他端(底面21)から出射される。このとき、出射された光L1,L2は、適宜、蛍光フィルタによって所望の光成分(例えば散乱光成分或いは透過光成分)にしてもよい。出射された光L1,L2は、検出手段5(光学検出器)にて、出射された前記光の光量を検出する。すなわち、増幅反応の進行に伴って生じる析出物質Pによる前記光の散乱光量を検出する。
【0035】
斯様に、濁度検出による核酸増幅反応において、テーパウェル形状に形成された反応領域に光を照射して、反応の進行に伴って析出する物質による前記光の散乱光量を検出する手順を含むが好適である。
そして、上述のように、反応領域として、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、領域断面積が小さくなるように形成されたテーパウェル形状を用いるのが好適である。
このように用いることにより、光線通過距離を長くしなくとも、前述のウェル底面側に、核酸増幅の結果生じるピロリン酸とこれと結合する金属イオンとにより生成される析出する物質の凝集度が高まることとなる。そして、この析出物質における散乱光量(或いは透過光量)が減少しやすくなるので、検出感度や検出精度が向上する。
【0036】
また、前記反応領域の内面の傾斜面が、滑面処理されたものが好適である。また、前記反応領域の内面が、円若しくは角の錐台面形状又は凹回転放物面形状であるのが好適である。また、前記反応領域の底面面積が、当該上面面積の1/2〜1/5であるのが好適である。また、前記核酸増幅反応の検出が、LAMP法又はPCR法による濁度検出であるのが好適である。これにより、析出物質がウェル底面側で高濃度になり易くなるので、検出感度及び検出精度が良好となる。
【0037】
(1)変形例
本発明の核酸増幅反応装置は、反応終了後の反応領域2を、前記温度制御手段3等に設置して、核酸増幅検出装置としても使用可能である。
また、LAMP装置やPCR装置として用い、濁度物質検出にて核酸を定量することも可能である。
(a)RT−LAMP装置の動作
以下に、RT−LAMP装置において、ステップSl1の手順での核酸の検出方法について説明する。
温度制御ステップ(ステップSl1)にて、反応領域2内が一定温度(60〜65℃)になるように設定することで、各反応領域2内の核酸が増幅されてゆく。尚、このLAMP法では、一本鎖から二本鎖への熱変性が必要なく、この等温条件下、プライマーのアニーリングと核酸伸長とが繰り返り行われる。
この核酸増幅反応の結果、ピロリン酸が生成され、このピロリン酸に金属イオンが結合して不溶性又は難溶性の塩が形成され、この塩が濁度物質となる(測定波長300〜800nm)。この濁度物質に入射光(光L)が照射されることで、散乱光(光L1,L2)となる。この散乱光の散乱光量をリアルタイムに検出手段5で測定し、定量化する。また、透過光量からも定量化することは可能である。
【0038】
(b)RT−PCR装置の動作
ここで、RT―PCR装置において、ステップSp1(熱変性)、ステップSp2(プライマーのアニーリング)、ステップSp3(DNA伸長)の手順での核酸の検出方法について説明する。
熱変性ステップ(ステップSp1)では、反応領域2内が95℃になるように前記温度制御手段にて制御し、二本鎖DNAを変性させ一本鎖DNAとする。
続くアニーリングステップ(ステップSp2)では、反応領域2内が55℃となるように設定することで、プライマーが当該一本鎖DNAと相補的な塩基配列と結合させる。
次のDNA伸長ステップ(ステップSp3)では、反応領域2内が72℃となるように制御することで、プライマーをDNA合成の開始点として、ポリメラーゼ反応を進行させてcDNAを伸長させる。
このようなステップSp1〜Sp3の温度サイクルを繰り返すことによって、各反応領域2内のDNAは増幅されてゆく。この核酸増幅反応の結果、ピロリン酸が生成され、上述のようにして濁度物質を検出し、核酸量を定量化する。
【産業上の利用可能性】
【0039】
本発明に係わる核酸増幅反応装置は、テーパウェル形状を採用して反応領域の水平断面積が小さくなるようにしてウェル底面側の局所的に析出物質の凝集度を高めるので、高い検出感度の測定が可能である。また、光線通過距離を長くしなくともよいことから、装置全体の小型化、特に薄型のハンディタイプ化も可能である。また、適宜蛍光検出も可能である。
【符号の説明】
【0040】
1 核酸増幅反応装置;2 反応領域;3 温度制御手段;4 照射手段;5 検出手段;6 基板;7 ピンホール;8 基板支持台;9 孔;10 光源;11 導光部材;L,L1,L2 光;P 析出物質;2A 角錐台形状;2B 凹型放物面形状;2C 円筒状ウェル;21 底面;22 上面;23 傾斜面
【特許請求の範囲】
【請求項1】
光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、反応領域の水平断面積が小さくなるようにテーパウェル形状に形成された、核酸増幅反応の反応場となる反応領域と、
前記反応領域を加熱する温度制御手段と、
前記反応領域に光を照射する照射手段と、
前記反応領域からの前記析出する物質による光の散乱光量を検出する検出手段と、
を備える、核酸増幅反応装置。
【請求項2】
前記反応領域の内面の傾斜面が、滑面処理されたものである請求項1記載の核酸増幅反応装置。
【請求項3】
前記反応領域の内面が、円若しくは角の錐台面形状又は凹回転放物面形状である請求項1又は2記載の核酸増幅反応装置。
【請求項4】
前記反応領域の底面面積が、当該上面面積の1/2〜1/5である請求項3記載の核酸増幅反応装置。
【請求項5】
前記核酸増幅反応の検出が、LAMP法又はPCR法による濁度検出である請求項4記載の核酸増幅反応装置。
【請求項6】
核酸増幅反応の反応場となる反応領域が形成され、
該反応領域は、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、領域断面積が小さくなるように形成されたテーパウェルである核酸増幅反応用マイクロチップ。
【請求項7】
前記反応領域の内面の傾斜面が、滑面処理されたものである請求項6記載の核酸増幅反応用マイクロチップ。
【請求項8】
核酸増幅反応の反応場となる反応領域に光を照射して、増幅反応の進行に伴って析出する物質による前記光の散乱光量を検出する手順を含み、
前記反応領域として、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、領域断面積が小さくなるように形成されたテーパウェルを用いる核酸増幅反応方法。
【請求項1】
光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、反応領域の水平断面積が小さくなるようにテーパウェル形状に形成された、核酸増幅反応の反応場となる反応領域と、
前記反応領域を加熱する温度制御手段と、
前記反応領域に光を照射する照射手段と、
前記反応領域からの前記析出する物質による光の散乱光量を検出する検出手段と、
を備える、核酸増幅反応装置。
【請求項2】
前記反応領域の内面の傾斜面が、滑面処理されたものである請求項1記載の核酸増幅反応装置。
【請求項3】
前記反応領域の内面が、円若しくは角の錐台面形状又は凹回転放物面形状である請求項1又は2記載の核酸増幅反応装置。
【請求項4】
前記反応領域の底面面積が、当該上面面積の1/2〜1/5である請求項3記載の核酸増幅反応装置。
【請求項5】
前記核酸増幅反応の検出が、LAMP法又はPCR法による濁度検出である請求項4記載の核酸増幅反応装置。
【請求項6】
核酸増幅反応の反応場となる反応領域が形成され、
該反応領域は、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、領域断面積が小さくなるように形成されたテーパウェルである核酸増幅反応用マイクロチップ。
【請求項7】
前記反応領域の内面の傾斜面が、滑面処理されたものである請求項6記載の核酸増幅反応用マイクロチップ。
【請求項8】
核酸増幅反応の反応場となる反応領域に光を照射して、増幅反応の進行に伴って析出する物質による前記光の散乱光量を検出する手順を含み、
前記反応領域として、光軸方向で核酸増幅反応の進行に伴って析出する物質が沈降する方向に従って、領域断面積が小さくなるように形成されたテーパウェルを用いる核酸増幅反応方法。
【図1】


【図2】




【図2】


【公開番号】特開2012−60912(P2012−60912A)
【公開日】平成24年3月29日(2012.3.29)
【国際特許分類】
【出願番号】特願2010−206752(P2010−206752)
【出願日】平成22年9月15日(2010.9.15)
【出願人】(000002185)ソニー株式会社 (34,172)
【Fターム(参考)】
【公開日】平成24年3月29日(2012.3.29)
【国際特許分類】
【出願日】平成22年9月15日(2010.9.15)
【出願人】(000002185)ソニー株式会社 (34,172)
【Fターム(参考)】
[ Back to top ]

