マイクロ波凝固療法用同軸アンテナ
【課題】 臓器内患部等への刺入を容易としながらも横方向の広範囲に亘って患部組織を加熱することができる。
【解決手段】 外部電極2と、この外部電極2の内側に絶縁体3を介して設けられ、外部電極2の先端部より導出した部分にマイクロ波照射部5を形成した中心電極4とを備える。マイクロ波照射部5は、中心電極4の先端部に、内側電極4bと外側電極4cとが一体で先端面4dが平坦なRL部4aが設けられている。RL部4aの平坦な先端面4dには、誘電体によって全体が先鋭をなす刺入頭部6が形成され、刺入頭部6の先端部には、導電体7が形成されている。
【解決手段】 外部電極2と、この外部電極2の内側に絶縁体3を介して設けられ、外部電極2の先端部より導出した部分にマイクロ波照射部5を形成した中心電極4とを備える。マイクロ波照射部5は、中心電極4の先端部に、内側電極4bと外側電極4cとが一体で先端面4dが平坦なRL部4aが設けられている。RL部4aの平坦な先端面4dには、誘電体によって全体が先鋭をなす刺入頭部6が形成され、刺入頭部6の先端部には、導電体7が形成されている。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、マイクロ波による生体組織の凝固を行うマイクロ波凝固療法用同軸アンテナに関する。
【背景技術】
【0002】
マイクロ波凝固療法用同軸アンテナは、外部電極の内側に絶縁体を介して設けられた中心電極を外部電極の先端より導出させてなり、この中心電極の先端部にマイクロ波照射部が設けられている。このマイクロ波照射部は、中心電極より供給される交流電流によって、生体組織内にマイクロ波を照射し、生体組織内に発生した誘電熱によって病変組織を熱凝固させる。
【0003】
この種のマイクロ波凝固療法用同軸アンテナには、例えば特許文献1のものがある。この特許文献1のマイクロ波凝固療法用同軸アンテナは、先端部に中心電極と一体の先鋭の刺入頭部が設けられている(特許文献1の図1参照)。これによれば、刺入頭部によって、臓器内患部等にも容易に刺入することができる。また、このマイクロ波手術器は、中心電極と一体の導電体で刺入頭部が形成されていることから、斜めの外周面から電気力線が出現することから、マイクロ波の照射範囲が中心軸線(縦)方向に長くなり、中心軸線(縦)方向の広範囲に亘ってマイクロ波を照射することになる。
【0004】
ところで、癌等の臓器内患部は、一般に球に近い楕円体をしていることが多い。したがって、このマイクロ波手術器のように、マイクロ波が中心軸線(縦)方向の広範囲に亘って発生すると、臓器への刺入時に臓器内患部だけでなくその周囲の正常組織まで破壊してしまうおそれがある。一方で、マイクロ波の照射範囲は、楕円体状の患部を広範囲に凝固することができるようにするため、中心軸線(縦)に対して略直角な横方向には広がりがあった方が良い。
【0005】
また、特許文献1には、先鋭の刺入頭部をセラミック等の絶縁体で形成し、刺入頭部の加熱温度を低くし、凝固組織の付着を低減することが記載されている(特許文献1の図2参照)。しかしながら、セラミックは、使用時に、破損してしまうおそれもある。
【0006】
【特許文献1】特開2004−187703号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明の目的は、臓器内患部等への刺入を容易としながらも中心軸線(縦)に対して略直角な横方向の広範囲に亘って患部組織を加熱凝固することができるマイクロ波凝固療法用同軸アンテナを提供することにある。
【0008】
また、本発明の目的は、先端に形成された刺入頭部を強固にしたマイクロ波凝固療法用同軸アンテナを提供することにある。
【課題を解決するための手段】
【0009】
本発明に係るマイクロ波凝固療法用同軸アンテナは、上述の課題を解決するために、外部電極と、この外部電極の内側に絶縁体を介して設けられ、上記外部電極の先端部より導出した部分にマイクロ波照射部を形成した中心電極とを備える。上記マイクロ波照射部は、中心電極の先端部に、内側電極と外側電極とが一体で先端面が平坦なRL(Reactive Load)部が設けられている。このRL部からは、平坦な先端面に対して垂直に電気力線が発生することから、中心軸線(縦)に対して略直角な横方向の広範囲に亘って臓器内患部を加熱凝固することができる。上記RL部の平坦な先端面には、誘電体によって全体が先鋭をなす刺入頭部が形成されており、臓器内患部に容易に刺入することができる。そして、上記刺入頭部の先端部は、導電体によって補強されている。
【発明の効果】
【0010】
本発明では、中心電極の先端部に内側電極と外側電極とが一体で先端面が平坦なRL部が形成されていることから、先端面に対して垂直な電気力線を発生させることができ、これにより、中心軸線(縦)に対して略直角な横方向に膨らみを持ったSAR(Specific Absorption Rate)分布を実現することができる。そして、誘電体によって略先鋭の刺入頭部が設けられていることから、この特性を維持しながら、臓器内患部等に容易に刺入することができる。この刺入頭部は、先端部に導電体が設けられていることから、強度補強がされており、使用時等に破壊することを防止することができる。
【発明を実施するための最良の形態】
【0011】
以下、本発明に係るマイクロ波凝固療法用同軸アンテナについて図面を参照して説明する。
【0012】
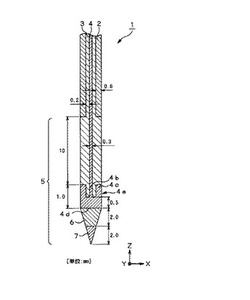
本発明に係るマイクロ波凝固療法用同軸アンテナ1(以下、単に「アンテナ1」という。)は、RL(Reactive Load)付同軸アンテナであり、先端部が先鋭で臓器内に刺入し易く構成されており、肝臓癌等の臓器内患部の凝固療法に用いられる。具体的に、図1に示すように、このアンテナ1は、外周部に外部電極2が設けられ、この外部電極2の内側に、テフロン(登録商標)等のフッ素樹脂で形成された筒状の絶縁体3を介して中心電極4が設けられている。中心電極4は、外部電極2の先端部より更に導出するように形成されており、絶縁体3は、外部電極2の内側のみならず、外部電極2の先端部より導出した中心電極4も被覆している。中心電極4には、電流が供給され、この中心電極4の外部電極2より導出した部分は、マイクロ波照射部5となる。マイクロ波照射部5は、その外表面を、テフロン(登録商標)等のフッ素樹脂や強度のあるセラミック等で、強度補強をしつつ、生体組織の付着を防止するようにしても良い。
【0013】
マイクロ波照射部5の先端側、すなわち中心電極4の先端部は、RL部4aとなっており、図2に示すように、内側電極4bの周囲に外側電極4cが一体的に形成され、先端面4dが平坦となるように形成されている。これにより、図2中矢印で示す電気力線(図中矢印で示す。)は、平坦な先端面4dに対して垂直となり、SAR(Specific Absorption Rate)分布を横方向(x−y方向)に膨らみを持たせることができる。
【0014】
更に、マイクロ波照射部5には、先端部に、臓器への刺入を行う易くするため、刺入等部6が設けられている。この刺入頭部6は、先鋭をなし、セラミック等の誘電体で形成されている。更に、刺入頭部6は、脆弱な先端部の補強のため、先端部に導電体7が設けられている。なお、刺入頭部6の先端部の導電体7は、誘電体の表面に形成しても良く、また、先端部を導電体で形成しても良い。
【0015】
以上のようなアンテナ1は、マイクロ波照射部5の先端部に刺入頭部6が設けられていることから、臓器内に容易に刺入することができると共に、導電体7で先端部が補強されていることから、治療中に刺入頭部6の先端部が破損することを防止することができる。また、中心電極4の先端部は、内側電極4bと外側電極4cとが一体で、更に、先端面が平坦に形成されたRL部5aとなっていることから、電気力線を平坦な先端面4dに対して略垂直に発生させることができ、SAR分布を横方向(x−y方向)に膨らみを持たせることができる。すなわち、横方向(x−y方向)の広範囲に亘って臓器内患部の凝固治療を行うことができる。
【0016】
以上のような本発明に係るアンテナ1の効果確認のため、比較例となる図3及び図4に示すマイクロ波凝固療法用同軸アンテナを作成した。図3に示すマイクロ波凝固療法用同軸アンテナ10(以下、単に「アンテナ10」という。)は、マイクロ波照射部5の先端部の刺入頭部6が中心電極4と一体的形成されていることを特徴とするものであり、上記特許文献1の図1と類似のものである。すなわち、刺入頭部6は、中心電極4と連続した導電体によって全体が形成されている。
【0017】
また、図4に示すマイクロ波凝固療法用同軸アンテナ20(以下、単に「アンテナ20」という。)は、刺入頭部6を設けないものであり、本発明に係るアンテナ1の前提となるものである。すなわち、このアンテナ20は、本発明のアンテナ1と同じRL部4aを有しており、RL部4aの先端面4dが平坦に形成されることで、電気力線を平坦な先端面4dに対して略垂直に発生させ、SAR分布を横方向(x−y方向)に膨らみを持たせることができる。このアンテナ20は、先端面が平坦であることから、臓器内患部への刺入に不向きであり、口腔内患部の加熱凝固治療に用いらている。なお、本発明のアンテナ1は、このアンテナ20の性能を維持しながら臓器内患部の加熱凝固治療を可能にするものである。
【0018】
アンテナ1,10,20の絶縁体3については、全て比誘電率ε1=2.03のテフロンを用いた。また、本発明のアンテナ1の刺入頭部6には、比誘電率ε2=10.0のセラミックを用いた。また、図1、図3及び図4に示すように、外部電極2、絶縁体3、中心電極4等の寸法は、同じにした。これらのマイクロ波凝固療法用同軸アンテナ1,10,20について、横断面(x−y)は(正)方形で近似し、励振点をスロット(絶縁体3が外周部に露出した図1、図3、図4中、長さ10mmの部分)中心から高さ63mm、その周波数f=2.45GHz、入力電力P=20Wとした。また、解析には、FDTD(Finite Difference Time Domain)法を用いた。計算領域を構成する微小セルは直方体(δx=δy=0.1mm、δz=0.5mm)であり、仮想六面には8層PML(A Perfectly Matched Layer)吸収境界条件を与えている。
【0019】
以上のような条件で、アンテナ1,10,20を肝臓内に刺入した際の肝臓内のSAR分布を図5(A)〜図5(C)に示す。なお、ここで使用した肝臓の誘電率ε3=43.0で導電率σ3は43.0である。また、図5(A)が本発明のアンテナ1のSAR分布で、図5(B)が本発明の比較例となるアンテナ10のSAR分布で、図5(C)が本発明の前提となるアンテナ20のSAR分布である。また、図5(A)〜図5(C)の上段は、z×x=40.0mm×25.6mm、下段は、x×y=25.6mm×25.6mmである。
【0020】
本発明の図5(A)に示したSAR分布と本発明の前提となる図5(C)に示したSAR分布とを比較すると、本発明のアンテナ1は、RL部4aの平坦な先端面4dから垂直に電気力線が発生することから、本発明の前提となるアンテナ20と同様に、横方向(x−y方向)に膨らみを持ったSAR分布となっている。これに対して、図5(B)の比較例となっているアンテナ10は、刺入頭部6の斜めの外周面から電気力線が出ることから、RLの効果が弱まり、図5(A)及び図5(C)よりSAR分布の膨らみが小さくなる。このことから、本発明のアンテナ1は、刺入頭部6を設けても、この刺入頭部6を誘電体で形成することによって、本発明の前提となるアンテナ20と同様なSAR分布を実現することができることが分かる。
【0021】
なお、本発明の図5(A)のSAR分布を見ると、刺入頭部6の導電体7に対応する部分にも、「点」状のSAR分布を確認することができる。これは、RL部4aからの変位電流及び/又は肝臓を介した迂回電流によるものである。「点」状のSAR分布の大きさは、RL部4aと導電体7との間の距離を可変することによって制御可能であり、例えば、導電体7とRL部4aとの距離を短くすると大きくすることができる。本発明のンテナ1では、刺入頭部6の導電体7を癌等の患部の最奥部に位置させ患部の凝固治療を行うことによって、臓器内患部の加熱凝固可能な範囲を広げることもできる。この場合には、本発明に係るアンテナ1の刺入頭部6も生体組織を凝固可能な温度まで上がり、凝固組織が付着する虞がある。そこで、使用時には、正常組織に凝固組織が付着することを防止するため、凝固組織が付着しない温度にまで下げてから、アンテナ1を臓器内患部より引き抜くことが必要となる。
【0022】
更に詳細なSAR分布を図6及び図7に示す。図6は、同軸中心からx=1.5mm、図7は同軸中心からx=3.0mmの同軸方向(z方向)のSAR分布である。これらの図中、線31は、図1に示すアンテナ1の特性を示し、線32は、図3に示す本発明の比較例となるアンテナ10の特性を示し、線33は、図4に示す本発明の前提となるアンテナ20の特性を示す。本発明のアンテナ1を示す線31及び本発明の前提のアンテナ20を示す線33を見ると、本発明のアンテナ1は、刺入頭部6が誘電体で形成されていることから、本発明の前提のアンテナ20と略同じ特性を有し、スロット中心のSARよりその両側のSAR分布が同じような強度をもって大きくなっている。なお、上昇温度特性を見たときには、スロット中心よりその両側が大きい特性は緩和されることから、スロット中心の谷部は小さくなり、均一な温度分布で生体組織の凝固治療が可能となる。
【0023】
そして、本発明のアンテナ1を示す線31及び本発明の前提のアンテナ20を示す線33は、本発明の比較例となるアンテナ10の線32より立ち上がりが速く、アンテナ1,20は、比較例のアンテナ10より中心軸線(縦)に対して略直角な横方向の広範囲に亘って凝固治療が可能であることを確認することができる。
【図面の簡単な説明】
【0024】
【図1】本発明に係るマイクロ波凝固療法用同軸アンテナの縦(z−x)断面図である。
【図2】本発明に係るマイクロ波凝固療法用同軸アンテナのRL部の拡大断面図である。
【図3】本発明の比較例となる導電体で刺入頭部が形成されたマイクロ波凝固療法用同軸アンテナの縦(z−x)断面図である。
【図4】本発明の前提となる先端面が平坦なRL部を有するマイクロ波凝固療法用同軸アンテナの縦(z−x)断面図である。
【図5A】肝臓内のSAR分布を示す写真であり、上段は横(x−y)断面、下段は縦(z−x)断面であり、図1に示した本発明に係るマイクロ波凝固療法用同軸アンテナのSAR分布を示す。
【図5B】肝臓内のSAR分布を示す写真であり、上段は横(x−y)断面、下段は縦(z−x)断面であり、図3に示した本発明の比較例となるマイクロ波凝固療法用同軸アンテナのSAR分布を示す。
【図5C】肝臓内のSAR分布を示す写真であり、上段は横(x−y)断面、下段は縦(z−x)断面であり、本発明の前提となるマイクロ波凝固療法用同軸アンテナのSAR分布を示す。
【図6】x=1.5mmの肝臓内のSAR特性を示す特性図である。
【図7】x=3.0mmの肝臓内のSAR特性を示す特性図である。
【符号の説明】
【0025】
1 マイクロ波凝固療法用同軸アンテナ、2 外部電極、3 絶縁体、4 中心電極、4a RL部、4b 内側電極、4c 外側電極、4d 先端面、5 マイクロ波照射部、6 刺入頭部、7 導電体、10 比較例のマイクロ波凝固療法用同軸アンテナ、20 本発明の前提となるマイクロ波凝固療法用同軸アンテナ
【技術分野】
【0001】
本発明は、マイクロ波による生体組織の凝固を行うマイクロ波凝固療法用同軸アンテナに関する。
【背景技術】
【0002】
マイクロ波凝固療法用同軸アンテナは、外部電極の内側に絶縁体を介して設けられた中心電極を外部電極の先端より導出させてなり、この中心電極の先端部にマイクロ波照射部が設けられている。このマイクロ波照射部は、中心電極より供給される交流電流によって、生体組織内にマイクロ波を照射し、生体組織内に発生した誘電熱によって病変組織を熱凝固させる。
【0003】
この種のマイクロ波凝固療法用同軸アンテナには、例えば特許文献1のものがある。この特許文献1のマイクロ波凝固療法用同軸アンテナは、先端部に中心電極と一体の先鋭の刺入頭部が設けられている(特許文献1の図1参照)。これによれば、刺入頭部によって、臓器内患部等にも容易に刺入することができる。また、このマイクロ波手術器は、中心電極と一体の導電体で刺入頭部が形成されていることから、斜めの外周面から電気力線が出現することから、マイクロ波の照射範囲が中心軸線(縦)方向に長くなり、中心軸線(縦)方向の広範囲に亘ってマイクロ波を照射することになる。
【0004】
ところで、癌等の臓器内患部は、一般に球に近い楕円体をしていることが多い。したがって、このマイクロ波手術器のように、マイクロ波が中心軸線(縦)方向の広範囲に亘って発生すると、臓器への刺入時に臓器内患部だけでなくその周囲の正常組織まで破壊してしまうおそれがある。一方で、マイクロ波の照射範囲は、楕円体状の患部を広範囲に凝固することができるようにするため、中心軸線(縦)に対して略直角な横方向には広がりがあった方が良い。
【0005】
また、特許文献1には、先鋭の刺入頭部をセラミック等の絶縁体で形成し、刺入頭部の加熱温度を低くし、凝固組織の付着を低減することが記載されている(特許文献1の図2参照)。しかしながら、セラミックは、使用時に、破損してしまうおそれもある。
【0006】
【特許文献1】特開2004−187703号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明の目的は、臓器内患部等への刺入を容易としながらも中心軸線(縦)に対して略直角な横方向の広範囲に亘って患部組織を加熱凝固することができるマイクロ波凝固療法用同軸アンテナを提供することにある。
【0008】
また、本発明の目的は、先端に形成された刺入頭部を強固にしたマイクロ波凝固療法用同軸アンテナを提供することにある。
【課題を解決するための手段】
【0009】
本発明に係るマイクロ波凝固療法用同軸アンテナは、上述の課題を解決するために、外部電極と、この外部電極の内側に絶縁体を介して設けられ、上記外部電極の先端部より導出した部分にマイクロ波照射部を形成した中心電極とを備える。上記マイクロ波照射部は、中心電極の先端部に、内側電極と外側電極とが一体で先端面が平坦なRL(Reactive Load)部が設けられている。このRL部からは、平坦な先端面に対して垂直に電気力線が発生することから、中心軸線(縦)に対して略直角な横方向の広範囲に亘って臓器内患部を加熱凝固することができる。上記RL部の平坦な先端面には、誘電体によって全体が先鋭をなす刺入頭部が形成されており、臓器内患部に容易に刺入することができる。そして、上記刺入頭部の先端部は、導電体によって補強されている。
【発明の効果】
【0010】
本発明では、中心電極の先端部に内側電極と外側電極とが一体で先端面が平坦なRL部が形成されていることから、先端面に対して垂直な電気力線を発生させることができ、これにより、中心軸線(縦)に対して略直角な横方向に膨らみを持ったSAR(Specific Absorption Rate)分布を実現することができる。そして、誘電体によって略先鋭の刺入頭部が設けられていることから、この特性を維持しながら、臓器内患部等に容易に刺入することができる。この刺入頭部は、先端部に導電体が設けられていることから、強度補強がされており、使用時等に破壊することを防止することができる。
【発明を実施するための最良の形態】
【0011】
以下、本発明に係るマイクロ波凝固療法用同軸アンテナについて図面を参照して説明する。
【0012】
本発明に係るマイクロ波凝固療法用同軸アンテナ1(以下、単に「アンテナ1」という。)は、RL(Reactive Load)付同軸アンテナであり、先端部が先鋭で臓器内に刺入し易く構成されており、肝臓癌等の臓器内患部の凝固療法に用いられる。具体的に、図1に示すように、このアンテナ1は、外周部に外部電極2が設けられ、この外部電極2の内側に、テフロン(登録商標)等のフッ素樹脂で形成された筒状の絶縁体3を介して中心電極4が設けられている。中心電極4は、外部電極2の先端部より更に導出するように形成されており、絶縁体3は、外部電極2の内側のみならず、外部電極2の先端部より導出した中心電極4も被覆している。中心電極4には、電流が供給され、この中心電極4の外部電極2より導出した部分は、マイクロ波照射部5となる。マイクロ波照射部5は、その外表面を、テフロン(登録商標)等のフッ素樹脂や強度のあるセラミック等で、強度補強をしつつ、生体組織の付着を防止するようにしても良い。
【0013】
マイクロ波照射部5の先端側、すなわち中心電極4の先端部は、RL部4aとなっており、図2に示すように、内側電極4bの周囲に外側電極4cが一体的に形成され、先端面4dが平坦となるように形成されている。これにより、図2中矢印で示す電気力線(図中矢印で示す。)は、平坦な先端面4dに対して垂直となり、SAR(Specific Absorption Rate)分布を横方向(x−y方向)に膨らみを持たせることができる。
【0014】
更に、マイクロ波照射部5には、先端部に、臓器への刺入を行う易くするため、刺入等部6が設けられている。この刺入頭部6は、先鋭をなし、セラミック等の誘電体で形成されている。更に、刺入頭部6は、脆弱な先端部の補強のため、先端部に導電体7が設けられている。なお、刺入頭部6の先端部の導電体7は、誘電体の表面に形成しても良く、また、先端部を導電体で形成しても良い。
【0015】
以上のようなアンテナ1は、マイクロ波照射部5の先端部に刺入頭部6が設けられていることから、臓器内に容易に刺入することができると共に、導電体7で先端部が補強されていることから、治療中に刺入頭部6の先端部が破損することを防止することができる。また、中心電極4の先端部は、内側電極4bと外側電極4cとが一体で、更に、先端面が平坦に形成されたRL部5aとなっていることから、電気力線を平坦な先端面4dに対して略垂直に発生させることができ、SAR分布を横方向(x−y方向)に膨らみを持たせることができる。すなわち、横方向(x−y方向)の広範囲に亘って臓器内患部の凝固治療を行うことができる。
【0016】
以上のような本発明に係るアンテナ1の効果確認のため、比較例となる図3及び図4に示すマイクロ波凝固療法用同軸アンテナを作成した。図3に示すマイクロ波凝固療法用同軸アンテナ10(以下、単に「アンテナ10」という。)は、マイクロ波照射部5の先端部の刺入頭部6が中心電極4と一体的形成されていることを特徴とするものであり、上記特許文献1の図1と類似のものである。すなわち、刺入頭部6は、中心電極4と連続した導電体によって全体が形成されている。
【0017】
また、図4に示すマイクロ波凝固療法用同軸アンテナ20(以下、単に「アンテナ20」という。)は、刺入頭部6を設けないものであり、本発明に係るアンテナ1の前提となるものである。すなわち、このアンテナ20は、本発明のアンテナ1と同じRL部4aを有しており、RL部4aの先端面4dが平坦に形成されることで、電気力線を平坦な先端面4dに対して略垂直に発生させ、SAR分布を横方向(x−y方向)に膨らみを持たせることができる。このアンテナ20は、先端面が平坦であることから、臓器内患部への刺入に不向きであり、口腔内患部の加熱凝固治療に用いらている。なお、本発明のアンテナ1は、このアンテナ20の性能を維持しながら臓器内患部の加熱凝固治療を可能にするものである。
【0018】
アンテナ1,10,20の絶縁体3については、全て比誘電率ε1=2.03のテフロンを用いた。また、本発明のアンテナ1の刺入頭部6には、比誘電率ε2=10.0のセラミックを用いた。また、図1、図3及び図4に示すように、外部電極2、絶縁体3、中心電極4等の寸法は、同じにした。これらのマイクロ波凝固療法用同軸アンテナ1,10,20について、横断面(x−y)は(正)方形で近似し、励振点をスロット(絶縁体3が外周部に露出した図1、図3、図4中、長さ10mmの部分)中心から高さ63mm、その周波数f=2.45GHz、入力電力P=20Wとした。また、解析には、FDTD(Finite Difference Time Domain)法を用いた。計算領域を構成する微小セルは直方体(δx=δy=0.1mm、δz=0.5mm)であり、仮想六面には8層PML(A Perfectly Matched Layer)吸収境界条件を与えている。
【0019】
以上のような条件で、アンテナ1,10,20を肝臓内に刺入した際の肝臓内のSAR分布を図5(A)〜図5(C)に示す。なお、ここで使用した肝臓の誘電率ε3=43.0で導電率σ3は43.0である。また、図5(A)が本発明のアンテナ1のSAR分布で、図5(B)が本発明の比較例となるアンテナ10のSAR分布で、図5(C)が本発明の前提となるアンテナ20のSAR分布である。また、図5(A)〜図5(C)の上段は、z×x=40.0mm×25.6mm、下段は、x×y=25.6mm×25.6mmである。
【0020】
本発明の図5(A)に示したSAR分布と本発明の前提となる図5(C)に示したSAR分布とを比較すると、本発明のアンテナ1は、RL部4aの平坦な先端面4dから垂直に電気力線が発生することから、本発明の前提となるアンテナ20と同様に、横方向(x−y方向)に膨らみを持ったSAR分布となっている。これに対して、図5(B)の比較例となっているアンテナ10は、刺入頭部6の斜めの外周面から電気力線が出ることから、RLの効果が弱まり、図5(A)及び図5(C)よりSAR分布の膨らみが小さくなる。このことから、本発明のアンテナ1は、刺入頭部6を設けても、この刺入頭部6を誘電体で形成することによって、本発明の前提となるアンテナ20と同様なSAR分布を実現することができることが分かる。
【0021】
なお、本発明の図5(A)のSAR分布を見ると、刺入頭部6の導電体7に対応する部分にも、「点」状のSAR分布を確認することができる。これは、RL部4aからの変位電流及び/又は肝臓を介した迂回電流によるものである。「点」状のSAR分布の大きさは、RL部4aと導電体7との間の距離を可変することによって制御可能であり、例えば、導電体7とRL部4aとの距離を短くすると大きくすることができる。本発明のンテナ1では、刺入頭部6の導電体7を癌等の患部の最奥部に位置させ患部の凝固治療を行うことによって、臓器内患部の加熱凝固可能な範囲を広げることもできる。この場合には、本発明に係るアンテナ1の刺入頭部6も生体組織を凝固可能な温度まで上がり、凝固組織が付着する虞がある。そこで、使用時には、正常組織に凝固組織が付着することを防止するため、凝固組織が付着しない温度にまで下げてから、アンテナ1を臓器内患部より引き抜くことが必要となる。
【0022】
更に詳細なSAR分布を図6及び図7に示す。図6は、同軸中心からx=1.5mm、図7は同軸中心からx=3.0mmの同軸方向(z方向)のSAR分布である。これらの図中、線31は、図1に示すアンテナ1の特性を示し、線32は、図3に示す本発明の比較例となるアンテナ10の特性を示し、線33は、図4に示す本発明の前提となるアンテナ20の特性を示す。本発明のアンテナ1を示す線31及び本発明の前提のアンテナ20を示す線33を見ると、本発明のアンテナ1は、刺入頭部6が誘電体で形成されていることから、本発明の前提のアンテナ20と略同じ特性を有し、スロット中心のSARよりその両側のSAR分布が同じような強度をもって大きくなっている。なお、上昇温度特性を見たときには、スロット中心よりその両側が大きい特性は緩和されることから、スロット中心の谷部は小さくなり、均一な温度分布で生体組織の凝固治療が可能となる。
【0023】
そして、本発明のアンテナ1を示す線31及び本発明の前提のアンテナ20を示す線33は、本発明の比較例となるアンテナ10の線32より立ち上がりが速く、アンテナ1,20は、比較例のアンテナ10より中心軸線(縦)に対して略直角な横方向の広範囲に亘って凝固治療が可能であることを確認することができる。
【図面の簡単な説明】
【0024】
【図1】本発明に係るマイクロ波凝固療法用同軸アンテナの縦(z−x)断面図である。
【図2】本発明に係るマイクロ波凝固療法用同軸アンテナのRL部の拡大断面図である。
【図3】本発明の比較例となる導電体で刺入頭部が形成されたマイクロ波凝固療法用同軸アンテナの縦(z−x)断面図である。
【図4】本発明の前提となる先端面が平坦なRL部を有するマイクロ波凝固療法用同軸アンテナの縦(z−x)断面図である。
【図5A】肝臓内のSAR分布を示す写真であり、上段は横(x−y)断面、下段は縦(z−x)断面であり、図1に示した本発明に係るマイクロ波凝固療法用同軸アンテナのSAR分布を示す。
【図5B】肝臓内のSAR分布を示す写真であり、上段は横(x−y)断面、下段は縦(z−x)断面であり、図3に示した本発明の比較例となるマイクロ波凝固療法用同軸アンテナのSAR分布を示す。
【図5C】肝臓内のSAR分布を示す写真であり、上段は横(x−y)断面、下段は縦(z−x)断面であり、本発明の前提となるマイクロ波凝固療法用同軸アンテナのSAR分布を示す。
【図6】x=1.5mmの肝臓内のSAR特性を示す特性図である。
【図7】x=3.0mmの肝臓内のSAR特性を示す特性図である。
【符号の説明】
【0025】
1 マイクロ波凝固療法用同軸アンテナ、2 外部電極、3 絶縁体、4 中心電極、4a RL部、4b 内側電極、4c 外側電極、4d 先端面、5 マイクロ波照射部、6 刺入頭部、7 導電体、10 比較例のマイクロ波凝固療法用同軸アンテナ、20 本発明の前提となるマイクロ波凝固療法用同軸アンテナ
【特許請求の範囲】
【請求項1】
外部電極と、この外部電極の内側に絶縁体を介して設けられ、上記外部電極の先端部より導出した部分にマイクロ波照射部を形成した中心電極とを備え、
上記マイクロ波照射部は、中心電極の先端部に、内側電極と外側電極とが一体で先端面が平坦なRL(Reactive Load)部が設けられ、
上記RL部の平坦な先端面には、誘電体によって全体が先鋭をなす刺入頭部が形成され、
上記刺入頭部の先端部には、導電体が形成されていることを特徴とするマイクロ波凝固療法用同軸アンテナ。
【請求項1】
外部電極と、この外部電極の内側に絶縁体を介して設けられ、上記外部電極の先端部より導出した部分にマイクロ波照射部を形成した中心電極とを備え、
上記マイクロ波照射部は、中心電極の先端部に、内側電極と外側電極とが一体で先端面が平坦なRL(Reactive Load)部が設けられ、
上記RL部の平坦な先端面には、誘電体によって全体が先鋭をなす刺入頭部が形成され、
上記刺入頭部の先端部には、導電体が形成されていることを特徴とするマイクロ波凝固療法用同軸アンテナ。
【図1】


【図2】


【図3】


【図4】


【図5A】


【図5B】


【図5C】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5A】


【図5B】


【図5C】


【図6】


【図7】


【公開番号】特開2007−29457(P2007−29457A)
【公開日】平成19年2月8日(2007.2.8)
【国際特許分類】
【出願番号】特願2005−217786(P2005−217786)
【出願日】平成17年7月27日(2005.7.27)
【出願人】(899000057)学校法人日本大学 (650)
【Fターム(参考)】
【公開日】平成19年2月8日(2007.2.8)
【国際特許分類】
【出願日】平成17年7月27日(2005.7.27)
【出願人】(899000057)学校法人日本大学 (650)
【Fターム(参考)】
[ Back to top ]

