ディーエスエム ファイン ケミカルズ オーストリア エヌエフジー ゲーエムベーハー ウント ツェーオー カーゲーにより出願された特許
1 - 10 / 13
連続乳化重合方法
Notice: Undefined index: from_cache in /mnt/www/gzt_applicant_list.php on line 189
シクロプロパン誘導体の生成方法
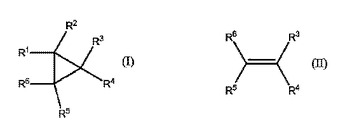
式(I)のシクロプロパン誘導体の調製方法であって、式(II)のオレフィンと式:CR1R2のカルベンとを反応容器中、銅金属または銅酸化物の存在下、場合によっては溶媒の存在下で、反応させるステップを含み、式中、R1およびR2はそれぞれ独立に、水素、C1〜C6アルキル、C2〜C6アルケニル、アリール、ヘテロアリール、ヘテロシクリル、カルボシクリル、ヘテロシクリル、−C(O)R7、または−NR82であり;R3、R4、R5、およびR6はそれぞれ独立に、水素、C1〜C6アルキル、C1〜C6アルコキシ、C2〜C6アルケニル、アリール、アリールオキシ、ヘテロアリール、ヘテロシクリル、カルボシクリル、ヘテロシクリル、−C(O)R9、−NR102、−SR11、−S(O)R11、または−SO2R11であり、あるいはR3およびR6は上記に定義された通りであり、かつR4とR5は一緒になって環を形成し、その環はカルボシクリル、ヘテロシクリル、芳香族またはヘテロ芳香族であり;R7は、水素、ヒドロキシ、C1〜C6アルキル、C1〜C6アルコキシ、アリール、アリールオキシ、ヘテロアリール、または−NR102であり;R8は、水素、C1〜C6アルキル、C1〜C6アルケニル、アリール、ヘテロアリール、カルボシクリル、またはヘテロシクリルであり;R9は、水素、ヒドロキシ、C1〜C6アルキル、C1〜C6アルコキシ、アリール、アリールオキシ、またはヘテロアリールであり;R10は、水素、C1〜C6アルキル、C2〜C6アルケニル、アリール、ヘテロアリール、カルボシクリル、ヘテロシクリル、またはC(O)R12であり;R11は、水素、C1〜C6アルキル、C2〜C6アルケニル、アリール、ヘテロアリール、カルボシクリル、またはヘテロシクリルであり;R12は、水素、ヒドロキシ、C1〜C6アルキル、C1〜C6アルコキシ、アリール、またはアリールオキシであり、連続プロセスである方法。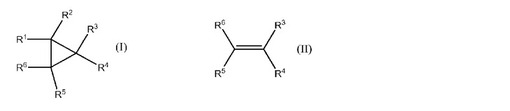
 (もっと読む)
(もっと読む)
3,4−ジ置換フェニル酢酸および新規な中間体の調製方法
式(I)、
【化1】
(式中、Xは、フッ素、塩素、臭素、またはヨウ素であり、Rは、C1〜C4アルキルチオ、C1〜C4アルキルスルホニル、またはC1〜C4アルキルスルホキシドである)の3,4−ジ置換フェニル酢酸の調製方法であって、式(II)、
【化2】
(式中、Xは、上記と同義であり、R1は、C1〜C4アルキルチオである)の2−ハロ−C1〜C4アルキルチオベンゼンから出発する方法。
(もっと読む)
エステラーゼ活性を有する新規なポリペプチドおよび組換えエステラーゼ、並びに、それらの使用
配列番号1のアミノ酸配列を示す、エステラーゼ活性を有するポリペプチドおよび組換えタンパク質、並びにその使用。 (もっと読む)
ラセミ体アルキル−5−ハロペンタ−4−エンカルボン酸または−カルボン酸エステルの調製方法
式(I)、
のラセミ体アルキル−5−ハロペンタ−4−エンカルボン酸およびそのエステルの調製方法であって、a)式(II)、
の金属アルコキシドの存在下に、有機溶媒中で、1,3−ジハロプロペンと反応させることによって、対応するアリル化マロン酸エステルを得るステップと、次いで、b)転化完了後、反応混合物に無機塩およびC1〜C6アルコールを添加し、この反応混合物を環流温度に加熱するステップと、次いで、c)抽出または直接蒸留によって所望の式(I)のラセミ体エステルを反応混合物から単離するステップと、d)所望の最終生成物がラセミ酸である場合は、エステル官能基を加水分解するステップとを含む方法。
(もっと読む)
高純度のハロゲン非含有o−フタルアルデヒドを製造するための方法
【課題】高純度のハロゲン非含有o−フタルアルデヒドを製造するための改善された方法を提供する。
【解決手段】a)テトラハロ−o−キシロールを155−160℃の温度および2〜5barの圧力において、場合により相転移触媒の存在下に、o−フタルアルデヒドに加水分解し、これを
b)0〜還流温度の温度における酸性のアルコール溶媒中で対応するジアルコキシフタランへ転換させ、次いで
c)pH>1.5〜pH7における酸性加水分解によってアセタール分解を行い、それによって高純度のハロゲン非含有o−フタルアルデヒドを得る。
(もっと読む)
カルボカチオンの関与による発熱反応の段階的実施法
本発明は、カルボカチオンの関与による反応を行うための方法に関し、それによって、反応の初期の最も強い発熱段階が、マイクロリアクター中で、高温(60〜120℃)および短い滞留時間(1〜30秒)で行われ、その後のより弱い発熱の複数の段階が、より滞留時間の長い(1〜30秒)2つ以上の滞留時間ユニット中で任意により低温で行われる。 (もっと読む)
キラルシアノヒドリンの酵素的加水分解によりキラルα−ヒドロキシカルボン酸を製造する方法
本発明は、(R)−又は(S)−シアノヒドリンを、ロードコッカス・エリスロポレス(Rhodococcus erythropolis)NCIMB 11540 の存在下の酵素的加水分解により、それぞれ(R)−又は(S)−α−ヒドロキシカルボン酸に変換することを特徴とする、結晶性のキラルα−ヒドロキシカルボン酸の製造方法に関する。 (もっと読む)
エナンチオピュアなE−(2S)−アルキル−5−ハロペンタ−4−エン酸およびエステルの製造方法
式(I)(式中、RはC1〜C6のアルキル基であり、R1はHまたはC1〜C4のアルキルであり、Xは塩素、臭素またはヨウ素である)で示されるエナンチオピュアなE−(2S)−アルキル−5−ハロペンタ−4−エン酸およびそれらのエステルを製造する方法であって、対応するラセミ体2−アルキル−5−ハロペンタ−4−エン酸を、a)溶剤中で、最初に(S)−3−メチル−2−フェニルブチルアミン、キニンまたはN−メチル−D−グルカミンと反応させ、b)対応する(R)−ペンテン酸の(S)−3−メチル−2−フェニルブチルアミン塩、キニンまたはグルカミン塩を沈殿させて除去し、c)残留ろ液を第2のキラル塩基または無機塩と混合し、対応する(S)−ペンテン酸の塩を沈殿させ、d)対応するE−(2S)−アルキル−5−ハロ−4−ペンテン酸に変換し、必要ならば、対応する式(I)(式中、R1はC1〜C4アルキルである)で示されるエステルに変換する製造方法。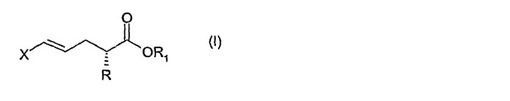 (もっと読む)
(もっと読む)
水性オルト−フタルアルデヒド溶液の製造方法
【課題】 水性オルト−フタルアルデヒド溶液の製造方法を提供する。
【解決手段】 o−フタルアルデヒドのアセタールを水に入れ、次いで酸の添加によってpH値を7未満にし、その後10℃〜90℃の温度下で前記アセタールを適切なアルコールの分離によってo−フタルアルデヒドに変える水性オルト−フタルアルデヒド溶液の製造方法、およびこの溶液を製造するためのOPAアセタールの使用。
(もっと読む)
1 - 10 / 13
[ Back to top ]



