国際特許分類[C07C17/25]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | 非環式化合物または炭素環式化合物 (64,036) | ハロゲン化された炭化水素の製造 (1,114) | ハロゲン化された炭化水素からのハロゲン化水素の脱離によるもの (168)
国際特許分類[C07C17/25]に分類される特許
1 - 10 / 168
(Z)−1−クロロ−3,3,3−トリフルオロプロペンの製造方法
【課題】
3−クロロ−1,1,1,3−テトラフルオロプロパン(HCFC−244fa)を含む(Z)−1−クロロ−3,3,3−トリフルオロプロペン(OF−1233Z)から実質的にHCFC−244faを含まないOF−1233Zを効率的に製造する。
【解決手段】
HCFC−244faを含むOF−1233Z組成物をトリエチルアミンなどの第三アミンと接触させてアミン処理組成物とする工程を含むOF−1233Zの製造方法。また、OF−1233Z組成物が2−クロロ−1,1,1,3,3−ペンタフルオロプロパンを含む組成物であるときは、第三アミンでアミン処理した後、さらに水酸化ナトリウムなどの無機塩基と接触させる工程を含むOF−1233Zの製造方法。これらの処理生成物は、さらに蒸留により精製する。
(もっと読む)
1−クロロ−3,3,3−トリフルオロプロピンの製造方法
【課題】本発明は、冷媒、エッチング剤、エアゾール等の機能材料又は生理活性物質、機能性材料の中間体、高分子化合物のモノマーとなりうる、1−クロロ−3,3,3−トリフルオロプロピンの製造方法を提供する。
【解決手段】本発明によれば、穏和な条件下、1−クロロ−2−ハロゲノ−3,3,3−トリフルオロプロペンに液相中、塩基を反応させることで、高収率で1−クロロ−3,3,3−トリフルオロプロピンを得ることが可能である。また、相間移動触媒を用いた場合でも、反応後に2層分離するため、精製及び廃棄物処理も負荷がかからず、工業的な製造方法として優位性が高い。
(もっと読む)
1−クロロ−3,3,3−トリフルオロプロピンの製造方法
【課題】本発明は、冷媒、エッチング剤、エアゾール等の機能材料又は生理活性物質、機能性材料の中間体、高分子化合物のモノマーとなりうる、1−クロロ−3,3,3−トリフルオロプロピンの製造方法を提供する。
【解決手段】本発明によれば、穏和な条件下、1−クロロ−1,2−ジハロゲノ−3,3,3−トリフルオロプロパンに液相中、塩基を反応させることで、高収率で1−クロロ−3,3,3−トリフルオロプロピンを得ることが可能である。また、相間移動触媒を用いた場合でも、反応後に2層分離するため、精製及び廃棄物処理も負荷がかからず、工業的な製造方法として優位性が高い。
(もっと読む)
ポリクロロプロペンの製造方法
【課題】 1,1,1,2,3−ペンタクロロプロパンなどの下記式(1)
CCl3−CCl(2−m)H(m)−CCl(3−n)Hn (1)
で示されるクロロクロパンを、選択率、転化率などを良好に1,1,2,3−テトラクロロプロパンなどの下記式(2)
CCl2=CCl(2−m)H(m−1)−CCl(3−n)Hn (2)
(上記式(1)及び(2)中、mは1又は2、nは0〜3の整数)
で示される不飽和化合物へと変換する。
【解決手段】 無水塩化アルミニウムを触媒として存在させることにより、脱塩化水素反応が生じ式(1)で示されるクロロプロパンが式(2)で示されるクロロプロペンへと容易に変換される。式(1)のクロロプロパンが1,1,1,2,3−ペンタクロロプロパンである場合、反応温度90〜140℃、反応時間0.5〜10時間程度で、収率95%以上で1,1,2,3−テトラクロロプロペンが得られる。
(もっと読む)
フルオロオレフィンの製造方法
【課題】フルオロオレフィン類の製造方法の提供。
【解決手段】相間移動触媒の存在下で、式:CF3C(R1aR2b)C(R3cR4d){式中、R1、R2、R3及びR4は独立して、水素原子または、フッ素、塩素、臭素及びヨウ素からなる群から選択されるハロゲンであり、ただしR1、R2、R3及びR4の少なくとも一つはハロゲンであり、且つ隣接する炭素原子には少なくとも一つの水素と一つのハロゲンとがあり;aとbは独立して0、1または2であり、且つ(a+b)=2であり;及びcとdは独立して0、1、2または3であり、且つ(c+d)=3である}の化合物と、少なくとも一種のアルカリ金属の水酸化物とを接触させることにより、式:CF3CY=CXnHpのフルオロオレフィン類を製造する。
(もっと読む)
α,β,β−トリフルオロスチレン類の工業的な製造方法
【課題】α,β,β−トリフルオロスチレン類の工業的な製造方法を提供する。
【解決手段】α,β,β−トリフルオロスチレン類の製造において、α−アリール−α,β,β,β−テトラフルオロエタン類をアルカリ金属ビス(トリメチルシリル)アミドと反応させる脱フッ化水素工程と、引き続いて行う、目的物のα,β,β−トリフルオロスチレン類と副生物のビス(トリメチルシリル)アミンとを含む混合物をフッ化水素、または、有機塩基とフッ化水素とからなる塩もしくは錯体と反応させる後処理工程を含む、α,β,β−トリフルオロスチレン類の製造方法を提供する。
(もっと読む)
塩化ビニルモノマーの製造方法
【課題】より低温/低圧力において、塩化ビニルモノマーを効率的に製造することを目的とする。
【解決手段】1,2−ジクロロエタンを、固体酸触媒による触媒反応により脱塩酸して製造する塩化ビニルモノマーの製造方法であって、例えば、固体酸触媒として、γ−アルミナ及びシリカアルミナ等のルイス酸性を示す固体触媒を好適に用いる。
(もっと読む)
液晶化合物、その製造方法、液晶組成物および液晶電気光学素子
【課題】粘性が低く、透明点が高く、化学的に安定な新規な液晶化合物、その製造方法、高速応答性、広い動作温度範囲などの条件を満たした液晶組成物、広い温度範囲で高速応答性に優れる液晶電気光学素子の提供。
【解決手段】式(1)R1-(A1-Z1)m-(A2-Z2)n-(A3-Z3)o-A4-CF2CF2CH=CH-A5-(Z4-A6)p-(Z5-A7)q-(Z6-A8)r-R2で示される液晶化合物。R1、R2:水素原子、ハロゲン原子、または炭素数1〜10の一価の非環式脂肪族炭化水素基。A1〜A8:トランス−1,4−シクロへキシレン基、1,4−フェニレン基などの環基。Z1〜Z6:単結合、−O−、−S−、−COO−または炭素数1〜4の二価の非環式脂肪族炭化水素基。m、n、o、p、q、r:相互に独立して0または1(ただし、m+n+o+p+q+r≦3)。上記各基中の水素原子はハロゲン原子で置換されてもよい。一または二価の非環式脂肪族炭化水素基中の炭素−炭素原子間または基の結合末端に−O−または−S−が挿入されていてもよい。環基中の=CH−基は窒素原子で、−CH2−基は−O−または−S−で置換されていてもよい。
(もっと読む)
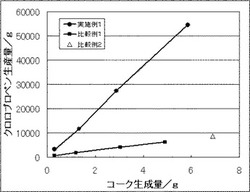
クロロプロペンの製造方法
【課題】高効率でクロロプロペンを製造する方法の提供。
【解決手段】1,1,1,3−テトラクロロプロパン等の下式1で示される原料クロロプロペンを熱分解して脱塩化水素させて、下式2で示されるクロロプロペンを得るに際し、コーキングを抑制し、長期間の連続運転を行うことを可能とし、もって生産性を向上させる。CCl3−CCl(2−m)Hm−CCl(3−n)Hn(1)CCl2=CCl(2−m)H(m−1)−CCl(3−n)Hn(2)(上記式中、いずれもmは1又は2、nは0〜3の整数である)
(もっと読む)
ヒドロフルオロカーボンまたはヒドロクロロフルオロカーボンの脱水方法、および該脱水方法を用いた1,3,3,3−テトラフルオロプロペンの製造方法
【課題】簡便な装置を用いることが可能なヒドロフルオロカーボンまたはヒドロクロロフルオロカーボンの脱水方法、および該脱水方法を用いた1,3,3,3−テトラフルオロプロペンの連続製造方法を提供する。
【解決手段】少なくとも水を含む気体状態のヒドロフルオロカーボンまたはヒドロクロロフルオロカーボンを熱交換器で冷却、凝縮液化し、前記水を氷結凝固させる工程を含む方法。例えば、1−クロロ−3,3,3−トリフルオロプロペンをフッ素化し、1,3,3,3−テトラフルオロプロペン、未反応原料、フッ化水素、塩化水素および副生成物を含む混合物を得る第1の工程、または脱フッ化水素し、1,3,3,3−テトラフルオロプロペン、未反応原料、副生物を含む混合物を得る第1の工程、酸性成分を除去する第2の工程、上記の脱水方法により脱水する第3の工程、蒸留精製する第4の工程からなる1,3,3,3−テトラフルオロプロペンの製造方法。
(もっと読む)
1 - 10 / 168
[ Back to top ]