国際特許分類[G01N21/65]の内容
物理学 (1,541,580) | 測定;試験 (294,940) | 材料の化学的または物理的性質の決定による材料の調査または分析 (128,275) | 光学的手段,すなわち.赤外線,可視光線または紫外線を使用することによる材料の調査または分析 (28,618) | 調査される材料が励起され,それにより光を発しまたは入射光の波長に変化を生ずるシステム (4,647) | 光学的励起 (4,229) | ラマン散乱 (680)
国際特許分類[G01N21/65]に分類される特許
631 - 640 / 680
生物学的細胞組織の分光分析用保護機構
本発明は、患者の関心体積中にある生物学的組織の特性を決定する分光分析系の保護機構を供する。分光系は高出力の放射線を利用し、かつ人体の感光性細胞組織が偶然に露光されるのを防ぐための保護機構を供するのが好ましい。本発明は、分光系の測定ヘッドが測定位置にあるか否かを検出するための様々な方法を提供する。測定ヘッドの測定位置は、たとえば、患者の皮膚の電気抵抗を測定する圧力センサの利用又は、関心体積の可視像を供する観察ビームの強度又は空間的構造を分析する光学的手段によって有効に決定することが可能である。  (もっと読む)
(もっと読む)
非侵襲血液分析用の測定ヘッド
本発明は、分光システム用の測定ヘッドを患者の皮膚の種々の異なる部分に取り付け及び固定する有効な方法を提供する。該測定ヘッドは、好ましくは、柔軟性のある取り扱いを提供すると共に、皮膚の種々の部分の複数の特性を考慮して非常に多様な付着領域を提供するような小型の設計を特徴とする。更に、該測定ヘッドは、対物レンズの光軸の横方向のずらしを必要としないような強固な且つ複雑でない光学設計を特徴とする。対物レンズと皮膚内の毛細血管との間の斯様な横断方向の相対移動は、好ましくは、皮膚を当該測定ヘッドの対物レンズに対して機械的にずらすことにより実行される。更に、本測定ヘッドは、該測定ヘッドと皮膚との間の接触圧を測定する1以上の圧力センサを有するように構成される。この圧力情報は、分光分析手段を校正すると共に、毛細血管の分光検査のための最適接触圧範囲を規定する所定の範囲内に接触圧を調節するために更に利用することができる。  (もっと読む)
(もっと読む)
自己相関関数を決定する方法
【課題】本発明は光信号の自己相関関数g(τ)の決定に関する。
【解決手段】本発明による方法は、光子が出現する時間(ti)を決定するステップと、所定の一連のパルス(w)に対して、関数s(w)=Sie−jwti、ここで、e−jwti=coswti+sinwi、を計算し、総ての受信パルスに渡る合計を計算するステップと、関数s(w)の絶対値の2乗S(w)を決定するステップと、所定の一連の時間間隔のパワースペクトラムS(w)のフーリエ変換g(τ)を計算するステップとを含む。
(もっと読む)
流体の分光分析に対するプローブヘッド
本発明は、患者の皮膚の表面下の関心体積を介して流れる流体の特性を確定する分光装置に係る。該分光装置は、励起ビームを関心体積へと案内し、また、関心体積からリターン放射線を収集するよう少なくとも1つのオブジェクティブを有するプローブヘッドを有する。該分光装置は、少なくとも分光分析ユニットと電源とを有するベースステーションを更に有する。当該装置は、多種の異なる光学信号を結合及び分離するよう、また、光学信号を関心体積内部で正確に位置付けるよう集束ユニット、フィルタユニット、及びビーム結合ユニットを活用する。ビーム結合ユニット、フィルタユニット、及び集束ユニットは、分光装置の特定の適用に依存してプローブヘッド又はベースステーションの内部で可変に実行され得、したがってプローブヘッドの可撓性がある小型の設計を可能にする。  (もっと読む)
(もっと読む)
スマートコンビナトリアルオペランド分光触媒システム
反応条件下でスクリーニングされている触媒材料の動的なバルク性質および表面性質と、表面の化学的な速度論情報および機構情報とを明らかにしながら、多数の触媒材料を同時にスクリーニングするための、触媒材料における構造-活性/選択性の関係性を究明するための、表面化学種だけでなく触媒材料における動的構造に関する情報を収集するための、デバイスおよびコンビナトリアル方法が開示される。これにより新規材料の発見プロセスを促進させることができ、関連コストを削減することができ、かつ、上記情報はまた、改善された材料および進歩した材料の設計をもたらし得る。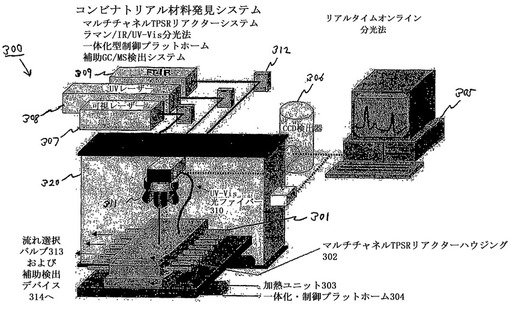
 (もっと読む)
(もっと読む)
表面増感ラマン分光法による分子結合を検出する方法
【解決手段】本願で提供されるのは、表面増感ラマン分光法(SERS)を用いて分子結合を検出する複数の方法である。SERS信号は、複数の結合相手の1つがSERS活性な粒子または基板と会合することによって生成される。2つの結合相手が互いに接触した後と、複数の結合相手が互いに接触する前とのSERS信号の変化を検出することにより、結合は検出される。方法は、複数の抗体の複数の抗原への結合、および複数の受容体の複数の配位子への結合のような複数の生物分子の結合の検出に有用である。 (もっと読む)
合成有機無機ナノクラスター
【解決手段】レーザによって励起された際に、複数の表面増感ラマン信号(SERS)を生成する、複数の合成有機無機ナノクラスター(COIN)が提供される。前記複数のナノクラスターは、複数の金属粒子およびラマン活性な有機化合物を含む。適切なSERS信号を達成するために必要とされる前記金属は、前記ナノクラスターに固有であり、広い種類のラマン活性な複数の有機化合物とその複数の組み合わせとを前記ナノクラスター内に組み込むことができる。さらに、前記複数のナノクラスターを含む複数の重合マイクロ球、およびそれらの複数の作成方法が提供される。前記複数のナノクラスターおよび前記複数のマイクロ球は、例えば、複数の生物製剤の分子の多重検出のための検定に用いられ得る。
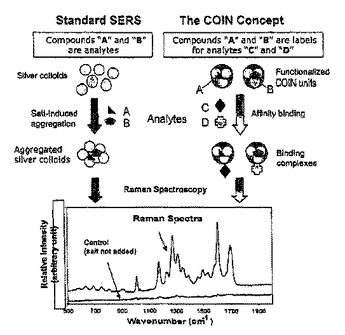 (もっと読む)
(もっと読む)
バイオ光学スキャニング較正方法
方法(188)、装置(10)、および組成物(30)は、インビボで非破壊的に組織の選択された分子構造を検出するバイオ光学スキャナーを較正する。装置(10)は、プロセッサー、メモリー、およびスキャナーを備え得る。スキャナーは、光を非破壊的に組織上にインビボで向け、次いで、検出器内へ戻る鏡およびレンズのシステムを通る放射応答の戻りを受容する。スキャナーを制御し、その出力を処理するソフトウェアは、組織の放射応答を模倣する合成材料(30)を使用して較正され得る。較正は、バックグラウンド蛍光および弾性散乱を考慮し得、目的のラマン散乱応答を実質的に有さない皮膚組織材料を模倣する。ドーパント(125c)は、組織内の選択された分子構造を模倣するためにホワイトスキャン材料のマトリクス(125b)に添加され得る。 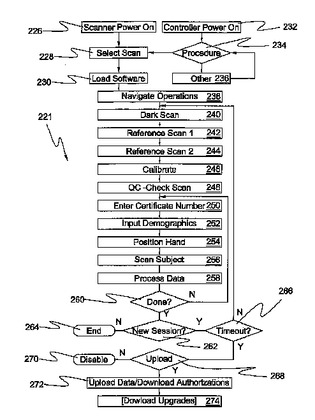 (もっと読む)
(もっと読む)
質量スペクトルと略同時に吸収・発光・散乱スペクトルを分析する分析装置および分析方法、並びに、エレクトロスプレーイオン化法を用いた質量分析装置および分析方法
濃度の高い被験試料をイオン気化した分析装置(10)のイオン化室に、イオン導入量制御手段(8)を設け、イオン引出電極(9)に導入する被験試料イオンの量を制御するため、質量スペクトルの分析および吸収・発光・散乱スペクトルの分析を略同時に行うことができる分析装置を提供することができる。さらに、スプレイヤー(104)に導入される前の上記被験試料溶液を冷却する低温浴(106)と、上記スプレイヤーおよび、上記スプレイヤー(104)に導入された上記被験試料溶液を冷却する、上記スプレイヤーとは独立した構造の冷却ガス導入管(108)とを備えことにより、高電圧印加時における被験試料の加熱を効果的に抑制することが可能となることから、極低温下でのみ安定な被験試料を用いた場合であっても、質量スペクトル分析と吸収・発光・散乱スペクトル分析とを略同時に行うことができる。 (もっと読む)
組織の光応答についての合成較正試料
バイオ光学スキャナを較正するための方法(188)、装置(10)、及び組成物のセット(30)を開示する。スキャナは、組織の選定された分子構造を、非破壊的にインビボで検出する。装置(10)には、スキャナに連結されたプロセッサ及びメモリを具えたコンピュータと、インビボの組織に光を非破壊的に導く照射装置と、光に対する組織の放射応答の強度を検出するための検出器と、光を被験体に導き、返ってくる放射応答を検出器に受けるためのプローブとを含めることができる。装置(10)は、生きた組織の放射応答を模擬した合成材料(30)を使用し、バックグラウンド蛍光及び弾性散乱を補正して較正される。合成材料(30)のマトリクス(125b)中のドーパント(125c)は、組織中の選定された分子構造を模擬している。  (もっと読む)
(もっと読む)
631 - 640 / 680
[ Back to top ]


