Fターム[4H039CA91]の内容
触媒を使用する低分子有機合成反応 (28,076) | 生成した置換基による反応の分類 (13,033) | ホウ素化 (32)
Fターム[4H039CA91]に分類される特許
21 - 32 / 32
光学活性なジアルキルホスフィノメタン誘導体の製造方法
【課題】高い光学収率で且つ工業的に有利な方法で光学活性なジアルキルホスフィノメタン誘導体を製造し得る方法を提供すること。
【解決手段】ジメチルアルキルホスフィンボラン等のホスフィンボラン化合物、触媒量の光学活性アミン及び溶媒の存在下、有機リチウム化合物を添加する第一工程、第一工程終了後に、モノハロゲン化ホスフィンを加えるか、又はジハロゲン化ホスフィンを加えた後にグリニアル試薬を加える第二工程、及び第二工程で得られた生成物にテトラヒドロフラン−ボラン錯体等を加える第三工程を有することを特徴とする光学活性なジアルキルホスフィノメタン誘導体の製造方法。モノハロゲン化ホスフィン又はジハロゲン化ホスフィンを加える前に、テトラヒドロフラン等の配位性溶媒を加えることが好ましい。光学活性アミンはスパルテインであることが好ましい。
(もっと読む)
オキサゾール−5−イルボロン酸誘導体、それらの製造方法及びそれらを用いたオキサゾール−5−イル基導入方法
【課題】医薬など幅広く利用されている5位置換オキサゾール誘導体の合成が可能であり、簡便に調製できるオキサゾール−5−イル基導入試薬を提供する。
【解決手段】一般式(1)
で示されるオキサゾール−5−イルボロン酸誘導体、それらの製造方法、およびそれらを用いたオキサゾール−5−イル基導入方法を提供するものである。
(式中、R1はアルキル基、アリール基などを表し、R2は水素原子、アリール基などを表し、R3及びR4は水素原子、アルキル基などを表し、R3とR4が一体となって環を形成してもよい。)
(もっと読む)
新規オルトジホウ素化アレーン化合物及びその製造方法
【課題】産業上有用なオルトジホウ素化アレーン化合物の効率的な製造方法及び新規なオルトジホウ素化アレーン化合物を提供する。
【解決手段】所定の芳香族化合物とホウ素−ホウ素結合を有するジボロン化合物とを、求核試薬及び白金触媒の存在下にて反応させることにより、産業上有用なオルトジホウ素化アレーン化合物の効率的な製造方法及び新規なオルトジホウ素化アレーン化合物を得ることができる。
(もっと読む)
ヘキサアルキルボラジンの製造方法
【課題】ホウ素原子および窒素原子の双方にアルキル基が結合しているヘキサアルキルボラジンを製造する過程において、大量合成の場合においても高い選択性で生成物を得る方法を提供する。
【解決手段】ボラジン化合物と、アルケン化合物とを、触媒存在下で反応させて、化学式2で表されるヘキサアルキルボラジンを合成する段階を有し、前記触媒および/または前記ボラジン化合物を徐々に反応系へ供給する、ヘキサアルキルボラジンの製造方法である。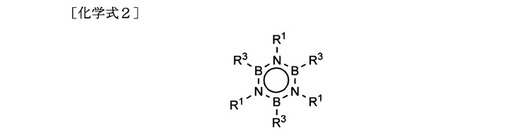 (もっと読む)
(もっと読む)
ビフェニレン誘導体、その用途、及びその製造方法
【課題】優れた耐酸化性を有し、塗布法による半導体活性相形成が可能な、ビフェニレン誘導体、それを用いた耐酸化性有機半導体材料並びに有機薄膜、及び該ビフェニレン誘導体を簡便に経済的に製造する方法を提供する。
【解決手段】下記一般式(1)で示されるビフェニレン誘導体を製造する。
(ここで、置換基R1〜R8は、水素原子、フッ素原子、アリール基、複素環基であり炭素原子で置換結合する基、アルキニル基、アルケニル基、アルキル基、又はフッ素化アルキル基を示す。但し、R1〜R8は同時にフェニル基であることはできず、R2及びR3は同時に水素原子又はフッ素原子であることはできず、又R6及びR7が同時に水素原子又はフッ素原子であることはできない。)
(もっと読む)
オキサゾール誘導体、それらの製造方法及びそれらを用いたオキサゾリル基導入方法
【課題】オキサゾール誘導体に関する。
【解決手段】一般式(1)(式中、R1はアルキル基、アラルキル基、芳香族基等を表し、R2は水素原子、アルキル基、アラルキル基、芳香族基等を表し、R3及びR4は同一又は相異ってアルキル基等を表し、R3とR4が一体となって環を形成してもよい。)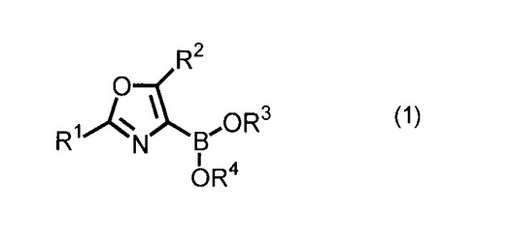
で示されるオキサゾール誘導体、それらの製造方法、およびそれらを用いたオキサゾリル基導入方法。
(もっと読む)
モノホスフィン化合物、その遷移金属錯体および該錯体を不斉触媒として用いる光学活性化合物の製造方法
【課題】 不斉付加反応、不斉共役付加反応や不斉ヒドロホウ素化反応等を高選択的に行うことを可能にし、さらに容易かつ安価に調製しうる不斉配位子およびそれを含む不斉遷移金属錯体を提供すること。
【解決手段】 一般式(I):
【化1】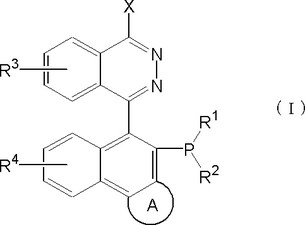
(式中、A環は存在しないかまたは置換基を有していてもよいベンゼン環を示し、R1およびR2はそれぞれ独立して、置換基を有していてもよいフェニル基、シクロヘキシル基等を示し、R3およびR4はそれぞれ独立して、水素原子、ハロゲン原子、低級アルキル基、低級アルコキシ基等を示し、Xは、−OR5または−NHR6(ここで、R5およびR6は置換基を有していてもよい低級アルキル基、置換基を有していてもよいアラルキル基等を示す。)で表される残基を示す。)で表される化合物、当該化合物を配位子として含有する不斉遷移金属錯体および当該錯体を不斉触媒として用いる光学活性化合物の製造方法。
(もっと読む)
4−ビフェニリルアゼチジン−2−オンの製造方法
本発明は、
式(1):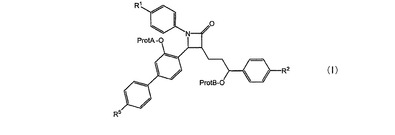
で表わされる4−ビフェニリルアゼチジン−2−オン誘導体の製造方法に関する。 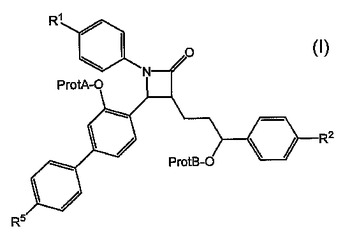 (もっと読む)
(もっと読む)
イオン性錯体の合成法
【課題】イオン性錯体の合成法を提供する。
【解決手段】一般式(1)のイオン性錯体を合成するに際し、一般式(2)と(3)の化合物と一般式(4)又は(5)のハロゲン含有化合物とを、1、2、13、14族元素を含む化合物の存在下で反応させる。 (もっと読む)
(もっと読む)
高分子固定化白金触媒及びその使用
【課題】 本発明は、白金触媒を両親媒性の架橋性高分子中に固定することにより調整された、高分子固定化白金触媒を用いる有機合成反応方法を提供する。
【解決手段】 白金を架橋高分子に担持させてなる高分子固定化白金触媒であって、該架橋高分子が芳香族側鎖及び親水性側鎖を有する架橋性高分子を架橋させてなることを特徴とする高分子固定化白金触媒である。この高分子担持白金触媒は、例えば極性溶媒を含む溶液中で該架橋性高分子に該白金の超微粒子を担持したミセルを形成した後、該架橋性高分子を架橋反応に付すことによって形成されることが好ましい。この触媒は、ヒドロシリル化反応、水素化反応、ホウ素化反応などに用いることができる。
(もっと読む)
大環状化合物を形成するための方法、組成物および装置
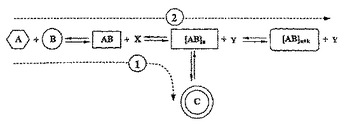
本発明は大環状化合物を製造するための方法、組成物および装置に関する。第1に、少なくとも環化反応を含む所望の反応経路を経て大環状化合物を形成できるとともに所望しないオリゴマー化を含む所望しない反応経路を経て所望しないオリゴマーをさらに形成できる1種以上の反応物が反応媒体中に提供される。反応媒体中のこうした反応のオリゴマー化は調節して、対応する非調節のオリゴマー化反応に比して、所望しないオリゴマーの形成を減らし、および/または反応媒体からの所望しないオリゴマーの分離を減らし、それによって大環状化合物の収率を最大にする。このようにして形成された大環状化合物は反応媒体から後で回収される。好ましくは、大環状化合物は相分離を経由して反応媒体から自然に分離する。より好ましくは、大環状化合物は反応媒体から自然に沈殿し、従って単純な濾過によって容易に回収することが可能である。
 (もっと読む)
(もっと読む)
ボロン酸エステルおよびボロン酸化合物の合成
本発明は、ボロン酸エステルおよび酸化合物の合成に関する。さらに詳細には、本発明は、ボロン酸エステル、および酸化合物(ペプチドボロン酸プロテアソームインヒビターボルテゾミブ(bortezomib)を含む)の大規模生成のための改良された合成プロセスを提供する。本明細書に記載されるプロセスは、利用可能な製造能力の大きさによってのみ限定される、大規模の数キログラムの規模でのバッチ生産のために適切である。本発明のプロセスは、α−アミノボロン酸エステルおよび酸化合物を含む、キラルボロン酸エステルおよび酸化合物の合成のために特に有利である。 (もっと読む)
21 - 32 / 32
[ Back to top ]

