Fターム[4C072CC06]の内容
N及び(O又はS)縮合複素環 (24,645) | 縮合環に含まれる異種原子の数 (4,367) | 窒素原子6個以上 (31)
Fターム[4C072CC06]に分類される特許
21 - 31 / 31
光学活性な大環状化合物、その製造法およびその利用
【課題】高い識別能と汎用性に優れた機能を有する光学活性な大環状化合物、その製造法およびその用途を提供する。
【解決手段】環を構成する原子鎖中に、ビナフチルの軸性キラリティーに基づく不斉識別部位と、水素結合供与部位および水素結合受容部位を有する光学活性な大環状化合物。具体的には2つの酸素原子と6つの窒素原子を含む25員環化合物と、2つのピリジン環、2つのナフタレン環及び1つのベンゼン環よりなる縮合環である光学活性な大環状化合物及びその製造方法。
(もっと読む)
アミノチアゾールおよびそれらの使用
本発明は、疾患の処置、予防および/または改善に有用な有機化合物を記載する。 (もっと読む)
治療薬としての縮合四環性mGluR1アンタゴニスト
本発明の多くの実施形態において、本発明は、代謝調節型グルタミン酸レセプター(mGluR)アンタゴニスト、特に選択的代謝調節型グルタミン酸レセプター1アンタゴニストとして有用な式(I)または式(II)(ここで、様々な部分とは、本明細書中に定義されるとおりである)の四環性化合物、その化合物を含む薬学的組成物、ならびに代謝調節型グルタミン酸レセプター(例えば、mGluR1)に関連する疾患(例えば、疼痛、片頭痛、不安、尿失禁およびアルツハイマー病などの神経変性疾患)を処置するためにその化合物および組成物を使用した処置の方法を提供する。 
 (もっと読む)
(もっと読む)
環式アニリノ−ピリジノトリアジン
本発明は式(I)
【化1】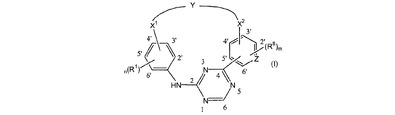
[式中、mは1を表し、nは1を表し、ZはNもしくはC、特にNを表し;−X1−はC1〜4アルキル、特にメチルを表し;−X2−は−C1〜4アルキル−もしくは−C1〜4アルキル−NR7−、特にプロピル、−エチル−NR7−もしくは−プロピル−NR7−を表し;−Y−は−NR2−C1〜6アルキル−CO−NR4−、−Het1−C1〜6アルキル−CO−NR5−もしくは−Het2−CO−NR6−を表し、そしてこここで、−NR2−C1〜6アルキル−CO−NR4−もしくは−Het1−C1〜6アルキル−CO−NR5−の−C1〜6アルキル−リンカーは場合によりヒドロキシ、ハロおよびフェニルから選択される1個または可能な場合には2個もしくはそれ以上の置換基で置換されていてもよく;R1は水素、クロロ、フルオロもしくはブロモを表し;R2は−C1〜4アルキル−、特にエチルもしくはメチルを表し;R7は水素を表し;R8は水素を表し;R4、R5およびR6は水素を表し;Het1はピペラジニルもしくはピペリジニル、特にピペラジニルから選択され;Het2はピロリジニルもしくはピペリジニル、特にピロリジニルから選択され、ここで、該ピロリジニルは場合によりヒドロキシで置換されていてもよい]
の化合物、そのN−オキシド形態、製薬学的に許容しうる付加塩および立体化学的異性体に関する。 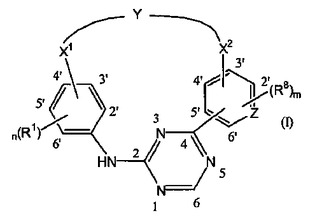 (もっと読む)
(もっと読む)
テロメスタチン誘導体
【課題】
テロメラーゼ阻害活性を有する新規なテロメスタチン誘導体を提供する。
【解決手段】
下記式(I):
[式中、例えば、Rは、水素原子;R1は、水素原子;R2は、水素原子;R3は、水素原子又は保護基;Xは、酸素原子である。]で表される化合物又はその薬学的に許容される塩。
(もっと読む)
抗生物質化合物
Nocardia種による栄養培地の発酵は、構造式(I)の新規な広域抗生物質化合物または医薬的に許容されるその塩、エステル、鏡像異性体、ジアステレオマーまたはそれらの混合物を産生する。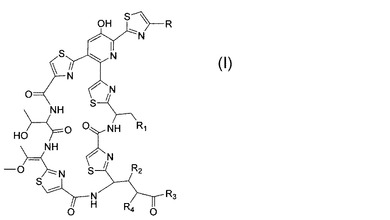
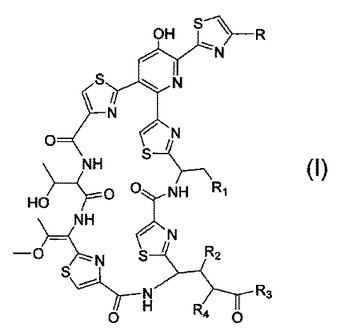 (もっと読む)
(もっと読む)
2,4(4,6)ピリミジン誘導体
本発明は式(I)
【化1】
[式中、Z1及びZ2はNHを表わし、Yは−C3−9アルキル−、−C3−9アルケニル−、−C1−5アルキル−NR6−C1−5アルキル−、−C1−5アルキル−NR7−CO−C1−5アルキル−、−C1−6アルキル−CO−NH−、−C1−6アルキル−NH−CO−、−C1−2アルキル−CO−Het10−CO−、−C1−3アルキル−NH−CO−Het3−、−Het4−C1−3アルキル−CO−NH−C1−3アルキル−、−C1−2アルキル−NH−CO−L1−NH−、−NH−CO−L2−NH−、−C1−2アルキル−CO−NH−L3−CO−、−C1−2アルキル−NH−CO−L1−NH−CO−C1−3アルキル−、−C1−2アルキル−CO−NH−L3−CO−NH−C1−3アルキル−、−C1−2アルキル−NR11−CH2−CO−NH−C1−3アルキル−、Het5−CO−C1−2アルキル−、−C1−5アルキル−CO−NH−C1−3アルキル−CO−NH−、−C1−5アルキル−NR13−CO−C1−3アルキル−NH−、−C1−3アルキル−NH−CO−Het27−CO−又は−C1−3アルキル−CO−Het28−CO−NH−を表わし、X1は直接結合、O、−O−C1−2アルキル−、−CO−C1−2アルキル−、−NR16−C1−2アルキル−、−CO−NR17−、Het23−C1−2アルキル−又はC1−2アルキルを表わし、X2は直接結合、O、−O−C1−2アルキル−、−CO−C1−2アルキル−、−NR18−C1−2アルキル−、−CO−NR19−、Het24−C1−2アルキル−又はC1−2アルキルを表わし、R1及びR5はそれぞれ独立して水素、ハロ、C1−6アルキルオキシ−あるいはHet1又はC1−4アルキルオキシ−で置換されたC1−6アルキルオキシ−を表わし、R2及びR4はそれぞれ独立して水素又はハロを表わし、R3は水素又はシアノを表わし、R6、R7、R13、R17及びR19は水素を表わし、R11は水素又はC1−4アルキルを表わし、R16及びR18は水素、C1−4アルキル又はHet17−C1−4アルキル−を表わし、L1、L2及びL3は、それぞれ独立して、任意にフェニル、メチルスルフィド、シアノ、ポリハロC1−4アルキル−フェニル−、C1−4アルキルオキシ、ピリジニル、モノ−もしくはジ(C1−4アルキル)−アミノ−又はC3−6シクロアルキルから選択される1個又は可能な場合には2個以上の置換基で置換されていてもよいC1−8アルキルを表わし、Het1、Het2、Het17はそれぞれ独立して、モルホリニル、オキサゾリル、イソオキサゾリル又はピペラジニルを表わし、Het3、Het4、Het5はそれぞれ独立してモルホリニル、ピペラジニル、ピペリジニル又はピロリジニルを表わし、Het10はピペラジニル、ピペリジニル、ピロリジニル又はアゼチジニルを表わし、Het22はモルホリニル、オキサゾリル、イソオキサゾリル又はピペラジニルを表わし、ここで該Het22は任意にC1−4アルキルで置換されていてもよく、Het23及びHet24はそれぞれ独立して、ピロリジニル、ピペラジニル又はピペリジニルから選択される複素環を表わし、ここで該Het23又はHet24は任意に、Het22−カルボニルで置換されていてもよく、Het27及びHet28はそれぞれ独立して、モルホリニル、ピペラジニル、ピペリジニル又は
ピロリジニルから選択される複素環を表わす]の化合物、それらのN−オキシド形態物、製薬学的に許容できる付加塩及び立体化学的異性体形態物に関する。  (もっと読む)
(もっと読む)
チアゾール環状多量体、その製造方法、その合成中間体およびその利用
式(I)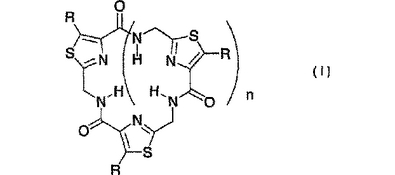
(式中、Rは、それぞれ、独立に、水素原子、置換基を有してもよい低級アルキル基、−CH2SHで表される基、ホルミル基またはカルボキシル基であり、nは1〜4のいずれかの整数である。)で表される新規なチアゾール環状多量体またはその薬理上許容される塩。上記化合物の製造方法および合成中間体、並びに、上記化合物を含有するテロメラーゼ阻害剤および医薬組成物が提供される。本発明の化合物は、テロメラーゼに選択的に作用し(すなわち、テロメラーゼへの阻害作用が大きく、Taq polymeraseや他の逆転写酵素への阻害作用が小さい)、かつ毒性がないあるいは低いので、テロメラーゼに対する選択的阻害剤としての利用価値が高い。 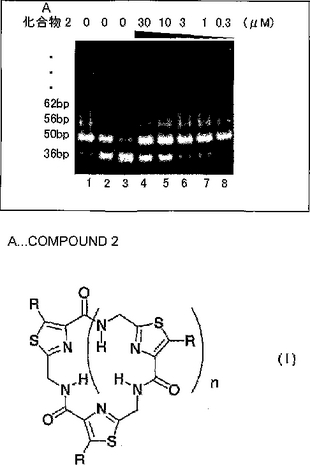 (もっと読む)
(もっと読む)
ベンゾオキサゾール樹脂前駆体、ポリベンゾオキサゾール樹脂、樹脂膜および半導体装置
【課題】 本発明の目的は、樹脂膜とした場合に低誘電率であるベンゾオキサゾール樹脂前駆体を提供することにある。
また、本発明の目的は、耐熱性および弾性率に優れかつ低誘電率である樹脂膜およびそれを用いた半導体装置を提供することにある。
【解決手段】本発明のベンゾオキサゾール樹脂前駆体は、大きい自由体積をもつ化合物を樹脂中に有する。また、本発明のポリベンゾオキサゾール樹脂は、上記に記載のベンゾオキサゾール樹脂前駆体を反応して得られることを特徴とするものである。また、本発明の樹脂膜は、上記に記載のポリベンゾオキサゾール樹脂を含む樹脂組成物で構成される。また、本発明の半導体装置は、上記に記載の樹脂膜を有するものである。
(もっと読む)
抗増殖剤としてのピリド−およびピリミドピリミジン誘導体
本発明は、式(I)
【化1】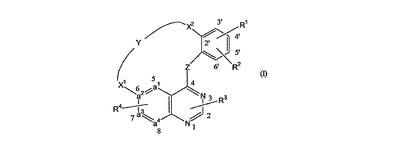
[式中、a1−a2=a3−a4は、N−CH=CH−CH、N−CH=N−CHもしくはCH−CH=N−CHから選択される2価の基を表し;ZはNHを表し;Yは−C3〜9アルキル−、−C1〜5アルキル−NR13−C1〜5アルキル−、−C1〜6アルキル−NH−CO−もしくは−CO−NH−C1〜6アルキル−を表し;X1は−O−もしくは−NR11−を表し;X2は−C1〜2アルキル−、−O−C1〜2アルキル、−O−もしくは−O−CH2−を表し;R1は水素もしくはハロを表し;R2は水素、シアノ、ハロ、ヒドロキシカルボニル−C1〜4アルキルオキシカルボニル−、Het16−カルボニル−もしくはAr5を表し;R3は水素を表し;R4はヒドロキシ、C1〜4アルキルオキシ−、Ar4−C1〜4アルキルオキシを表すか、あるいはR4はC1〜4アルキルオキシ−もしくはHet2−から選択される1個または可能であれば2個もしくはそれ以上の置換基で置換されたC1〜4アルキルオキシを表し;R11は水素を表し;R12は水素、C1〜4アルキル−もしくはC1〜4アルキル−オキシ−カルボニル−を表し;R13はHet14−C1〜4アルキル、特にモルホリニル−C1〜4アルキルを表し;Het2は場合によりC1〜4アルキル、好ましくはメチルで置換されていてもよいモルホリニルもしくはピペリジニルから選択される複素環を表し;Het14はモルホリニルを表し;Het16はモルホリニルもしくはピロリジニルから選択される複素環を表し;Ar4はフェニルを表し;Ar5は場合によりシアノで置換されていてもよいフェニルを表す]
の化合物、そのN−オキシド形態、製薬学的に許容しうる付加塩および立体化学的異性体に関する。 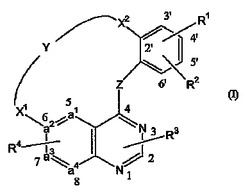 (もっと読む)
(もっと読む)
ククルビットウリルの製造方法
本発明は、ククルビットウリルの製造方法に関する。この方法は、ククルビットウリルを形成するために酸の存在下において、グリコールウリル、グリコールウリル類縁体及び/又はグリコールウリルもしくはグリコールウリル類縁体のオリゴマーから選択される1つ以上の化合物と、2から11の結合されたグリコールウリル又はグリコールウリル類縁体からなるオリゴマーを反応させることを含む。該方法は、ククルビットウリルにおける特定の位置に特定の置換されたユニットを有する可変の置換ククルビットウリルを製造するために使用し得る。本発明はまた、本発明の方法により製造されるククルビットウリルを提供する。本発明はさらに、新規なククルビットウリルを提供する。 (もっと読む)
21 - 31 / 31
[ Back to top ]


