国際特許分類[A61K31/661]の内容
生活必需品 (1,310,238) | 医学または獣医学;衛生学 (978,171) | 医薬用,歯科用又は化粧用製剤 (357,440) | 有機活性成分を含有する医薬品製剤 (142,694) | リン化合物 (1,985) | P−C結合を持たないリン酸またはそのエステル,例.ホスフオサル,ジクロロボス,マラチオン (452)
国際特許分類[A61K31/661]の下位に属する分類
国際特許分類[A61K31/661]に分類される特許
51 - 60 / 363
非放射性リン脂質化合物、組成物、及び使用方法
本発明は、リン脂質エーテル及びアルキルリン脂質化合物、並びにそれらと他の癌治療剤との組合せを提供する。より具体的には、本発明は、ヨウ素の「コールド(cold)」同位体、例えば127I、又はHを有するリン脂質エーテル化合物の、癌の処置のための使用、並びに、放射性(即ち「ホット(hot)」)及び非放射性(即ち「コールド(cold)」)ヨウ素同位体の組合せに関する。 (もっと読む)
水溶性ベンゾアゼピン化合物及び医薬組成物
【課題】本発明の目的は、トルバプタンの水に対する溶解性が向上し、注射剤としての使用に適した新規なベンゾアゼピン化合物を提供することである。
【解決手段】本発明は、下記一般式(1)で表されるベンゾアゼピン化合物またはその塩を提供する。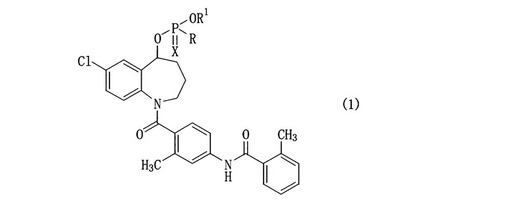
[式中、Rは、水素原子、保護基を有するヒドロキシ基等を示す。R1は、水
素原子またはヒドロキシ保護基を示す。Xは酸素原子または硫黄原子を示す。]
(もっと読む)
カンナビノイド受容体モジュレーター
本発明はカンナビノイドCB2受容体の活性をモジュレートする特定の式Iaの化合物およびその医薬組成物に関する。本発明はさらにCB1受容体およびCB2受容体の両方の活性をモジュレートする特定の式Iaの化合物およびその医薬組成物に関する。本発明の化合物および医薬組成物は、疼痛、例えば、骨および関節疼痛、筋肉疼痛、歯痛、頭痛、炎症性疼痛、神経因性疼痛、治療の有害作用として生じる疼痛ならびに変形性関節症に随伴する疼痛;痛覚過敏;異痛症;炎症性痛覚過敏;神経障害性痛覚過敏;急性侵害受容;骨粗鬆症;多発性硬化症に関連する痙縮;自己免疫障害;アレルギー反応;CNS炎症;アテローム硬化症;望ましくない免疫細胞活性および炎症;加齢性黄斑変性;咳;白血病;リンパ腫;CNS腫瘍;前立腺癌;アルツハイマー病;卒中誘発損傷;認知症;筋萎縮性側索硬化症およびパーキンソン病を治療する際に有用な方法を対象とする。 (もっと読む)
リボフラビンベースのエアロゾル及び臨床試験におけるプラセボとしての使用
個体の第1集団にエアロゾル吸入を介して試験化合物を投与するステップと;個体の第2集団にエアロゾル吸入を介してリボフラビン5’−リン酸から成るプラセボを投与するステップと;前記2つの集団の生物学的マーカーを比較するステップとを具えるエアロゾル化試験化合物の評価方法である。リボフラビン5’−リン酸(フラビンモノヌクレオチドとしても知られている)から成るエアロゾルは臨床試験におけるプラセボ、又は治療的に使用しうる。 (もっと読む)
ジフェニルスルフィド誘導体及びそれらを有効成分とする医薬
【課題】優れたスフィンゴシン−1−リン酸3アンタゴニスト活性を有し、かつ副作用の少ないジフェニルスルフィド誘導体を提供する。
【解決手段】下式(1)で表されるジフェニルスルフィド誘導体若しくは薬理学的に許容されるその塩又はそれらの水和物。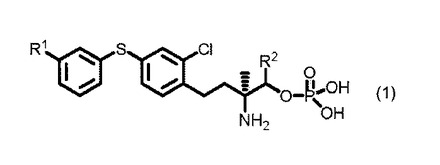
[式中、R1はトリフルオロメチル基、ベンジルオキシ基、炭素数1〜4のアシル基又はシアノ基を示し、R2は水素原子又は炭素数1〜6のアルキル基を示し、ただしR2が水素原子のときは、R1はベンジルオキシ基を除く]
(もっと読む)
脂質付加オキソアデニン誘導体
ホスホ脂質又はホスホノ脂質に共有結合した窒素でへテロシクリル置換されたオキソアデニン分子を含む新規の脂質付加オキソアデニンは、インターフェロンα又はそのほかの免疫賦活性サイトカインの誘導剤であることが示される。該化合物は、免疫賦活剤及びアジュバントとして有用である。 (もっと読む)
重水素化2,4−ピリミジンジアミン化合物およびそのプロドラッグならびにそれらの使用
本開示は、生物学的に活性な、式(1)の重水素化2,4-ピリミジンジアミン化合物およびそのプロドラッグ、重水素化化合物を含む組成物、重水素化化合物を合成するための中間体および方法、ならびに様々な適用における重水素化化合物および組成物の使用法を提供する。
 (もっと読む)
(もっと読む)
末梢静脈投与用輸液製剤
【課題】本発明の目的は、常温下で安定保存可能であって、ビタミンB1やビタミンC等のビタミンの栄養状態が低下することが予想される又は低下している患者の栄養状態を維持・改善でき、更には抗酸化ストレス作用をも有効に発揮でき、安定な末梢静脈投与用輸液製剤を提供することである。
【解決手段】M連通可能な仕切り手段で仕切られた容器に、糖を70〜150g/Lの濃度で含有する輸液(A)と、アミノ酸を50〜150g/Lの濃度で含有する輸液(B)が分別収容され、前記輸液(A)は、亜硫酸塩を含まず、ビタミンB1を含み、前記輸液(A)と輸液(B)のいずれか少なくとも一方にビタミンCを含み、pHが3〜5であり、更に前記輸液(A)と輸液(B)とを混合した混合液において、ビタミンCの濃度が200〜400mg/Lであり、且つビタミンCの1日当たりの投与量が400〜800mgとなるように設定して梢静脈投与用輸液製剤を製造する。
(もっと読む)
後嚢混濁を予防するためのコンブレタスタチン
後嚢混濁の処置および予防のための方法および組成物が提供される。この方法は、後嚢混濁に罹患しているかまたは後嚢混濁を発症するリスクのある被験体に対して、治療上有効な量のコンブレタスタチンを投与することを包含する。特定の実施では、このコンブレタスタチンは、コンブレタスタチンA−4、またはその誘導体、プロドラッグもしくはアナログである。特定の実施では、このコンブレタスタチンは、コンブレタスタチンA−4リン酸塩(CA4P)またはその薬学的に許容され得る塩である。このコンブレタスタチンは全身的に、例えば、静脈内に、または非全身的に、例えば、被験体の眼に対して局所的に投与される。特定の実施では、このコンブレタスタチンは、眼内レンズを挿入するため手術の間に投与され、必要に応じてその後、その被験体の眼に対して同じまたは異なる用量の引き続く投与が全身にまたは局所に行われる。  (もっと読む)
(もっと読む)
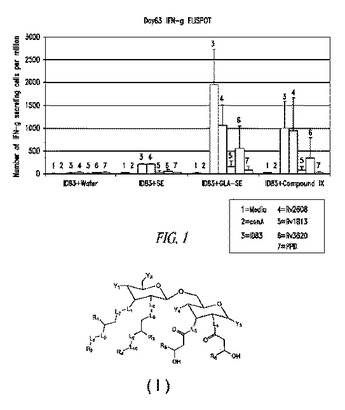
合成グルコピラノシル脂質アジュバント
下記の構造(I)を有する化合物、特にグルコピラノシル脂質アジュバント(GLA)化合物、またはその医薬的に許容し得る塩が提供される(式中、L1、L2、L3、L4、L5、L6、L7、L8、L9、L10、Y1、Y2、Y3、Y4、R1、R2、R3、R4、R5、R6は本明細書で定義する通りである)。免疫反応を誘導または増強するための医薬組成物、ワクチン組成物および関連する方法も提供される。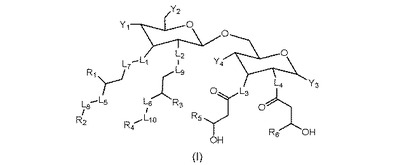
 (もっと読む)
(もっと読む)
51 - 60 / 363
[ Back to top ]

