国際特許分類[C07K1/22]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | ペプチド (29,849) | ペプチドの製造のための一般方法 (1,853) | 抽出;分離;精製 (1,152) | クロマトグラフィーによるもの (651) | アフィニティー・クロマトグラフィー,または選択的吸着プロセスに基づく関連技術 (302)
国際特許分類[C07K1/22]に分類される特許
51 - 60 / 302
多重特異性受容体の精製の改善
一の作用物質と結合する受容体(典型的には、分子インプリントポリマー、MIP)に富み、該受容体の各々が該作用物質上の少なくとも2個所の別個の部位に特異的に結合する、組成物の製造方法であって、受容体の一のサンプルを、作用物質の一の結合部位が受容体と結合するのにアクセスできない作用物質を用いるアフィニティ精製の第一の工程に付し、つづいてその精製された受容体を、作用物質の第二の結合部位がアクセスできない作用物質を用いるアフィニティ精製の少なくとも1つのさらなる工程に付すことで製造される方法を開示する。また、フェニルケトン尿症(PKU、Fφlling病)、高フェニルアラニン血症(HPA)、アルカプトン尿症(黒色尿病)、チロシン血症、高チロシン血症、重症筋無力症、ヒスチジン血症、ウロカニン酸尿症、メープルシロップ尿症(MSUD)、イソ吉草酸血症(イソバレリル−CoAデヒドロゲナーゼ欠損症)、ホモシステイン尿症、プロピオン酸血症、メチルマロン酸血症、グルタル酸尿症1型(GA−1)およびガラクトース血症からなる群より選択される疾患の治療、緩和または予防方法であって、その必要とする患者の胃腸管に、有効量の分子インプリントポリマー(MIP)の組成物を投与することを含み、該組成物が該疾患の病徴誘発物質との結合能を有するところの、方法。 (もっと読む)
2−アシルアミノチアゾール誘導体及びその製造方法
【課題】 タンパク質の分析又は精製のための低分子化合物を提供すること。
【解決手段】 タンパク質の分析又は精製に有用な、一般式(1)
【化1】
(式中、R1及びR2は水素原子又は置換されていてもよい炭素数1から6のアルキル基を表し、R3はヒドロキシ基、ホルミル基、メルカプト基、カルボキシル基、アミノキシ基、アセトキシ基、フタルイミドオキシ基、又は炭素数1から6のアルコキシチオカルボニルチオ基を表し、Arは置換されていてもよい芳香族基を表し、nは1から12の整数を表す。)で表されるチアゾール誘導体を提供するものである。
(もっと読む)
改変されたプロテインA溶離による向上したタンパク質精製
本発明は、ポリペプチドをプロテインAに結合させ、低pHで始まるpH勾配で溶離させることを含む、CH2/CH3領域を含むポリペプチドを精製する方法を提供する。 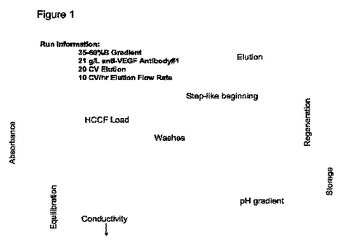 (もっと読む)
(もっと読む)
変異タンパク質の製造方法
【課題】プリオン病の診断又は検査に有効なシステムを提供し、試料中の異常型プリオン蛋白を特異的に除去するツールを提供すること。
【解決手段】H-T-V-T-T-T-T-K-G-E-N-F-T-E-T-D-Xaa(Xaaは、V、I又はMである)で表されるアミノ酸配列からなる保存領域を含むタンパク質の該保存領域において、少なくとも3個のアミノ酸残基に、置換、付加、欠失又はそれらの組み合わせによる変異を導入する工程を含む、変異タンパク質の製造方法。
(もっと読む)
試料中の1つ以上の不純物から標的タンパク質を精製するための方法
本発明は、タンパク質精製の改良された方法に、少なくとも部分的に関する。特に、本発明は、Fc領域含有タンパク質および1つ以上の不純物を含む組成物から、Fc領域含有タンパク質を精製するための方法に、少なくとも部分的に関するものであり、この方法は、集積タンクおよび/またはバッファー交換のステップの必要性を排除する。 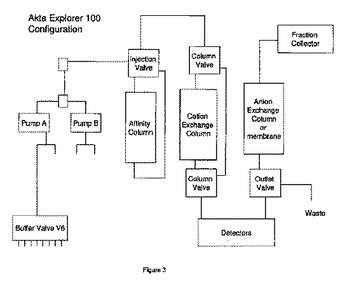 (もっと読む)
(もっと読む)
酵素による抗体処理方法
本発明は、次の工程を含む、所定の糖鎖構造をもつ免疫グロブリンまたは免疫グロブリンフラグメントを生産するための方法を含む:a)免疫グロブリンまたは免疫グロブリンフラグメントを含有するアフィニティークロマトグラフィーカラム溶出液を用意する工程;b)アフィニティークロマトグラフィーカラム溶出液を、植物由来の(α1,3)ガラクトシダーゼ、例えば生コーヒー豆由来の(α1,3)ガラクトシダーゼ(EC 3.2.1.22)とインキュベートする工程;c)インキュベートしたアフィニティークロマトグラフィーカラム溶出液をプロテインAクロマトグラフィー材料にアプライし、かつプロテインAクロマトグラフィー材料から免疫グロブリンまたは免疫グロブリンフラグメントを回収し、それによって所定の糖鎖構造をもつ免疫グロブリンまたは免疫グロブリンフラグメントを生産する工程。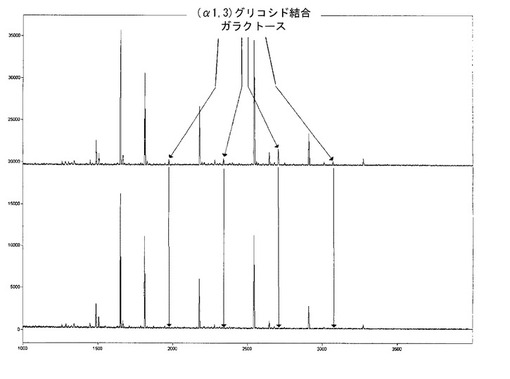
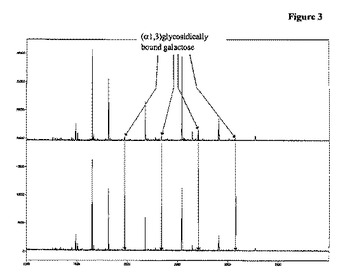 (もっと読む)
(もっと読む)
抗体製造の最適化
例えば特定の収集時点及び/又は特定の精製スキームを選択することにより、例えば治療効果を向上させるために、クロマトグラフィー法による抗体変異体からの抗体分子の分離により精製された抗体を製造するための一般的方法が提供される。よって、本発明は、抗体分子とその変異体を含有する試料を提供し、上記試料の一定分量中における、抗体分子及び/又はその変異体の存在、及び/又は抗体分子とその変異体の量の合計に対する抗体分子とその変異体の量の比を決定し、先に得られたデータに基づいて次の収集時点及び/又は抗体精製スキームを決定する工程を含み、それによって抗体分子とその変異体を含有する抗体組成物を製造する、抗体分子とその変異体を含有する抗体組成物を製造する方法を報告する。 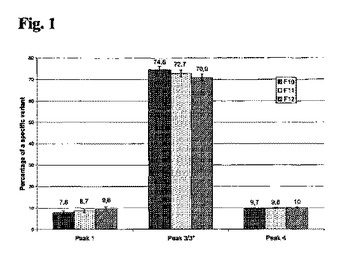 (もっと読む)
(もっと読む)
免疫グロブリンFcポリペプチド
グリコシル化されていない抗体Fcドメインを有しているポリペプチドを含む方法および組成物。特定の実施形態では、ポリペプチドは、天然のFcドメインと比較して1つ以上の置換を含むグリコシル化されていないFcドメインを有する。さらに、いくつかの実施形態では、いくつかのFc受容体に結合するが、他のものには結合しないFcドメインが含まれる。例えば、グリコシル化されたFcドメインの2倍以内のレベルでFcγRIに選択的に結合するが、他のFc受容体に対する結合については有意には減少させられたグリコシル化されていないFcドメインを持つポリペプチドが提供される。さらに、修飾されたグリコシル化されていないFcドメインと第2の非Fc結合ドメイン(これは、抗体の抗原結合領域または非抗原結合領域であり得る)を有しているポリペプチドを使用して抗体依存性細胞媒介性細胞傷害性を促進するための方法および組成物が提供される。  (もっと読む)
(もっと読む)
抗原ペプチドの同定法
【課題】本発明は、抗原ペプチドの同定法を提供することを課題とする。
【解決手段】本発明は、哺乳類生物体由来の限定量の細胞または体液から、それらの配列および同一性を決定するのに十分な量の抗原ペプチドを単離するのに有用な方法を提供する。従って本発明は、診断または治療の目的で利用される新規の疾患関連抗原、例えば腫瘍抗原および自己免疫疾患関連抗原を同定する方法を提供する。本発明の方法を、ワクチンの品質を管理するために利用することもできる。より具体的には、本発明の方法を、生体の最も重要な抗原提示細胞およびワクチン接種用の有用な道具である樹状細胞のペプチド受容体を介して提示された抗原ペプチドの配列を決定するために使用することができる。
(もっと読む)
タンパク質精製方法
【課題】より簡単な方法で、DNA夾雑物やウイルスといった不純物を確実に除去でき、しかも生理活性タンパク質の損失が少なく、かつ実施コストの低い生理活性タンパク質、特に抗体の精製方法を提供する。
【解決手段】以下の段階:
1)生理活性タンパク質含有試料を、該生理活性タンパク質の等電点よりも低いpHの低伝導度水溶液状態とし、
2)生じる粒子を除去する、
を含む、生理活性タンパク質含有試料中の不純物を除去する方法。
(もっと読む)
51 - 60 / 302
[ Back to top ]

