国際特許分類[C07C255/56]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | 非環式化合物または炭素環式化合物 (64,036) | カルボン酸ニトリル (1,628) | シアノ基が,炭素骨格の6員芳香環の炭素原子に結合しているもの (653) | シアノ基と,炭素骨格に結合している二重結合の酸素原子とを含有するもの (32)
国際特許分類[C07C255/56]に分類される特許
21 - 30 / 32
スフィンゴシンキナーゼ阻害剤
本発明は、式(I)の置換アダマンタン化合物、その医薬組成物、それらの製造方法ならびにスフィンゴシンキナーゼの阻害方法および過剰増殖性疾患、炎症性疾患または血管新生性疾患の治療方法または予防方法に関する。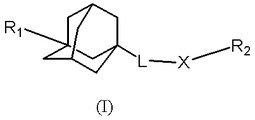
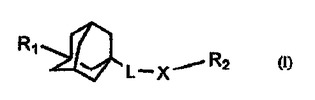 (もっと読む)
(もっと読む)
新規な化合物
式I:
【化1】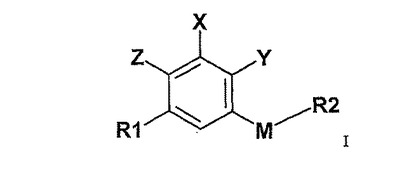
[式中、Xは水素、ハロ、-CN、-CONH2、-CON(C1-6アルキル)H、-CON(C1-6アルキル)2及び複素環式基から選択され;R1はC1-6アルキル及びC3-6シクロアルキルから選択され;ここで、Yが-C1-6アルキルである場合、Zは-OHであり、Mは-C(O)-、-CH(ORa)-、-N(Ra)-及び-S(O)r-から選択され、ここでRaは水素又はC1-6アルキルであり、そしてrは0、1又は2であり、R2はC1-6アルキル、C3-6シクロアルキル、ヘテロシクロアルキル、アリール、アルキルアリール及びヘテロアリールから選択され、R2はハロ、-NO2、-CN、-OH、-CF3、-OCF3、-NH2及び/又は-CONH2で置換され;又は、Yが-C1-6アルコキシである場合、Zは-C1-6アルコキシであり、Mは単結合であり、R2はC1-6アルキル、C3-6シクロアルキル、ヘテロシクロアルキル、アリール、アルキルアリール及びヘテロアリールから選択される]の化合物、又はその医薬として許容し得る塩。 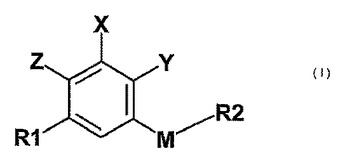 (もっと読む)
(もっと読む)
触媒組成物及びそれを用いたクロスカップリング化合物の製造方法
【課題】有機合成上非常に重要な反応技術であるクロスカップリング反応用に極めて高活性な触媒組成物を提供する。
【解決手段】下記式で示されるニッケル塩とアミン化合物との錯体及びトリフェニルホスフィンからなる触媒組成物の存在下にクロスカップリング反応させる。
(R1〜R4はアルキル基、アリール基、ヘテロアリール基、またはアルケニル基、nは1〜6の整数、Xはハロゲン、水酸基、硝酸基または酢酸基を表わす。)
(もっと読む)
グルタミン酸受容体の増強剤
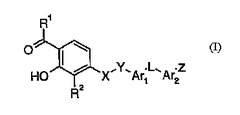
本発明は、式Iの化合物、その医薬組成物、並びにその使用方法、及びその調製方法、更にはその化合物の中間体を提供する。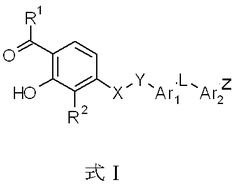
 (もっと読む)
(もっと読む)
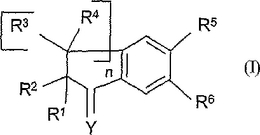
インデノンカルボン酸誘導体ならびに糖尿病および脂質代謝異常を治療および予防するためのそれらの使用
本発明は、脂質代謝異常、アテローム性動脈硬化症、および糖尿病の治療に用いることのできる、式(I)の化合物に関し、式中、nは、1、2、および3から選択された整数であり、Yは、O、R9がHまたは飽和炭化水素ベース脂肪族基を表すN−OR9、R10およびR11が同一でも異なっていてもよく、Hまたは飽和炭化水素ベース脂肪族基を表すCR10R11を表し、R1およびR2は、同一でも異なっていてもよく、Hまたは飽和脂肪族炭化水素ベース鎖を表すか、あるいはR1およびR2は合わせて、場合によって置換された飽和脂肪族炭化水素ベース鎖を形成し、基R3およびR4は、同一でも異なっていてもよく、R1およびR2に関して上述した任意の意味を持つか、あるいはR1およびCR1R2への炭素アルファに結合する基R4は、何も表さず、二重結合が、CR1R2炭素をアルファCR3R4炭素と結合するか、あるいは基R1およびR2の1つは、基R3およびR4の1つと共に、場合によって置換された飽和または不飽和脂肪族炭化水素ベース鎖を形成し、基R5およびR6の1つはWを表し、他方はZを表し、Zは、飽和または不飽和脂肪族炭化水素ベース基、場合によって置換された飽和、不飽和、および/または芳香族炭素環または複素環基、alkがアルキレン鎖を表し、Cyが場合によって置換された飽和、不飽和、および/または芳香族複素環または炭素環基を表す基−alk−Cyから選択され、Wは、−XL−CO2R7、−X−L−Tetを表し、式中、XおよびLは、下に定義するとおりであり、Tetは、場合によって置換されたテトラゾールを表し、式中、Lは、場合によって置換されている、および/または場合によって置換されたアリーレンによって場合によって中断されている飽和または不飽和脂肪族炭化水素ベース鎖を表し、Xは、O、R8がH、飽和脂肪族炭化水素ベース基、R’がR7に関して下に示すHを除く任意の意味を持つ基−CO−R’もしくは−SO2−R’、または場合によって置換された芳香族炭素環基を表すNR8、あるいはmが0、1、および2から選択されるS(O)mを表し、R7は、H、飽和または不飽和脂肪族炭化水素ベース基、場合によって置換された飽和、不飽和、および/または芳香族炭素環基、場合によって置換された飽和、不飽和、および/または芳香族複素環基を表す化合物、ならびに薬剤として許容されるそれらの誘導体、塩、溶媒和物、および立体異性体、ならびにあらゆる割合のそれらの混合物に関する。
【化1】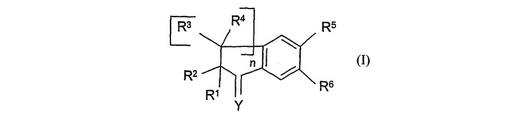
 (もっと読む)
(もっと読む)
鉄またはコバルト触媒によるアリール、アルケンおよびアルキンと銅試薬との炭素−炭素カップリング反応
本発明は、アリール、ヘテロアリール、アルケンまたはアルキンの銅化合物と、適当な離脱基を有するアリール、ヘテロアリール、アルケンまたはアルキン化合物とから出発する炭素−炭素結合形成法に関する。銅化合物は、とりわけ、グリニャールまたはリチウム化合物からのトランスメタル化反応により生成し得る。ハロゲン置換アリール化合物を用いたこれらの化合物のクロスカップリングは、鉄またはコバルト触媒と、適当な溶媒および適当な添加物とを用いて実施する。 (もっと読む)
α、β‐不飽和カルボニル化合物の水素化法
α、β‐不飽和カルボニル化合物の化学選択的水素化法を開示する。一般式(I)(式中、R1は、H、1〜30個の炭素原子を含み、かつ適当な置換基を含んでもよく、前記炭素鎖中に1若しくは2以上のヘテロ原子を含んでもよい分岐若しくは非分岐鎖であり飽和若しくは不飽和の炭化水素ラジカル、または適当な置換基を含んでもよいアリール基若しくはヘテロアリール基を表す。R2、R3、R4はそれぞれ独立に、H、F、Cl、Br、I、OH、CN、NO2、NO、SO2、SO3、アミノ、モノ‐若しくはジ‐(C1‐C24‐アルキル)‐置換アミノ、モノ‐若しくはジ‐(C5‐C20‐アリール)‐置換アミノ、イミノ、ホスホノ、ホスホナト、ホスフィナト、ホスホ、ホスフィノ、1〜30個の炭素原子を含み、かつ適当な置換基を含んでもよく、前記炭素鎖中に1若しくは2以上のヘテロ原子を含んでもよい分岐もしくは非分岐鎖であり飽和若しくは不飽和の炭化水素ラジカル、または適当な置換基を含んでもよいアリール基若しくはヘテロアリール基を表す。R2、R3、R4は、それぞれ芳香族化合物、脂環式化合物、複素環式芳香族化合物、複素環式脂環式化合物である5員環若しくは6員環または縮合5員環及び/若しくは6員環であってもよく、最大4つまでの置換基を有していてもよい。)の化合物が、水素化物供与体と反応して、一般式(II)(一般式中、R1、R2、R3、R4は、それぞれ上記において定義したものである。)の化合物となる。上記方法により、金属触媒を使うことなく、α、β‐不飽和アルデヒド及びケトンの選択的水素化が可能となる。 (もっと読む)
3−ホルミル−5−トリフルオロメチルベンゾニトリル誘導体とその製造方法
【課題】 医・農薬中間体、溶剤として有用な3−ホルミル−5−トリフルオロメチルベンゾニトリル誘導体を工業的規模で製造する方法を提供する。
【解決手段】3−ジハロゲノメチルベンゾトリフルオリドを臭素化して1−ブロモ−3−ジハロゲノメチルベンゾトリフルオリドを得る。次いでこれを加水分解して、1−ブロモ−3−ホルミル−5−トリフルオロメチルベンゼンを得る。次いでこれをオキシム化し脱水して3−ブロモ−5−トリフルオロメチルベンゾニトリルを得る。次いでこれを3−トリフルオロメチル−5−シアノフェニルマグネシウムハライドに変換した後、ホルミル化して3−ホルミル−5−トリフルオロメチルベンゾニトリルを得る。次いでこれを還元して3−ヒドロキシメチル−5−トリフルオロメチルベンゾニトリルを得る。最後にこれを臭素化して3−ブロモメチル−5−トリフルオロメチルベンゾニトリルを得る。
(もっと読む)
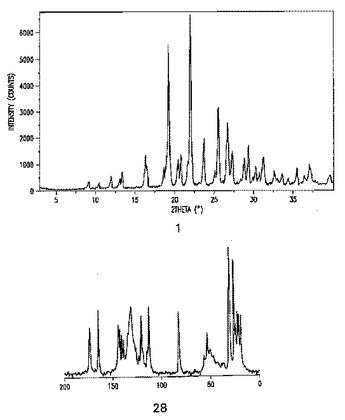
四置換エナミドの形成およびこの立体選択的還元
本発明は、以下に示すように、第1級アミド(IV)と構造式(III)の化合物とをパラジウムで触媒してカップリングさせることにより、エナミド(II)を調製するための実用的な方法を対象とし、加えてこの方法により生成される化合物の結晶形態、特に無水結晶形態、形態B、ならびにタイプ1、タイプ2、およびタイプ3の3種類に分類される結晶性溶媒和物、ならびにこの方法において生成される結晶性中間化合物を対象とする。さらに、本発明は、四置換エナミド(II)を、対応するアミド(I)へ立体選択的還元することに関する。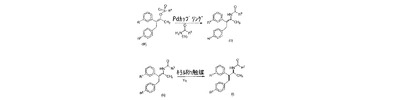
 (もっと読む)
(もっと読む)
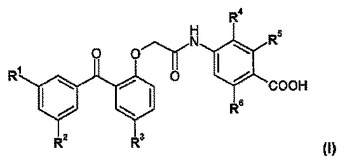
非ヌクレオシド系逆転写酵素阻害剤である安息香酸誘導体
式(I)の化合物:式中、R1、R2、R3、R4、R5及びR6は、本件明細書において定義されるようなものである。化合物は、HIVに対する逆転写酵素阻害剤として有用である。特に、化合物は、HIVの野生型及び単一又は二重突然変異体菌株に対して活性である。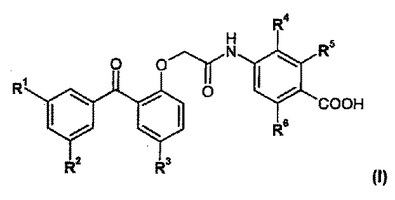
 (もっと読む)
(もっと読む)
21 - 30 / 32
[ Back to top ]