国際特許分類[C07C51/367]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | 非環式化合物または炭素環式化合物 (64,036) | カルボン酸またはその塩,酸ハロゲン化物または酸無水物の製造 (2,554) | カルボキシル基の生成を伴わない反応によるもの (314) | 単結合の酸素を含有する官能基の導入によるもの (74)
国際特許分類[C07C51/367]に分類される特許
51 - 60 / 74
6,6’−(アルキレンジオキシ)ジ−2−ナフトエ酸の製造法
【課題】本発明は縮合重合体の原料である6,6’−(アルキレンジオキシ)ジ−2−ナフトエ酸の製造方法および精製方法を提供する。
【解決手段】1)カリウムイオンを含む水溶液の存在下、2−ヒドロキシ−6−ナフトエ酸とジハロゲン化物とを反応させて粗6,6’−(アルキレンジオキシ)ジ−2−ナフトエ酸カリウム塩を得て、2)水に懸濁し80℃〜300℃にて反応させ(あるいは酸析してから)、3)得られた反応混合物を固液分離する6,6’−(アルキレンジオキシ)ジ−2−ナフトエ酸の製造方法。
(もっと読む)
ヒドロキシ芳香族樹脂の調製方法、ヒドロキシ芳香族樹脂、およびその変性
本発明は、ヒドロキシ芳香族化合物およびグリオキシル酸を合一して反応させることによって調製されるヒドロキシ芳香族樹脂に関する。さらに本発明は、この樹脂の接着剤、積層板、および塗料における使用に関する。 (もっと読む)
置換アリールシクロアルカノール誘導体を調製するためのプロセス
置換アリールシクロアルカノール誘導体、特に以下の一般式: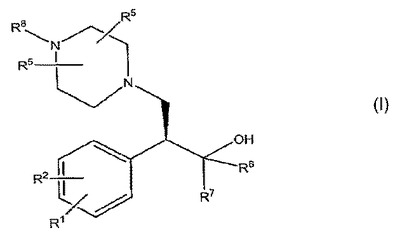
のキラル置換アリールシクロアルカノール誘導体を調製するプロセスを開示する。本発明の置換アリールシクロアルカノール誘導体は、血管運動症状(VMS)、性機能障害、胃腸および尿生殖器疾患、慢性疲労症候群、線維筋痛症候群、神経系疾患、およびこれらの組み合わせを含めたモノアミン再取り込みによって改善される病態、特に、大抑鬱性障害、血管運動症状、ストレス性および切迫性尿失禁、線維筋痛、疼痛、糖尿病性神経障害、およびこれらの組み合わせからなる群から選択される病態の予防および治療のために、単独でまたは組成物中で有用である。 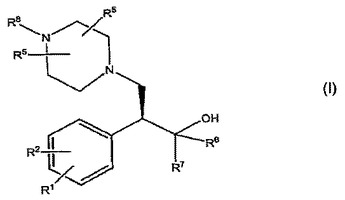 (もっと読む)
(もっと読む)
9−クロロ−15−デオキシプロスタグランジン誘導体類、それらの調製方法及び薬剤としてのそれらの使用
本発明は、受精能問題の処理のために好都合である、一般式(I)の9−クロロプロスタグランジン誘導体に関する。 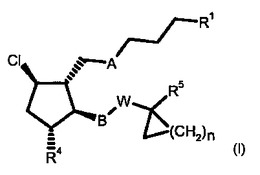 (もっと読む)
(もっと読む)
不飽和脂肪族ヒドロキシ酸の新規な製造方法
本発明は、式(I)[式中、R3およびR1は特にHを表し、nは4より大きい]の化合物の製造方法であって、ホスホン酸塩とラクトールとのWitting−Horner反応を行い、ヒドロキシエステルを得、必要に応じてこのヒドロキシエステルのケン化反応させることを含んでなるに関する。
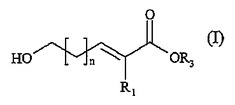 (もっと読む)
(もっと読む)
フェニレンジオキシ二酢酸の製造方法及びその使用
フェニレンジオキシ二酢酸の製造工程は:(a)反応条件下、ハロ酢酸を添加しない溶液中で、ジヒドロキシベンゼンをハロ酢酸塩と接触させてフェニレンジオキシ二酢酸を製造すること;及び(b)任意にフェニレンジオキシ二酢酸塩を、遊離フェニレンジオキシ二酢酸へと変換すること;を含む。いくつかの実施態様において、1,3−フェニレンジオキシ二酢酸(RDOA)を、約7〜約11の範囲のpHを有する反応混合物中、約70℃〜105℃の温度で、レゾルシノールをクロロ酢酸ナトリウムと反応させることで製造する。該反応条件を調整することにより、相対的に高収率の1,3−フェニレンジオキシ二酢酸(すなわち、80%よりも高い)が得られる。精製した酸は、ポリエチレンテレフタレートなどのポリエステル合成に使用できる。 (もっと読む)
ヒドロキシカルボン酸の製造方法
【課題】アミノ酸とヒドロキシカルボン酸との間の無触媒変換反応を提供する。
【解決手段】350−400℃、22.1−40MPaの高温高圧水を反応媒体とする反応場において、3秒以下の反応時間で、アミノ酸と対応するヒドロキシカルボン酸との間の変換反応を光学活性を維持して可逆的に行うことを可能とする光学活性アミノ酸又はヒドロキシカルボン酸の変換方法。
【効果】L−又はD−アミノ酸を無触媒で光学活性を維持して対応するヒドロキシカルボン酸に変換することができる。
(もっと読む)
アダマンタン誘導体の調製方法
本発明は、一般式(1)
【化1】
を有する3−ヒドロキシアダマンタングリオキシル酸或いはその誘導体又は塩の調製方法に関する。当該方法において、式(2):
【化2】
(式中、Rは、C1〜C5ヒドロカルビル、CH2OH、CHO又はCOOHである)を有するアダマンタンの1−アシル誘導体は、3−ヒドロキシアダマンタングリオキシル酸(1)或いはその誘導体又は塩を導く酸化条件下で酸化剤と接触する。 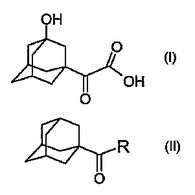 (もっと読む)
(もっと読む)
ジホスフィン類及び金属錯体
式(I)又は(I’)[式中、基R1は、それぞれ相互に独立に、水素原子又はC1−C4−アルキルであり、かつR’1は、C1−C4−アルキルであり;X1及びX2は、それぞれ相互に独立に、sec−ホスフィノ基であり;R2は、水素、R01R02R03Si−;ハロゲン−、ヒドロキシル−、C1−C8−アルコキシ−若しくはR04R05N−置換C1−C18−アシルであるか;又はR06−X01−C(O)−であり;R01、R02及びR03は、それぞれ相互に独立に、C1−C12−アルキル;非置換又はC1−C4−アルキル−若しくはC1−C4−アルコキシ−置換のC6−C10−アリール又はC7−C12−アラルキルであり;R04及びR05は、それぞれ相互に独立に、水素、C1−C12−アルキル、C3−C8−シクロアルキル、C6−C10−アリール又はC7−C12−アラルキルであるか、あるいはR04及びR05は、一緒になってトリメチレン、テトラメチレン、ペンタメチレン又は3−オキサペンチレンであり;R06は、C1−C18−アルキル;非置換又はC1−C4−アルキル−若しくはC1−C4−アルコキシ−置換のC3−C8−シクロアルキル、C6−C10−アリール又はC7−C12−アラルキルであり;X01は、−O−又は−NH−であり;Tは、C結合C3−C20−ヘテロアリーレンであり;vは、0又は1〜4の整数であり;ヘテロアリーレンのヘテロ環中のX1は、T−C*結合に対してオルト位に結合しており;そして*は、ラセミ体若しくはエナンチオマーとして純粋なジアステレオマーの混合物、又は純粋なラセミ体若しくはエナンチオマーとして純粋なジアステレオマーを示す]で示される化合物。本化合物は、プロキラル有機化合物の水素化用のエナンチオ選択性触媒として優れた金属錯体のキラル配位子である。 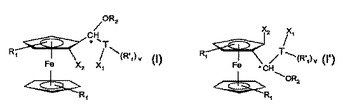 (もっと読む)
(もっと読む)
カルボン酸の合成方法
【課題】 高純度で所望の化合物を得ることができ、使用する溶媒を適切に選択することで、後処理も容易な生産適性の高いカルボン酸の合成方法を提供すること。
【解決手段】 下記一般式(I)に表されるカルボン酸の合成方法において、対応するフェノール類またはチオフェノール類、4−ブチロラクトン、反応溶媒及び塩基を反応容器に順次加え、100℃以上150℃未満の反応温度で反応させることを特徴とするカルボン酸の合成方法。
【化1】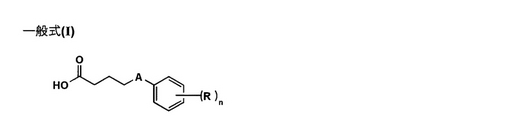
(一般式(I)において、Rは水素原子または置換基を表す。nは1から5の整数を表す。AはOまたはSを表す。)
(もっと読む)
51 - 60 / 74
[ Back to top ]


