国際特許分類[C07K14/605]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | ペプチド (29,849) | 21個以上のアミノ酸を含有するペプチド;ガストリン;ソマトスタチン;メラノトロピン;その誘導体 (11,573) | 動物から;ヒトから (7,664) | ホルモン (776) | グルカゴン (148)
国際特許分類[C07K14/605]に分類される特許
51 - 60 / 148
グルカゴン/GLP−1受容体コアゴニスト
グルカゴン受容体に対する効力が天然グルカゴンよりも強化された、修飾グルカゴンペプチドが開示される。ラクタム架橋の形成、またはアミド基による末端カルボン酸の置換により、該グルカゴンペプチドを更に修飾することによって、グルカゴン/GLP−1受容体コアゴニスト活性を示すペプチドが生産される。これらの高効力グルカゴン類縁体の溶解性および安定性は、該ポリペプチドを、ペグ化、アシル化、アルキル化、カルボキシ末端アミノ酸の置換、C末端切断、又は、配列番号26(GPSSGAPPPS)、配列番号27(K−RNRNNIA)、及び配列番号28(KRNR)から成る群から選ばれるカルボキシ末端ペプチドの付加、によって修飾することで、更に向上させることがでっきる。  (もっと読む)
(もっと読む)
癌の抑制
本発明は、癌の抑制または治療方法、特に、結腸直腸癌、乳癌、前立腺癌および/または肺癌の1またはそれ以上の抑制または治療方法に関する。療法は非細胞毒性プロテアーゼの使用を用い、これは、下垂体細胞などの成長ホルモン分泌細胞に標的される。そうして送達されると、プロテアーゼはインターナリゼーションされ、そしてこの細胞からの成長ホルモンの分泌/伝達を阻害する。本発明はまた、この方法に使用するポリペプチドおよび核酸に関する。 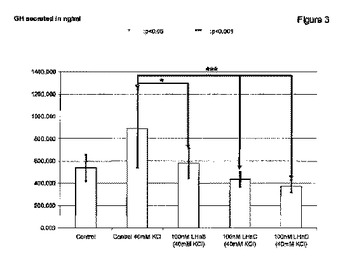 (もっと読む)
(もっと読む)
摂食行動の修正
【課題】対象におけるカロリー摂取、食物摂取、および食欲を低下させる方法が開示される。
【解決手段】方法は、PYYまたはそのアゴニストと、GLP−1またはそのアゴニストとを同時にまたは逐次に、対象に末梢的に投与し、それによって、対象のカロリー摂取を低下させることを含む。
(もっと読む)
胃腸管上部の機能を強化する方法
【課題】グルカゴン関連ペプチドを食道および胃を含む胃腸管上部にかかわる障害を予防または治療するために配合した組成物を提供する。
【解決手段】GLP-2受容体アゴニストおよび1種類以上のペプチドホルモンの血清レベルを増加させるように哺乳動物の胃腸管上部組織の増殖を促進するための組成物であって、有効成分として該アゴニストおよびペプチドホルモンを含み、該アゴニストはGLP-2またはGLP-2類似体であり、かつ該ペプチドホルモンは、IGF-1、IGF-1類似体、IGF-2、IGF-2類似体、GHおよびGH類似体の中から選択される組成物。
(もっと読む)
固相合成法により調製されたペプチドの精製
本発明は、固相ペプチド合成法により調製されたペプチドを精製するための効率的な方法に関する。また、本発明は、前記方法用の試薬を含むキット、及び前記方法により得られた精製ペプチドも含む。 (もっと読む)
過剰体重を防止または治療するためのオキシンソモジュリン
【課題】哺乳動物における過剰体重の防止または治療に使用するための組成物および方法を提供する。
【解決手段】組成物は、食物摂取を低減するのが示されるオキシントモジュリンを含む。
(もっと読む)
エステルに基づいたペプチドプロドラッグ
生体活性ポリペプチドのプロドラッグ製剤が提供され、ここで生体活性ポリペプチドは、ジペプチドの、エステル結合を介した生体活性ポリペプチドへの結合により修飾されている。本明細書に開示されているプロドラッグは、幾つかの実施態様において、少なくとも1.5時間(例えば、少なくとも10時間)、より典型的には20時間を超えて70時間未満の延長された半減期を有し、化学不安定性により駆動される非酵素反応により、生理学的条件下で活性形態に変換される。 (もっと読む)
GLP−1アナログの半組換え調製
組換え発現技術と化学的ペプチド合成法を組み合わせた非タンパク新生アミノ酸をN末端部に有するGLP−1アナログ及び誘導体の生産の半組換え方法が開示される。 (もっと読む)
固相及び溶液相の組み合わせ技術を使用したインシュリン分泌性ペプチド合成
本発明は、固相及び溶液相(「ハイブリッド」)アプローチを使用して合成されるインシュリン分泌性ペプチドの調製に関する。一般的に、アプローチは、固相化学を使用して3つの異なるペプチド中間体フラグメントを合成することを含む。溶液相化学を次に使用して、追加のアミノ酸材料を第3のフラグメントに加えて、それを次に第2のフラグメントに、そして次に第1のフラグメントに溶液中で結合させる。あるいは、異なる第2のフラグメントを、第1のフラグメントに固相中で結合させる。次に、溶液相化学を次に使用して、追加のアミノ酸材料を異なる第3のフラグメントに加える。後に、この異なる第3のフラグメントを、結合した第1の及び異なる第2のフラグメントに溶液相中で結合させる。フラグメントの1つにおける疑似プロリンの使用によって、そのフラグメントの固相合成が容易になり、また、このフラグメントの他のフラグメントへの後の溶液相結合が容易になる。本発明は、インシュリン分泌性ペプチド、例えばGLP−1(7−36)並びにその天然及び非天然対応物などを形成するために非常に有用である。 (もっと読む)
グルカゴンアンタゴニスト及びGLP−1アゴニスト活性を示す化合物
グルカゴンアンタゴニストとGLP−1アゴニストの両方の活性を示すグルカゴン類縁体が開示される。一つの実施態様において、グルカゴンアンタゴニスト/GLP−1アゴニストは、修飾された天然グルカゴンのアミノ酸配列を含み、ここで、天然グルカゴンの最初の1〜5個のN末端アミノ酸が欠失しており、アルファ−へリックスが安定化されている。 (もっと読む)
51 - 60 / 148
[ Back to top ]