国際特許分類[C12N9/80]の内容
化学;冶金 (1,075,549) | 生化学;ビール;酒精;ぶどう酒;酢;微生物学;酵素学;突然変異または遺伝子工学 (115,607) | 微生物または酵素;その組成物 (68,222) | 酵素,例.リガーゼ;酵素の調製,活性化,阻害,分離または精製方法 (6,067) | 加水分解酵素 (2,152) | ペプチド結合以外のC―N結合に作用するもの (106) | 鎖状アミドのアミド結合に作用するもの (47)
国際特許分類[C12N9/80]の下位に属する分類
アスパラギナーゼ (9)
ペニシリンアミダーゼ
国際特許分類[C12N9/80]に分類される特許
21 - 30 / 38
脂肪酸アミドヒドロラーゼのインヒビター
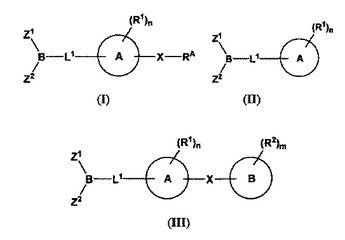
本発明は、式(I)、(II)、または(III)を含む、化合物およびその薬学的組成物を提供する。本発明はまた、治療有効量の式(I)、(II)、または(III)の化合物またはその薬学的組成物を、FAAH媒介性の疾患、障害、または容態の治療を必要とする患者に投与することによる上記疾患、障害、または容態を治療する方法を提供する。さらに、本発明は、治療有効量の式(I)、(II)、または(III)の化合物またはその薬学的組成物を、FAAHの阻害を必要とする患者に投与することによるFAAHを阻害する方法を提供する。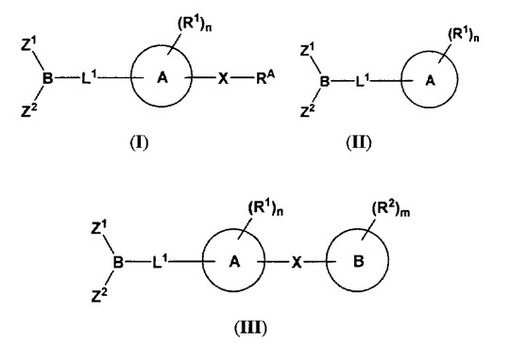
 (もっと読む)
(もっと読む)
ヘリコバクター感染に対する免疫原性組成物、該組成物に用いられるポリぺプチドおよび該ポリぺプチドをコードする核酸配列
【課題】ヘリコバクター感染に対する防御抗体を誘発することが可能な免疫原性組成物の提供。
【解決手段】i) ヘリコバクター・ピロリ由来のウレアーゼ構造ポリぺプチドの少なくとも1つのサブユニット、もしくはヘリコバクター・フェリスウレアーゼと反応する抗体によって認識されるそれらの断片、および/またはヘリコバクター・フェリス由来のウレアーゼ構造ポリぺプチドの少なくとも1つのサブユニット、もしくはヘリコバクター・ピロリウレアーゼと反応する抗体によって認識されるそれらの断片、ii)および/またはヘリコバクター由来の熱ショック蛋白質(HSP)。すなわちシャペロニン、もしくは該蛋白質の断片を包含する免疫原性組成物。この免疫原性組成物の組換え手段による調製。
(もっと読む)
D−アミノ酸の製造方法
【課題】本発明は、従来法より効率的なD−アミノ酸の製造方法の提供を課題とする。
【解決手段】また、N−サクシニルアミノ酸を原料として、D−アミノ酸を酵素的に製造する方法を提供する。N−アシルアミノ酸ラセマーゼを用いてN−サクシニルアミノ酸をラセミ化する反応、およびD−アミノアシラーゼによるD体特異的加水分解反応を組合せることにより、医薬品原料などとして有用なD−アミノ酸を効率的に得ることができる。
(もっと読む)
N−アセチル−(R,S)−β−アミノ酸アシラーゼ遺伝子
【課題】 N−アセチル−(R,S)−β−アミノ酸アシラーゼの遺伝子を単離同定し、大腸菌のような宿主を用いて、これら遺伝子を高発現する系を構築するために、これらの酵素を菌体から単離精製し、該酵素をコードする遺伝子の塩基配列を決定すること。
【解決手段】Burkholderia sp. AJ 110349が産生するN−アセチル−(R)−β−アミノ酸アシラーゼ、及び、該酵素をコードする遺伝子、;Burkholderia sp. AJ 110349が産生するN−アセチル−(S)−β−アミノ酸アシラーゼ、及び、該酵素をコードする遺伝子;又は、Variovorax sp. AJ 110348が産生するN−アセチル−(R)−β−アミノ酸アシラーゼ、及び、該酵素をコードする遺伝子。
(もっと読む)
ペプチジルアルギニンデイミナーゼ、およびシトルリン化タンパク質およびペプチド生成におけるその使用
本出願は、ジベレラ・ゼアエ(Gibberella zeae)(フザリウム・グラミネアルム(Fusarium graminearum)とも称される)からのペプチジルアルギニンデイミナーゼ酵素(EC3.5.3.15)の単離に関する。本出願は、前記アルギニンデイミナーゼを使用して酵素的に生成されたシトルリン化タンパク質およびペプチド、およびこのようなシトルリン化タンパク質およびペプチドの食材中での使用を開示する。本発明は、タンパク質、ペプチドまたはタンパク質加水分解産物中に元々存在するアルギニン残基の少なくとも15%、好ましくは少なくとも30%、より好ましくは少なくとも45%、なおもより好ましくは少なくとも60%、最も好ましくは少なくとも80%がシトルリン残基に転換された、修飾タンパク質、ペプチドまたはタンパク質加水分解産物に関する。 (もっと読む)
ファージに由来する抗微生物活性
本発明は、感染症を含む微生物コロニーの増殖を減少させるための方法および組成物を提供し、かつ、治療的組成物、感染症を治療するための方法、およびその他のそのような組成物を同定するための方法を含む。
 (もっと読む)
(もっと読む)
ヒストンデアセチラーゼ1/2選択的インヒビターアッセイ
本発明は、(i)HDAC1および/または2酵素を、MTA−2、MTA−1、MTA−3のようなMTAタンパク質中に見出されまたCoREST、CoREST2、CoREST3およびMI−ER1中にも見出されるSANTおよびELM2領域を含有するタンパク質と共に、適当なアッセイバッファ中でインキュベートする段階と、(ii)有望なHDACインヒビターおよび適当な基質を添加してインキュベートする段階と、(iii)インキュベーションを中止し、推定HDACインヒビターが酵素活性に与えた効果を標準との比較によって定量する段階と、を含むヒストンデアセチラーゼHDAC1および/または2インヒビター特異的アッセイに関する。 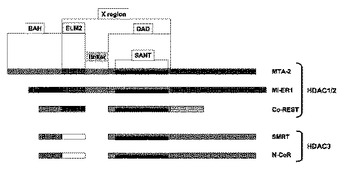 (もっと読む)
(もっと読む)
ノルボルナン誘導体の加水分解に関与するDNA
【課題】(S)-2-エキソ-アセトアミドノルボルナンのアセトアミド加水分解酵素をコードするDNAおよび光学活性2-エキソ-アセトアミドノルボルナンの新規な製造方法の提供。
【解決手段】(S)-2-エキソ-アセトアミドノルボルナンのアセトアミド基を加水分解し、(S)-2-エキソ-アミノノルボルナンへ変換する能力を有するタンパク質を一部にまたは全体としてコードするDNA、コリネバクテリウム(Corynebacterium)属に属する微生物から取得するその単離方法、そのDNAによりコードされるタンパク質、そのDNAを担持するプラスミド、そのプラスミドで形質転換した形質転換体、その形質転換体等を用いた光学活性2-エキソ-アセトアミドノルボルナンの製造方法。
(もっと読む)
新規なアミダーゼ及びその遺伝子
【課題】アンモニア耐性が高い、アミダーゼ活性を有するタンパク質、及び該タンパク質をコードするアミダーゼ遺伝子の提供。
【解決手段】シュードノカルディア・サーモフィラJCM3095から新規なアミダーゼを単離し、その遺伝子を同定した。そのアミダーゼは、アンモニア耐性が高く、かつ2−ヒドロキシ−4−メチルチオブチルアミドに対して非常に高い比活性を示す。すなわち、(a)pH9.0の反応条件において、0.2Mアンモニア存在下でも、アンモニア非存在下の50%以上のアミダーゼ活性を示し、(b)メチオニンアミドよりも、2−ヒドロキシ−4−メチルチオブチルアミドに対して、より高い比活性を示し、(c)SDS−PAGE上での、みかけの分子質量が53kDa、(d)活性の至適温度が60から70℃、(e)中性付近のpHにおいて、60℃以下の温度で安定、(f)pH5.5〜pH10.0の広いpH範囲で高い活性を示す。
(もっと読む)
アミド化合物の分解方法及びニトリル化合物の分解方法
【課題】 アミド化合物及びニトリル化合物を効率的に分解することができるアミド化合物の分解方法及びニトリル化合物の分解方法を提供する。
【解決手段】 アミド化合物の分解方法は、アミド化合物を含む溶液にアミダーゼ処理を施す工程を含む。アミダーゼ処理は、アミダーゼ活性を有する微生物の菌体若しくは該菌体由来のアミダーゼ含有物を用いて実施される。前記微生物は、ロドコッカス・エスピー NITE P−79株であることが好ましい。ニトリル化合物の分解方法は、ニトリル化合物を含む溶液にニトリルヒドラターゼ処理及び前記アミダーゼ処理を施すものである。ニトリルヒドラターゼ処理は、ニトリルヒドラターゼ活性を有する微生物の菌体又は該菌体由来のニトリルヒドラターゼ含有物を用いて実施される。
(もっと読む)
21 - 30 / 38
[ Back to top ]