エプレレノン結晶形
【課題】貯蔵および使用を行なうときの常温において比較的優れた物理的安定性を示す、アルドステロンレセプター拮抗薬である新規の結晶形を有するエプレレノンの提供。
【解決手段】L型結晶エプレレノンを調製する方法、および、選択的には、別に一種類以上の固体型エプレレノン、例えばH型エプレレノンを一緒に含む90%から100%のL型エプレレノンを含む薬剤物質。全投薬単位当たり約10 mgから約1000 mgのエプレレノン、さらには、一種類以上の賦形剤を含む薬学的組成物。アルドステロンが関与する症状または疾患を予防および/または治療する方法において、含まれるエプレレノンの少なくとも一部がL型エプレレノンである、治療上有効な量のエプレレノンを対象者に投与することを含む方法。
【解決手段】L型結晶エプレレノンを調製する方法、および、選択的には、別に一種類以上の固体型エプレレノン、例えばH型エプレレノンを一緒に含む90%から100%のL型エプレレノンを含む薬剤物質。全投薬単位当たり約10 mgから約1000 mgのエプレレノン、さらには、一種類以上の賦形剤を含む薬学的組成物。アルドステロンが関与する症状または疾患を予防および/または治療する方法において、含まれるエプレレノンの少なくとも一部がL型エプレレノンである、治療上有効な量のエプレレノンを対象者に投与することを含む方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、アルドステロンレセプター拮抗薬、より詳しくは、アルドステロンレセプター拮抗薬であるエプレレノンとしての活性をもつ薬剤の技術分野に含まれる。具体的には、本発明は、エプレレノンの新規の結晶形、該結晶形を調製する方法、該結晶形を含む薬学的組成物、該結晶形を使用して、高血圧症などの抗アルドステロン症に関連する症状および疾患など、アルドステロンが関与する症状および/または疾患を予防および/または治療する方法、および、薬剤の製造において該結晶形を使用することに関する。
【背景技術】
【0002】
下記構造式(I)をもつγ-ラクトンであり、エプレレノンとして知られる化合物、メチル9,11-エポキシ-17-ヒドロキシ-3-オキソプレグン-4-エン(ene)-7,21-ジカルボン酸(metyl hydrogen 9,11-epoxy-17-hydroxy-3-oxopregn-4-ene-7,21-dicarboxylate)は、9,11-エポキシステロイド化合物とそれらの塩類開示ている、Grobらに付与された特許文献1で初めて報告された。エプレレノンは、アルドステロンレセプター拮抗薬であって、高血圧症、心不全などの心機能障害、および肝硬変などの抗アルドステロン症に関連する症状を治療するときなど、アルドステロンレセプター拮抗薬の使用が指示されている場面で、治療上有効な量にして投与することができる。
【化1】

【0003】
参照として本明細書に組み入れられる、上記引用文献の特許文献1は、一般的に、エプレレノンの調製剤、およびエプレレノンを含む薬学的組成物の調合剤を開示している。エプレレノンを含む9,11-エポキシステロイド化合物、およびそれらの塩を調製するための別法が、特許文献2および3に開示されている。
【0004】
非特許文献1は、塩化メチレン/ジエチルエステル溶媒系からエプレレノンを結晶化して調製したエプレレノン溶媒和化合物のX線結晶構造解析結果を開示している。
【0005】
非特許文献2は、エプレレノンの一回服用量実験において、20μmの粒子サイズをもつ非処方化エプレレノンの使用を開示している。
【0006】
スピロノラクトンは、アルドステロンレセプター拮抗薬の活性をもつ構造式(II)の20-スピロノキサン-ステロイドで、高血圧を治療するために市販されている。しかし、スピロノラクトンは、男性に女性化乳房と性的不能をもたらすことのある抗アンドロゲン活性をもつ。また、女性の月経不順を生じさせることのある弱いプロゲステロン活性ももつ。このため、グルココルチコイド、黄体ホルモン、およびアンドロゲンのステロイドレセプターシステムなど他のステロイドレセプターシステムと相互作用せず、また/または、より広い治療範囲を提供するエプレレノンのような別の活性アルドステロンレセプター拮抗薬を開発する利点がある。
【化2】

【0007】
非特許文献3は、スピロノラクトンのアセトニトリル溶媒和化合物、エタノール溶媒和化合物、酢酸エチル溶媒和化合物、メタノール溶媒和化合物、および2種類の非溶媒和多形性結晶形を開示している。同様に、非特許文献4は、スピロノラクトンのこれらの固体型結晶形を開示している。
【0008】
エプレレノンの水性媒体中での可溶性は非常に低いため、経口用剤形から消化管に薬剤を放出することが、しばしば、この薬剤の生物学的利用能、より詳しくは、経口投与してから治療薬効果が現れるまでの速さに対する律速要素となっている。
【0009】
【特許文献1】米国特許第4,559,332号
【特許文献2】国際公開公報第97/21720号
【特許文献3】国際公開公報第98/25948号
【非特許文献1】グロブ(Grob)ら(1997)、「ステロイド性アルドステロン拮抗薬:9α,11-エポキシ誘導化合物の高選択性(Steroidal aldosterone antagonists; increased selectivity of 9α,11-epoxy derivatives)」, Helvetica Chimica Acta, 80, 556〜585
【非特許文献2】デ・ガスパロ(De Gasparo)ら(1989)、「抗アルドステロン薬:性的副作用の発生と防止(Antialdosterones: incidence and prevention of sexual side effects)」, Journal of Steroid Biochemistry, 32(13), 223〜227
【非特許文献3】アガフォノフ(Agafonov)ら(1991)、「スピロノラクトンの多形性(Polymorphism of spironolactone)」, Pharmaceutical Science, 80(2), 181〜185
【非特許文献4】ブリッタン(Brittan)ら(1999)、「薬剤用固体の多形性(Polymorphism in Pharmaceutical Solids)」, pp. 114〜116, 207, 235および261(マーセル・デッカー社(Marcel Dekker))
【発明の開示】
【0010】
発明の概要
ここで、貯蔵および使用における通常の温度での高程度の物理的安定性を有し、他の固体型のエプレレノンに較べて独特の性質をもつ新規のエプレレノン結晶形を提供する。結晶形の特徴については、本明細書で完全に後述するが、便宜上「L型」と略称する。
【0011】
本発明は、第一の態様において、エプレレノンそのものの新規のL型結晶形を提供する。「H型」と呼ばれる他の結晶形からL型を区別する特性のうち、H型は単斜晶系、2θが8.0±0.2度(degree)のピークをもつX線粉末回折パターン、および以下に記載するように本明細書において調製された方法により、約223℃から約242℃の範囲内の融点を示す。
【0012】
第二の局面において、本発明は、少なくとも検出可能量のL型エプレレノンを含むエプレレノン薬剤物質を提供する。
【0013】
第三の局面において、本発明は、実質的に位相が純粋なL型エプレレノンであるエプレレノン薬剤物質を提供する。ここで、「位相が純粋な」という語は、他の固体型のエプレレノンに対して純粋であることを意味し、他の化合物に対して、化学的に高度に純粋であることを必ずしも意味しない。
【0014】
第四の局面において、本発明は、脱溶媒したときに、L型エプレレノンを回収することのできるエプレレノン溶媒和結晶形を提供する。
【0015】
第五の局面において、本発明は、L型エプレレノン、選択的には、別に一種類以上の固体形エプレレノンを一緒に含み、エプレレノンの投薬量が一単位全部で約10 mgから約1000 mgであり、さらに一種類以上の賦形剤を含む薬学的組成物を提供する。
【0016】
第六の局面において、本発明は、L型エプレレノンを調製する方法、およびL型エプレレノンを含む組成物を調製する方法を提供する。
【0017】
第七の局面において、アルドステロンが関与する症状または疾患を予防および/または治療する方法において、含まれるエプレレノンの少なくとも一部がH型エプレレノンである、治療上有効な量のエプレレノンを対象者に投与することを含む方法を提供する。
【0018】
本発明のその他の局面は、本出願明細書全体で検討されている。
【0019】
発明の詳細な説明
すべての薬学的化合物および組成物でも言えるように、エプレレノンの化学的および物理的特性が、それを商業的に開発する上では重要である。これらの特性には、(1)モル体積、密度、および吸湿性などの充填特性、(2)融点、蒸気圧および可溶性などの熱力学特性、(3)溶解速度および安定性など(大気条件、特に湿度に対する安定性、および貯蔵条件下での安定性など)の動力学的特性、(4)表面積、湿潤性、界面張力、および形などの表面特性、(5)硬度、張力、強度、成形性、操作性、流量、および混和などの機械的性質、および(6)濾過性などがあるが、これらに限定されない。これらの特性は、例えば、エプレレノンを含む薬学的組成物の加工および貯蔵に影響を与えることがある。他の固体型のエプレレノンに対してこれらの特性の一つ以上が改良された固体型エプレレノンが望ましい。
【0020】
本発明によって、新規の固体型エプレレノンが提供される。これらは、特に、少なくとも2種類の非溶媒和化結晶形と非水和結晶形(「H型」および「F型」と名付けられている)を含む、さまざまな溶媒和化結晶形、および無定形型エプレレノンが含まれる。本願に記載された各固体型エプレレノンは、本明細書またはこれ以外の文献に記載されている他の固体型と比較して、上記化学的および/または物理的に有利な特性の一つ以上をもっている。H型およびL型は、本明細書で優先権主張されている書類では、それぞれ、「I型」および「II型」と呼ばれたり、時には、それぞれ、「高融点多形体」および「低融点多形体」と記載されている。
【0021】
本発明は、L型エプレレノンに関する。L型は、互変的遷移温度(enantiotropic transition temperature)(後述)よりも低い温度では、例えば、H型エプレレノンよりも高い物理的な安定性をもつ。例えば、製造加工の間(例えば、粒子サイズを小さくして表面積を大きくした材料を得るためにエプレレノンを粉末化する間など)物理的に安定している固体型エプレレノンを選択すれば、特別な処理条件、およびそのような特別な処理条件に一般的に伴う費用増加を必要としなくて済む。同様に、(特に、エプレレノン製品の耐用期間に生じうるさまざまな貯蔵条件を考えると)広範な貯蔵条件にわたって物理的に安定した固体型エプレレノンを選択することが、製品の消失や製品の効能低下をもたらすエプレレノンの多形化またはその他の分解による変化を防止するのに役立つ。したがって、L型のように、より物理的に安定した固体型エプレレノンを選択することが、より安定性の低い型のエプレレノンを選択することよりも有意な利益をもたらす。
【0022】
H型エプレレノンも、他の固体型よりは有利である。特に、互変的遷移温度(enantiotropic transition temperature)(後述)では、L型エプレレノンよりも、水性溶媒において、より速い溶解速度(約30%速い)を示す。消化管におけるエプレレノンの溶解速度が、標的細胞または組織へのエプレレノン輸送の律速段階となる場合には、溶解度が速くなれば、生物学的利用能が向上する。したがって、H型は、L型よりも優れた生物学的利用能プロフィールを提供することができる。さらに、より速い溶解速度をもつ固体型エプレレノンを選択することは、溶解速度が遅い他の固体型に較べ、特に、エプレレノンを迅速に放出させるための薬学的組成物に対する賦形剤の選択、およびそれらの処方において、さらに高い融通性を提供することになる。
【0023】
本発明は、また、溶媒和した結晶形のエプレレノンに関する。これらの溶媒和型は、H型およびL型のエプレレノンを調製するときの中間体として有益であり、特に、本発明に照らせば、脱溶媒したときに、L型エプレレノンを回収できる溶媒和結晶形のエプレレノンが有利である。中間体としての溶媒和結晶形の使用によって得られる特別の利益は、本願において後述するように、脱溶媒する際にもたらされる結晶の「真性微粉化(intrinsic micronizing)」である。このような「真性微粉化」によって、粉末化する必要を低下またはなくすことができる。さらに、さらに粉末化する必要がまだあるときにも、H型やL型の溶媒和結晶形を脱溶媒した後に粉末化するよりも、脱溶媒工程の前に一定の溶媒和化合物を粉末化する方が容易である。
【0024】
エプレレノンの薬学的に許容される溶媒和結晶形も、薬学的組成物で直接用いることができる。一つの実施態様において、このような組成物を直接調製するときに有用な溶媒和結晶形は、塩化メチレン、イソプロパノール、またはエチルエーテルを含まず、別の態様においては、塩化メチレン、イソプロパノール、エチルエーテル、メチルエチルケトン、またはエタノールを含まず、また、さらに別の、別の態様においては、塩化メチレン、イソプロパノール、エチルエーテル、メチルエチルケトン、エタノール、酢酸エチル、またはアセトンを含まない。このような使用にとって、もっとも好ましくは、エプレレノンの溶媒和結晶形は、実質的に、薬学的に許容される溶媒でない溶媒を含まない。
【0025】
薬学的組成物で用いられる溶媒和結晶形は、一般的に、かつ好ましくは、薬学的に許容される、高沸点で、かつ/または水素結合する溶媒、例えば、ブタノールであるが、これに限定されない溶媒を含む。溶媒和結晶形はまとまって、さまざまな溶解速度範囲を提供することができるため、消化管におけるエプレレノンの溶解速度が、標的細胞または組織へのエプレレノン輸送の律速段階となる場合には、H型およびL型に較べてもさまざまな範囲の生物学的利用能を提供することができる。
【0026】
本発明は、無定形型のエプレレノンにも関する。無定形型のエプレレノンは、H型およびL型を調製するときの中間体として有用である。さらに、無定形エプレレノンは、さまざまな溶解速度をもつため、無定形型エプレレノンが薬学的組成物中に存在し、かつ、消化管におけるエプレレノンの溶解速度が、標的細胞へのエプレレノン輸送の律速段階となる場合には、このような無定形エプレレノンが、H型およびL型に較べてもさまざまな範囲の生物学的利用能を提供することができる。
【0027】
H型エプレレノン、L型エプレレノン、溶媒和結晶形エプレレノン、および無定形エプレレノンからなる群より選択される固体型を組み合わせることも興味深い。このような組合せは、例えば、制御放出組成物など、さまざまな溶解プロフィールをもつ薬学的組成物を調製するときに有用である。本発明の一つの実施態様において、少なくとも検出可能量のL型エプレレノンと、H型エプレレノン、溶媒和結晶形エプレレノン、および無定形エプレレノンからなる群より選択される一種類以上の固体型である残り分と含む固体型の組合せが提供される。
【0028】
固体型エプレレノンの使用目的によっては、加工上の配慮から、特定の固体型、またはこのような固体型の特定の組合せを選択することが好まれるかもしれない。例えば、位相が純粋なL型は、一般的に、位相が純粋なH型よりも簡単に調製することができる。しかし、H型とL型の混合物の方が、一般的に、位相が純粋なL型よりもより簡単に調製することができるため、比較的化学的純度の低いエプレレノン出発物質として使用することができる。組成物において、H型またはL型の代わりに溶媒和結晶形を使用すると、それを使用しないと溶媒和結晶形の脱溶媒によって進められる加工工程、すなわち脱溶媒化を省くことができる。または、例えば、中間体溶媒和結晶形の調製および脱溶媒化を妨害することなく、適当な溶媒からL型を直接結晶化すれば、この脱溶媒化工程を省くことができよう。
【0029】
定義
本明細書において、エプレレノンについて用いられるとき、「無定形」という用語は、エプレレノン分子が無秩序な配置でその中に存在し、区別できる結晶格子または単位格子を形成していない固体を意味する。X線粉末回折を行なうと、無定形エプレレノンは、特徴的な結晶ピークを生じない。
【0030】
本明細書において、物質または溶液の沸点について言及する場合には、「沸点」は、適用処理条件下での物質または溶液の沸点を意味する。
【0031】
本明細書において、エプレレノンについて用いられるとき、「結晶形」は、(i)区別できる単位格子を含み、また、(ii)X線粉末回折を行なうと、回折ピークが得られるという区別できる結晶格子を形成するように、エプレレノン分子が配置されている固体を意味する。
【0032】
本明細書において、「結晶化」とは、エプレレノン出発材料の調製に関する適用環境によって、結晶化、および/または再結晶化を意味することがある。
【0033】
本明細書において、「温浸」とは、溶媒または溶媒混合液中の固形エプレレノンの懸濁液を、適用処理条件下で、該溶媒または溶媒混合液の沸点で加熱する処理を意味する。
【0034】
本明細書において、「直接の結晶化」とは、中間的な溶媒和結晶固体型のエプレレノンを生成したり、脱溶媒化することなく、適当な溶媒からエプレレノンを直接結晶化することを意味する。
【0035】
本明細書において、「エプレレノン薬剤物質」とは、この語が使用される文脈によっては、エプレレノンそのものを意味し、処方されていないエプレレノンや、薬学的組成物の成分として存在するエプレレノンを意味することもある。
【0036】
本明細書において、「粒子サイズ」とは、当技術分野において公知のレザー光散乱、沈降フィールドフローフラクショネーション(sedimentation field flow fractionation)、フォトン相関分光測定法(photon correlation spectroscopy)、またはディスク遠心分離法(disk centrifugation)などの通常の粒子サイズ測定技術によって測定された粒子の大きさを意味する。「D90粒子サイズ」は、粒子の重量の90%が、このような通常の粒子サイズ測定技術によって測定されたD90粒子サイズよりも小さい粒子サイズである。
【0037】
「DSC」という用語は、示差走査熱量測定法の意味である。
【0038】
「HPLC」という用語は、高圧液体クロマトグラフィーの意味である。
【0039】
「IR」という用語は、赤外線の意味である。
【0040】
本明細書において、「純度」という用語は、別段の記載がない限り、通常のHPLCアッセイ法によるエプレレノンの化学的純度を意味する。ここで、「低純度エプレレノン」とは、一般的に、有効量のH型結晶成長促進物質および/またはL型結晶成長阻害物質を含むエプレレノンを意味する。ここで、「高純度エプレレノン」とは、一般的に、H型結晶成長促進物質および/またはL型結晶成長阻害物質を全く含まないか、有効量よりも少ない量しか含まないエプレレノンを意味する。
【0041】
本明細書において、「位相が純粋な」という用語は、本明細書記載の赤外線分光測定解析法によって測定された特定の結晶形または無定形型のエプレレノンについてのエプレレノン固体純度を意味する。
【0042】
「XRPD」という用語は、X線粉末回折の意味である。
【0043】
「rpm」という用語は、1分間あたりの回転数を意味する。
【0044】
「TGA」という用語は、熱重量分析法を意味する。
【0045】
「Tm」という用語は、融点を意味する。
【0046】
結晶形の特徴づけ
1.分子の立体構造
単結晶X線解析によって、エプレレノン分子の立体構造がH型とL型とでは異なり、特に、ステロイド環の第7位でエステル基の方向が異なっていることが示されている。エステル基の方向は、C8-C7-C23-O1ねじれ角によって定義することができる。
【0047】
H型結晶格子において、エプレレノン分子は、エステル基のメトキシ基が、第7位でC-H結合とほぼ並列し、カルボニル基がB-ステロイド環のほぼ中央を覆うところに位置するという構造を採っている。この立体構造では、C8-C7-C23-O1ねじれ角は約-73.0°である。この方向では、エステル基のカルボニルの酸素原子(O1)が、9,11-エポキシド環の酸素原子(O4)に近接する。O1-O4の距離は、約2.97Åで、ファンデルワールス接触距離である3.0Åよりも僅かに短い(酸素原子のファンデルワールス半径を1.5Åとした場合)。
【0048】
L型結晶格子では、エプレレノン分子は、H型の分子に対してエステル基が約150°回転しており、約+76.9°のC8-C7-C23-O1ねじれ角をもつ立体構造をとっている。この方向では、エステルのメトキシ基は、Aステロイド環の4,5-アルケン分節の方向を向いている。この方向では、エステル基のどちらの酸素原子(O1、O2)と、9,11-エポキシド環の酸素原子(O4)との間の距離も、H型について測定された距離よりも長くなる。O2-O4の距離は、約3.04Åで、ファンデルワールス接触距離である3.0Åよりも僅かに長い。O1-O4の距離は約3.45Åである。
【0049】
単結晶X線回折によって今までに解析された溶媒和結晶形では、エプレレノン分子は、L型の立体構造の特徴を採っているように見える。
【0050】
2.単結晶X線回折
シーメンス(Siemens)D5000粉末回折計またはアイネル(Inel)多目的回折計によって、エプレレノンのさまざまな結晶形を分析した。シーメンス(Siemens)D5000粉末回折計については、生データを2から50まで、0.020および2秒間隔というステップ毎に2θ(シータ)値を測定した。アイネル(Inel)多目的回折計については、試料をアルミニウム製のサンプルホルダーに入れ、生データをすべての2θ値を30分間同時に収集した。
【0051】
表1A、1Bおよび1Cは、それぞれ、H型(低純度エプレレノンの温浸によって得られたエタノール溶媒和化合物の脱溶媒化によって調製されたもの)、L型(高純度エプレレノンの再結晶化によって得られたメチルエチルケトン溶媒和化合物の脱溶媒化によって調製されたもの)、およびメチルエチルケトン溶媒和化合物(高純度エプレレノンのメチルエチルケトン中での室温懸濁物転換によっ調製されたもの)という結晶形のエプレレノンの2θ値と強度に関する主要ピークの重要なパラメータを示している(波長1.54056ÅでのX線照射)。
【0052】
H型およびL型の製造経路(すなわち、溶媒和化合物の脱溶媒化)に関連して、結晶回折面の間隔が不完全になる結果、H型とL型の回折パターンにおいて、ピーク位置の僅かな変化が存在することがある。なお、H型は、粗製エプレレノンの温浸によって調製された溶媒和化合物から単離されている。この方法は、全体的に化学的純度の低い(約90%の)H型を生じる。最後に、エプレレノンの溶媒和型は、結晶格子の中で溶媒チャネル内の溶媒分子の移動度が増すために、回折ピークの位置にいくらかの変化が見られることが予想される。
【表1A】


X線回折データ、H型
【表1B】


X線回折データ、L型
【表1C】


X線回折データ、メチルエチルケトン溶媒和化合物
【0053】
エプレレノンのH型、L型、およびメチルエチルケトン溶媒和化合物の結晶形のグラフ例を、それぞれ、図1-A、1-B、および1-Cに示す。H型は、7.0±0.2度、8.3±0.2度、および12.0±0.2度の2θで際だったピークを示す。L型は、2θが8.0±0.2度、12.4±0.2度、12.8±0.2度および13.3±0.2度で際だったピークを示す。メチルエチルケトン溶媒和化合物は、2θが7.6±0.2度、7.8±0.2度、および13.6±0.2度で際だったピークを示す。
【0054】
以下の溶媒和結晶形のエプレレノンに関するX線回折パターンの実例を図1-Dから1-Oに示す。それぞれ、n-プロピルアルコール、テトラヒドロフラン、エチルプロピオン酸、酢酸、アセトン、トルエン、イソプロパノール、エタノール、酢酸イソブチル、酢酸ブチル、酢酸メチル、酢酸プロピルの溶媒和化合物。
【0055】
3.融解/分解温度
非溶媒和化エプレレノン結晶形の融解および/または分解温度を、TAインスツルメンツ(TA Instruments)2920示差走査熱量測定計を用いて決定した。1〜2 mg量の各試料を、シール付きまたはシールなしのアルミニウム鍋の上に置いて加熱し、約10℃/分の温度上昇速度を得た。融解/分解温度の範囲は、融解/分解吸熱の推定開始温度から最大値までである。
【0056】
H型およびL型エプレレノンの融解は、化学分解、および結晶格子に捉えられていた溶媒の消失に伴って起きた。融解/分解温度も、解析前の固体処理による影響を受けた。例えば、適当な溶媒、または適当な溶媒もしくは溶媒混合液中の高純度エプレレノンの結晶化によって得られた溶媒和化合物の脱溶媒物から直接結晶化することによって調製された約180〜450μmというD90粒子サイズの未粉末化L型の融解/分解温度は、一般的に、約237℃から約242℃までの範囲にある。適当な溶媒もしくは溶媒混合液中の高純度エプレレノンの溶液から溶媒和化合物を結晶化し、脱溶媒し、得られたL型を粉末化して調製された、約80〜100μmのD90粒子サイズをもつ粉末化L型の融解/分解温度は、一般的に、約223℃から約234℃までの範囲にある。低純度エプレレノンの温浸によって得られた溶媒和化合物を脱溶媒して調製された約180〜450μmのD90粒子サイズをもつ未粉末化L型の融解/分解温度は、一般的に、約247℃から約251℃までの範囲にある。それぞれ、(a)メチルエチルケトンから直接結晶化した未粉末化L型エプレレノン、(b)メチルエチルケトンから高純度エプレレノンを結晶化して得られた溶媒和物の脱溶媒によって調製した未粉末化L型エプレレノン、(c)メチルエチルケトンから高純度エプレレノンを結晶化して得られた溶媒和化合物の脱溶媒化による産物を粉末化して調製したL型エプレレノン、(d)メチルエチルケトンから低純度エプレレノンを温浸して得られた溶媒和物を脱溶媒化して調製した未粉末化H型エプレレノンのDSC熱記録の例を図2-A、2-B、2-Cおよび2-Dに示す。
【0057】
エプレレノンの溶媒和型のDSC熱記録をパーキンエルマー(Perkin Elmer)Pyris 1示差走査熱量計を用いて測定した。各1〜2 μgの試料を、シールをしないでアルミニウム鍋に入れ、約10℃/分の温度上昇率になるよう加熱した。低温での一種類以上の吸熱現象は、溶媒和化合物の結晶格子から溶媒が失われるにつれて起こるエンタルピー変化と関連していた。最も高熱の吸熱は、H型またはL型のエプレレノンの融解/分解に伴って起きた。エプレレノン溶媒和化合物である、n-プロピルアルコール、テトラヒドロフラン、エチルプロピオン酸、酢酸、クロロホルム、アセトン、トルエン、イソプロパノール、酢酸t-ブチル、エタノール、酢酸イソブチル、酢酸ブチル、酢酸メチル、酢酸プロピル、n-ブタノール、およびn-オクタノールの溶媒和化合物のDSC熱記録を、それぞれ、図2-Eから2-Tに示す。
【0058】
4.赤外線吸収スペクトル分析
非溶媒和型のH型およびL型エプレレノンの赤外線吸収スペクトルを、ニコレットDRIFT社(Nicolet DRIFT)の(拡散反射赤外線のフーリエ変換)Magna System 550を用いて得た。Spectra-Tech Collector装置と微量試料容器を用いた。試料(5%)を臭化カリウム中で解析し、400から4000 cm-1で走査して解析した。稀釈したクロロホルム溶液(3%)中、または溶媒和した結晶形のエプレレノンの赤外線吸収スペクトルを、Bio-rad FTS-45分光光度計を用いて得た。クロロホルム溶液試料を、塩化ナトリウム塩プレートをもつ、0.2 mm間隔の溶液用セルを用いて分析した。溶媒和FTIRスペクトルをIBM社のマイクロ-MIR(micro-MIR)(複数内部反射)補助装置を用いて回収した。試料を400から4000 cm-1で走査した。(a)H型、(b)L型、(c)メチルエチルケトン溶媒和物、および(d)クロロホルム溶液中のエプレレノンにおける赤外線吸収スペクトルの例を、それぞれ、図3-A、3-B、3-Cおよび3-Dに示す。
【0059】
表2は、H型、L型、およびメチルエチルケトン溶媒和型の結晶形に関する吸収バンドを具体的に示している。比較のために、クロロホルム溶液中のエプレレノンの吸収バンドの具体例も示してある。例えば、スペクトルのカルボニル領域で、H型と、L型またはメチルエチルケトン溶媒和型の間には違いが見られた。H型は、約1739 cm-1のエステルカルボニルストレッチ(ester carbonyl stretch)をもつが、L型およびメチルエチルケトン溶媒和型で対応するストレッチは、それぞれ、約1724と1722 cm-1である。クロロホルム溶液中のエプレレノンでは、エステルカルボニルストレッチは、約1727 cm-1である。H型とL型の間におけるストレッチ頻度の変化は、この2つの結晶形でエステル基の方向が変化していることしていることを反映している。なお、A型ステロイド環における、結合ケトンのエステル基のストレッチは、H型またはメチルエチルケトン溶媒和型で約1664〜1667 cm-1であり、L型で約1665 cm-1である。対応するカルボニル基のストレッチは、クロロホルム溶液中では約1665 cm-1である。
【0060】
H型とL型とのもう一つの違いは、C-H屈曲領域に見られた。H型には、L型、メチルエチルケトン溶媒和型、またはクロロホルム溶液中のエプレレノンでは見られない約1399 cm-1で吸光を示す。カルボニル基に隣接するC2およびC1のメチレン基を切断するためのCH2領域には、約1399 cm-1のストレッチが存在する。
【表2】

エプレレノンの各型におけるIR吸収バンド(cm-1)
【0061】
エプレレノンの溶媒和化合物である、n-プロピルアルコール溶媒和化合物、テトラヒドロフラン溶媒和化合物、エチルプロピオン酸溶媒和化合物、酢酸溶媒和化合物、アセトン溶媒和化合物、トルエン溶媒和化合物、イソプロパノール溶媒和化合物、エタノール溶媒和化合物、酢酸イソブチル溶媒和化合物、酢酸ブチル溶媒和化合物、酢酸プロピル溶媒和化合物、酢酸メチル溶媒和化合物、プロピレングリコール溶媒和化合物、および酢酸t-ブチル溶媒和化合物について、それぞれの赤外線吸収スペクトルの例を図3-Eから3-Sに示す。
【0062】
5.核磁気共鳴(NMR)分析法
31.94 MHzのフィールドにおける13C NMRスペクトルを得た。H型およびL型エプレレノンの13C NMRスペクトルの実例を、それぞれ、図4および5に示す。図4に示したデータを得るために解析されたH型エプレレノンは、位相が純粋ではなく、少量のL型エプレレノンを含んでいた。H型は、約64.8 ppm、24.7 ppm、および19.2 ppmにおける炭素共鳴によってもっとも明確に区別された。
【0063】
6.熱重量分析
TAインスツルメンツ(TA Instruments)TGA 2950熱重量分析計を用いて熱重量分析を行なった。決定した。各試料は、シールなしのアルミニウム鍋上に、窒素をパージした状態で置いた。開始温度は25℃で、約10℃/分の割合で温度を上昇させた。
【0064】
以下のエプレレノン溶媒和化合物、すなわち、メチルエチルケトン溶媒和化合物、n-プロピルアルコール溶媒和化合物、テトラヒドロフラン溶媒和化合物、エチルプロピオン酸溶媒和化合物、酢酸溶媒和化合物、クロロホルム溶媒和化合物、アセトン溶媒和化合物、トルエン溶媒和化合物、イソプロパノール溶媒和化合物、エタノール、酢酸イソブチル、酢酸ブチル、酢酸メチル、酢酸プロピル溶媒和化合物、プロピレングリコール溶媒和化合物、n-ブタノール溶媒和化合物、および酢酸t-ブチル溶媒和化合物それぞれについて、熱重量測定分析プロフィールの例を図6-Aから6-Rに示す。
【0065】
7.顕微鏡法
ツァイス社(Zeiss)製全面偏光顕微鏡(Universal Polarized Light Microscope)付きのリンカム社(Linkam)のTHMS 600ホットステージ(Hot Stage)を用いて、メチルエチルケトン溶媒和化合物の単結晶に対して高熱期顕微鏡法を行なった。室温での偏光下では、溶媒和化合物の結晶は複屈折性かつ半透明で、結晶格子が非常に規則的であることを示している。温度を約60℃まで上昇させるにつれて、結晶の長軸方向に沿って顕著な欠陥が生じ始めた。メチルエチルケトン溶媒和化合物の脱溶媒によって得られたL型エプレレノンの走査電子顕微鏡写真を図7に示すが、結晶格子内で表面の欠損、孔、亀裂、および破砕が起きているのが分かる。エチル酢酸からの直接の結晶化によって得られたL型エプレレノンの走査電子顕微鏡写真が図8に示されているが、結晶格子内での同じような表面の欠損、孔、亀裂、および破砕は見られない。
【0066】
8.単位格子のパラメータ
以下の表3A、3Bおよび3Cは、H型、L型、およびいくつかのエプレレノン溶媒和結晶形について決定された単位格子パラメータをまとめたものである。
【表3A】


エプレレノン結晶形の単位格子パラメータ
【表3B】

エプレレノン結晶形の単位格子パラメータ
1酢酸ブチル溶媒和化合物分子は、チャネル内にある溶媒分子が不規則であるため、完全には精製されていなかった。
【表3C】

エプレレノン結晶形の単位格子パラメータ
1溶媒和化合物分子は、チャネル内にある溶媒分子が不規則であるため、完全には精製されていなかった。
【0067】
エプレレノンの選択された結晶形に関する別の情報が、下の表4に記載されている。メチルエチルケトン溶媒和化合物について、上記表3Aに記載されている単位格子データは、これら、さらに別のエプレレノン結晶溶媒和化合物の多くについての単位格子パラメータを代表するものである。試験されたエプレレノン結晶溶媒和化合物のほとんどは、実質的に、互いに同じ構造をもっている。取り込まれた溶媒分子の大きさによっては、一つの溶媒和結晶形から別の溶媒和結晶形へ、X線粉末回折ピークが僅かに変化することがあるが、全体的な回折パターンは実質的に同じであって、単位格子パラメータおよび分子位置は、試験した溶媒和化合物のほとんどについて実質的に同一である。
【表4】

エプレレノン溶媒和化合物に関する付加的情報
1窒素パージ条件下で10℃/分の加熱速度で行なった熱重量解析によって測定される、溶媒和の最終重量減少工程から推定された脱溶媒温度と定義される。しかし、脱溶媒温度は、溶媒和化合物の製造方法による影響を受ける。低温では、さまざまな方法によって、溶媒和化合物において脱溶媒化を開始することのできる核生成部位をさまざまな数作り出すことができる。
【0068】
溶媒和化合物の単位格子は4個のエプレレノン分子からなる。この単位格子におけるエプレレノン分子および溶媒分子の化学量も、多数の溶媒和化合物について、上記表4に記載されている。H型の単位格子は4個のエプレレノン分子からなる。L型の単位格子は2個のエプレレノン分子からなる。溶媒和化合物の単位格子は、脱溶媒の過程で、溶媒分子が残した間隙を埋めるために、エプレレノン分子が平行移動や回転されると、H型および/またはL型の単位格子に転換される。表4には、多数の異なった溶媒和化合物の脱溶媒温度も記載されている。
【0069】
9.不純物の結晶特性
エプレレノンの不純物の中には、溶媒和化合物を脱溶媒する過程でH型の形成を誘導できるものがある。特に、以下の2種類の不純物分子を評価した。すなわち、7-メチル水素4α,5α;9α,11α-ジエポキシ-17ヒドロキシ-3-オキソ-17α-プレグナン-7α,21-ジカルボン酸、γラクトン(III)(「ジエポキシド」)、および7-メチル水素11α,12α-エポキシ-17ヒドロキシ-3-オキソ-17α-プレグン-4-エン-7α,21-ジカルボン酸、γ-ラクトン(IV)(「11,12-エポキシド」)。
【化3】

【化4】

脱溶媒により生じるエプレレノン結晶形に対する、これらの不純物の効果については、本明細書の実施例においてさらに詳しく説明する。
【0070】
7-メチル水素-17ヒドロキシ-3-オキソ-17α-プレグナ-4,9(11)-ジエン-7α,21-ジカルボン酸であるγ-ラクトン(V)(「9,11-オレフィン」)とH型エプレレノンの単結晶構造における類似性から、9,11-オレフィンも、溶媒和化合物を脱溶媒する過程でH型の形成を誘導することができるという仮説が立てられている。
【化5】

【0071】
単結晶を核不純化合物から単離した。ジエポキシド、11,12-エポキシド、および9,11-オレフィンで単離された結晶形のX線粉末回折パターンを、それぞれ図9、10および11に示す。各不純物分子のX線粉末回折パターンは、H型のX線粉末回折パターンに類似しており、これは、H型と3種類の不純化合物が、同じ単結晶構造をもっていることを示唆するものである。
【0072】
各不純化合物の単結晶も単離して、X線による構造決定を行ない、これら3種類の化合物が、H型の単結晶構造に類似した単結晶構造を採用していることを証明した。11,12-エポキシドの単結晶をイソプロパノールから単離した。9,11-オレフィンの単結晶は、n-ブタノールから単離した。各不純化合物の結晶形について決定した結晶構造データを表5に示す。得られた結晶系と格子パラメータは、H型、ジエポキシド、11,12-エポキシド、および9,11-オレフィンの結晶形で実質的に同一であった。
【表5】


H型エプレレノンとの比較による、不純物結晶に関する単位格子パラメータ
【0073】
表5に記載されている4種類の化合物を、同一の間隙グループに結晶化し、類似した格子パラメータをもつ(すなわち、同一構造である)。ジエポキシド、11,12-エポキシド、および9,11-オレフィンは、H型立体構造を採るという仮説が立てられている。どの不純化合物についても、(溶液から直接に)H型充填を単離することが比較的容易だということは、このH型格子が、これら一連の構造的に類似した化合物にとって安定した充填方式であることを示している。H型エプレレノンと、実質的に結晶学上同一の構造をもつ化合物は、溶液からH型エプレレノンを結晶化するときの添加不純物(dopant)として有用な可能性があると考えられる。
【0074】
したがって、具体的な実施態様において、溶媒または溶媒混合液中のエプレレノン溶液からH型エプレレノンを結晶化することを促進する方法、結晶化する前に、結晶学上実質的にH型エプレレノンと同一構造をもつ化合物の有効量によって不純物添加処理することを含む方法が提供される。ここで、「不純物添加処理」とは、積極的処理、すなわち、不純物添加処理用化合物を意図的に添加しても、または、消極的処理、すなわち、該溶液中に不純物添加処理用化合物が不純物として存在していても、どちらでもよい。
【0075】
本実施態様に関して好適な不純物添加処理用化合物は、それぞれ、上記化合物(III)、(IV)および(V)であるジエポキシド、11,12-エポキシド、および9,11-オレフィンである。
【0076】
エプレレノンの調製
本発明に係る新規の結晶形を調製するためのエプレレノン出発物質は、上記国際公開公報第97/21720号および第98/25948号で開示されている方法、特に、これら刊行物で開示されているスキーム1など、それ自体は既知の方法によって調製することができる。
【0077】
結晶形の調製
1.溶媒和型結晶形の調製
エプレレノンの溶媒和型結晶形は、適当な溶媒、または適当な溶媒の混合液からエプレレノンを結晶化して調製することができる。適当な溶媒、または適当な溶媒の混合液は、一般的に、高温下でエプレレノンを不純物と一緒に可溶化するが、冷却すると、溶媒和化合物を選択的に結晶化する有機溶媒、または有機溶媒の混合液を含む。このような溶媒、または溶媒の混合液におけるエプレレノンの可溶性は、一般的に、室温で約5から約200 mg/mlである。溶媒、または溶媒の混合液は、好ましくは、その前にエプレレノン出発物質を調製する処理工程で使用した溶媒で、特に、それが、エプレレノン結晶形を含む最終薬学的組成物に含まれるときには、薬学的に許容されるものである溶媒から選択する。例えば、塩化メチレンを含む溶媒和化合物が回収される、塩化メチレンを含む溶媒系は望ましくない。
【0078】
用いられる溶媒は、好ましくは、薬学的に許容される溶媒であり、特に、「不純物:残留溶媒の手引き(Impurities: guideline for residual solvents)」、人体に使用するための薬剤を登録するための技術的要件の統一化に関する国際会議(International Conference On Harmonization Of Technical Requirements For Registration Of Pharmaceuticals For Human Use)(ICH運営委員会により、1997年7月17日のICHプロセスのステップ4の採用が推奨された)において、クラス2またはクラス3として定義されている溶媒である。さらに好ましくは、溶媒、または溶媒の混合液は、メチルエチルケトン、1-プロパノール、2-ペンタノン、酢酸、アセトン、酢酸ブチル、クロロホルム、、エタノール、イソブタノール、酢酸イソブチル、酢酸メチル、プロピオン酸エチル、n-ブタノール、n-オクタノール、イソプロパノール、酢酸プロピル、プロピレングリコール、t-ブタノール、テトラヒドロフラン、トルエン、メタノール、および酢酸t-ブチルからなる群より選択される。
【0079】
本処理法の別の実施態様において、溶媒、または溶媒の混合液は、1-プロパノール、2-ペンタノン、酢酸、アセトン、酢酸ブチル、クロロホルム、イソブタノール、酢酸イソブチル、酢酸メチル、プロピオン酸エチル、n-ブタノール、n-オクタノール、酢酸プロピル、プロピレングリコール、t-ブタノール、テトラヒドロフラン、トルエン、メタノール、および酢酸t-ブチルからなる群より選択される。
【0080】
本処理法の別の実施態様において、溶媒、または溶媒の混合液は、1-プロパノール、2-ペンタノン、酢酸、アセトン、酢酸ブチル、クロロホルム、イソブタノール、酢酸イソブチル、酢酸メチル、プロピオン酸エチル、n-ブタノール、n-オクタノール、n-プロパノール、酢酸プロピル、プロピレングリコール、t-ブタノール、テトラヒドロフラン、トルエン、メタノール、および酢酸t-ブチルからなる群より選択される。
【0081】
エプレレノンの溶媒和型結晶形を調製するために、一定量のエプレレノン出発物質を一定量の溶媒で可溶化し、結晶が形成されるまで冷却した。エプレレノンを溶媒に加える溶媒温度は、一般的に、溶媒または溶媒の混合液の溶解曲線に基づいて選択される。例えば、本明細書記載の溶媒のほとんどでは、この溶媒温度は、一般的に、約25℃以上であり、好ましくは、約30℃から溶媒の沸点までであり、また、より好ましくは、溶媒の沸点よりも約25℃低い温度から、溶媒の沸点までである。
【0082】
または、加熱した溶媒をエプレレノンに加えて、混合液を結晶が形成されるまで冷却することも可能である。エプレレノンを加える時の溶媒の温度は、一般的に、溶媒または溶媒の混合液の溶解曲線に基づいて選択される。例えば、本明細書記載の溶媒のほとんどでは、この溶媒温度は、一般的に、約25℃以上であり、好ましくは、約50℃から溶媒の沸点までであり、また、より好ましくは、溶媒の沸点よりも約15℃低い温度から、溶媒の沸点までである。
【0083】
同様に、一定容量の溶媒と混合するエプレレノン出発物質の量は、溶媒、または溶媒の混合液の溶解曲線に依存する。一般的には、溶媒に加えるエプレレノンの量は、室温では完全に溶解されない。例えば、本明細書記載の溶媒のほとんどでは、一定容量の溶媒と混合するエプレレノン出発物質の量は、約1.5倍から約4.0倍であり、好ましくは、約2.0倍から約3.5倍であり、より好ましくは、約2.5倍であるが、このエプレレノン量で、該容量の溶媒に室温で溶解する。
【0084】
エプレレノン出発物質が溶媒に完全に溶けたら、一般的には、溶液をゆっくりと冷却して、エプレレノンの溶媒和化した結晶形を結晶化する。例えば、本明細書記載の溶媒のほとんどでは、溶液を、約20℃/分よりも遅い速度で冷却し、好ましくは、約10℃/分よりも遅い速度で、また、より好ましくは、約5℃/分よりも遅い速度で、さらにより好ましくは、約1℃/分よりも遅い速度で冷却する。
【0085】
溶媒和型結晶形を回収する終点温度は、溶媒、または溶媒の混合液の溶解曲線に依存する。例えば、本明細書記載の溶媒のほとんどでは、この終点温度は、一般的に、約25℃よりも低く、好ましくは、約5℃よりも低く、より好ましくは、約−5℃よりも低い。終点温度を低くする方が、一般的には、溶媒和型結晶形の形成には有利である。
【0086】
または、別の技術を用いて溶媒和化合物を調製することも可能である。このような技術の例には、(i)エプレレノン出発物質を一つの溶媒に溶かして、溶媒和型結晶形の結晶化を促進するために共溶媒を加える方法、(ii)溶媒和化合物の蒸気拡散成長(vapor diffusion growth)、(iii)回転式乾燥のような乾燥法によって、溶媒和化合物を単離する方法、および(iv)懸濁液の転換法(slurry conversion)などを含むが、これらに限定されない。
【0087】
上記したところにしたがって調製された溶媒和型結晶形の結晶は、濾過、または遠心分離などの通常の適当な方法によって溶媒から分離することができる。結晶化の過程で溶媒系を強く振とうすると、一般的に、より小さな結晶粒子が生じる。
【0088】
2.L型溶媒和化合物の調製
L型エプレレノンは、脱溶媒化によって、溶媒和型結晶形から直接調製することができる。脱溶媒は、溶媒和化合物の加熱、溶媒和化合物の周りの大気圧の減圧、または、これらの併用などがあるが、これらに限定されない適当な脱溶媒化手段によって行なうことができる。溶媒和化合物をオーブンなどの中で加熱して溶媒を除去すれば、この処理中の溶媒の温度は、一般的には、H型およびL型の互変性遷移温度を超えることはない。この温度は、好ましくは、150℃を超えない。
【0089】
脱溶媒圧力および脱溶媒化時間は、厳密には重要ではない。脱溶媒圧力は、好ましくは、約1気圧以下である。しかし、脱溶媒圧力を低下させるにつれて、脱溶媒を行なうことのできる温度、および/または、脱溶媒化時間も同様に減少してゆく。特に、高い脱溶媒温度をもつ溶媒和化合物では、真空乾燥すると、より低い乾燥温度を用いることができる。脱溶媒化時間は、単に、脱溶媒を行なわせるのに十分であることだけが必要で、そうすればL型が形成されて完成する。
【0090】
実質的にL型だけを含む産物が調製されたことを確認するためには、エプレレノン出発物質は、一般的に高純度エプレレノンであり、好ましくは、実質的に純粋なエプレレノンである。L型エプレレノンを調製するために用いられるエプレレノン出発物質は、一般的に、90%以上の純度、好ましくは、95%以上の純度、そして、より好ましくは、99%以上の純度である。本願の別の箇所でより詳しく説明されているように、エプレレノン出発物質における、ある種の不純物は、本処理法によって得られた産物の収量やL型含有量に有害な効果を与えることがある。
【0091】
高純度エプレレノン出発物質から、このようにして調製された結晶化エプレレノン産物は、通常、10%以上のL型、好ましくは、50%以上のL型、より好ましくは、75%以上のL型、さらにより好ましくは、90%以上のL型、さらに好ましくは、約95%以上のL型、および、さらに一層好ましくは、実質的に位相が純粋なL型である。
【0092】
3.溶媒和化合物からのH型の調製
H型を含む産物は、(i)高純度エプレレノン出発物質ではなく低純度エプレレノン出発物質を使用し、(ii)位相が純粋なH型結晶を溶媒系に播種し、あるいは、(iii)、(i)と(ii)を組み合わせて調製することができる。
【0093】
3.1.結晶成長促進物質および阻害物質としての不純物の使用
エプレレノン出発物質中のすべての不純物の全体量ではなく、エプレレノン出発物質に含まれる一定の不純物の存在と含量が、溶媒和化合物の脱溶媒化の過程でH型結晶を形成する能力に影響を与える。一定の不純物は、通常、H型成長促進物質、またはL型成長阻害物質である。これらは、エプレレノン出発物質に含まれていたり、エプレレノン出発物質を加える前から溶媒、または溶媒の混合液に含まれていることがあり、また/または、エプレレノン出発物質を加えた後で、溶媒、または溶媒の混合液に加えることもある。ボナフェーデ(Bonafede)ら、(1995)は、参照として本明細書に組み入れられる、「分子結晶基質に対するリッジダイレクティドエピタクシーによる有機多形の選択的核生成および成長(Selective nucleation and growth of an organic polymorph by ledge-directed epitaxy on a molecular crystal substrate)」、J. Amer. Chem. Soc., 117(3)において、成長促進物質および成長阻害物質を多形系で使用することを考察している。本発明では、通常、適当な不純物は、H型エプレレノンの単結晶構造と実質的に同一の単結晶構造をもつ化合物を含む。不純物は、好ましくは、H型エプレレノンのX線粉末回折パターンと実質的に同一のX線粉末回折パターンを示す化合物であり、より好ましくは、ジエポキシド、11,12-エポキシド、および9,11-オレフィン、およびこれらの組合せからなる群より選択される。
【0094】
H型結晶を調製するのに必要な不純物の量は、一般的には、部分的には、溶媒または溶媒の混合液、および不純物のエプレレノンに対する可溶性によって決まる。例えば、メチルエチルケトン溶媒和化合物からのH型の結晶化において、ジエポキシの低純度エプレレノン出発物質に対する重量比は、一般的には、約1:100以上、好ましくは、約3:100以上、より好ましくは、約3:100から約1:5、さらに好ましくは、約3:100から約1:10である。11,12-エポキシドは、メチルエチルケトンの中では、ジエポキシドよりも可溶性が高いため、通常、H型エプレレノン結晶を調製するためには、より大量の11,12-エポキシドが必要である。不純物が11,12-エポキシドを含む場合には、、ジエポキシドの低純度エプレレノン出発物質に対する重量比は、一般的には、約1:5以上、好ましくは、約3:25以上、そして、より好ましくは、約3:25から約1:5である。ジエポキシドおよび11,12-エポキシド不純物の両方をH型結晶の調製に使用する場合には、各不純物のエプレレノン出発物質に対する重量比は、一方の不純物だけをH型結晶の調製に用いるときの比率よりも低くなる。
【0095】
選択された不純物を含む溶媒和化合物を脱溶媒すると、通常、H型エプレレノンおよびL型エプレレノンの混合物が得られる。溶媒水和化合物の脱溶媒化を開始して得られる産物に含まれるH型の重量画分は、一般的には、約50%よりも少ない。下で説明するように、この産物をさらに結晶化または温浸によって処理すると、通常、産物中のL型の重量画分が増加する。
【0096】
3.2.播種
H型結晶は、エプレレノンを結晶化する前に、溶媒系に位相が純粋なH型結晶(または、上記で考察したH型成長物質および/またはL型成長阻害物質)を播種することによって調製することもできる。エプレレノン出発物質は、低純度エプレレノンでも、高純度エプレレノンでもよい。いずれかの出発物質から調製してできた溶媒水和化合物を脱溶媒化すると、産物中のH型の重量画分は、一般的に、約70%以上であるが、約100%になることもある。
【0097】
溶媒系に添加するH型の種結晶の出発物質に対する重量比は、一般的には、約0.75:100以上、好ましくは、約0.75:100から約1:20、より好ましくは、約1:100から約1:50である。H型種結晶は、本願において、H型結晶を調製するために検討した方法のいずれによっても調製することができるが、下で説明するような温浸によるH型結晶の調製法によって調製することができる。
【0098】
H型種結晶は、一度に加えたり、何回にも加えたり、または実質的に一定時間にわたって連続して加えることもできる。しかし、H型種結晶の添加は、通常、エプレレノンが溶液から結晶化し始める前に完了している。すなわち、播種は曇点(準安定域の下端)に達する前に完了している。播種は、一般的には、溶液温度が、曇点よりも約0.5℃高い温度から、曇点よりも約10℃高い温度までの範囲で、好ましくは、曇点よりも約2℃から約3℃高い温度のときに行なうことができる。種結晶を加えるときの曇点よりも高い温度を上げると、通常は、H型結晶を結晶化させるために必要となる播種量が増加する。
【0099】
播種は、曇点よりも高い温度であるだけでなく、準安定域の範囲内で行なわれることが好ましい。曇点も準安定域も、エプレレノンの可溶性と、溶媒、または溶媒の混合液中での濃度によって決まる。例えば、メチルエチルケトンの12倍容稀釈液では、準安定域の上端は、通常、約70℃から約73℃であり、準安定域の下端(すなわち曇点)は、通常、約57℃から約63℃である。メチルエチルケトンの8倍濃縮液では、溶液が過飽和状態にあるため、準安定域はさらに狭くなる。この濃度では、溶液の曇点は約75℃から約76℃のところに存在する。大気条件下でメチルエチルケトンの沸点は約80℃であるため、この溶液への播種は、一般的には、約76.5℃と沸点の間で行なう。
【0100】
H型による播種の非制限的な具体例が、本明細書の実施例7に記載されている。
【0101】
H型成長促進物質またはL型成長阻害物質用い、および/またはH型を播種して得られた結晶化エプレレノン産物は、通常、2%以上のH型、好ましくは、5%以上のH型、より好ましくは、7%以上のH型、さらに一層好ましくは、約10%以上のH型を含む。残りの結晶化エプレレノン産物は、通常L型である。
【0102】
3.3.エプレレノンの磨砕によるH型の調製
さらに、別の代替的態様において、エプレレノンを適当に磨砕することによって、少量のH型を調製できることが発見されている。磨砕されたエプレレノンのH型の濃度が3%にもなることが観察されている。
【0103】
4.低純度エプレレノンから調製された溶媒和化合物からのL型の調製
上記したように、溶媒和化合物を生成するための低純度エプレレノンの結晶化と、その後の溶媒和化合物の脱溶媒化によって、通常、H型およびL型の両方を含む産物が回収される。位相が純粋なL型結晶を溶媒系に播種することによって、または、L型成長促進物質および/またはH型成長阻害物質を用いてH型を調製するために上記した方法と実質的に同一の方法で、低純度エプレレノンから、L型含量のより多い産物を調製することができる。播種プロトコール、および、溶媒系に加えられるエプレレノン出発物質の量に対する溶媒系に加えるH型種結晶の量の重量比は、通常、位相が純粋なH型結晶の播種によるH型エプレレノンの調製に関して既に前記したそれらの比率と同じである。
【0104】
このようにして調製した結晶化エプレレノン産物は、通常、、10%以上のL型、好ましくは、50%以上のL型、より好ましくは、75%以上のL型、さらに好ましくは、90%以上のL型、さらに一層好ましくは、約95%以上のL型、なお一層好ましくは、実質的に位相が純粋なH型を含む。
【0105】
H型エプレレノンの調製について、本明細書で説明した播種プロトコールによって、結晶化したエプレレノンの粒子サイズの調節法を改良することもできよう。
【0106】
5.溶液からの直接的なL型結晶化
中間的な溶媒和化合物を形成したり、それに伴う脱溶媒化を行なう必要なしに、適当な溶媒、または溶媒の混合液から直接結晶化することによって、L型エプレレノンを調製することもできる。一般的には、(i)溶媒は、溶媒和化合物の結晶格子の中で利用可能なチャネル間隙に適合しない分子サイズをもつ、(ii)エプレレノンとそれに含まれる不純物は、高温で、溶媒に溶ける、(iii)冷却すると、非溶媒和性のL型エプレレノンの結晶化が起こる。溶媒、または溶媒の混合液におけるエプレレノンの可溶性は、室温で、通常、約5〜200 mg/mlである。溶媒、または溶媒の混合液は、好ましくは、メタノール、酢酸エチル、酢酸イソプロピル、アセトニトリル、ニトロベンゼン、水、およびエチルベンゼンからなる群より選択される一種類以上の溶媒を含む。
【0107】
溶液から直接L型エプレレノンを結晶化するためには、一定量のエプレレノン出発物質を一定量の溶媒に溶解してから、結晶が形成されるまで冷却する。エプレレノンを溶媒に加える溶媒温度は、一般的に、溶媒または溶媒の混合液の溶解曲線に基づいて選択される。本明細書記載の溶媒のほとんどでは、この溶媒温度は、一般的に、約25℃以上であり、好ましくは、約30℃から溶媒の沸点までであり、また、より好ましくは、溶媒の沸点よりも約25℃低い温度から、溶媒の沸点までである。
【0108】
または、加熱した溶媒をエプレレノンに加えて、結晶が形成されるまで混合液を冷却することも可能である。エプレレノンを加える時の溶媒の温度は、一般的に、溶媒または溶媒の混合液の溶解曲線に基づいて選択される。本明細書記載の溶媒のほとんどでは、この溶媒温度は、一般的に、約25℃以上であり、好ましくは、約50℃から溶媒の沸点までであり、また、より好ましくは、溶媒の沸点よりも約15℃低い温度から、溶媒の沸点までである。
【0109】
同様に、一定容量の溶媒と混合するエプレレノン出発物質の量は、溶媒または溶媒の混合液の溶解曲線に依存する。一般的には、溶媒に加えるエプレレノンの量は、室温では完全に溶解されない。本明細書記載の溶媒のほとんどでは、一定容量の溶媒と混合するエプレレノン出発物質の量は、約1.5倍から約4.0倍であり、好ましくは、約2.0倍から約3.5倍であり、より好ましくは、約2.5倍であるが、このエプレレノン量は、該容量の溶媒に室温で溶解する量である。
【0110】
実質的に位相が純粋なL型を含む産物が調製されたことを確認するためには、エプレレノン出発物質は、通常、高純度エプレレノンである。エプレレノン出発物質は、好ましくは、約65%以上の純度、より好ましくは、約90%以上の純度、さらに好ましくは、約98%以上の純度、そして、もっとも好ましくは、約99%以上の純度である。
【0111】
エプレレノン出発物質が溶媒に完全に溶けたら、一般的には、溶液をゆっくりと冷却して、L型エプレレノンを結晶化させる。本明細書記載の溶媒のほとんどでは、溶液を約1℃/分よりも遅い速度で冷却し、好ましくは、約0.2℃/分よりも遅い速度で、より好ましくは、約0.05℃/分から約0.1℃/分の速度で冷却する。
【0112】
L型結晶を回収する終点温度は、溶媒または溶媒の混合液の溶解曲線に依存する。本明細書記載の溶媒のほとんどでは、この終点温度は、一般的に約25℃よりも低く、好ましくは、約5℃よりも低く、より好ましくは、約−5℃よりも低い。
【0113】
または、別の技術を用いてL型エプレレノンの結晶を調製することも可能である。このような技術の例には、(i)エプレレノン出発物質を一つの溶媒に溶かして、L型エプレレノンの結晶化を促進するために共溶媒を加える方法、(ii)L型エプレレノンの蒸気拡散成長法(vapor diffusion growth)、(iii)回転式乾燥などの乾燥法によって、L型エプレレノンを単離する方法、および(iv)懸濁液転換法(slurry conversion)などを含むが、これらに限定されない。
【0114】
上記したようにして調製されたL型エプレレノンの結晶は、濾過または遠心分離など、通常の適当な方法によって溶媒から分離することができる。
【0115】
なお、L型エプレレノンは、高純度エプレレノンをメチルエチルケトンの懸濁液を(後述するようにして)温浸し、この懸濁液の沸点で、温浸されたエプレレノンを濾過することによって調製することができる。
【0116】
6.溶液からのH型の調製
H型およびL型の互変遷移温度(Tt)を超える温度で結晶化を行なうと、特に、H型成長促進物質またはL型成長阻害物質が存在するか、位相が純粋なH型結晶を溶媒に播種すると、H型の方がこのように高い温度では安定しているため、溶液から直接H型が結晶化されるという仮説がたてられている。好適に使用される溶媒系は、ニトロベンゼン等、高沸点溶媒を含む。適当なH型成長促進物質には、上記で定義されたジエポキシドおよび9,11-オレフィン化合物などがあるが、これらに限定されない。
【0117】
7.溶媒によるエプレレノンの温浸
エプレレノンの溶媒和結晶形、H型およびL型は、適当な溶媒または溶媒の混合液の中で、エプレレノン出発物質を温浸することによって調製することもできる。温浸処理では、エプレレノンの懸濁液を、溶媒または溶媒の混合液の沸点で加熱する。例えば、エプレレノン出発物質の一定量を、溶媒、または溶媒の混合液の一定容量と組み合わせて、加熱して還流し、留出物を除去すると同時に追加量の溶媒を加えながら、留出物を除去する。または、温浸処理過程で、より以上の溶媒を加えることなく、留出物を濃縮したり、再利用したりすることもできる。一般的には、溶媒の最初の容量を除去、または濃縮および再利用したところで、懸濁液を冷却して、結晶形を溶媒和する。溶媒和した結晶は、濾過、または遠心分離などの通常の適当な方法によって溶媒から分離することができる。前述したような溶媒和化合物の脱溶媒化によって、溶媒和結晶中に一定の不純物が存在したりしなかったりに応じて、H型またはL型のエプレレノンのいずれかが回収される。
【0118】
適当な溶媒または溶媒の混合液は、一般的に、本明細書において既述した溶媒を一種類以上含む。該溶媒は、例えば、メチルエチルケトンおよびエタノールからなる群より選択することができる。
【0119】
温浸処理に使用される溶媒に添加するエプレレノン出発物質の量は、溶媒または溶媒の混合液の沸点で、懸濁液(すなわち、溶媒または溶媒の混合液中のエプレレノンが完全に可溶化されていない)を維持するのに十分な量である。具体例としては、メチルエチルケトンにおいて約0.25 g/ml、またはエタノールにおいて約0.125 g/mlのエプレレノン濃度が有用であると思われる。
【0120】
溶媒の変換が完了して、エプレレノンの溶媒和結晶形が結晶化されたところで、通常、懸濁液をゆっくりと冷却する。試験した溶媒では、懸濁液を、約20℃/分よりも遅い速度で冷却し、好ましくは、約10℃/分よりも遅い速度で、また、より好ましくは、約5℃/分よりも遅い速度で、さらにより好ましくは、約1℃/分よりも遅い速度で冷却する。
【0121】
溶媒和結晶形を回収する終点温度は、溶媒または溶媒の混合液の溶解曲線に依存する。本明細書記載の溶媒のほとんどでは、この終点温度は、一般的に、約25℃よりも低く、好ましくは、約5℃よりも低く、より好ましくは、約−5℃よりも低い。
【0122】
主に、または専ら、L型が所望であれば、一般的には、高純度エプレレノン出発物質を温浸する。高純度エプレレノン出発物質は、好ましくは、約98%以上の純度、より好ましくは、約99%以上の純度、さらに好ましくは、約99.5%以上の純度である。こうして調製される温浸エプレレノン産物は、通常、10%以上、好ましくは、50%以上、より好ましくは、75%以上、さらにより好ましくは、90%以上、さらにいっそう好ましくは、約95%以上のL型、および、もっとも好ましくは、実質的に位相が純粋なL型である。
【0123】
主に、または専ら、H型が所望であれば、一般的には、低純度エプレレノン出発物質を温浸する。低純度エプレレノン出発物質は、通常、H型を回収するのに必要なだけの量のH型成長促進物質および/またはL型成長阻害物質を含む。低純度エプレレノン出発物質は、好ましくは、約65%以上の純度、より好ましくは、約75%以上の純度、さらに好ましくは、約80%以上の純度である。こうして調製される温浸エプレレノン産物は、通常、10%以上、好ましくは、50%以上、より好ましくは、75%以上、さらにより好ましくは、90%以上、さらにいっそう好ましくは、約95%以上のH型、および、もっとも好ましくは、実質的に位相が純粋なH型である。
【0124】
8.無定形エプレレノンの調製
無定形エプレレノンは、圧搾、磨砕、および/または微粉化などにより、固体を適当に粉砕して、少量で調製することができる。位相が純粋な無定形エプレレノン、すなわち、実質的に結晶化エプレレノンを含まない無定形エプレレノンを、例えば、エプレレノン溶液、特に、エプレレノンの水溶液を凍結乾燥させて調製することができる。本明細書の実施例13および14において、これらの処理過程の具体例を示す。
【0125】
付加的な処理条件
1.熱力学的安定性条件
大気温度では、H型よりもL型の方が熱力学的に安定している。本明細書の実施例5で説明されているように、等量のH型およびL型を含む有機懸濁液を一晩室温放置して、残った固体を回収してX線粉末回折によって分析すると、分析結果は、エプレレノンが完全にL型に転換したことを示した。上記で検討された示差走査熱量測定(DSC)データは、H型の方が融解/分解温度が高いため、高温では、L型よりも熱力学的に安定していることを示している。総合すると、懸濁液転換、およびDSCデータは、低温ではL型がより安定していつつも、H型とL型が互変的に関係している、すなわち、この2種類の多形間での安定性の関係の変化が、互変遷移温度(Tt)付近で起きることを示している。図12は、H型およびL型のエプレレノンのような互変的な関係にある多形で一般的に見られる、ギブス自由エネルギーの温度に対する関係を示している。ここで、IおよびIIは、それぞれH型とL型を意味し、Ttは、遷移温度を意味し、Tmは、H型およびL型の融点を意味し、Lは、液状または融解状態を意味する。
【0126】
したがって、L型を含む組成物を調製する間は、処理温度を遷移温度よりも低く保つことが好ましい。例えば、脱溶媒に用いる乾燥温度は、一般的には、約150℃よりも低く、好ましくは、約125℃よりも低く、より好ましくは、約115℃よりも低く、より好ましくは、約110℃よりも低く、さらにより好ましくは、約80℃から約110℃である。さらに、粒子サイズを減少させる処理工程では、L型結晶の温度を遷移温度よりも低く保つために冷却を行なう(液体窒素を使用するなどして)必要があるかもしれない。
【0127】
2.真性微粉化条件
結晶化エプレレノンを調製するために用いられる方法が、その結果できた結晶形の特性に影響を与えることがある。例えば、溶媒和化合物の脱溶媒によって調製されたL型は、溶液から直接結晶化して調製されたL型よりも、結晶格子内で表面に欠損、孔、亀裂、および破砕を生じやすい。この脱溶媒化結晶の「微粉化」によって、結晶の利用可能な表面積、および結晶の溶解速度の上昇がもたらされる。したがって、脱溶媒によって調製されたL型を選択することによって溶解時間を短縮させることができ、直接の結晶化によって調製されたL型結晶を選択することによって溶解時間を長くすることができ、または、これら以外に、脱溶媒によって調製されたL型と直接の結晶化によって調製されたL型の適当な組合せを選択することによって、溶解時間を調節することができる。
【0128】
脱溶媒によって調製されたL型結晶を薬学的組成物の調製に使用する場合には、真性微粉化によって、処理工程過程で結晶の粒子サイズを小さくする必要を効果的に低下または消失させることもできる。しかしながら、このようなL型結晶を使用することの短所の一つは、直接の結晶化によって調製されたL型結晶ならば必要のない脱溶媒工程が必要になることである。
【0129】
方法限定固体型
本発明の実施態様には、本願において開示された方法にしたがって調製された特異的な固体型エプレレノン、およびそれらを組み合わせたものも含まれる。特に、単独、または一種類以上の別の固体型(本願の記載に従って調製された溶媒和結晶形、L型、および無定形エプレレノン)と組み合わせたものでも、H型エプレレノンが本発明の実施態様である。さらに、脱溶媒によってH型エプレレノンを調製するときの中間体として有用で、本願で示したようにして調製された溶媒和型結晶形が本発明の実施態様である。
【0130】
固体型の組合せ
第一の固形型エプレレノンと第二の固形型エプレレノンを含む組合せで、第一の固形型および第二の固形型エプレレノンが、H型、L型、溶媒和エプレレノン、および無定形エプレレノンから選択される組合せにおいて、第一の固形型と第二の固形型は適当な重量比を用いることができる。通常、このような組合せにおいて、第一の固形型と第二の固形型の重量比は、好ましくは、約1:99から約99:1であり、より好ましくは、約1:9以上であり、より好ましくは、約1:1以上であり、より好ましくは、約2:1以上であり、より好ましくは、約5:1以上であり、もっとも好ましくは、約9:1である。
【0131】
本発明の実施態様によれば、第一の固形型はH型であり、第二の固形型はL型である。
【0132】
別の実施態様では、第三の固体型も存在する。
【0133】
エプレレノンの粒子サイズ
上記した固体型エプレレノンと、それらを組み合わせたものは、広範なエプレレノン粒子サイズを含むことがあり、固体型のエプレレノンの粒子サイズを、約400μmよりも小さなD90粒子サイズになるように削減すると、未処方のエプレレノン、およびこの固形型エプレレノンを含む薬学的組成物の生物利用可能性を向上させ得ることが発見されている。したがって、未処方のエプレレノン、または薬学的組成物調製における出発物質として使用されるエプレレノンのD90粒子サイズは、通常、約400μmよりも小さく、好ましくは、約200μmよりも小さく、より好ましくは、約150μmよりも小さく、さらに好ましくは、約100μmよりも小さく、なおいっそう好ましくは、約90μmよりも小さい。
【0134】
一つの実施態様において、D90粒子サイズは、約25μmよりは小さくない。約25μmから約400μmまでのD90粒子サイズが、通常、ほとんどの目的に許容できる生物利用可能性を有すると認められ、より小さい寸法に粉末化することに伴う費用や環境への排出調節をする必要性が高まることを避けることができる。少なくとも部分的には、H型エプレレノンの溶解速度が速くなることから、このサイズ範囲で許容される生物利用可能性は、特に、実質的なエプレレノン画分がH型エプレレノンとして存在するときに得ることができる。本実施態様による、適当なD90粒子サイズ範囲は、約40〜約100μmである。もう一つの適当な範囲は、約30〜約50μmである。さらに別の適当な範囲は、約50〜約150μmである。さらに別の適当な範囲は、約75〜約125μmである。
【0135】
粉末化、磨砕、微粉化、またはその他、当技術分野において既知の粒子サイズ削減法を用いて、固体エプレレノンを、上で示した所望のサイズ範囲にすることができる。例えば、エアジェットまたは破砕粉末化(fragmentation milling)が、この目的にとっては有効である。
【0136】
費用にはこだわらずに、できるだけ高い生物利用可能性を得ようとするときには、固体型エプレレノンの粒子サイズを約15μmよりも小さなD90粒子サイズに削減すると、未処方のエプレレノン、およびこの固形型エプレレノンを含む薬学的組成物の生物利用可能性を、上で定義したD90粒子サイズ範囲と比較しても、さらに向上させることができることが発見されている。したがって、一つの実施態様において、D90粒子サイズは、約0.01μm(10 nm)から約15μmである。好ましくは、この実施態様において、D90粒子サイズは、約10μmよりも小さく、より好ましくは、約1μmよりも小さく、さらにより好ましくは、約800 nmよりも小さく、さらにいっそう好ましくは、、約600 nmよりも小さく、もっとも好ましくは、約400 nmよりも小さい。応用場面によって、D90粒子サイズの適当な範囲は、約100 nmから約800 nmになる。別の適当な範囲は、約200 nmから約600 nmである。さらに別の適当な範囲は、約400 nmから約800 nmである。さらに別の適当な範囲は、約500 nmから約1μmである。
【0137】
D90粒子サイズが約15μmよりも小さな固体型エプレレノンを、当技術分野において既知で、利用可能な粒子サイズ削減技術にしたがって調製することができる。このような技術には、参照として本明細書に組み入れられる以下の特許および刊行物に記載されている技術があるが、これらに限定されることはない。


【0138】
具体的な処理例では、粗製固体エプレレノンが本質的に不溶でプレミックス懸濁液となるように、粗製固体エプレレノンを液体培地に加える。液体培地におけるエプレレノン濃度は、0.1%から60%まで変えることができるが、好ましくは、重量にして、約5%から約30%である。プレミックス懸濁液のみかけの粘性は、1000 cPよりも低いことが好ましい。
【0139】
このプレミックスは、例えば、ボールミルを用いるなど、エプレレノンのD90粒子サイズを所望の大きさにするために、直接、機械的な装置にかけることができる。または、まず、例えば、回転ミルやコールズ(Cawles)型ミキサーを用いてプレミックスを激しく撹拌し、大きな塊が裸眼で見えなくなって均一な分散液に見えるようにしてから、例えば、培地再循環式ミルを用いるなどして摩滅させる。
【0140】
粒子は、例えば、ポリマーや湿潤剤などの表面修飾剤存在下で粉末化することができる。または、摩滅後、粒子を表面修飾剤と接触させることもできる。表面修飾剤は、粒子が塊になるのを抑えたり、その他の利点をもつ。
【0141】
エプレレノンがあまり分解されない温度下で、粒子の大きさを減少させなければならない。通常は、約30〜40℃よりも低い処理温度が好適である。望ましい場合には、通常の冷却装置によって処理装置を冷却してもよい。本方法は、大気温度、および粉末化処理にとって安全で効果的な処理圧力で適宜行なうことができる。例えば、ボールミル、摩擦ミル、および振動ミルでは、大気圧で処理を行なうのが一般的である。覆いをしたり、氷水の中にミルチャンバーを浸すなどして、温度調節を行うことができる。約0.07から約3.5 kg/cm2までの処理圧力が想定されるが、約0.7から約1.4 kg/cm2という圧力が一般的である。
【0142】
粉末化が完了したら、濾過、メッシュスクリーンなどによる篩など、通常の分離技術を用いて、乾燥して、または液状になって分散している状態の粉末化産物から磨砕用培地を分離する。
【0143】
薬学的組成物
本発明の範囲には、(i)L型エプレレノン、選択的には、H型、溶媒和した結晶形、および無定形のエプレレノンからなる群より選択される、一種類以上のさらに別の固体型エプレレノンをともに含むL型エプレレノン、(ii)一種類以上の薬学的に許容される担体および/または稀釈剤および/またはアジュバント(まとめて「賦形剤」と称する)、および、選択的には、(iii)エプレレノン以外の一種類以上の活性成分を含む薬学的組成物も含まれる。好適な態様においては、組成物に含まれるエプレレノンの全量が本質的に、位相が純粋なL型として存在し、たとえ、固体型を組み合わせたものが存在する場合でも、固体型の重量比が本明細書で上記したものとなっている。
【0144】
または、組成物に含まれるエプレレノンの全量が、本質的に、位相が純粋な溶媒和結晶エプレレノンとして、または無定形エプレレノンとして存在しうる。
【0145】
本発明の別の実施態様において、組成物は、H型とL型の両方を含む。組成物における、H型に対するL型の重量比は、通常、約1:20から約20:1である。別の実施態様では、この重量比は、約10:1から約1:10;約5:1から約1:5;約2:1から約1:2;例示的には、この重量比は1:1でもよい。
【0146】
本発明に係る組成物は、経口経路、口内経路、舌下経路、例えば、血管内、腹膜内、皮下または筋肉内など非経口経路、局所経路、および(例えば、坐薬などの)直腸経路など、適当な経路のいずれにも適合させることができる。これらの組成物は、所望の量のエプレレノンを、所望の投与経路に適した、薬学的に許容される一種類以上の賦形剤とともに含む。
【0147】
1.経口組成物およびその賦形剤
このような組成物の経口投薬用剤形は、好ましくは、希釈剤、崩壊剤、結合剤および接着剤、界面活性剤、潤滑剤および固結防止剤からなる群より選択される一種類以上の賦形剤を含む。より好ましくは、このような経口投薬用剤形は、投与するのに便利なように錠剤にしたりカプセルに詰めたりする。その結果できた錠剤またはカプセルは、例えば、ヒドロキシプロピルメチルセルロース(HPMC)にエプレレノンを分散させて提供することのできるような、即放性処方剤および/または徐放性処方剤を含むことができる。
【0148】
賦形剤を適宜選択および組み合わせることにより、数ある特性の中でも、効能、生物学的利用能、クリアランス時間、安定性、賦形剤に対するエプレレノンの親和性、安全性、溶解プロフィール、分解プロフィールならびに/または他の薬物動態学的特性、化学的特性ならびに/または物理的特性などに関して、効率が改善した組成物を提供することができる。賦形剤は、好ましくは水溶性または水分散性であり、エプレレノンの低水溶度を相殺する湿潤特性をもっている。組成物が錠剤で処方される場合、選択された賦形剤の組合わせは、数ある特性の中で、溶解性もしくは分解性のプロフィール、硬度、破砕強度および/もしくは破砕性において改善を示す錠剤を提供することができる。
【0149】
1.1.希釈剤
本発明の構成物は、選択的に、賦形剤として薬学的に許容される希釈剤を一種類以上含む。適切な希釈剤は、具体的には、以下のものを単独または組み合わせたものがある。すなわち、無水ラクトースおよび一水和ラクトースなどのラクトース;直接圧縮性(directly compressible)デンプンおよびデンプン加水分解物などのデンプン(例えば、登録商標セリュタブ(Celutab)および登録商標エムデックス(Emudex));マンニトール;ソルビトール;キシリトール;デキストロース(例えば、登録商標セレロース2000(Cererose 2000))およびデキストロース一水和物;二塩基性リン酸カルシウム二水和物;スクロース希釈剤;精製糖;一塩基性硫酸カルシウム一水和物;硫酸カルシウム二水和物;顆粒状の乳酸カルシウム三水和物;デキストラン酸;イノシトール;加水分解した固形穀類;アミロース;微結晶化セルロースなどのセルロース;食用α-セルロースおよび無定形セルロース(例えば、商標登録レクセル(Rexcel))ならびに粉末セルロース;炭酸カルシウム;グリシン;ベントナイト;ポリビニルピロリドンなどである。このような希釈剤が存在する場合には、全部で、組成物の全重量の約5%から99%、好ましくは約10%から85%、およびより好ましくは約20%から80%を構成する。選択された希釈剤は、好ましくは、適切な流動特性、また、錠剤が望ましい場合には圧縮性を示す。
【0150】
ラクトースおよび微結晶化セルロースが、単独でも組み合わせても、好ましい希釈剤となる。どちらの希釈剤もエプレレノンと化学的親和性がある。極顆粒状の微結晶化セルロース(すなわち、乾燥過程のあとに、湿った顆粒化組成物に添加した微結晶化セルロース)を、(錠剤のための)硬度および/または分解時間を改善するために用いることができる。ラクトース、特に、ラクトース一水和物が好ましい。ラクトースは、一般的に、比較的希釈剤が低価で、エプレレノンの適切な放出速度、安定性、圧縮前の流動性、および/または乾燥性などの特性を付与する。ラクトースは、(湿式造粒法を用いる場合)造粒中の固化を促進する高密度基質を提供し、その結果、混合物の流動性を向上させる。
【0151】
1.2.崩壊剤
本発明に係る組成物は、特に錠剤として投与するために、選択的に、一種類以上の薬学的に許容される崩壊剤を賦形剤として含む。適切な崩壊剤には、以下のものを単独または組み合わせたものがある。すなわち、グリコール酸ナトリウムデンプン(例えば、パン・ウェスト社(Pan West)の登録商標エクスプロタブ(Exprotab))およびアルファ化コーンスターチ(例えば、登録商標ナショナル(National)1551、登録商標ナショナル(National)1550、および登録商標コロコーン(Colocorn)1550)、粘土(例えば、登録商標ビーガム(Veegum)HV)、精製セルロース、微結晶化セルロース、メチルセルロース、カルボキシメチルセルロースおよびカルボキシメチルセルロースナトリウムなどのセルロース、クロスカルメロースナトリウム(例えば、FMC社の商標登録Ac‐Di‐Sol(Ac-Di-Sol))、アルギン酸、クロスポビドン、ならびに寒天、グアールガム、ローカストビーンガム、カラヤゴム、ペクチンおよびトラガカントガムなどの増粘剤などである。
【0152】
崩壊剤は、組成物を調製する間の適当な工程、特に造粒前の工程、または圧縮処理の前の潤滑処理工程で加えることができる。このような崩壊剤が存在する場合には、全部で、組成物の全重量の約0.2%から30%、好ましくは約0.2%から10%、およびより好ましくは約0.2%から5%を構成する。
【0153】
クロスカルメロースナトリウムは、錠剤またはカプセルを分解するための好適な崩壊剤であり、これがが存在する場合には、好ましくは、全体で、組成物の全重量の約0.2%から30%、より好ましくは約0.2%から7%、およびよりいっそう好ましくは約0.2%から5%を構成する。クロスカルメロースナトリウムは、本発明の顆粒化組成物に優れた顆粒内分解能を与える。
【0154】
1.3.結合剤
本発明に係る組成物は、特に錠剤として投与するために、選択的に、薬学的に許容される一種類以上の結合剤または粘着剤を賦形剤として含む。このような結合剤および粘着剤は、好ましくは、分粒、潤滑、圧縮および包装などの通常の加工作業を可能にするが、摂取されると錠剤が分解して組成物の吸収を可能にするような粘着力を、錠剤処理中の粉末に与える。適切な結合剤および粘着剤には、以下のものを単独または組み合わせたものがあるが、これらに限定されない。すなわち、アラビアゴム;トラガカントガム;ショ糖;ゼラチン;ブドウ糖;アルファ化デンプン(例えば、登録商標ナショナル(National)1551、登録商標ナショナル(National)1550、および登録商標コロコーン(Colocorn)1550)などのデンプン;メチルセルロースおよびカルボキシメチルセルロースナトリウム(例えば、登録商標タイロース(Tylose))などのセルロース;アルギン酸およびアルギン酸塩;ケイ酸マグネシウムアルミニウム;ポリエチレングリコール(PEG);グアールガム;ポリサッカライド酸;ベントナイト;例えば、ポビドンK-15、K-30およびK-29/32のようなポリビニルピロリドン(ポビドンまたはPVP);ポリメタクリル酸;HPMC;ヒドロキシプロピルセルロース(例えば、登録商標クルセル(Klucel));エチルセルロース(例えば、登録商標エトセル(Ethocel))などがあるが、これらに限定されない。このような結合剤および/または粘着剤が存在する場合には、好ましくは、全体で、組成物の全重量の約5.5%から25%、好ましくは、約0.75%から15%、およびより好ましくは、約1%から10%を構成する。
【0155】
HPMCは、エピレレノン処方剤の混合粉末に粘性を与えるために用いるのに好適な結合剤である。HPMCが存在する場合には、好ましくは、全体で、組成物の全重量の約0.15%から10%、好ましくは、約1%から8%、およびより好ましくは、約2%から4%を構成する。粘度が約2 cP(センチポイズ)から6 cP、特に粘度が約2 cPから4 cPが好ましいが、一般的には、約2 cPから8 cPの粘度をもつ低分子量HPMCが用いられる。HPMCの粘度は、20℃で2パーセント水溶液として測定される。HPMCのメトキシ基含有量は、一般的に約15%から約35%であり、一方、ヒドロキシプロピル含有量は、一般的には、最大約15%まで、好ましくは最大約12%である。
【0156】
1.4.湿潤剤
エピレレノンは、水溶液中でおおむね不溶である。したがって、本発明に係る組成物は、選択的にではあるが、好ましくは、一種類以上の薬学的に許容される湿潤剤を賦形剤として含む。このような湿潤剤は、好ましくは、エピレレノンを水になじませておくために、すなわち組成物の相対的生物利用可能性が向上すると考えられている状態を維持するために選択される。
【0157】
本発明に係る組成物において湿潤剤として用いることのできる界面剤の制限的でない例には以下のものがある。例えば、塩化ベンズアルコニウム、塩化ベンズエトニウムおよび塩化セチルピリジニウムなどの第4アンモニア化合物、ジオクチルスルホサクシン酸ナトリウム、例えば、ノンオキシノール9、ノンオキシノール10およびオクトキシノール9などのポリオキシエチレンアルキフェニルエーテル、ポルオキサマー(ポリオキシエチレンおよびポロオキシプロピレンのブロック共重合体)、例えば、ポリオキシエチレン(8)カプリルモノグリセリドおよびジグリセリド(例えば、ガットフォセ社(Gattefosse)のラブラゾル(Labrasol))、ポリオキシエチレン(35)、ひまし油およびポリオキシエチレン(40)硬化ひまし油などのポリオキシエチレン脂肪酸グリセリドおよびポリオキシエチレン脂肪酸グリセリド油;例えば、ポリオキシエチレン(20)セトステアリルエーテルなどのポリオキシエチレンアルキルエーテル、例えば、ステアリン酸ポリオキシエチレン(40)などのポリオキシエチレン脂肪酸エステル、例えば、ポリソルベート20およびポリソルベート80(ICI社の登録商標トゥイーン(Tween))などのポリオキシエチレンソルビタンエステル、例えば、ラウリン酸プロピレングリコール(例えば、ガットフォセ社(Gattefosse)の登録商標ラウログリコール(Lauroglycol))などのプロピレングリコール脂肪酸エステル、ラウリル硫酸ナトリウム、例えば、オレイン酸、オレイン酸ナトリウムおよびオレイン酸トリエタノールアミンなどの脂肪酸およびその塩、例えば、モノステアリン酸グリセリンなどのグリセリル脂肪酸エステル、例えば、ソルビタンモノラウレート、ソルビタンモノオレエート、ソルビタンモノパルミテートおよびソルビタンモノモノステアレートなどのソルビタンエステル、チロキサポールおよびその混合物などである。このような湿潤剤が存在する場合には、好ましくは、全体で、組成物の全重量の約0.25%から15%、好ましくは約0.4%から10%、およびより好ましくは約0.5%から5%を構成する。
【0158】
陰イオン界面活性剤である湿潤剤が好ましい。ラウリル硫酸ナトリウムが特に好ましい湿潤剤である。ラウリル硫酸ナトリウムが存在する場合には、好ましくは、全体で、組成物の全重量の約0.25%から7%、より好ましくは約0.4%から4%、およびよりいっそう好ましくは約0.5%から2%を構成する。
【0159】
1.5.潤滑剤、流動促進剤および固結防止剤
本発明に係る組成物は、選択的に、一種類以上の薬学的に許容される潤滑剤および/または流動促進剤を賦形剤として含む。適当な潤滑剤および/または流動促進剤には、以下のものを単独または組み合わせたものがある。すなわち、グリセリルビハペート(glyceryl behapate)(例えば、登録商標コンプリトール(Compritol)888);ステアリン酸マグネシウム、ステアリン酸カルシウムおよびステアリン酸ナトリウムなどのステアリン酸およびその塩;硬化植物油(例えば、登録商標ステロテックス(Sterotex));コロイド状シリカ;タルク;蝋;ホウ酸;安息香酸ナトリウム;酢酸ナトリウム;フマル酸ナトリウム;塩化ナトリウム;DL-ロイシン;ポリエチレングリコール(登録商標カーボワックス(Carbowax)4000および登録商標カーボワックス(Carbowax)6000);オレイン酸ナトリウム;ラウリル硫酸ナトリウム;ならびにラウリル硫酸マグネシウム。このような潤滑剤および/または流動促進剤が存在する場合には、好ましくは、全体で、組成物の全重量の約0.1%から10%、より好ましくは約0.2%から8%、およびよりいっそう好ましくは約0.25%から5%を構成する。
【0160】
ステアリン酸マグネシウムが、例えば、、錠剤処方剤の圧縮中に生じる、装置と顆粒混合物との間の摩擦を減らすために用いる。好ましい潤滑剤である。
【0161】
適切な固結防止剤には、タルク、DL-ロイシン、コーンスターチ、ラウリル硫酸ナトリウムおよび金属ステアリン酸がある。タルクは、例えば、装置の表面への処方の付着を減らしたり、また、混合物の静電気を減らしたりするのに用いる、好ましい固結防止剤または流動促進剤である。タルクが存在する場合には、好ましくは、全体で、組成物の全重量の約0.1%から10%、より好ましくは約0.2%から5%、およびよりいっそう好ましくは約0.5%から2%を構成する。
【0162】
1.6.他の賦形剤
着色料、香料、甘味料などの他の賦形剤が製薬技術分野において既知であり、本発明の組成物中に使用することができる。錠剤は、例えば、腸溶コーティングなどでコーティングしたり、コーティングしなかったりすることができる。本発明に係る組成物は、さらに、例えば、緩衝剤などを含むことがある。
【0163】
1.7.好適な経口用組成物
一つの実施態様において、本発明に係る組成物は、所望量のエプレレノン、および一種類以上のセルロース賦形剤を含む。「セルロース賦形剤」とは、セルロースまたはそれの誘導体を含む賦形剤を包含し、精製セルロース、微結晶化セルロース、アルキルセルロースおよびそれらの誘導体と塩(例えば、メチルセルロース、エチルセルロース、ヒドロキシプロピルセルロース、HPMC、カルボキシメチルセルロース、クロスカルメロースナトリウムなどのカルボキシメチルセルロースナトリウム)など。好ましくは、このように存在するセルロース賦形剤の少なくとも一種類は、(C1-6アルキル)セルロース、およびそれらの誘導体と塩からなる群より選択される。さらにより好ましくは、このセルロース賦形剤は、ヒドロキシ(C2-4アルキル)-(C1-4アルキル)-セルロース、およびそれらの誘導体と塩からなる群より選択される。
【0164】
本実施態様の組成物は、好ましくは、さらに、希釈剤、崩壊剤、結合剤、湿潤剤、潤滑剤および固結防止剤からなる群より選択される一種類以上の賦形剤を含む。より好ましくは、これらの組成物は、ラクトース、微結晶化セルロース、クロスカルメロースナトリウム、HPMC、ラウリル硫酸ナトリウム、ステアリン酸マグネシウム、およびタルクからなる群より選択される一種類以上の賦形剤を含む。よりいっそう好ましくは、これらの組成物は、ラクトース一水和物、微結晶化セルロース、クロスカルメロースナトリウム、およびHPMCを含み、もっとも好ましくは、さらに、ラウリル硫酸ナトリウム、ステアリン酸マグネシウム、およびタルクからなる群より選択される一種類以上の別の賦形剤を含む。
【0165】
本実施態様において、上記した各賦形剤は、所望であれば、選択的に、他の適当な賦形剤に代えることができる。許容できる代替賦形剤は、エプレレノンともその他の賦形剤とも化学的に親和性のあるものである。これ以外の希釈剤、崩壊剤、結合剤および接着剤、湿潤剤、潤滑剤、および/または固結防止剤、または滑動剤(glindant agent)を用いることができるが、ナノ粒子エプレレノン、ラクトース、微結晶化セルロース、クロスカルメロースナトリウム、およびHPMC、さらに、選択的には、ラウリル硫酸ナトリウム、ステアリン酸マグネシウム、および/またはタルクを含む組成物が、通常、この種の他の組成物に較べて、薬物動態学上、化学的に、および/または物理上優れた特性の組合せである。
【0166】
別の実施態様において、本発明に係る組成物は、
約1%から約95%のエプレレノン、
約5%から約99%の薬学的に許容される希釈剤、
約0.5%から約30%の薬学的に許容される崩壊剤、および
約0.5%から約25%の薬学的に許容される結合剤を含むが、これらの割合はすべて重量単位である。このような組成物は、選択的に、さらに、約0.25%から約15%の薬学的に許容される湿潤剤;約0.1%から約10%の薬学的に許容される潤滑剤;および/または約0.1%から約15%の薬学的に許容される固結防止剤を含むことができる。
【0167】
さらに別の実施態様において、本発明に係る組成物は、好ましくは、錠剤またはカプセルであり、エプレレノン、および上記定義によるセルロース賦形剤を含んだ経口投薬剤形にある。好ましくは、該組成物は、ラクトース一水和物、微結晶化セルロース、クロスカルメロースナトリウム、ヒドロキシプロピルメチルセルロース、ラウリル硫酸ナトリウム、ステアリン酸マグネシウム、およびタルクからなる群より選択される一種類以上の賦形剤を含む。
【0168】
2.非経口用組成物
本発明に係る固体型エプレレノンは、例えば、食塩水、デキストロース溶液または水などの担体液中の固体エプレレノンの懸濁液を、例えば、静脈内、筋肉内、または皮下などの注射によって非経口的に投与することができる。懸濁組成物は、本明細書で経口用組成物について開示したものから選択される適当な賦形剤成分を含むことができる。
【0169】
3.経皮用組成物
例えば、約0.75%から約30%、好ましくは、重量で約0.2%から約20%、より好ましくは、重量で約0.4%から約15%の量の固体エプレレノンが分散している、局所用または経皮用軟膏またはクリームの形にすることができる。このような局所用または経皮用組成物は、望ましくは、エプレレノンが皮膚に吸収または貫通することを促進する組成物を含む。このような皮膚透過促進化合物は、ジメチルスルホキシドおよびその関連化合物を含む。
【0170】
新規の固体型エプレレノンは、貯蔵容器または多孔性メンブレン型または固体マトリックス型のいずれかのパッチを用いて経皮的に投与することができる。どちらの場合にも、エプレレノンは、貯蔵容器から、または微小カプセルから、メンブレンを通って、対象者の皮膚または粘膜に接触しているエプレレノン透過接着剤の中に連続的に輸送される。エプレレノンが皮膚を通って吸収されると、制御されかつ予め決められたエプレレノンの流れがレシピエントに投与される。微小カプセルの場合には、カプセル化剤がメンブレンの働きをすることもできる。
【0171】
治療または予防の方法
本発明は、アルドステロンを媒介とする状態または疾患の治療および/または予防のための方法であって、治療効果を有する量の固体エプレレノンまたは固体エプレレノンを含む医薬組成物を用いて、少なくとも、L型エプレレノンおよび他に一つまたは複数のH型エプレレノン、溶媒和した結晶エプレレノンおよびアモルファスエプレレノンを含む検出可能な割合の固体エプレレノンを用いて、このような状態または疾患を持つまたは生じやすい被検者を治療する工程を含む方法を含む。このような方法は、アルドステロンアンタゴニストの投与を必要とする被検者において、状態または疾患の治療および/または予防のために有用であり、このような治療には、高血圧、心不全を含む心臓疾患、肝硬変、過剰なコラーゲン、線維症、良性前立腺肥大およびうつ病といった高アルドステロン症の状態の治療が含まれるが、それに限らない。
【0172】
ヒトの治療に有用である上に、これらの固体状エプレレノンおよびその医薬組成物は、コンパニオンアニマル、外来性の動物および家畜、例えば、ウマ、イヌおよびネコの獣医学的治療にも有用である。
【0173】
固体状エプレレノンおよびその医薬組成物は、(i)他のアルドステロン受容体アンタゴニストの部分的な、または、完全な代わりとして組み合わせ治療において、および/または、(ii)他の薬剤との組み合わせ治療において用いることもできる。「組み合わせ治療」とは、薬剤の組み合わせの有益な効果を提供する投薬計画において、それぞれの薬剤を順次投与することを含み、同様に、薬剤を実質的に同時に共同して投与すること、例えば、これらの作用物質を固定された比で含む単独のカプセルまたは注射剤において、または、一つにつき一つの物質を含む複数の別々の投与形態または注射剤において投与することも含む。このような併用療法の非限定的な例には、国際公開公報第96/24373号に記載されているような、アルドステロンレセプター拮抗薬とアンギオテンシンIIレセプター拮抗薬を併用して用いる、心臓血管疾患の治療法、国際公開公報第96/40257号に記載されているような、アルドステロンレセプター拮抗薬とアンギオテンシンIIレセプター拮抗薬を併用して用いる、鬱血性心臓疾患の治療法、および、国際公開公報第96/24373号に記載されているような、アルドステロンレセプター拮抗薬、ACEインヒビター、および利尿剤を併用して用いる、心臓疾患の治療法があり、これらの刊行物はすべて、参照として本明細書に組み入れられる。
【0174】
実施例
以下の実施例は、本明細書に記載したエプレレノンの様々な固相状態の調製方法の詳細な説明を含む。これらの詳細な説明は、本発明の範囲に含まれ、その範囲を如何なるようにも制限することなく本発明を説明する。百分率は、特に明記していない限り、全て重量である。以下の実施例のそれぞれにおいて用いられるエプレレノン開始材料は、先に引用した国際公開公報第98/25948号に記載のスキーム1に従って調製した。
【0175】
実施例1:高純度エプレレノン開始材料からのメチルエチルケトン溶媒和化合物の調製と溶媒和化合物からのL型エプレレノンの調製
A. メチルエチルケトン溶媒和化合物の調製
高純度エプレレノン(純度>99%で、ジエポキシドおよび11,12-エポキドの全量が<0.2%)437 mgを、900 rpmで磁石攪拌子によって攪拌しながらホットプレート上で沸騰するまで加熱することによって、メチルエチルケトン10 mlに溶解した。得られた溶液を、磁石攪拌子によって絶えず攪拌しながら室温まで冷却した。室温に達した後、溶液を1℃の水浴に移して1時間攪拌する。冷溶液から固体のメチルエチルケトン溶媒和化合物を真空濾過によって回収した。
【0176】
B. L型エプレレノンの調製
上記のように調製した固体メチルエチルケトン溶媒和化合物を、100℃の炉の中で大気圧で4時間乾燥させた。乾燥した固体は、DSCおよびXRPD分析によって純粋なL型であると決定された。
【0177】
実施例2.高純度エプレレノン開始材料からのさらなる溶媒和化合物の調製
メチルエチルケトンを以下の溶媒のそれぞれに置換することによって、さらなる溶媒和結晶型を実質的に実施例1に記載のように調製した:n-プロパノール、2-ペンタノン、酢酸、アセトン、酢酸ブチル、クロロホルム、エタノール、イソブタノール、酢酸イソブチル、イソプロパノール、酢酸メチル、プロピオン酸エチル、n-ブタノール、n-オクタノール、酢酸プロピル、プロピレングリコール、t-ブタノール、テトラヒドロフラン、およびトルエン。
【0178】
実施例3:気相拡散成長によるメチルエチルケトン溶媒和化合物の調製
エプレレノン(純度>99.9%)400 mgを、ホットプレート上で加温することによってメチルエチルケトン20 mlに溶解して、保存液を調製した。保存液8mlをメチルエチルケトン10 mlで希釈して、得られた溶液を80%希釈試料と呼ぶ。保存液4 mlを、メチルエチルケトンで10 mlで希釈した(40%希釈試料)。保存液2 mlをメチルエチルケトン10 mlで希釈した(20%希釈試料)。20 mlシンチレーションバイアルに入った様々な希釈試料を、抗溶媒として少量のヘキサンを含むデシケータ瓶に移した。デシケータ瓶を密封して、ヘキサン蒸気をメチルエチルケトン溶液に拡散させた。エプレレノンのメチルエチルケトン溶媒和化合物の結晶は、80%希釈試料において24時間以内に成長した。
【0179】
実施例4.ロータリー・エバポレーターによるエプレレノンの溶媒和化合物結晶型の調製
エプレレノン(純度>99.9%)約400 mgを250 ml丸底フラスコに計り取った。メチルエチルケトンおよび実施例2に記載した溶媒から選択される溶媒150 mlをフラスコに加え、必要であれば、エプレレノンが溶解するまで溶液を緩く加熱する。得られた透明な溶液を、85℃の水浴を備えたブッキロータリーエバポレーターに入れて、溶媒を真空で除去した。溶媒約10 mlがフラスコに残った時点で、溶媒除去を停止する。得られた固体を、結晶型の決定のために適当な方法(例えば、XRPD、DSC、TGA、顕微鏡等)によって分析する。
【0180】
実施例5:スラリーの変換
L型エプレレノン約150 mgおよびH型エプレレノン150 mgを酢酸エチル5 mlに加えた。得られたスラリーを300 rpmで磁石攪拌子によって一晩攪拌した。翌日、得られた固体の試料を濾過によって回収した。XRPDによる試料の分析から、試料が完全にL型エプレレノンで構成されていることが示された。
【0181】
実施例6:(a)低純度エプレレノン開始材料からの溶媒和化合物の調製および(b)得られた溶媒和化合物からのH型結晶エプレレノンの調製
本明細書に記載した様々な量のジエポキシド、または11,12-エポキシド不純物を含む試料は、不純物の所望の量を、総試料塊が100 mgとなるために十分なエプレレノンの量と共に7 mlシンチレーションバイアルに加えることによって調製した。それぞれの試料中の不純物の含有量を表6Aおよび6Bに示し、不純物はそれぞれジエポキシドまたは11,12-エポキシドである。それぞれのシンチレーションバイアルに、メチルエチルケトン1 mlと共に微小磁石攪拌子を加えた。バイアルに緩くキャップをして、固体をホットプレート上で磁石攪拌子によって攪拌しながら加熱還流して溶解した。溶解が完了すれば、得られた溶液を絶えず攪拌しながら室温まで冷却した。次に、得られた固体を真空濾過によって回収して、XRPDによって直ちに分析した。次に固体を100℃の炉に入れて、大気圧で1時間乾燥した。乾燥した固体のH型含有量を、約12.1゜2θでのH型回折ピークの面積をモニターすることによって、XRPDによって分析した。XRPD回折パターンは全て、アイネル多目的回折計を用いて記録した。
【0182】
【表6A】

実施例6におけるエプレレノン原料の組成
【表6B】

実施例6におけるエプレレノン開始材料の組成
【0183】
A.ジエポキシドの結果
図13は、(a)0%、(b)1%、(c)3%および(d)5%ジエポキシドを処理したメチルエチルケトン結晶から得られたメチルエチルケトン溶媒和化合物の湿ケークのXRPDパターンを示す。ピーク強度は比較を容易にするために標準化した。H型またはジエポキシドに特徴的なピークは回折パターンに存在しない。パターンは、エプレレノンのメチルエチルケトン溶媒和化合物の特徴を示す。
【0184】
図14は、(a)0%、(b)1%、(c)3%および(d)5%ジエポキシドを処理したメチルエチルケトン結晶から得られた乾燥固体のXRPDパターンを示す。ピーク強度は比較を容易にするために標準化した。ジエポキシド処理レベルが0%または1%である場合、メチルエチルケトン結晶に対応する乾燥試料中にH型は検出されなかった。処理レベルが3%または5%である場合、メチルエチルケトン結晶に対応する乾燥試料中にH型を検出した。各試料について約12.1゜2θでのH型回折ピーク面積およびH型推定含有量を表6Cに示す。
【表6C】

実施例6におけるメチルエチルケトン結晶からのデータ
【0185】
表6Cに報告した結果から、ジエポキシドの存在は溶媒除去の際のH型エプレレノンの形成に影響を及ぼすことが確認される。H型の形成は、ジエポキシドがメチルエチルケトン溶媒和化合物結晶に組み入れられたおよび/または吸着された場合に誘導される。
【0186】
第二の3%ジエポキシド処理実験を行って、溶媒除去の際に形成されたH型の量に及ぼす調製経路の影響を分析した。この実験では、処理した結晶から得られたエチルメチルケトン溶媒和化合物を2つの部分に分けた。第一の部分は無処置のままであり、第二の部分は、乳鉢と乳棒で軽くすりつぶして、より高いレベルの結晶のきずを誘導した。2つの部分はいずれも100℃の大気圧で1時間乾燥させた。乾燥した固体をXRPDによって分析した。乾燥前に溶媒和化合物を(a)すりつぶさない場合および(b)すりつぶした場合のジエポキシドの3%処理による、メチルエチルケトン結晶からの乾燥固体に関して、XRPDパターンを図15に示す。XRPDパターンによって、すりつぶしていない試料と比較してすりつぶした試料ではH型の量がより多いことが示された。これらの結果は、メチルエチルケトン溶媒和化合物を単離して取り扱う条件が、溶媒除去によって得られた結晶型に影響を及ぼしうることを示唆している。
【0187】
B.11,12-エポキシドの結果
図16は、(a)0%、(b)1%、(c)5%および(d)10%11,12-エポキシド処理メチルエチルケトン結晶から得られたメチルエチルケトン溶媒和化合物湿ケークのXRPDパターンを示す。ピーク強度は比較を容易にするために標準化した。H型または11,12-エポキシドに特徴的なピークは回折パターンに存在しない。パターンは、エプレレノンのメチルエチルケトン溶媒和化合物の特徴を示す。
【0188】
図17は、(a)0%、(b)1%、(c)5%および(d)10%11,12-エポキシドを処理したメチルエチルケトン結晶から得られた乾燥固体のXRPDパターンを示す。ピーク強度は比較を容易にするために標準化した。11,12-エポキシド処理レベルが0%、1%または5%である場合、メチルエチルケトン結晶に対応する乾燥試料中にH型は検出されなかった。11,12-エポキシド処理レベルが10%である場合、メチルエチルケトン結晶に対応する乾燥試料中にH型を検出した。各試料について約12.1゜2θでのH型回折ピーク面積およびH型推定含有量を表6Dに示す。
【表6D】

実施例6におけるメチルエチルケトン結晶からのデータ
【0189】
表6Dに報告した結果は、11,12-エポキシドの存在が溶媒除去の際のH型エプレレノンの形成に影響を及ぼすことを確認する。H型エプレレノンの形成を誘導するために必要なメチルエチルケトン結晶中の不純物のレベルは、11,12-エポキシドではジエポキシドの場合より大きいように思われる。
【0190】
実施例7:最終結晶型に及ぼす結晶化と乾燥の影響
最終結晶型に及ぼす結晶化と乾燥の影響を分析する以下の4つの実験を実施した:(i)エプレレノンのメチルエチルケトン結晶(実験の23+3統計デザイン)、(ii)低品質母液残査の結晶化、(iii)H型シード添加による高純度エプレレノンの結晶化、および(iv)L型シード添加による低純度エプレレノンの結晶化。これらの実験における変数には、冷却速度、開始材料純度レベル、および結晶化のエンドポイント温度が含まれた。この実施例の目的に関して、高純度エプレレノンは、超純粋(HPLCによる)粉砕エプレレノンとして定義し、低純度エプレレノンは純度89%のエプレレノンとして定義した。低純度エプレレノンを調製するために、エプレレノンの調製のためのプロセスから得られる結晶除去後の母液を分析して、61.1%エプレレノン、12.8%ジエポキシドおよび7.6%11,12-エポキシドである材料を生成するように混和した。次に、この材料を高純度エプレレノンの十分量と混和すると、89%エプレレノンが得られた。
【0191】
A.メチルエチルケトンの結晶化
メチルエチルケトン結晶化実験において、全ての実験は高純度エプレレノン60 gを用いて実施した。高エンドポイントは45℃として定義し、低エンドポイントは5℃として定義した。高冷却速度は3℃/分として定義し、低冷却速度は0.1℃/分として定義した。中心点は、冷却速度1.5℃/分、エプレレノンの純度94.5%、およびエンドポイント25℃であった。
【0192】
FTIRについてバックグラウンドの読みとりを行った後、メチルエチルケトン250 mlを1LのメトラーRC-1、MP10リアクターに加えて、100 rpmで攪拌した。数回スキャンした後、エプレレノンをリアクターに加えた後、メチルエチルケトン470 mlをさらに加えた。攪拌を500 rpmに増加させて、固体を懸濁させて、バッチ温度を80℃に上昇させた。エプレレノンを確実に溶解させるため、バッチ温度を80℃で保持した。得られた透明な溶液中に、黒または白色の斑点が一般的に見えた。次に、バッチ温度を所望の速度で所望のエンドポイントまで徐々に冷却することによって低下させ、この温度を1時間維持してから、移動用フラスコに入れて濾過すると湿ケークが得られた。次に、リアクター、移動用フラスコおよび湿ケークをメチルエチルケトン120 mlで洗浄した。それぞれの湿ケーク約10 gを、公称条件75℃で軽く窒素を抽気して真空で乾燥させた。湿ケークを高および低条件で流動床乾燥によって乾燥させた。流動層乾燥の高条件は、100℃で送風機の設定を4として定義し、低条件は40℃で送風機の設定を1として定義した。
【0193】
B.低品質母液残査の結晶化
低品質母液残査の結晶化を含む実験において、純度61.1%のエプレレノン60 gおよびメチルエチルケトン720 mlを、1LメトラーRC-1、MP10リアクターに直接加えた。不純物含有エプレレノンは、リアクターに加える前に、高純度エプレレノンと混和しなかった。得られた混合物を80℃に加熱すると、その温度では不透明なスラリーが得られた。結晶化を継続して、混合物を速い冷却条件で45℃で濾過した。
【0194】
C.H型のシード添加
H型シード添加実験において、高純度エプレレノン60 gおよびメチルエチルケトン720 mlを1LメトラーRC-1、MP10リアクターに加えた。混合物を80℃に加熱した後、冷却速度1.5℃/分で25℃に冷却した。溶液が62℃まで冷却されると、相純粋なH型結晶3 gをシード添加して、結晶化を開始させた。H型シード結晶は、下記の実施例9に説明する温浸プロセスによって調製した。
【0195】
D.L型のシード添加
L型シード添加実験において、89.3%エプレレノン66.6 g(高純度エプレレノン48.3 gと61.1%エプレレノン18.3 gの混合によって調製)およびメチルエチルケトン720 mlを1LメトラーRC-1、MP10リアクターに加えた。混合物を80℃に加熱した後、冷却速度1.5℃/分で25℃に冷却した。溶液が63℃に冷却されると、相純粋なL型結晶3 gをシード添加して、結晶化を開始させた。L型シード結晶は、上記の実施例1に説明する結晶化および溶媒除去プロセスによって調製した。
【0196】
E.結果
実験結果を表7Aに報告する。
【0197】
メチルエチルケトン結晶化実験において、H型はジエポキシドを含む低純度エプレレノンを用いた場合に限って検出された。最終産物におけるジエポキシドレベルの上昇も同様に、より高い冷却速度の場合に認められた。
【0198】
低品質母液残査の結晶化を含む実験は、XRPDによって分析するとジエポキシドとH型エプレレノンの混合物であるように思われる低品質材料を生成した。
【0199】
H型シード添加実験(高純度エプレレノンにH型のシードを添加した)は、XRPD分析に基づいてH型77%であるが、DSCに基づくと完全にH型である産物を生じた。しかし、XRPDモデルは、H型が約15%を超えた場合の直線性に関して試験していなかった。この実験は、ジエポキシドの非存在下でH型が形成されたこの実施例の4つの実験の唯一のものであった。
【0200】
L型シード添加実験(低純度エプレレノンにL型のシードを添加した)は、完全にL型である産物を生成した。
【0201】
エプレレノンの高条件流動床乾燥から得られたデータは、真空炉乾燥の場合に得られたデータに対応するように思われた。低条件流動床乾燥は、真空炉乾燥の場合とは異なる結果を生じた。
【0202】
【表7A】

実施例7の結果
1 75℃の真空炉で溶媒和化合物を乾燥後の重量%。
2 XRPDによって分析するとH型とジエポキシドとの混合物であるように思われる。
3 XRPDではH型77%、DSCではH型100%であるように思われる。
ND=検出されない
【0203】
F.材料の純度
表7Aで報告したデータに基づく材料の純度、開始材料の純度、冷却速度およびエンドポイント温度の立方プロットを図18に示す。立方プロットは、結晶化開始時に高純度材料を用いれば、より純度の高い産物を生成することを示唆している。結晶化のエンドポイント温度は、産物の純度に大きい影響を及ぼさないように思われる。しかし、冷却速度は何らかの作用を有するように思われ、冷却速度がより速ければ得られた産物の純度はわずかに低い。実際に、ジエポキシドのレベルは一般的に、冷却速度が速ければ高かった。
【0204】
図19は、変数が、もしあるとすれば産物の純度に統計学的に有意な影響を及ぼすか否かを決定するために、立方プロットの結果を用いて調製した半正常プロットを示す。開始材料の純度は産物の純度に対して最大の統計学的に有意な影響を及ぼしたが、冷却速度の影響と、冷却速度と開始材料純度のあいだの相互作用も同様に統計学的に有意であると見なされた。
【0205】
図20は、これらの結果に基づく相互作用グラフであり、産物の純度に及ぼす開始材料純度と冷却速度との相互作用を示している。エプレレノンの純度が高ければ、冷却速度は最終的な純度にほとんどまたは全く影響を及ぼさないように思われる。しかし、エプレレノンの純度が低ければ(89.3%エプレレノン開始材料)、産物の純度は冷却速度が増加するにつれて減少する。この結果は、結晶化をより速い冷却速度で実施すると、より多くの不純物が結晶化することを示唆している。
【0206】
G.H型の含有量
表7Aにおいて報告したデータに基づくH型重量分画、開始材料産物純度、冷却速度およびエンドポイントデータの立方プロットを図21に示す。立方プロットは、結晶化開始時に高純度のエプレレノンを用いれば、H型の量は少なくなることを示唆している。結晶化のエンドポイント温度は、最終生成物の型に影響を及ぼすように思われる。冷却速度はH型の形成に大きく影響を及ぼさないように思われるが、いくつかのH型は、不純物が存在する場合の低エンドポイント温度でのより速い冷却の結果であるかも知れない。
【0207】
図22は、変数が、もしあるとすれば、最終材料におけるH型の量に統計学的に有意な影響を及ぼすか否かを決定するために、立方プロットの結果を用いて調製した半正常プロットを示す。開始材料の純度、結晶化のエンドポイント温度、およびこれらの2つの変数の相互作用は、統計学的に有意な作用であると見なされた。
【0208】
図23は、これらの結果に基づく相互作用グラフであり、最終的なH型含有量に及ぼす開始材料純度とエンドポイント温度のあいだの相互作用を示す。高純度エプレレノンを用いると、エンドポイント温度はH型含有量にほとんど影響を及ぼさないように思われる。いずれの場合でも純粋なエプレレノンを用いれば、H型は生成されなかった。低純度エプレレノン(89.3%エプレレノン開始材料)では、H型は双方の場合について存在し、より高いエンドポイント温度では有意により多くのH型が存在した。
【0209】
表7Bは、流動床(ラブライン・P.R.L.、高速流動床乾燥器、ラブラインインストルメンツインク)または真空炉(バクスター・サイエンティフィックプロダクツ真空乾燥炉、モデルDP-32)のいずれかを用いて乾燥させた材料において測定したH型の重量分画を報告する。高速流動床または真空炉のいずれにおいても、乾燥させた同等の材料について類似のH型含有量を認めた。しかし、真空炉の場合と比較して低速流動床で乾燥させた同等の材料については差を認めた。
【0210】
【表7B】

H型含有量に及ぼすプロセス変数の影響
ND=検出されない
【0211】
実施例8:溶媒除去の際のメチルエチルケトンからのL型の結晶化
H型エプレレノン10 gをメチルエチルケトン80 mlと混合した。混合物を加熱還流して(79℃)室温で約30分攪拌した。スラリーを65℃、50℃、35℃、および25℃で、それぞれの温度で約90分維持することによる段階的なホールドポイントプロトコールによって、得られたスラリーを冷却した。スラリーを濾過して、メチルエチルケトン約20 mlによってすすいだ。得られた単離固体を濾紙上で乾燥させた後、40〜50℃の真空炉で乾燥させた。乾燥は90〜100℃の真空炉で完了させた。溶媒除去した固体は回収率82%で得られた。XRPD、MIRおよびDSCによって、固体がL型結晶構造を有することを確認した。
【0212】
実施例9:低純度エプレレノン開始材料の溶媒による温浸によりH型を生成する
A.エタノール溶媒による温浸
低純度エプレレノン(HPLCアッセイによって64%)24.6 gをエタノール3A 126 mlと混合した。スラリーを加熱還流して、留出物を除去した。溶媒126 mlを大気圧蒸留によって除去すると同時にエタノール3A 126 mlをさらに加えた。溶媒の交換が終了した後、混合物を25℃に冷却して、1時間攪拌した。得られた固体を濾過してエタノール3Aによってすすぎ、風乾させて、エタノール溶媒和化合物を生成した。溶媒和化合物を90〜100℃の真空炉でさらに6時間乾燥させると、H型エプレレノン14.9 gが得られた。
【0213】
B.メチルエチルケトン溶媒による温浸
もう一つの温浸プロセスにおいて、低純度エプレレノン1 g(約65%アッセイ)をメチルエチルケトン4 ml中で2時間温浸し、その後、混合物を室温に冷却した。冷却後、得られた固体を真空濾過によって回収して、XRPD分析によってメチルエチルケトン溶媒和化合物であると決定した。固体を100℃で30〜60分乾燥させた。乾燥した固体はXRPDによって純粋なH型であると決定された。
【0214】
実施例10:高純度エプレレノンの溶媒による温浸によりL型を調製する
A.エタノール溶媒による温浸
高純度エプレレノン1 gをエタノール8 mlに約2時間温浸した。次に溶液を室温まで冷却して、固体を真空濾過によって回収した。濾過後直ちに固体をXRPDによって分析すると、固体は溶媒和化合物(おそらくエタノール溶媒和化合物)であることが示された。その後固体を、100℃の大気圧で30分乾燥させた。乾燥した固体をXRPDによって分析したところ、L型が多数を占めることが決定された(H型は検出されなかった)。
【0215】
B.メチルエチルケトン溶媒による温浸
高純度エプレレノン1 gをメチルエチルケトン4 mlに2時間温浸し、その後、混合物を室温に冷却して、得られた固体を真空濾過によって回収した。固体を直ちにXRPD分析によって分析して、エプレレノンの溶媒和化合物(おそらくメチルエチルケトン溶媒和化合物)であると決定した。その後溶媒和化合物を100℃の大気圧で30〜60分乾燥させた。乾燥した固体をXRPDによって分析したところ、主にL型であると決定され、H型の回折ピークは存在しなかった。
【0216】
実施例11:溶液から直接L型の結晶化
技法A
エプレレノン2.5 gを、75℃に加熱することによって酢酸エチルに溶解した。溶液を75℃で30分維持して、完全に溶解させた後、冷却速度1℃/分で13℃まで冷却した。得られたスラリーを750 rpmのオーバーヘッド攪拌子によって2時間攪拌した。固体を真空濾過によって回収して、40℃の真空炉で1時間乾燥させた。固体のXRPDパターンおよびDSCサーモグラムは、L型エプレレノンの特徴であった。固体のTGAは200℃まで固体からの重量喪失がないことを示した。
【0217】
技法B
もう一つの技法において、エプレレノン2 gを、ホットプレート上で磁石攪拌子によって攪拌しながら加熱することによって、15%アセトニトリルと85%水の混合液350 mlに溶解した。エプレレノンが溶解した後、溶液を磁石攪拌子で攪拌しながら室温まで一晩冷却した。得られた固体を真空濾過によって回収した。結晶は、複屈折であり、三角形の平板状晶癖を有した。固体にXRPDおよびDSC分析を行うと、L型エプレレノンの特徴を示した。TGAは200℃まで重量の喪失がないことを示した。
【0218】
技法C
さらにもう一つの技法において、エプレレノン640 mgを、エチルベンゼン20 mlを加えた50 mlフラスコに入れた。得られたスラリーを116℃に加熱すると、透明な溶液が得られ、これを30分かけて25℃に冷却した。核生成は、冷却期間のあいだに84℃で始まった。得られた固体を溶液から濾過して、風乾させると、固体530 mgが得られた(収率83%)。温ステージ顕微鏡およびXRPDにより、固体がL型エプレレノン結晶であることを確認した。
【0219】
技法D
さらにもう一つの技法において、エプレレノン1.55 gをニトロベンゼン2.0 mlに加えて、200℃に加熱した。得られたスラリーを200℃で一晩攪拌して、透明な溶液になった後、自然の空気対流によって室温まで冷却して、固体を単離した。固体は、XRPDおよび偏光顕微鏡によってL型エプレレノンであると決定された。
【0220】
技法E
さらにもう一つの技法において、エプレレノン5.0 g(純度>99%)をメタノール82 g(104 ml)に加えた。210 rpmで攪拌しながら、溶液を60℃に加熱して、その温度で20分維持して完全に溶解させた。溶液を攪拌しながら0.16℃/分の速度で−5℃まで冷却した。得られた結晶を濾過して回収して、40℃の真空炉で20時間乾燥させた。乾燥した固体は、DSCおよびXRPD分析によってL型エプレレノンであると決定された。
【0221】
技法F
もう一つの技法において、エプレレノン6.0 g(9%エタノールを含み、補正純度95.2%であるエタノール溶媒和化合物)をメタノール82 g(104 ml)に加えた。210 rpmで攪拌しながら、溶液を60℃に加熱して、その温度で20分維持して完全に溶解させた。次に、溶液を0.14℃/分の速度で50℃に冷却して、その温度を2.5時間維持した。次に、溶液を攪拌しながら0.13℃/分の速度で−5℃まで冷却した。得られた結晶を濾過して回収して、40℃の真空炉で16時間乾燥させた。乾燥した固体は、DSCおよびXRPD分析によってL型エプレレノンであると決定された。
【0222】
実施例12:溶液から直接のH型の結晶化
ジエポキシド150.5 mgおよびエプレレノン2.85 gをニトロベンゼン1.5 mlに加えた。混合物を200℃で数時間磁石攪拌子によって攪拌した。次に、得られたスラリーを自然の空気対流によって室温まで冷却した。試料を乾燥させて、偏光顕微鏡およびXRPDによって分析した。XRPD分析によって、試料がH型とL型の混合物であることが示された。結晶は顕微鏡で見ると半透明であり、溶媒除去(およびH型またはL型への変換)が起こっていないことを示している。
【0223】
実施例13:粉砕によるアモルファスエプレレノンの調製
鋼鉄製のウィグLバグ容器の約半分に、エプレレノン(純度>99.9%)約60 gを加えた。鋼鉄製のボールとキャップを試料容器に入れて、ウィグLバグ装置によって30秒間攪拌した。エプレレノンは、ウィグLバグ容器の表面から剥がれ落ちて、容器をさらに30秒間攪拌した。得られた固体をXRPDおよびDSCによって分析すると、アモルファスエプレレノンとL型結晶エプレレノンの混合物であると決定された。
【0224】
実施例14:凍結乾燥によるアモルファスエプレレノンの調製
粗エプレレノン約100 mgを、水400 mlを含むビーカーに計り取った。得られた混合物を5分間軽く加熱した後、超音波処理して、さらに5分間攪拌しながら加熱すると、分散液が得られた。エプレレノン分散液約350 mlを、HPLC用水50 mlを含む1000 mlの丸底フラスコに濾過した。分散液をドライアイス/アセトン浴中で1〜2分のあいだに急速に凍結した。フラスコをラブコンコフリーゾーン4.5凍結乾燥装置に接続して、内容物を一晩乾燥させた。フラスコ中の固体を小さい褐色瓶に移した。少量を偏光顕微鏡で、カージル(cargille)油(1.404)中で10倍、1.25倍で観察し、少なくとも95%アモルファスエプレレノンであることを観察した。図24および25は、アモルファスエプレレノンについて得られたXRPDパターンおよびDSCサーモグラムを示している。図24において39゜2θで認められたピークは、アルミニウム製の試料容器によるものである。
【0225】
実施例15:L型エプレレノンの溶解度
L型エプレレノンの水に対する溶解度をpH 7(100 mM燐酸緩衝液)で、5、25、および40℃で測定した。L型エプレレノン約30 mgを緩衝液約10 mlと混合すると、5℃および25℃ではいずれもエプレレノンのスラリーを形成した。H型エプレレノン約40 mgを緩衝液10 mlと混合すると、40℃でエプレレノンのスラリーを形成した。試料はそれぞれの条件について2つずつ調製した。スラリーは、振とう水浴中で適当な温度で平衡にして、溶液を1、5、12、19、27および36日間隔で紫外線可視分析(245 nm)によってエプレレノン含有量を分析した。各温度からのデータを適切に平均して、各温度でのエプレレノンの溶解度を決定して、表8に報告する。36日間の平衡終了後、各時点での残留固体をDSCおよびTGAによって分析して、L型エプレレノンであると決定した。
【0226】
【表8】

L型エプレレノンの溶解度
【0227】
実施例16:固有の溶解速度の測定
固有溶解速を、以下の4つのエプレレノン多形試料について測定した:(i)実施例11の技法Bと同じように、抗溶媒として水を用いてアセトニトリルから直接結晶化によって調製したL型エプレレノン、(ii)実施例10の技法Aと同じようにエタノールにおける温浸によって調製したH型エプレレノン、(iii)5%H型と95%L型との混合物、および(iv)粉砕して以下の粒子サイズ分布を提供するL型エプレレノン:9μm未満の粒子の重量が10%、22 μm未満の粒子重量が50%、および41 μm未満の粒子の重量が90%。
【0228】
エプレレノン150 mgを計り取って、ファンケル固有溶解測定腔に入れた。カーバープレスを用いて粉末を8280 kPaで圧縮して、錠剤を生成した。次に試料を固有溶解装置に載せた。用いた溶解培地は、1%ドデシル硫酸ナトリウム(SDS)のHPLC水溶液であった。試験は全て、37℃で2時間実施した。実験の開始前に溶解培地500 mlを溶解水浴チャンバー中で37℃で30分平衡にした。最初の試料を各溶解管から採取して、試験の初回時間(T0)とした。エプレレノン錠剤を溶解培地に沈めた。試料を既定の間隔で採取して溶解度の測定を行った。錠剤表面に気泡を形成しないように注意した。試料を243 nmでのUV吸収検出によって分析した。固有の溶解速度は、容積に関して補正し、溶解錠の表面積(0.5 cm2)に関して標準化した濃度対時間プロフィールの直線部分の勾配から計算した。
【0229】
図26は、4つの試料について測定した固有溶解速度を報告する。これらの試験は、H型エプレレノンはL型エプレレノンより固有の溶解速度が速いことを示している。圧縮および非圧縮エプレレノンを比較するXRPD測定によって、多形が圧縮時または溶解試験の経過中に相互変換しないことを確認した。
【0230】
実施例17:エプレレノン多形組成物
表9に示す組成を有するL型エプレレノン25 mg、50 mg、100 mgおよび200 mgを含む錠剤を調製する。
【表9】

実施例17の錠剤の組成
【0231】
実施例18:エプレレノン多形組成物
エプレレノン100 mg用量を含み、表10に示す組成を有するカプセル(硬ゼラチンカプセル、#0)を調製する。
【表10】

実施例18の100 mgカプセルの組成
【0232】
実施例19:エプレレノン多形組成物
エプレレノン200 mg用量を含み、表11に示す組成を有するカプセル(硬ゼラチンカプセル、サイズ#0)を調製する。
【表11】

実施例19の200 mgカプセルの組成
【0233】
実施例20:粉砕したエプレレノンの調製
エプレレノンの乾燥メチルエチルケトン溶媒和化合物をまず、溶媒和化合物をフィッツミル上の20メッシュスクリーンに通過させることによって塊をほぐす。次に、ほぐした塊を、供給速度約250 kg/時間でアルパインホサカワ・スタッドディスクピンミルを用いて、液体窒素冷却下で操作して、細かく粉砕する。ピンミリング技法は約65〜100 μmのD90粒子径を有する粉砕したエプレレノンを生じる。
【0234】
実施例21:イヌの試験における薬物動態パラメータに及ぼすエプレレノン粒子径の影響
エプレレノン血漿濃度および相対的生物学的利用能に及ぼすL型エプレレノンの粒子径の影響をイヌモデルにおいて調べた。体重8〜12 kgの健康な雌性ビーグル犬4匹に、下記の表12に記載した処方を含む即時放出カプセル(#0、白色半透明)1個を胃内投与して、水約10 mlを与えた。
【表12】


実施例21において用いられたエプレレノンカプセルの組成
【0235】
イヌを15〜20時間絶食してからカプセルを投与して、用量の投与後少なくとも4時間は餌を与えなかった。血液試料(約3ml)を、用量の投与後0、0.5、1、2、3、4、6、8および24時間に、ヘパリンを含む冷試験管に静脈穿刺によって採取した。血液試料を氷中に直ちに入れた。血液試料からの血漿の分離は、遠心を約15分行うことによって完了した。得られた血漿試料は、分析するまで約−20℃で凍結して保存した。分析はLC/MS/MS技法を用いて実施した。
【0236】
同じイヌ4匹を、それぞれが表12に示す組成を有するが、エプレレノン粒子径が異なる3つの製剤の試験に用いた。エプレレノン開始材料のD90粒子径はそれぞれ、約212 μm、約86 μm、および約36 μmであった。一連の製剤の投与のあいだは、少なくとも5日間の薬剤回復期間を設けた。結果の平均値を下記の表13および14に報告する。相対的生物学的利用率はAUCの結果から計算し、D90が86 μmである製剤を標準物質として選択した。
【0237】
【表13】

血液血清エプレレノン濃度(μg/ml)、実施例21
【0238】
【表14】

実施例21のデータから計算した薬物動態(PK)パラメータ
【0239】
実施例22:ヒトの試験における薬物動態パラメータに及ぼすエプレレノン粒子径の影響
エプレレノン血漿濃度および生物学的利用率に及ぼすL型エプレレノンの粒子径の影響を、下記の表15に説明する製剤組成物3つを用いてヒトモデルにおいて調べた。無作為化スケジュールに従って、被験者に1、8、15、22および29日に薬剤としてL型エプレレノン組成物100 mgを1回投与した。薬剤は全て午前8時に水180 mlと共に投与した。エプレレノンの薬物動態分析の血液試料は、−0.5(投与前)、投与後0.5、1、2、3、4、6、8、10、12、16、24、36、および48時間に採取した。
【0240】
エプレレノンの血漿濃度は、MS/MS検出を備えた確認されたHPLC法を用いて決定した。薬物動態データは表16に報告する。組成物の調製において用いたL型エプレレノンの粒子径分布は、レーザー光散乱を用いて乾燥粉末状態で決定した。
【0241】
【表15】

1 7.5%顆粒内、10%顆粒外
実施例22において用いたエプレレノン組成物(重量%)
【0242】
【表16】

実施例22のデータから計算した薬物動態(PK)パラメータ
【0243】
本発明は、特定の態様に関して説明してきたが、これらの態様の詳細は制限すると解釈されない。
【図面の簡単な説明】
【0244】
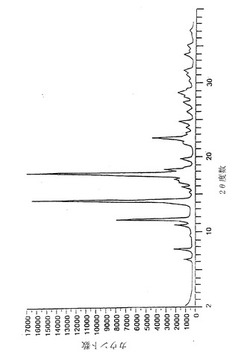
【図1A】H型エプレレノン溶媒和化合物のX線粉末回折パターンを示す。
【図1B】L型エプレレノン溶媒和化合物のX線粉末回折パターンを示す。
【図1C】エプレレノン溶媒和化合物のメチルエチルケトン溶媒和化合物のX線粉末回折パターンを示す。
【図1D】エプレレノンのn-プロピルアルコール溶媒和化合物のX線粉末回折パターンを示す。
【図1E】エプレレノンのテトラヒドロフラン溶媒和化合物のX線粉末回折パターンを示す。
【図1F】エプレレノンのエチルプロピオン酸溶媒和化合物のX線粉末回折パターンを示す。
【図1G】エプレレノンの酢酸溶媒和化合物のX線粉末回折パターンを示す。
【図1H】エプレレノンのアセトン溶媒和化合物のX線粉末回折パターンを示す。
【図1I】エプレレノンのトルエン溶媒和化合物のX線粉末回折パターンを示す。
【図1J】エプレレノンのイソプロパノール溶媒和化合物のX線粉末回折パターンを示す。
【図1K】エプレレノンのエタノール溶媒和化合物のX線粉末回折パターンを示す。
【図1L】エプレレノンの酢酸イソブチル溶媒和化合物のX線粉末回折パターンを示す。
【図1M】エプレレノンの酢酸ブチル溶媒和化合物のX線粉末回折パターンを示す。
【図1N】エプレレノンの酢酸メチル溶媒和化合物のX線粉末回折パターンを示す。
【図1O】エプレレノンの酢酸プロピル溶媒和化合物のX線粉末回折パターンを示す。
【図2A】メチルエチルケトンから直接結晶化した未粉末化L型エプレレノンの示差走査熱量測定(DSC)熱記録を示す。
【図2B】メチルエチルケトンから高純度エプレレノンを結晶化して得られた溶媒和物の脱溶媒化によって調製した未粉末化L型エプレレノンのDSC熱記録を示す。
【図2C】メチルエチルケトンから高純度エプレレノンを結晶化して得られた溶媒和化合物の脱溶媒化による産物を粉末化して調製したL型エプレレノンのDSC熱記録を示す。
【図2D】適当な溶媒から低純度エプレレノンを温浸して得られた溶媒和物の脱溶媒化によって調製した未粉末化H型エプレレノンのDSC熱記録を示す。
【図2E】エプレレノンのn-プロピルアルコール溶媒和化合物のDSC熱記録を示す。
【図2F】エプレレノンのテトラヒドロフラン溶媒和化合物のDSC熱記録を示す。
【図2G】エプレレノンのエチルプロピオン酸溶媒和化合物のDSC熱記録を示す。
【図2H】エプレレノンの酢酸溶媒和化合物のDSC熱記録を示す。
【図2I】エプレレノンのクロロホルム溶媒和化合物のDSC熱記録を示す。
【図2J】エプレレノンのアセトン溶媒和化合物のDSC熱記録を示す。
【図2K】エプレレノンのトルエン溶媒和化合物のDSC熱記録を示す。
【図2L】エプレレノンのイソプロパノール溶媒和化合物のDSC熱記録を示す。
【図2M】エプレレノンのエタノール溶媒和化合物のDSC熱記録を示す。
【図2N】エプレレノンの酢酸t-ブチル溶媒和化合物のDSC熱記録を示す。
【図2O】エプレレノンの酢酸イソブチル溶媒和化合物のDSC熱記録を示す。
【図2P】エプレレノンの酢酸ブチル溶媒和化合物のDSC熱記録を示す。
【図2Q】エプレレノンの酢酸メチル溶媒和化合物のDSC熱記録を示す。
【図2R】エプレレノンの酢酸プロピル溶媒和化合物のDSC熱記録を示す。
【図2S】エプレレノンのn-ブタノール溶媒和化合物のDSC熱記録を示す。
【図2T】エプレレノンのn-オクタノール溶媒和化合物のDSC熱記録を示す。
【図3A】H型エプレレノンの赤外線(IR)スペクトル(拡散反射率、DRIFT)を示す。
【図3B】L型エプレレノンのIRスペクトル(拡散反射率、DRIFT)を示す。
【図3C】エプレレノンのメチルエチルケトン溶媒和化合物のIRスペクトル(拡散反射率、DRIFT)を示す。
【図3D】クロロホルム溶液中のエプレレノンのIRスペクトル(拡散反射率、DRIFT)を示す。
【図3E】エプレレノンのn-プロピルアルコール溶媒和化合物のIRスペクトルを示す。
【図3F】エプレレノンのテトラヒドロフラン溶媒和化合物のIRスペクトルを示す。
【図3G】エプレレノンのエチルプロピオン酸溶媒和化合物のIRスペクトルを示す。
【図3H】エプレレノンの酢酸溶媒和化合物のIRスペクトルを示す。
【図3I】エプレレノンのアセトン溶媒和化合物のIRスペクトルを示す。
【図3J】エプレレノンのトルエン溶媒和化合物のIRスペクトルを示す。
【図3K】エプレレノンのイソプロパノール溶媒和化合物のIRスペクトルを示す。
【図3L】エプレレノンのエタノール溶媒和化合物のIRスペクトルを示す。
【図3M】エプレレノンの酢酸イソブチル溶媒和化合物のIRスペクトルを示す。
【図3N】エプレレノンの酢酸ブチル溶媒和化合物のIRスペクトルを示す。
【図3O】エプレレノンの酢酸プロピル溶媒和化合物のIRスペクトルを示す。
【図3P】エプレレノンの酢酸メチル溶媒和化合物のIRスペクトルを示す。
【図3Q】エプレレノンのプロピレングリコール溶媒和化合物のIRスペクトルを示す。
【図3R】エプレレノンの酢酸t-ブチル溶媒和化合物のIRスペクトルを示す。
【図4】H型エプレレノンの13C NMRスペクトルを示す。
【図5】L型エプレレノンの13C NMRスペクトルを示す。
【図6A】エプレレノンのメチルエチルケトン溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6B】エプレレノンのn-プロピルアルコール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6C】エプレレノンのテトラヒドロフラン溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6D】エプレレノンのエチルプロピオン酸溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6E】エプレレノンの酢酸溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6F】エプレレノンのクロロホルム溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6G】エプレレノンのアセトン溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6H】エプレレノンのトルエン溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6I】エプレレノンのイソプロパノール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6J】エプレレノンのエタノール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6K】エプレレノンの酢酸イソブチル溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6L】エプレレノンの酢酸ブチル溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6M】エプレレノンの酢酸メチル溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6N】エプレレノンの酢酸プロピル溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6O】エプレレノンのプロピレングリコール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6P】エプレレノンのn-ブタノール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6Q】エプレレノンのn-オクタノール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6R】エプレレノンの酢酸t-ブチル溶媒和化合物の熱重量測定分析プロフィールを示す。
【図7】エプレレノンのメチルエチルケトンの溶媒和化合物を脱溶媒化して調製したL型エプレレノンの走査型電子顕微鏡写真。
【図8】酢酸エチルから直接結晶化して調製したL型エプレレノンの走査型電子顕微鏡写真。
【図9】メチルエチルケトンから単離された7-メチル水素4α,5α;9α,11α-ジエポキシ-17ヒドロキシ-3-オキソ-17α-プレグナン-7α,21-ジカルボン酸であるγラクトン(「ジエポキシド」)の結晶形のX線粉末回折パターンを示す。
【図10】イソプロパノールから単離された7-メチル11α,12α-エポキシ-17ヒドロキシ-3-オキソ-17α-プレグン-4-エン-7α,21-ジカルボン酸であるγ-ラクトン(「11,12-エポキシド」)の結晶形のX線粉末回折パターンを示す。
【図11】n-ブタノールから単離された7-メチル水素-17ヒドロキシ-3-オキソ-17α-プレグナ-4,9(11)-ジエン-7α,21-ジカルボン酸であるγ-ラクトン(「9,11-オレフィン」)の結晶形のX線粉末回折パターンを示す。
【図12】互変的な関係にある多形についての、ギブス自由エネルギーと温度との関係を図示する。n-ブタノールから単離された7-メチル水素-17ヒドロキシ-3-オキソ-17α-プレグナ-4,9(11)-ジエン-7α,21-ジカルボン酸であるγ-ラクトン(「9,11-オレフィン」)の結晶形のX線粉末回折パターンを示す。
【図13】(a) 0%, (b) 1%, (c) 3%、および(d) 5%のジエポキシ不純物添加処理によるメチルエチルケトン結晶化により得られたメチルエチルケトン溶媒和化合物の湿塊のX線粉末回折パターンを示す。
【図14】(a) 0%, (b) 1%, (c) 3%、および(d) 5%のジエポキシ・不純物添加処理によるメチルエチルケトン結晶化により得られた乾燥固体のX線粉末回折パターンを示す。
【図15】乾燥する前に溶媒和化合物を(a) 磨砕せず、また (b) 磨砕して、 3%ジエポキシ不純物添加処理によるメチルエチルケトン結晶化により得られた乾燥固体のX線粉末回折パターンを示す。
【図16】(a) 0%, (b) 1%, (c) 5%、および(d) 10%の11,12-エポキシ・不純物添加処理によるメチルエチルケトン結晶化により得られたメチルエチルケトン溶媒和化合物の湿塊のX線粉末回折パターンを示す。
【図17】(a) 0%, (b) 1%, (c) 5%、および(d) 10%の11,12-エポキシ・不純物添加処理によるメチルエチルケトン結晶化により得られた乾燥固体のX線粉末回折パターンを示す。
【図18】本明細書の実施例7の表7Aで報告されているデータに基づく、産物の純度、出発物質の純度、冷却速度、および終点温度の立体プロットを示す。
【図19】最終物質の純度に対して統計的に有意な効果をもつ変数を決定するために、図18の立体プロットを用いて作成された半定位プロットを示す。
【図20】最終物質の純度に対する効果について、出発物質の純度と冷却速度の間の相互作用を示す、本明細書の実施例7の表7Aで報告されているデータに基づいた相互作用グラフ。
【図21】本明細書の実施例7の表7Aで報告されているデータに基づく、H型重量画分、出発物質の純度、冷却速度、および終点温度の立体プロットを示す。
【図22】最終物質の純度に対して統計的に有意な効果をもつ変数を決定するために、図21の立体プロットを用いて作成された半定位プロットを示す。
【図23】最終物質の純度に対する効果について、出発物質の純度と終点温度の間の相互作用を示す、本明細書の実施例7の表7Aで報告されているデータに基づいた相互作用グラフ。
【図24】無定形エプレレノンのX線回折パターンを示す。
【図25】無定形エプレレノンのDSC熱記録を示す。
【図26】4種類のエプレレノン多形試料について測定した溶解速度を示す。
【技術分野】
【0001】
本発明は、アルドステロンレセプター拮抗薬、より詳しくは、アルドステロンレセプター拮抗薬であるエプレレノンとしての活性をもつ薬剤の技術分野に含まれる。具体的には、本発明は、エプレレノンの新規の結晶形、該結晶形を調製する方法、該結晶形を含む薬学的組成物、該結晶形を使用して、高血圧症などの抗アルドステロン症に関連する症状および疾患など、アルドステロンが関与する症状および/または疾患を予防および/または治療する方法、および、薬剤の製造において該結晶形を使用することに関する。
【背景技術】
【0002】
下記構造式(I)をもつγ-ラクトンであり、エプレレノンとして知られる化合物、メチル9,11-エポキシ-17-ヒドロキシ-3-オキソプレグン-4-エン(ene)-7,21-ジカルボン酸(metyl hydrogen 9,11-epoxy-17-hydroxy-3-oxopregn-4-ene-7,21-dicarboxylate)は、9,11-エポキシステロイド化合物とそれらの塩類開示ている、Grobらに付与された特許文献1で初めて報告された。エプレレノンは、アルドステロンレセプター拮抗薬であって、高血圧症、心不全などの心機能障害、および肝硬変などの抗アルドステロン症に関連する症状を治療するときなど、アルドステロンレセプター拮抗薬の使用が指示されている場面で、治療上有効な量にして投与することができる。
【化1】

【0003】
参照として本明細書に組み入れられる、上記引用文献の特許文献1は、一般的に、エプレレノンの調製剤、およびエプレレノンを含む薬学的組成物の調合剤を開示している。エプレレノンを含む9,11-エポキシステロイド化合物、およびそれらの塩を調製するための別法が、特許文献2および3に開示されている。
【0004】
非特許文献1は、塩化メチレン/ジエチルエステル溶媒系からエプレレノンを結晶化して調製したエプレレノン溶媒和化合物のX線結晶構造解析結果を開示している。
【0005】
非特許文献2は、エプレレノンの一回服用量実験において、20μmの粒子サイズをもつ非処方化エプレレノンの使用を開示している。
【0006】
スピロノラクトンは、アルドステロンレセプター拮抗薬の活性をもつ構造式(II)の20-スピロノキサン-ステロイドで、高血圧を治療するために市販されている。しかし、スピロノラクトンは、男性に女性化乳房と性的不能をもたらすことのある抗アンドロゲン活性をもつ。また、女性の月経不順を生じさせることのある弱いプロゲステロン活性ももつ。このため、グルココルチコイド、黄体ホルモン、およびアンドロゲンのステロイドレセプターシステムなど他のステロイドレセプターシステムと相互作用せず、また/または、より広い治療範囲を提供するエプレレノンのような別の活性アルドステロンレセプター拮抗薬を開発する利点がある。
【化2】

【0007】
非特許文献3は、スピロノラクトンのアセトニトリル溶媒和化合物、エタノール溶媒和化合物、酢酸エチル溶媒和化合物、メタノール溶媒和化合物、および2種類の非溶媒和多形性結晶形を開示している。同様に、非特許文献4は、スピロノラクトンのこれらの固体型結晶形を開示している。
【0008】
エプレレノンの水性媒体中での可溶性は非常に低いため、経口用剤形から消化管に薬剤を放出することが、しばしば、この薬剤の生物学的利用能、より詳しくは、経口投与してから治療薬効果が現れるまでの速さに対する律速要素となっている。
【0009】
【特許文献1】米国特許第4,559,332号
【特許文献2】国際公開公報第97/21720号
【特許文献3】国際公開公報第98/25948号
【非特許文献1】グロブ(Grob)ら(1997)、「ステロイド性アルドステロン拮抗薬:9α,11-エポキシ誘導化合物の高選択性(Steroidal aldosterone antagonists; increased selectivity of 9α,11-epoxy derivatives)」, Helvetica Chimica Acta, 80, 556〜585
【非特許文献2】デ・ガスパロ(De Gasparo)ら(1989)、「抗アルドステロン薬:性的副作用の発生と防止(Antialdosterones: incidence and prevention of sexual side effects)」, Journal of Steroid Biochemistry, 32(13), 223〜227
【非特許文献3】アガフォノフ(Agafonov)ら(1991)、「スピロノラクトンの多形性(Polymorphism of spironolactone)」, Pharmaceutical Science, 80(2), 181〜185
【非特許文献4】ブリッタン(Brittan)ら(1999)、「薬剤用固体の多形性(Polymorphism in Pharmaceutical Solids)」, pp. 114〜116, 207, 235および261(マーセル・デッカー社(Marcel Dekker))
【発明の開示】
【0010】
発明の概要
ここで、貯蔵および使用における通常の温度での高程度の物理的安定性を有し、他の固体型のエプレレノンに較べて独特の性質をもつ新規のエプレレノン結晶形を提供する。結晶形の特徴については、本明細書で完全に後述するが、便宜上「L型」と略称する。
【0011】
本発明は、第一の態様において、エプレレノンそのものの新規のL型結晶形を提供する。「H型」と呼ばれる他の結晶形からL型を区別する特性のうち、H型は単斜晶系、2θが8.0±0.2度(degree)のピークをもつX線粉末回折パターン、および以下に記載するように本明細書において調製された方法により、約223℃から約242℃の範囲内の融点を示す。
【0012】
第二の局面において、本発明は、少なくとも検出可能量のL型エプレレノンを含むエプレレノン薬剤物質を提供する。
【0013】
第三の局面において、本発明は、実質的に位相が純粋なL型エプレレノンであるエプレレノン薬剤物質を提供する。ここで、「位相が純粋な」という語は、他の固体型のエプレレノンに対して純粋であることを意味し、他の化合物に対して、化学的に高度に純粋であることを必ずしも意味しない。
【0014】
第四の局面において、本発明は、脱溶媒したときに、L型エプレレノンを回収することのできるエプレレノン溶媒和結晶形を提供する。
【0015】
第五の局面において、本発明は、L型エプレレノン、選択的には、別に一種類以上の固体形エプレレノンを一緒に含み、エプレレノンの投薬量が一単位全部で約10 mgから約1000 mgであり、さらに一種類以上の賦形剤を含む薬学的組成物を提供する。
【0016】
第六の局面において、本発明は、L型エプレレノンを調製する方法、およびL型エプレレノンを含む組成物を調製する方法を提供する。
【0017】
第七の局面において、アルドステロンが関与する症状または疾患を予防および/または治療する方法において、含まれるエプレレノンの少なくとも一部がH型エプレレノンである、治療上有効な量のエプレレノンを対象者に投与することを含む方法を提供する。
【0018】
本発明のその他の局面は、本出願明細書全体で検討されている。
【0019】
発明の詳細な説明
すべての薬学的化合物および組成物でも言えるように、エプレレノンの化学的および物理的特性が、それを商業的に開発する上では重要である。これらの特性には、(1)モル体積、密度、および吸湿性などの充填特性、(2)融点、蒸気圧および可溶性などの熱力学特性、(3)溶解速度および安定性など(大気条件、特に湿度に対する安定性、および貯蔵条件下での安定性など)の動力学的特性、(4)表面積、湿潤性、界面張力、および形などの表面特性、(5)硬度、張力、強度、成形性、操作性、流量、および混和などの機械的性質、および(6)濾過性などがあるが、これらに限定されない。これらの特性は、例えば、エプレレノンを含む薬学的組成物の加工および貯蔵に影響を与えることがある。他の固体型のエプレレノンに対してこれらの特性の一つ以上が改良された固体型エプレレノンが望ましい。
【0020】
本発明によって、新規の固体型エプレレノンが提供される。これらは、特に、少なくとも2種類の非溶媒和化結晶形と非水和結晶形(「H型」および「F型」と名付けられている)を含む、さまざまな溶媒和化結晶形、および無定形型エプレレノンが含まれる。本願に記載された各固体型エプレレノンは、本明細書またはこれ以外の文献に記載されている他の固体型と比較して、上記化学的および/または物理的に有利な特性の一つ以上をもっている。H型およびL型は、本明細書で優先権主張されている書類では、それぞれ、「I型」および「II型」と呼ばれたり、時には、それぞれ、「高融点多形体」および「低融点多形体」と記載されている。
【0021】
本発明は、L型エプレレノンに関する。L型は、互変的遷移温度(enantiotropic transition temperature)(後述)よりも低い温度では、例えば、H型エプレレノンよりも高い物理的な安定性をもつ。例えば、製造加工の間(例えば、粒子サイズを小さくして表面積を大きくした材料を得るためにエプレレノンを粉末化する間など)物理的に安定している固体型エプレレノンを選択すれば、特別な処理条件、およびそのような特別な処理条件に一般的に伴う費用増加を必要としなくて済む。同様に、(特に、エプレレノン製品の耐用期間に生じうるさまざまな貯蔵条件を考えると)広範な貯蔵条件にわたって物理的に安定した固体型エプレレノンを選択することが、製品の消失や製品の効能低下をもたらすエプレレノンの多形化またはその他の分解による変化を防止するのに役立つ。したがって、L型のように、より物理的に安定した固体型エプレレノンを選択することが、より安定性の低い型のエプレレノンを選択することよりも有意な利益をもたらす。
【0022】
H型エプレレノンも、他の固体型よりは有利である。特に、互変的遷移温度(enantiotropic transition temperature)(後述)では、L型エプレレノンよりも、水性溶媒において、より速い溶解速度(約30%速い)を示す。消化管におけるエプレレノンの溶解速度が、標的細胞または組織へのエプレレノン輸送の律速段階となる場合には、溶解度が速くなれば、生物学的利用能が向上する。したがって、H型は、L型よりも優れた生物学的利用能プロフィールを提供することができる。さらに、より速い溶解速度をもつ固体型エプレレノンを選択することは、溶解速度が遅い他の固体型に較べ、特に、エプレレノンを迅速に放出させるための薬学的組成物に対する賦形剤の選択、およびそれらの処方において、さらに高い融通性を提供することになる。
【0023】
本発明は、また、溶媒和した結晶形のエプレレノンに関する。これらの溶媒和型は、H型およびL型のエプレレノンを調製するときの中間体として有益であり、特に、本発明に照らせば、脱溶媒したときに、L型エプレレノンを回収できる溶媒和結晶形のエプレレノンが有利である。中間体としての溶媒和結晶形の使用によって得られる特別の利益は、本願において後述するように、脱溶媒する際にもたらされる結晶の「真性微粉化(intrinsic micronizing)」である。このような「真性微粉化」によって、粉末化する必要を低下またはなくすことができる。さらに、さらに粉末化する必要がまだあるときにも、H型やL型の溶媒和結晶形を脱溶媒した後に粉末化するよりも、脱溶媒工程の前に一定の溶媒和化合物を粉末化する方が容易である。
【0024】
エプレレノンの薬学的に許容される溶媒和結晶形も、薬学的組成物で直接用いることができる。一つの実施態様において、このような組成物を直接調製するときに有用な溶媒和結晶形は、塩化メチレン、イソプロパノール、またはエチルエーテルを含まず、別の態様においては、塩化メチレン、イソプロパノール、エチルエーテル、メチルエチルケトン、またはエタノールを含まず、また、さらに別の、別の態様においては、塩化メチレン、イソプロパノール、エチルエーテル、メチルエチルケトン、エタノール、酢酸エチル、またはアセトンを含まない。このような使用にとって、もっとも好ましくは、エプレレノンの溶媒和結晶形は、実質的に、薬学的に許容される溶媒でない溶媒を含まない。
【0025】
薬学的組成物で用いられる溶媒和結晶形は、一般的に、かつ好ましくは、薬学的に許容される、高沸点で、かつ/または水素結合する溶媒、例えば、ブタノールであるが、これに限定されない溶媒を含む。溶媒和結晶形はまとまって、さまざまな溶解速度範囲を提供することができるため、消化管におけるエプレレノンの溶解速度が、標的細胞または組織へのエプレレノン輸送の律速段階となる場合には、H型およびL型に較べてもさまざまな範囲の生物学的利用能を提供することができる。
【0026】
本発明は、無定形型のエプレレノンにも関する。無定形型のエプレレノンは、H型およびL型を調製するときの中間体として有用である。さらに、無定形エプレレノンは、さまざまな溶解速度をもつため、無定形型エプレレノンが薬学的組成物中に存在し、かつ、消化管におけるエプレレノンの溶解速度が、標的細胞へのエプレレノン輸送の律速段階となる場合には、このような無定形エプレレノンが、H型およびL型に較べてもさまざまな範囲の生物学的利用能を提供することができる。
【0027】
H型エプレレノン、L型エプレレノン、溶媒和結晶形エプレレノン、および無定形エプレレノンからなる群より選択される固体型を組み合わせることも興味深い。このような組合せは、例えば、制御放出組成物など、さまざまな溶解プロフィールをもつ薬学的組成物を調製するときに有用である。本発明の一つの実施態様において、少なくとも検出可能量のL型エプレレノンと、H型エプレレノン、溶媒和結晶形エプレレノン、および無定形エプレレノンからなる群より選択される一種類以上の固体型である残り分と含む固体型の組合せが提供される。
【0028】
固体型エプレレノンの使用目的によっては、加工上の配慮から、特定の固体型、またはこのような固体型の特定の組合せを選択することが好まれるかもしれない。例えば、位相が純粋なL型は、一般的に、位相が純粋なH型よりも簡単に調製することができる。しかし、H型とL型の混合物の方が、一般的に、位相が純粋なL型よりもより簡単に調製することができるため、比較的化学的純度の低いエプレレノン出発物質として使用することができる。組成物において、H型またはL型の代わりに溶媒和結晶形を使用すると、それを使用しないと溶媒和結晶形の脱溶媒によって進められる加工工程、すなわち脱溶媒化を省くことができる。または、例えば、中間体溶媒和結晶形の調製および脱溶媒化を妨害することなく、適当な溶媒からL型を直接結晶化すれば、この脱溶媒化工程を省くことができよう。
【0029】
定義
本明細書において、エプレレノンについて用いられるとき、「無定形」という用語は、エプレレノン分子が無秩序な配置でその中に存在し、区別できる結晶格子または単位格子を形成していない固体を意味する。X線粉末回折を行なうと、無定形エプレレノンは、特徴的な結晶ピークを生じない。
【0030】
本明細書において、物質または溶液の沸点について言及する場合には、「沸点」は、適用処理条件下での物質または溶液の沸点を意味する。
【0031】
本明細書において、エプレレノンについて用いられるとき、「結晶形」は、(i)区別できる単位格子を含み、また、(ii)X線粉末回折を行なうと、回折ピークが得られるという区別できる結晶格子を形成するように、エプレレノン分子が配置されている固体を意味する。
【0032】
本明細書において、「結晶化」とは、エプレレノン出発材料の調製に関する適用環境によって、結晶化、および/または再結晶化を意味することがある。
【0033】
本明細書において、「温浸」とは、溶媒または溶媒混合液中の固形エプレレノンの懸濁液を、適用処理条件下で、該溶媒または溶媒混合液の沸点で加熱する処理を意味する。
【0034】
本明細書において、「直接の結晶化」とは、中間的な溶媒和結晶固体型のエプレレノンを生成したり、脱溶媒化することなく、適当な溶媒からエプレレノンを直接結晶化することを意味する。
【0035】
本明細書において、「エプレレノン薬剤物質」とは、この語が使用される文脈によっては、エプレレノンそのものを意味し、処方されていないエプレレノンや、薬学的組成物の成分として存在するエプレレノンを意味することもある。
【0036】
本明細書において、「粒子サイズ」とは、当技術分野において公知のレザー光散乱、沈降フィールドフローフラクショネーション(sedimentation field flow fractionation)、フォトン相関分光測定法(photon correlation spectroscopy)、またはディスク遠心分離法(disk centrifugation)などの通常の粒子サイズ測定技術によって測定された粒子の大きさを意味する。「D90粒子サイズ」は、粒子の重量の90%が、このような通常の粒子サイズ測定技術によって測定されたD90粒子サイズよりも小さい粒子サイズである。
【0037】
「DSC」という用語は、示差走査熱量測定法の意味である。
【0038】
「HPLC」という用語は、高圧液体クロマトグラフィーの意味である。
【0039】
「IR」という用語は、赤外線の意味である。
【0040】
本明細書において、「純度」という用語は、別段の記載がない限り、通常のHPLCアッセイ法によるエプレレノンの化学的純度を意味する。ここで、「低純度エプレレノン」とは、一般的に、有効量のH型結晶成長促進物質および/またはL型結晶成長阻害物質を含むエプレレノンを意味する。ここで、「高純度エプレレノン」とは、一般的に、H型結晶成長促進物質および/またはL型結晶成長阻害物質を全く含まないか、有効量よりも少ない量しか含まないエプレレノンを意味する。
【0041】
本明細書において、「位相が純粋な」という用語は、本明細書記載の赤外線分光測定解析法によって測定された特定の結晶形または無定形型のエプレレノンについてのエプレレノン固体純度を意味する。
【0042】
「XRPD」という用語は、X線粉末回折の意味である。
【0043】
「rpm」という用語は、1分間あたりの回転数を意味する。
【0044】
「TGA」という用語は、熱重量分析法を意味する。
【0045】
「Tm」という用語は、融点を意味する。
【0046】
結晶形の特徴づけ
1.分子の立体構造
単結晶X線解析によって、エプレレノン分子の立体構造がH型とL型とでは異なり、特に、ステロイド環の第7位でエステル基の方向が異なっていることが示されている。エステル基の方向は、C8-C7-C23-O1ねじれ角によって定義することができる。
【0047】
H型結晶格子において、エプレレノン分子は、エステル基のメトキシ基が、第7位でC-H結合とほぼ並列し、カルボニル基がB-ステロイド環のほぼ中央を覆うところに位置するという構造を採っている。この立体構造では、C8-C7-C23-O1ねじれ角は約-73.0°である。この方向では、エステル基のカルボニルの酸素原子(O1)が、9,11-エポキシド環の酸素原子(O4)に近接する。O1-O4の距離は、約2.97Åで、ファンデルワールス接触距離である3.0Åよりも僅かに短い(酸素原子のファンデルワールス半径を1.5Åとした場合)。
【0048】
L型結晶格子では、エプレレノン分子は、H型の分子に対してエステル基が約150°回転しており、約+76.9°のC8-C7-C23-O1ねじれ角をもつ立体構造をとっている。この方向では、エステルのメトキシ基は、Aステロイド環の4,5-アルケン分節の方向を向いている。この方向では、エステル基のどちらの酸素原子(O1、O2)と、9,11-エポキシド環の酸素原子(O4)との間の距離も、H型について測定された距離よりも長くなる。O2-O4の距離は、約3.04Åで、ファンデルワールス接触距離である3.0Åよりも僅かに長い。O1-O4の距離は約3.45Åである。
【0049】
単結晶X線回折によって今までに解析された溶媒和結晶形では、エプレレノン分子は、L型の立体構造の特徴を採っているように見える。
【0050】
2.単結晶X線回折
シーメンス(Siemens)D5000粉末回折計またはアイネル(Inel)多目的回折計によって、エプレレノンのさまざまな結晶形を分析した。シーメンス(Siemens)D5000粉末回折計については、生データを2から50まで、0.020および2秒間隔というステップ毎に2θ(シータ)値を測定した。アイネル(Inel)多目的回折計については、試料をアルミニウム製のサンプルホルダーに入れ、生データをすべての2θ値を30分間同時に収集した。
【0051】
表1A、1Bおよび1Cは、それぞれ、H型(低純度エプレレノンの温浸によって得られたエタノール溶媒和化合物の脱溶媒化によって調製されたもの)、L型(高純度エプレレノンの再結晶化によって得られたメチルエチルケトン溶媒和化合物の脱溶媒化によって調製されたもの)、およびメチルエチルケトン溶媒和化合物(高純度エプレレノンのメチルエチルケトン中での室温懸濁物転換によっ調製されたもの)という結晶形のエプレレノンの2θ値と強度に関する主要ピークの重要なパラメータを示している(波長1.54056ÅでのX線照射)。
【0052】
H型およびL型の製造経路(すなわち、溶媒和化合物の脱溶媒化)に関連して、結晶回折面の間隔が不完全になる結果、H型とL型の回折パターンにおいて、ピーク位置の僅かな変化が存在することがある。なお、H型は、粗製エプレレノンの温浸によって調製された溶媒和化合物から単離されている。この方法は、全体的に化学的純度の低い(約90%の)H型を生じる。最後に、エプレレノンの溶媒和型は、結晶格子の中で溶媒チャネル内の溶媒分子の移動度が増すために、回折ピークの位置にいくらかの変化が見られることが予想される。
【表1A】


X線回折データ、H型
【表1B】


X線回折データ、L型
【表1C】


X線回折データ、メチルエチルケトン溶媒和化合物
【0053】
エプレレノンのH型、L型、およびメチルエチルケトン溶媒和化合物の結晶形のグラフ例を、それぞれ、図1-A、1-B、および1-Cに示す。H型は、7.0±0.2度、8.3±0.2度、および12.0±0.2度の2θで際だったピークを示す。L型は、2θが8.0±0.2度、12.4±0.2度、12.8±0.2度および13.3±0.2度で際だったピークを示す。メチルエチルケトン溶媒和化合物は、2θが7.6±0.2度、7.8±0.2度、および13.6±0.2度で際だったピークを示す。
【0054】
以下の溶媒和結晶形のエプレレノンに関するX線回折パターンの実例を図1-Dから1-Oに示す。それぞれ、n-プロピルアルコール、テトラヒドロフラン、エチルプロピオン酸、酢酸、アセトン、トルエン、イソプロパノール、エタノール、酢酸イソブチル、酢酸ブチル、酢酸メチル、酢酸プロピルの溶媒和化合物。
【0055】
3.融解/分解温度
非溶媒和化エプレレノン結晶形の融解および/または分解温度を、TAインスツルメンツ(TA Instruments)2920示差走査熱量測定計を用いて決定した。1〜2 mg量の各試料を、シール付きまたはシールなしのアルミニウム鍋の上に置いて加熱し、約10℃/分の温度上昇速度を得た。融解/分解温度の範囲は、融解/分解吸熱の推定開始温度から最大値までである。
【0056】
H型およびL型エプレレノンの融解は、化学分解、および結晶格子に捉えられていた溶媒の消失に伴って起きた。融解/分解温度も、解析前の固体処理による影響を受けた。例えば、適当な溶媒、または適当な溶媒もしくは溶媒混合液中の高純度エプレレノンの結晶化によって得られた溶媒和化合物の脱溶媒物から直接結晶化することによって調製された約180〜450μmというD90粒子サイズの未粉末化L型の融解/分解温度は、一般的に、約237℃から約242℃までの範囲にある。適当な溶媒もしくは溶媒混合液中の高純度エプレレノンの溶液から溶媒和化合物を結晶化し、脱溶媒し、得られたL型を粉末化して調製された、約80〜100μmのD90粒子サイズをもつ粉末化L型の融解/分解温度は、一般的に、約223℃から約234℃までの範囲にある。低純度エプレレノンの温浸によって得られた溶媒和化合物を脱溶媒して調製された約180〜450μmのD90粒子サイズをもつ未粉末化L型の融解/分解温度は、一般的に、約247℃から約251℃までの範囲にある。それぞれ、(a)メチルエチルケトンから直接結晶化した未粉末化L型エプレレノン、(b)メチルエチルケトンから高純度エプレレノンを結晶化して得られた溶媒和物の脱溶媒によって調製した未粉末化L型エプレレノン、(c)メチルエチルケトンから高純度エプレレノンを結晶化して得られた溶媒和化合物の脱溶媒化による産物を粉末化して調製したL型エプレレノン、(d)メチルエチルケトンから低純度エプレレノンを温浸して得られた溶媒和物を脱溶媒化して調製した未粉末化H型エプレレノンのDSC熱記録の例を図2-A、2-B、2-Cおよび2-Dに示す。
【0057】
エプレレノンの溶媒和型のDSC熱記録をパーキンエルマー(Perkin Elmer)Pyris 1示差走査熱量計を用いて測定した。各1〜2 μgの試料を、シールをしないでアルミニウム鍋に入れ、約10℃/分の温度上昇率になるよう加熱した。低温での一種類以上の吸熱現象は、溶媒和化合物の結晶格子から溶媒が失われるにつれて起こるエンタルピー変化と関連していた。最も高熱の吸熱は、H型またはL型のエプレレノンの融解/分解に伴って起きた。エプレレノン溶媒和化合物である、n-プロピルアルコール、テトラヒドロフラン、エチルプロピオン酸、酢酸、クロロホルム、アセトン、トルエン、イソプロパノール、酢酸t-ブチル、エタノール、酢酸イソブチル、酢酸ブチル、酢酸メチル、酢酸プロピル、n-ブタノール、およびn-オクタノールの溶媒和化合物のDSC熱記録を、それぞれ、図2-Eから2-Tに示す。
【0058】
4.赤外線吸収スペクトル分析
非溶媒和型のH型およびL型エプレレノンの赤外線吸収スペクトルを、ニコレットDRIFT社(Nicolet DRIFT)の(拡散反射赤外線のフーリエ変換)Magna System 550を用いて得た。Spectra-Tech Collector装置と微量試料容器を用いた。試料(5%)を臭化カリウム中で解析し、400から4000 cm-1で走査して解析した。稀釈したクロロホルム溶液(3%)中、または溶媒和した結晶形のエプレレノンの赤外線吸収スペクトルを、Bio-rad FTS-45分光光度計を用いて得た。クロロホルム溶液試料を、塩化ナトリウム塩プレートをもつ、0.2 mm間隔の溶液用セルを用いて分析した。溶媒和FTIRスペクトルをIBM社のマイクロ-MIR(micro-MIR)(複数内部反射)補助装置を用いて回収した。試料を400から4000 cm-1で走査した。(a)H型、(b)L型、(c)メチルエチルケトン溶媒和物、および(d)クロロホルム溶液中のエプレレノンにおける赤外線吸収スペクトルの例を、それぞれ、図3-A、3-B、3-Cおよび3-Dに示す。
【0059】
表2は、H型、L型、およびメチルエチルケトン溶媒和型の結晶形に関する吸収バンドを具体的に示している。比較のために、クロロホルム溶液中のエプレレノンの吸収バンドの具体例も示してある。例えば、スペクトルのカルボニル領域で、H型と、L型またはメチルエチルケトン溶媒和型の間には違いが見られた。H型は、約1739 cm-1のエステルカルボニルストレッチ(ester carbonyl stretch)をもつが、L型およびメチルエチルケトン溶媒和型で対応するストレッチは、それぞれ、約1724と1722 cm-1である。クロロホルム溶液中のエプレレノンでは、エステルカルボニルストレッチは、約1727 cm-1である。H型とL型の間におけるストレッチ頻度の変化は、この2つの結晶形でエステル基の方向が変化していることしていることを反映している。なお、A型ステロイド環における、結合ケトンのエステル基のストレッチは、H型またはメチルエチルケトン溶媒和型で約1664〜1667 cm-1であり、L型で約1665 cm-1である。対応するカルボニル基のストレッチは、クロロホルム溶液中では約1665 cm-1である。
【0060】
H型とL型とのもう一つの違いは、C-H屈曲領域に見られた。H型には、L型、メチルエチルケトン溶媒和型、またはクロロホルム溶液中のエプレレノンでは見られない約1399 cm-1で吸光を示す。カルボニル基に隣接するC2およびC1のメチレン基を切断するためのCH2領域には、約1399 cm-1のストレッチが存在する。
【表2】

エプレレノンの各型におけるIR吸収バンド(cm-1)
【0061】
エプレレノンの溶媒和化合物である、n-プロピルアルコール溶媒和化合物、テトラヒドロフラン溶媒和化合物、エチルプロピオン酸溶媒和化合物、酢酸溶媒和化合物、アセトン溶媒和化合物、トルエン溶媒和化合物、イソプロパノール溶媒和化合物、エタノール溶媒和化合物、酢酸イソブチル溶媒和化合物、酢酸ブチル溶媒和化合物、酢酸プロピル溶媒和化合物、酢酸メチル溶媒和化合物、プロピレングリコール溶媒和化合物、および酢酸t-ブチル溶媒和化合物について、それぞれの赤外線吸収スペクトルの例を図3-Eから3-Sに示す。
【0062】
5.核磁気共鳴(NMR)分析法
31.94 MHzのフィールドにおける13C NMRスペクトルを得た。H型およびL型エプレレノンの13C NMRスペクトルの実例を、それぞれ、図4および5に示す。図4に示したデータを得るために解析されたH型エプレレノンは、位相が純粋ではなく、少量のL型エプレレノンを含んでいた。H型は、約64.8 ppm、24.7 ppm、および19.2 ppmにおける炭素共鳴によってもっとも明確に区別された。
【0063】
6.熱重量分析
TAインスツルメンツ(TA Instruments)TGA 2950熱重量分析計を用いて熱重量分析を行なった。決定した。各試料は、シールなしのアルミニウム鍋上に、窒素をパージした状態で置いた。開始温度は25℃で、約10℃/分の割合で温度を上昇させた。
【0064】
以下のエプレレノン溶媒和化合物、すなわち、メチルエチルケトン溶媒和化合物、n-プロピルアルコール溶媒和化合物、テトラヒドロフラン溶媒和化合物、エチルプロピオン酸溶媒和化合物、酢酸溶媒和化合物、クロロホルム溶媒和化合物、アセトン溶媒和化合物、トルエン溶媒和化合物、イソプロパノール溶媒和化合物、エタノール、酢酸イソブチル、酢酸ブチル、酢酸メチル、酢酸プロピル溶媒和化合物、プロピレングリコール溶媒和化合物、n-ブタノール溶媒和化合物、および酢酸t-ブチル溶媒和化合物それぞれについて、熱重量測定分析プロフィールの例を図6-Aから6-Rに示す。
【0065】
7.顕微鏡法
ツァイス社(Zeiss)製全面偏光顕微鏡(Universal Polarized Light Microscope)付きのリンカム社(Linkam)のTHMS 600ホットステージ(Hot Stage)を用いて、メチルエチルケトン溶媒和化合物の単結晶に対して高熱期顕微鏡法を行なった。室温での偏光下では、溶媒和化合物の結晶は複屈折性かつ半透明で、結晶格子が非常に規則的であることを示している。温度を約60℃まで上昇させるにつれて、結晶の長軸方向に沿って顕著な欠陥が生じ始めた。メチルエチルケトン溶媒和化合物の脱溶媒によって得られたL型エプレレノンの走査電子顕微鏡写真を図7に示すが、結晶格子内で表面の欠損、孔、亀裂、および破砕が起きているのが分かる。エチル酢酸からの直接の結晶化によって得られたL型エプレレノンの走査電子顕微鏡写真が図8に示されているが、結晶格子内での同じような表面の欠損、孔、亀裂、および破砕は見られない。
【0066】
8.単位格子のパラメータ
以下の表3A、3Bおよび3Cは、H型、L型、およびいくつかのエプレレノン溶媒和結晶形について決定された単位格子パラメータをまとめたものである。
【表3A】


エプレレノン結晶形の単位格子パラメータ
【表3B】

エプレレノン結晶形の単位格子パラメータ
1酢酸ブチル溶媒和化合物分子は、チャネル内にある溶媒分子が不規則であるため、完全には精製されていなかった。
【表3C】

エプレレノン結晶形の単位格子パラメータ
1溶媒和化合物分子は、チャネル内にある溶媒分子が不規則であるため、完全には精製されていなかった。
【0067】
エプレレノンの選択された結晶形に関する別の情報が、下の表4に記載されている。メチルエチルケトン溶媒和化合物について、上記表3Aに記載されている単位格子データは、これら、さらに別のエプレレノン結晶溶媒和化合物の多くについての単位格子パラメータを代表するものである。試験されたエプレレノン結晶溶媒和化合物のほとんどは、実質的に、互いに同じ構造をもっている。取り込まれた溶媒分子の大きさによっては、一つの溶媒和結晶形から別の溶媒和結晶形へ、X線粉末回折ピークが僅かに変化することがあるが、全体的な回折パターンは実質的に同じであって、単位格子パラメータおよび分子位置は、試験した溶媒和化合物のほとんどについて実質的に同一である。
【表4】

エプレレノン溶媒和化合物に関する付加的情報
1窒素パージ条件下で10℃/分の加熱速度で行なった熱重量解析によって測定される、溶媒和の最終重量減少工程から推定された脱溶媒温度と定義される。しかし、脱溶媒温度は、溶媒和化合物の製造方法による影響を受ける。低温では、さまざまな方法によって、溶媒和化合物において脱溶媒化を開始することのできる核生成部位をさまざまな数作り出すことができる。
【0068】
溶媒和化合物の単位格子は4個のエプレレノン分子からなる。この単位格子におけるエプレレノン分子および溶媒分子の化学量も、多数の溶媒和化合物について、上記表4に記載されている。H型の単位格子は4個のエプレレノン分子からなる。L型の単位格子は2個のエプレレノン分子からなる。溶媒和化合物の単位格子は、脱溶媒の過程で、溶媒分子が残した間隙を埋めるために、エプレレノン分子が平行移動や回転されると、H型および/またはL型の単位格子に転換される。表4には、多数の異なった溶媒和化合物の脱溶媒温度も記載されている。
【0069】
9.不純物の結晶特性
エプレレノンの不純物の中には、溶媒和化合物を脱溶媒する過程でH型の形成を誘導できるものがある。特に、以下の2種類の不純物分子を評価した。すなわち、7-メチル水素4α,5α;9α,11α-ジエポキシ-17ヒドロキシ-3-オキソ-17α-プレグナン-7α,21-ジカルボン酸、γラクトン(III)(「ジエポキシド」)、および7-メチル水素11α,12α-エポキシ-17ヒドロキシ-3-オキソ-17α-プレグン-4-エン-7α,21-ジカルボン酸、γ-ラクトン(IV)(「11,12-エポキシド」)。
【化3】

【化4】

脱溶媒により生じるエプレレノン結晶形に対する、これらの不純物の効果については、本明細書の実施例においてさらに詳しく説明する。
【0070】
7-メチル水素-17ヒドロキシ-3-オキソ-17α-プレグナ-4,9(11)-ジエン-7α,21-ジカルボン酸であるγ-ラクトン(V)(「9,11-オレフィン」)とH型エプレレノンの単結晶構造における類似性から、9,11-オレフィンも、溶媒和化合物を脱溶媒する過程でH型の形成を誘導することができるという仮説が立てられている。
【化5】

【0071】
単結晶を核不純化合物から単離した。ジエポキシド、11,12-エポキシド、および9,11-オレフィンで単離された結晶形のX線粉末回折パターンを、それぞれ図9、10および11に示す。各不純物分子のX線粉末回折パターンは、H型のX線粉末回折パターンに類似しており、これは、H型と3種類の不純化合物が、同じ単結晶構造をもっていることを示唆するものである。
【0072】
各不純化合物の単結晶も単離して、X線による構造決定を行ない、これら3種類の化合物が、H型の単結晶構造に類似した単結晶構造を採用していることを証明した。11,12-エポキシドの単結晶をイソプロパノールから単離した。9,11-オレフィンの単結晶は、n-ブタノールから単離した。各不純化合物の結晶形について決定した結晶構造データを表5に示す。得られた結晶系と格子パラメータは、H型、ジエポキシド、11,12-エポキシド、および9,11-オレフィンの結晶形で実質的に同一であった。
【表5】


H型エプレレノンとの比較による、不純物結晶に関する単位格子パラメータ
【0073】
表5に記載されている4種類の化合物を、同一の間隙グループに結晶化し、類似した格子パラメータをもつ(すなわち、同一構造である)。ジエポキシド、11,12-エポキシド、および9,11-オレフィンは、H型立体構造を採るという仮説が立てられている。どの不純化合物についても、(溶液から直接に)H型充填を単離することが比較的容易だということは、このH型格子が、これら一連の構造的に類似した化合物にとって安定した充填方式であることを示している。H型エプレレノンと、実質的に結晶学上同一の構造をもつ化合物は、溶液からH型エプレレノンを結晶化するときの添加不純物(dopant)として有用な可能性があると考えられる。
【0074】
したがって、具体的な実施態様において、溶媒または溶媒混合液中のエプレレノン溶液からH型エプレレノンを結晶化することを促進する方法、結晶化する前に、結晶学上実質的にH型エプレレノンと同一構造をもつ化合物の有効量によって不純物添加処理することを含む方法が提供される。ここで、「不純物添加処理」とは、積極的処理、すなわち、不純物添加処理用化合物を意図的に添加しても、または、消極的処理、すなわち、該溶液中に不純物添加処理用化合物が不純物として存在していても、どちらでもよい。
【0075】
本実施態様に関して好適な不純物添加処理用化合物は、それぞれ、上記化合物(III)、(IV)および(V)であるジエポキシド、11,12-エポキシド、および9,11-オレフィンである。
【0076】
エプレレノンの調製
本発明に係る新規の結晶形を調製するためのエプレレノン出発物質は、上記国際公開公報第97/21720号および第98/25948号で開示されている方法、特に、これら刊行物で開示されているスキーム1など、それ自体は既知の方法によって調製することができる。
【0077】
結晶形の調製
1.溶媒和型結晶形の調製
エプレレノンの溶媒和型結晶形は、適当な溶媒、または適当な溶媒の混合液からエプレレノンを結晶化して調製することができる。適当な溶媒、または適当な溶媒の混合液は、一般的に、高温下でエプレレノンを不純物と一緒に可溶化するが、冷却すると、溶媒和化合物を選択的に結晶化する有機溶媒、または有機溶媒の混合液を含む。このような溶媒、または溶媒の混合液におけるエプレレノンの可溶性は、一般的に、室温で約5から約200 mg/mlである。溶媒、または溶媒の混合液は、好ましくは、その前にエプレレノン出発物質を調製する処理工程で使用した溶媒で、特に、それが、エプレレノン結晶形を含む最終薬学的組成物に含まれるときには、薬学的に許容されるものである溶媒から選択する。例えば、塩化メチレンを含む溶媒和化合物が回収される、塩化メチレンを含む溶媒系は望ましくない。
【0078】
用いられる溶媒は、好ましくは、薬学的に許容される溶媒であり、特に、「不純物:残留溶媒の手引き(Impurities: guideline for residual solvents)」、人体に使用するための薬剤を登録するための技術的要件の統一化に関する国際会議(International Conference On Harmonization Of Technical Requirements For Registration Of Pharmaceuticals For Human Use)(ICH運営委員会により、1997年7月17日のICHプロセスのステップ4の採用が推奨された)において、クラス2またはクラス3として定義されている溶媒である。さらに好ましくは、溶媒、または溶媒の混合液は、メチルエチルケトン、1-プロパノール、2-ペンタノン、酢酸、アセトン、酢酸ブチル、クロロホルム、、エタノール、イソブタノール、酢酸イソブチル、酢酸メチル、プロピオン酸エチル、n-ブタノール、n-オクタノール、イソプロパノール、酢酸プロピル、プロピレングリコール、t-ブタノール、テトラヒドロフラン、トルエン、メタノール、および酢酸t-ブチルからなる群より選択される。
【0079】
本処理法の別の実施態様において、溶媒、または溶媒の混合液は、1-プロパノール、2-ペンタノン、酢酸、アセトン、酢酸ブチル、クロロホルム、イソブタノール、酢酸イソブチル、酢酸メチル、プロピオン酸エチル、n-ブタノール、n-オクタノール、酢酸プロピル、プロピレングリコール、t-ブタノール、テトラヒドロフラン、トルエン、メタノール、および酢酸t-ブチルからなる群より選択される。
【0080】
本処理法の別の実施態様において、溶媒、または溶媒の混合液は、1-プロパノール、2-ペンタノン、酢酸、アセトン、酢酸ブチル、クロロホルム、イソブタノール、酢酸イソブチル、酢酸メチル、プロピオン酸エチル、n-ブタノール、n-オクタノール、n-プロパノール、酢酸プロピル、プロピレングリコール、t-ブタノール、テトラヒドロフラン、トルエン、メタノール、および酢酸t-ブチルからなる群より選択される。
【0081】
エプレレノンの溶媒和型結晶形を調製するために、一定量のエプレレノン出発物質を一定量の溶媒で可溶化し、結晶が形成されるまで冷却した。エプレレノンを溶媒に加える溶媒温度は、一般的に、溶媒または溶媒の混合液の溶解曲線に基づいて選択される。例えば、本明細書記載の溶媒のほとんどでは、この溶媒温度は、一般的に、約25℃以上であり、好ましくは、約30℃から溶媒の沸点までであり、また、より好ましくは、溶媒の沸点よりも約25℃低い温度から、溶媒の沸点までである。
【0082】
または、加熱した溶媒をエプレレノンに加えて、混合液を結晶が形成されるまで冷却することも可能である。エプレレノンを加える時の溶媒の温度は、一般的に、溶媒または溶媒の混合液の溶解曲線に基づいて選択される。例えば、本明細書記載の溶媒のほとんどでは、この溶媒温度は、一般的に、約25℃以上であり、好ましくは、約50℃から溶媒の沸点までであり、また、より好ましくは、溶媒の沸点よりも約15℃低い温度から、溶媒の沸点までである。
【0083】
同様に、一定容量の溶媒と混合するエプレレノン出発物質の量は、溶媒、または溶媒の混合液の溶解曲線に依存する。一般的には、溶媒に加えるエプレレノンの量は、室温では完全に溶解されない。例えば、本明細書記載の溶媒のほとんどでは、一定容量の溶媒と混合するエプレレノン出発物質の量は、約1.5倍から約4.0倍であり、好ましくは、約2.0倍から約3.5倍であり、より好ましくは、約2.5倍であるが、このエプレレノン量で、該容量の溶媒に室温で溶解する。
【0084】
エプレレノン出発物質が溶媒に完全に溶けたら、一般的には、溶液をゆっくりと冷却して、エプレレノンの溶媒和化した結晶形を結晶化する。例えば、本明細書記載の溶媒のほとんどでは、溶液を、約20℃/分よりも遅い速度で冷却し、好ましくは、約10℃/分よりも遅い速度で、また、より好ましくは、約5℃/分よりも遅い速度で、さらにより好ましくは、約1℃/分よりも遅い速度で冷却する。
【0085】
溶媒和型結晶形を回収する終点温度は、溶媒、または溶媒の混合液の溶解曲線に依存する。例えば、本明細書記載の溶媒のほとんどでは、この終点温度は、一般的に、約25℃よりも低く、好ましくは、約5℃よりも低く、より好ましくは、約−5℃よりも低い。終点温度を低くする方が、一般的には、溶媒和型結晶形の形成には有利である。
【0086】
または、別の技術を用いて溶媒和化合物を調製することも可能である。このような技術の例には、(i)エプレレノン出発物質を一つの溶媒に溶かして、溶媒和型結晶形の結晶化を促進するために共溶媒を加える方法、(ii)溶媒和化合物の蒸気拡散成長(vapor diffusion growth)、(iii)回転式乾燥のような乾燥法によって、溶媒和化合物を単離する方法、および(iv)懸濁液の転換法(slurry conversion)などを含むが、これらに限定されない。
【0087】
上記したところにしたがって調製された溶媒和型結晶形の結晶は、濾過、または遠心分離などの通常の適当な方法によって溶媒から分離することができる。結晶化の過程で溶媒系を強く振とうすると、一般的に、より小さな結晶粒子が生じる。
【0088】
2.L型溶媒和化合物の調製
L型エプレレノンは、脱溶媒化によって、溶媒和型結晶形から直接調製することができる。脱溶媒は、溶媒和化合物の加熱、溶媒和化合物の周りの大気圧の減圧、または、これらの併用などがあるが、これらに限定されない適当な脱溶媒化手段によって行なうことができる。溶媒和化合物をオーブンなどの中で加熱して溶媒を除去すれば、この処理中の溶媒の温度は、一般的には、H型およびL型の互変性遷移温度を超えることはない。この温度は、好ましくは、150℃を超えない。
【0089】
脱溶媒圧力および脱溶媒化時間は、厳密には重要ではない。脱溶媒圧力は、好ましくは、約1気圧以下である。しかし、脱溶媒圧力を低下させるにつれて、脱溶媒を行なうことのできる温度、および/または、脱溶媒化時間も同様に減少してゆく。特に、高い脱溶媒温度をもつ溶媒和化合物では、真空乾燥すると、より低い乾燥温度を用いることができる。脱溶媒化時間は、単に、脱溶媒を行なわせるのに十分であることだけが必要で、そうすればL型が形成されて完成する。
【0090】
実質的にL型だけを含む産物が調製されたことを確認するためには、エプレレノン出発物質は、一般的に高純度エプレレノンであり、好ましくは、実質的に純粋なエプレレノンである。L型エプレレノンを調製するために用いられるエプレレノン出発物質は、一般的に、90%以上の純度、好ましくは、95%以上の純度、そして、より好ましくは、99%以上の純度である。本願の別の箇所でより詳しく説明されているように、エプレレノン出発物質における、ある種の不純物は、本処理法によって得られた産物の収量やL型含有量に有害な効果を与えることがある。
【0091】
高純度エプレレノン出発物質から、このようにして調製された結晶化エプレレノン産物は、通常、10%以上のL型、好ましくは、50%以上のL型、より好ましくは、75%以上のL型、さらにより好ましくは、90%以上のL型、さらに好ましくは、約95%以上のL型、および、さらに一層好ましくは、実質的に位相が純粋なL型である。
【0092】
3.溶媒和化合物からのH型の調製
H型を含む産物は、(i)高純度エプレレノン出発物質ではなく低純度エプレレノン出発物質を使用し、(ii)位相が純粋なH型結晶を溶媒系に播種し、あるいは、(iii)、(i)と(ii)を組み合わせて調製することができる。
【0093】
3.1.結晶成長促進物質および阻害物質としての不純物の使用
エプレレノン出発物質中のすべての不純物の全体量ではなく、エプレレノン出発物質に含まれる一定の不純物の存在と含量が、溶媒和化合物の脱溶媒化の過程でH型結晶を形成する能力に影響を与える。一定の不純物は、通常、H型成長促進物質、またはL型成長阻害物質である。これらは、エプレレノン出発物質に含まれていたり、エプレレノン出発物質を加える前から溶媒、または溶媒の混合液に含まれていることがあり、また/または、エプレレノン出発物質を加えた後で、溶媒、または溶媒の混合液に加えることもある。ボナフェーデ(Bonafede)ら、(1995)は、参照として本明細書に組み入れられる、「分子結晶基質に対するリッジダイレクティドエピタクシーによる有機多形の選択的核生成および成長(Selective nucleation and growth of an organic polymorph by ledge-directed epitaxy on a molecular crystal substrate)」、J. Amer. Chem. Soc., 117(3)において、成長促進物質および成長阻害物質を多形系で使用することを考察している。本発明では、通常、適当な不純物は、H型エプレレノンの単結晶構造と実質的に同一の単結晶構造をもつ化合物を含む。不純物は、好ましくは、H型エプレレノンのX線粉末回折パターンと実質的に同一のX線粉末回折パターンを示す化合物であり、より好ましくは、ジエポキシド、11,12-エポキシド、および9,11-オレフィン、およびこれらの組合せからなる群より選択される。
【0094】
H型結晶を調製するのに必要な不純物の量は、一般的には、部分的には、溶媒または溶媒の混合液、および不純物のエプレレノンに対する可溶性によって決まる。例えば、メチルエチルケトン溶媒和化合物からのH型の結晶化において、ジエポキシの低純度エプレレノン出発物質に対する重量比は、一般的には、約1:100以上、好ましくは、約3:100以上、より好ましくは、約3:100から約1:5、さらに好ましくは、約3:100から約1:10である。11,12-エポキシドは、メチルエチルケトンの中では、ジエポキシドよりも可溶性が高いため、通常、H型エプレレノン結晶を調製するためには、より大量の11,12-エポキシドが必要である。不純物が11,12-エポキシドを含む場合には、、ジエポキシドの低純度エプレレノン出発物質に対する重量比は、一般的には、約1:5以上、好ましくは、約3:25以上、そして、より好ましくは、約3:25から約1:5である。ジエポキシドおよび11,12-エポキシド不純物の両方をH型結晶の調製に使用する場合には、各不純物のエプレレノン出発物質に対する重量比は、一方の不純物だけをH型結晶の調製に用いるときの比率よりも低くなる。
【0095】
選択された不純物を含む溶媒和化合物を脱溶媒すると、通常、H型エプレレノンおよびL型エプレレノンの混合物が得られる。溶媒水和化合物の脱溶媒化を開始して得られる産物に含まれるH型の重量画分は、一般的には、約50%よりも少ない。下で説明するように、この産物をさらに結晶化または温浸によって処理すると、通常、産物中のL型の重量画分が増加する。
【0096】
3.2.播種
H型結晶は、エプレレノンを結晶化する前に、溶媒系に位相が純粋なH型結晶(または、上記で考察したH型成長物質および/またはL型成長阻害物質)を播種することによって調製することもできる。エプレレノン出発物質は、低純度エプレレノンでも、高純度エプレレノンでもよい。いずれかの出発物質から調製してできた溶媒水和化合物を脱溶媒化すると、産物中のH型の重量画分は、一般的に、約70%以上であるが、約100%になることもある。
【0097】
溶媒系に添加するH型の種結晶の出発物質に対する重量比は、一般的には、約0.75:100以上、好ましくは、約0.75:100から約1:20、より好ましくは、約1:100から約1:50である。H型種結晶は、本願において、H型結晶を調製するために検討した方法のいずれによっても調製することができるが、下で説明するような温浸によるH型結晶の調製法によって調製することができる。
【0098】
H型種結晶は、一度に加えたり、何回にも加えたり、または実質的に一定時間にわたって連続して加えることもできる。しかし、H型種結晶の添加は、通常、エプレレノンが溶液から結晶化し始める前に完了している。すなわち、播種は曇点(準安定域の下端)に達する前に完了している。播種は、一般的には、溶液温度が、曇点よりも約0.5℃高い温度から、曇点よりも約10℃高い温度までの範囲で、好ましくは、曇点よりも約2℃から約3℃高い温度のときに行なうことができる。種結晶を加えるときの曇点よりも高い温度を上げると、通常は、H型結晶を結晶化させるために必要となる播種量が増加する。
【0099】
播種は、曇点よりも高い温度であるだけでなく、準安定域の範囲内で行なわれることが好ましい。曇点も準安定域も、エプレレノンの可溶性と、溶媒、または溶媒の混合液中での濃度によって決まる。例えば、メチルエチルケトンの12倍容稀釈液では、準安定域の上端は、通常、約70℃から約73℃であり、準安定域の下端(すなわち曇点)は、通常、約57℃から約63℃である。メチルエチルケトンの8倍濃縮液では、溶液が過飽和状態にあるため、準安定域はさらに狭くなる。この濃度では、溶液の曇点は約75℃から約76℃のところに存在する。大気条件下でメチルエチルケトンの沸点は約80℃であるため、この溶液への播種は、一般的には、約76.5℃と沸点の間で行なう。
【0100】
H型による播種の非制限的な具体例が、本明細書の実施例7に記載されている。
【0101】
H型成長促進物質またはL型成長阻害物質用い、および/またはH型を播種して得られた結晶化エプレレノン産物は、通常、2%以上のH型、好ましくは、5%以上のH型、より好ましくは、7%以上のH型、さらに一層好ましくは、約10%以上のH型を含む。残りの結晶化エプレレノン産物は、通常L型である。
【0102】
3.3.エプレレノンの磨砕によるH型の調製
さらに、別の代替的態様において、エプレレノンを適当に磨砕することによって、少量のH型を調製できることが発見されている。磨砕されたエプレレノンのH型の濃度が3%にもなることが観察されている。
【0103】
4.低純度エプレレノンから調製された溶媒和化合物からのL型の調製
上記したように、溶媒和化合物を生成するための低純度エプレレノンの結晶化と、その後の溶媒和化合物の脱溶媒化によって、通常、H型およびL型の両方を含む産物が回収される。位相が純粋なL型結晶を溶媒系に播種することによって、または、L型成長促進物質および/またはH型成長阻害物質を用いてH型を調製するために上記した方法と実質的に同一の方法で、低純度エプレレノンから、L型含量のより多い産物を調製することができる。播種プロトコール、および、溶媒系に加えられるエプレレノン出発物質の量に対する溶媒系に加えるH型種結晶の量の重量比は、通常、位相が純粋なH型結晶の播種によるH型エプレレノンの調製に関して既に前記したそれらの比率と同じである。
【0104】
このようにして調製した結晶化エプレレノン産物は、通常、、10%以上のL型、好ましくは、50%以上のL型、より好ましくは、75%以上のL型、さらに好ましくは、90%以上のL型、さらに一層好ましくは、約95%以上のL型、なお一層好ましくは、実質的に位相が純粋なH型を含む。
【0105】
H型エプレレノンの調製について、本明細書で説明した播種プロトコールによって、結晶化したエプレレノンの粒子サイズの調節法を改良することもできよう。
【0106】
5.溶液からの直接的なL型結晶化
中間的な溶媒和化合物を形成したり、それに伴う脱溶媒化を行なう必要なしに、適当な溶媒、または溶媒の混合液から直接結晶化することによって、L型エプレレノンを調製することもできる。一般的には、(i)溶媒は、溶媒和化合物の結晶格子の中で利用可能なチャネル間隙に適合しない分子サイズをもつ、(ii)エプレレノンとそれに含まれる不純物は、高温で、溶媒に溶ける、(iii)冷却すると、非溶媒和性のL型エプレレノンの結晶化が起こる。溶媒、または溶媒の混合液におけるエプレレノンの可溶性は、室温で、通常、約5〜200 mg/mlである。溶媒、または溶媒の混合液は、好ましくは、メタノール、酢酸エチル、酢酸イソプロピル、アセトニトリル、ニトロベンゼン、水、およびエチルベンゼンからなる群より選択される一種類以上の溶媒を含む。
【0107】
溶液から直接L型エプレレノンを結晶化するためには、一定量のエプレレノン出発物質を一定量の溶媒に溶解してから、結晶が形成されるまで冷却する。エプレレノンを溶媒に加える溶媒温度は、一般的に、溶媒または溶媒の混合液の溶解曲線に基づいて選択される。本明細書記載の溶媒のほとんどでは、この溶媒温度は、一般的に、約25℃以上であり、好ましくは、約30℃から溶媒の沸点までであり、また、より好ましくは、溶媒の沸点よりも約25℃低い温度から、溶媒の沸点までである。
【0108】
または、加熱した溶媒をエプレレノンに加えて、結晶が形成されるまで混合液を冷却することも可能である。エプレレノンを加える時の溶媒の温度は、一般的に、溶媒または溶媒の混合液の溶解曲線に基づいて選択される。本明細書記載の溶媒のほとんどでは、この溶媒温度は、一般的に、約25℃以上であり、好ましくは、約50℃から溶媒の沸点までであり、また、より好ましくは、溶媒の沸点よりも約15℃低い温度から、溶媒の沸点までである。
【0109】
同様に、一定容量の溶媒と混合するエプレレノン出発物質の量は、溶媒または溶媒の混合液の溶解曲線に依存する。一般的には、溶媒に加えるエプレレノンの量は、室温では完全に溶解されない。本明細書記載の溶媒のほとんどでは、一定容量の溶媒と混合するエプレレノン出発物質の量は、約1.5倍から約4.0倍であり、好ましくは、約2.0倍から約3.5倍であり、より好ましくは、約2.5倍であるが、このエプレレノン量は、該容量の溶媒に室温で溶解する量である。
【0110】
実質的に位相が純粋なL型を含む産物が調製されたことを確認するためには、エプレレノン出発物質は、通常、高純度エプレレノンである。エプレレノン出発物質は、好ましくは、約65%以上の純度、より好ましくは、約90%以上の純度、さらに好ましくは、約98%以上の純度、そして、もっとも好ましくは、約99%以上の純度である。
【0111】
エプレレノン出発物質が溶媒に完全に溶けたら、一般的には、溶液をゆっくりと冷却して、L型エプレレノンを結晶化させる。本明細書記載の溶媒のほとんどでは、溶液を約1℃/分よりも遅い速度で冷却し、好ましくは、約0.2℃/分よりも遅い速度で、より好ましくは、約0.05℃/分から約0.1℃/分の速度で冷却する。
【0112】
L型結晶を回収する終点温度は、溶媒または溶媒の混合液の溶解曲線に依存する。本明細書記載の溶媒のほとんどでは、この終点温度は、一般的に約25℃よりも低く、好ましくは、約5℃よりも低く、より好ましくは、約−5℃よりも低い。
【0113】
または、別の技術を用いてL型エプレレノンの結晶を調製することも可能である。このような技術の例には、(i)エプレレノン出発物質を一つの溶媒に溶かして、L型エプレレノンの結晶化を促進するために共溶媒を加える方法、(ii)L型エプレレノンの蒸気拡散成長法(vapor diffusion growth)、(iii)回転式乾燥などの乾燥法によって、L型エプレレノンを単離する方法、および(iv)懸濁液転換法(slurry conversion)などを含むが、これらに限定されない。
【0114】
上記したようにして調製されたL型エプレレノンの結晶は、濾過または遠心分離など、通常の適当な方法によって溶媒から分離することができる。
【0115】
なお、L型エプレレノンは、高純度エプレレノンをメチルエチルケトンの懸濁液を(後述するようにして)温浸し、この懸濁液の沸点で、温浸されたエプレレノンを濾過することによって調製することができる。
【0116】
6.溶液からのH型の調製
H型およびL型の互変遷移温度(Tt)を超える温度で結晶化を行なうと、特に、H型成長促進物質またはL型成長阻害物質が存在するか、位相が純粋なH型結晶を溶媒に播種すると、H型の方がこのように高い温度では安定しているため、溶液から直接H型が結晶化されるという仮説がたてられている。好適に使用される溶媒系は、ニトロベンゼン等、高沸点溶媒を含む。適当なH型成長促進物質には、上記で定義されたジエポキシドおよび9,11-オレフィン化合物などがあるが、これらに限定されない。
【0117】
7.溶媒によるエプレレノンの温浸
エプレレノンの溶媒和結晶形、H型およびL型は、適当な溶媒または溶媒の混合液の中で、エプレレノン出発物質を温浸することによって調製することもできる。温浸処理では、エプレレノンの懸濁液を、溶媒または溶媒の混合液の沸点で加熱する。例えば、エプレレノン出発物質の一定量を、溶媒、または溶媒の混合液の一定容量と組み合わせて、加熱して還流し、留出物を除去すると同時に追加量の溶媒を加えながら、留出物を除去する。または、温浸処理過程で、より以上の溶媒を加えることなく、留出物を濃縮したり、再利用したりすることもできる。一般的には、溶媒の最初の容量を除去、または濃縮および再利用したところで、懸濁液を冷却して、結晶形を溶媒和する。溶媒和した結晶は、濾過、または遠心分離などの通常の適当な方法によって溶媒から分離することができる。前述したような溶媒和化合物の脱溶媒化によって、溶媒和結晶中に一定の不純物が存在したりしなかったりに応じて、H型またはL型のエプレレノンのいずれかが回収される。
【0118】
適当な溶媒または溶媒の混合液は、一般的に、本明細書において既述した溶媒を一種類以上含む。該溶媒は、例えば、メチルエチルケトンおよびエタノールからなる群より選択することができる。
【0119】
温浸処理に使用される溶媒に添加するエプレレノン出発物質の量は、溶媒または溶媒の混合液の沸点で、懸濁液(すなわち、溶媒または溶媒の混合液中のエプレレノンが完全に可溶化されていない)を維持するのに十分な量である。具体例としては、メチルエチルケトンにおいて約0.25 g/ml、またはエタノールにおいて約0.125 g/mlのエプレレノン濃度が有用であると思われる。
【0120】
溶媒の変換が完了して、エプレレノンの溶媒和結晶形が結晶化されたところで、通常、懸濁液をゆっくりと冷却する。試験した溶媒では、懸濁液を、約20℃/分よりも遅い速度で冷却し、好ましくは、約10℃/分よりも遅い速度で、また、より好ましくは、約5℃/分よりも遅い速度で、さらにより好ましくは、約1℃/分よりも遅い速度で冷却する。
【0121】
溶媒和結晶形を回収する終点温度は、溶媒または溶媒の混合液の溶解曲線に依存する。本明細書記載の溶媒のほとんどでは、この終点温度は、一般的に、約25℃よりも低く、好ましくは、約5℃よりも低く、より好ましくは、約−5℃よりも低い。
【0122】
主に、または専ら、L型が所望であれば、一般的には、高純度エプレレノン出発物質を温浸する。高純度エプレレノン出発物質は、好ましくは、約98%以上の純度、より好ましくは、約99%以上の純度、さらに好ましくは、約99.5%以上の純度である。こうして調製される温浸エプレレノン産物は、通常、10%以上、好ましくは、50%以上、より好ましくは、75%以上、さらにより好ましくは、90%以上、さらにいっそう好ましくは、約95%以上のL型、および、もっとも好ましくは、実質的に位相が純粋なL型である。
【0123】
主に、または専ら、H型が所望であれば、一般的には、低純度エプレレノン出発物質を温浸する。低純度エプレレノン出発物質は、通常、H型を回収するのに必要なだけの量のH型成長促進物質および/またはL型成長阻害物質を含む。低純度エプレレノン出発物質は、好ましくは、約65%以上の純度、より好ましくは、約75%以上の純度、さらに好ましくは、約80%以上の純度である。こうして調製される温浸エプレレノン産物は、通常、10%以上、好ましくは、50%以上、より好ましくは、75%以上、さらにより好ましくは、90%以上、さらにいっそう好ましくは、約95%以上のH型、および、もっとも好ましくは、実質的に位相が純粋なH型である。
【0124】
8.無定形エプレレノンの調製
無定形エプレレノンは、圧搾、磨砕、および/または微粉化などにより、固体を適当に粉砕して、少量で調製することができる。位相が純粋な無定形エプレレノン、すなわち、実質的に結晶化エプレレノンを含まない無定形エプレレノンを、例えば、エプレレノン溶液、特に、エプレレノンの水溶液を凍結乾燥させて調製することができる。本明細書の実施例13および14において、これらの処理過程の具体例を示す。
【0125】
付加的な処理条件
1.熱力学的安定性条件
大気温度では、H型よりもL型の方が熱力学的に安定している。本明細書の実施例5で説明されているように、等量のH型およびL型を含む有機懸濁液を一晩室温放置して、残った固体を回収してX線粉末回折によって分析すると、分析結果は、エプレレノンが完全にL型に転換したことを示した。上記で検討された示差走査熱量測定(DSC)データは、H型の方が融解/分解温度が高いため、高温では、L型よりも熱力学的に安定していることを示している。総合すると、懸濁液転換、およびDSCデータは、低温ではL型がより安定していつつも、H型とL型が互変的に関係している、すなわち、この2種類の多形間での安定性の関係の変化が、互変遷移温度(Tt)付近で起きることを示している。図12は、H型およびL型のエプレレノンのような互変的な関係にある多形で一般的に見られる、ギブス自由エネルギーの温度に対する関係を示している。ここで、IおよびIIは、それぞれH型とL型を意味し、Ttは、遷移温度を意味し、Tmは、H型およびL型の融点を意味し、Lは、液状または融解状態を意味する。
【0126】
したがって、L型を含む組成物を調製する間は、処理温度を遷移温度よりも低く保つことが好ましい。例えば、脱溶媒に用いる乾燥温度は、一般的には、約150℃よりも低く、好ましくは、約125℃よりも低く、より好ましくは、約115℃よりも低く、より好ましくは、約110℃よりも低く、さらにより好ましくは、約80℃から約110℃である。さらに、粒子サイズを減少させる処理工程では、L型結晶の温度を遷移温度よりも低く保つために冷却を行なう(液体窒素を使用するなどして)必要があるかもしれない。
【0127】
2.真性微粉化条件
結晶化エプレレノンを調製するために用いられる方法が、その結果できた結晶形の特性に影響を与えることがある。例えば、溶媒和化合物の脱溶媒によって調製されたL型は、溶液から直接結晶化して調製されたL型よりも、結晶格子内で表面に欠損、孔、亀裂、および破砕を生じやすい。この脱溶媒化結晶の「微粉化」によって、結晶の利用可能な表面積、および結晶の溶解速度の上昇がもたらされる。したがって、脱溶媒によって調製されたL型を選択することによって溶解時間を短縮させることができ、直接の結晶化によって調製されたL型結晶を選択することによって溶解時間を長くすることができ、または、これら以外に、脱溶媒によって調製されたL型と直接の結晶化によって調製されたL型の適当な組合せを選択することによって、溶解時間を調節することができる。
【0128】
脱溶媒によって調製されたL型結晶を薬学的組成物の調製に使用する場合には、真性微粉化によって、処理工程過程で結晶の粒子サイズを小さくする必要を効果的に低下または消失させることもできる。しかしながら、このようなL型結晶を使用することの短所の一つは、直接の結晶化によって調製されたL型結晶ならば必要のない脱溶媒工程が必要になることである。
【0129】
方法限定固体型
本発明の実施態様には、本願において開示された方法にしたがって調製された特異的な固体型エプレレノン、およびそれらを組み合わせたものも含まれる。特に、単独、または一種類以上の別の固体型(本願の記載に従って調製された溶媒和結晶形、L型、および無定形エプレレノン)と組み合わせたものでも、H型エプレレノンが本発明の実施態様である。さらに、脱溶媒によってH型エプレレノンを調製するときの中間体として有用で、本願で示したようにして調製された溶媒和型結晶形が本発明の実施態様である。
【0130】
固体型の組合せ
第一の固形型エプレレノンと第二の固形型エプレレノンを含む組合せで、第一の固形型および第二の固形型エプレレノンが、H型、L型、溶媒和エプレレノン、および無定形エプレレノンから選択される組合せにおいて、第一の固形型と第二の固形型は適当な重量比を用いることができる。通常、このような組合せにおいて、第一の固形型と第二の固形型の重量比は、好ましくは、約1:99から約99:1であり、より好ましくは、約1:9以上であり、より好ましくは、約1:1以上であり、より好ましくは、約2:1以上であり、より好ましくは、約5:1以上であり、もっとも好ましくは、約9:1である。
【0131】
本発明の実施態様によれば、第一の固形型はH型であり、第二の固形型はL型である。
【0132】
別の実施態様では、第三の固体型も存在する。
【0133】
エプレレノンの粒子サイズ
上記した固体型エプレレノンと、それらを組み合わせたものは、広範なエプレレノン粒子サイズを含むことがあり、固体型のエプレレノンの粒子サイズを、約400μmよりも小さなD90粒子サイズになるように削減すると、未処方のエプレレノン、およびこの固形型エプレレノンを含む薬学的組成物の生物利用可能性を向上させ得ることが発見されている。したがって、未処方のエプレレノン、または薬学的組成物調製における出発物質として使用されるエプレレノンのD90粒子サイズは、通常、約400μmよりも小さく、好ましくは、約200μmよりも小さく、より好ましくは、約150μmよりも小さく、さらに好ましくは、約100μmよりも小さく、なおいっそう好ましくは、約90μmよりも小さい。
【0134】
一つの実施態様において、D90粒子サイズは、約25μmよりは小さくない。約25μmから約400μmまでのD90粒子サイズが、通常、ほとんどの目的に許容できる生物利用可能性を有すると認められ、より小さい寸法に粉末化することに伴う費用や環境への排出調節をする必要性が高まることを避けることができる。少なくとも部分的には、H型エプレレノンの溶解速度が速くなることから、このサイズ範囲で許容される生物利用可能性は、特に、実質的なエプレレノン画分がH型エプレレノンとして存在するときに得ることができる。本実施態様による、適当なD90粒子サイズ範囲は、約40〜約100μmである。もう一つの適当な範囲は、約30〜約50μmである。さらに別の適当な範囲は、約50〜約150μmである。さらに別の適当な範囲は、約75〜約125μmである。
【0135】
粉末化、磨砕、微粉化、またはその他、当技術分野において既知の粒子サイズ削減法を用いて、固体エプレレノンを、上で示した所望のサイズ範囲にすることができる。例えば、エアジェットまたは破砕粉末化(fragmentation milling)が、この目的にとっては有効である。
【0136】
費用にはこだわらずに、できるだけ高い生物利用可能性を得ようとするときには、固体型エプレレノンの粒子サイズを約15μmよりも小さなD90粒子サイズに削減すると、未処方のエプレレノン、およびこの固形型エプレレノンを含む薬学的組成物の生物利用可能性を、上で定義したD90粒子サイズ範囲と比較しても、さらに向上させることができることが発見されている。したがって、一つの実施態様において、D90粒子サイズは、約0.01μm(10 nm)から約15μmである。好ましくは、この実施態様において、D90粒子サイズは、約10μmよりも小さく、より好ましくは、約1μmよりも小さく、さらにより好ましくは、約800 nmよりも小さく、さらにいっそう好ましくは、、約600 nmよりも小さく、もっとも好ましくは、約400 nmよりも小さい。応用場面によって、D90粒子サイズの適当な範囲は、約100 nmから約800 nmになる。別の適当な範囲は、約200 nmから約600 nmである。さらに別の適当な範囲は、約400 nmから約800 nmである。さらに別の適当な範囲は、約500 nmから約1μmである。
【0137】
D90粒子サイズが約15μmよりも小さな固体型エプレレノンを、当技術分野において既知で、利用可能な粒子サイズ削減技術にしたがって調製することができる。このような技術には、参照として本明細書に組み入れられる以下の特許および刊行物に記載されている技術があるが、これらに限定されることはない。


【0138】
具体的な処理例では、粗製固体エプレレノンが本質的に不溶でプレミックス懸濁液となるように、粗製固体エプレレノンを液体培地に加える。液体培地におけるエプレレノン濃度は、0.1%から60%まで変えることができるが、好ましくは、重量にして、約5%から約30%である。プレミックス懸濁液のみかけの粘性は、1000 cPよりも低いことが好ましい。
【0139】
このプレミックスは、例えば、ボールミルを用いるなど、エプレレノンのD90粒子サイズを所望の大きさにするために、直接、機械的な装置にかけることができる。または、まず、例えば、回転ミルやコールズ(Cawles)型ミキサーを用いてプレミックスを激しく撹拌し、大きな塊が裸眼で見えなくなって均一な分散液に見えるようにしてから、例えば、培地再循環式ミルを用いるなどして摩滅させる。
【0140】
粒子は、例えば、ポリマーや湿潤剤などの表面修飾剤存在下で粉末化することができる。または、摩滅後、粒子を表面修飾剤と接触させることもできる。表面修飾剤は、粒子が塊になるのを抑えたり、その他の利点をもつ。
【0141】
エプレレノンがあまり分解されない温度下で、粒子の大きさを減少させなければならない。通常は、約30〜40℃よりも低い処理温度が好適である。望ましい場合には、通常の冷却装置によって処理装置を冷却してもよい。本方法は、大気温度、および粉末化処理にとって安全で効果的な処理圧力で適宜行なうことができる。例えば、ボールミル、摩擦ミル、および振動ミルでは、大気圧で処理を行なうのが一般的である。覆いをしたり、氷水の中にミルチャンバーを浸すなどして、温度調節を行うことができる。約0.07から約3.5 kg/cm2までの処理圧力が想定されるが、約0.7から約1.4 kg/cm2という圧力が一般的である。
【0142】
粉末化が完了したら、濾過、メッシュスクリーンなどによる篩など、通常の分離技術を用いて、乾燥して、または液状になって分散している状態の粉末化産物から磨砕用培地を分離する。
【0143】
薬学的組成物
本発明の範囲には、(i)L型エプレレノン、選択的には、H型、溶媒和した結晶形、および無定形のエプレレノンからなる群より選択される、一種類以上のさらに別の固体型エプレレノンをともに含むL型エプレレノン、(ii)一種類以上の薬学的に許容される担体および/または稀釈剤および/またはアジュバント(まとめて「賦形剤」と称する)、および、選択的には、(iii)エプレレノン以外の一種類以上の活性成分を含む薬学的組成物も含まれる。好適な態様においては、組成物に含まれるエプレレノンの全量が本質的に、位相が純粋なL型として存在し、たとえ、固体型を組み合わせたものが存在する場合でも、固体型の重量比が本明細書で上記したものとなっている。
【0144】
または、組成物に含まれるエプレレノンの全量が、本質的に、位相が純粋な溶媒和結晶エプレレノンとして、または無定形エプレレノンとして存在しうる。
【0145】
本発明の別の実施態様において、組成物は、H型とL型の両方を含む。組成物における、H型に対するL型の重量比は、通常、約1:20から約20:1である。別の実施態様では、この重量比は、約10:1から約1:10;約5:1から約1:5;約2:1から約1:2;例示的には、この重量比は1:1でもよい。
【0146】
本発明に係る組成物は、経口経路、口内経路、舌下経路、例えば、血管内、腹膜内、皮下または筋肉内など非経口経路、局所経路、および(例えば、坐薬などの)直腸経路など、適当な経路のいずれにも適合させることができる。これらの組成物は、所望の量のエプレレノンを、所望の投与経路に適した、薬学的に許容される一種類以上の賦形剤とともに含む。
【0147】
1.経口組成物およびその賦形剤
このような組成物の経口投薬用剤形は、好ましくは、希釈剤、崩壊剤、結合剤および接着剤、界面活性剤、潤滑剤および固結防止剤からなる群より選択される一種類以上の賦形剤を含む。より好ましくは、このような経口投薬用剤形は、投与するのに便利なように錠剤にしたりカプセルに詰めたりする。その結果できた錠剤またはカプセルは、例えば、ヒドロキシプロピルメチルセルロース(HPMC)にエプレレノンを分散させて提供することのできるような、即放性処方剤および/または徐放性処方剤を含むことができる。
【0148】
賦形剤を適宜選択および組み合わせることにより、数ある特性の中でも、効能、生物学的利用能、クリアランス時間、安定性、賦形剤に対するエプレレノンの親和性、安全性、溶解プロフィール、分解プロフィールならびに/または他の薬物動態学的特性、化学的特性ならびに/または物理的特性などに関して、効率が改善した組成物を提供することができる。賦形剤は、好ましくは水溶性または水分散性であり、エプレレノンの低水溶度を相殺する湿潤特性をもっている。組成物が錠剤で処方される場合、選択された賦形剤の組合わせは、数ある特性の中で、溶解性もしくは分解性のプロフィール、硬度、破砕強度および/もしくは破砕性において改善を示す錠剤を提供することができる。
【0149】
1.1.希釈剤
本発明の構成物は、選択的に、賦形剤として薬学的に許容される希釈剤を一種類以上含む。適切な希釈剤は、具体的には、以下のものを単独または組み合わせたものがある。すなわち、無水ラクトースおよび一水和ラクトースなどのラクトース;直接圧縮性(directly compressible)デンプンおよびデンプン加水分解物などのデンプン(例えば、登録商標セリュタブ(Celutab)および登録商標エムデックス(Emudex));マンニトール;ソルビトール;キシリトール;デキストロース(例えば、登録商標セレロース2000(Cererose 2000))およびデキストロース一水和物;二塩基性リン酸カルシウム二水和物;スクロース希釈剤;精製糖;一塩基性硫酸カルシウム一水和物;硫酸カルシウム二水和物;顆粒状の乳酸カルシウム三水和物;デキストラン酸;イノシトール;加水分解した固形穀類;アミロース;微結晶化セルロースなどのセルロース;食用α-セルロースおよび無定形セルロース(例えば、商標登録レクセル(Rexcel))ならびに粉末セルロース;炭酸カルシウム;グリシン;ベントナイト;ポリビニルピロリドンなどである。このような希釈剤が存在する場合には、全部で、組成物の全重量の約5%から99%、好ましくは約10%から85%、およびより好ましくは約20%から80%を構成する。選択された希釈剤は、好ましくは、適切な流動特性、また、錠剤が望ましい場合には圧縮性を示す。
【0150】
ラクトースおよび微結晶化セルロースが、単独でも組み合わせても、好ましい希釈剤となる。どちらの希釈剤もエプレレノンと化学的親和性がある。極顆粒状の微結晶化セルロース(すなわち、乾燥過程のあとに、湿った顆粒化組成物に添加した微結晶化セルロース)を、(錠剤のための)硬度および/または分解時間を改善するために用いることができる。ラクトース、特に、ラクトース一水和物が好ましい。ラクトースは、一般的に、比較的希釈剤が低価で、エプレレノンの適切な放出速度、安定性、圧縮前の流動性、および/または乾燥性などの特性を付与する。ラクトースは、(湿式造粒法を用いる場合)造粒中の固化を促進する高密度基質を提供し、その結果、混合物の流動性を向上させる。
【0151】
1.2.崩壊剤
本発明に係る組成物は、特に錠剤として投与するために、選択的に、一種類以上の薬学的に許容される崩壊剤を賦形剤として含む。適切な崩壊剤には、以下のものを単独または組み合わせたものがある。すなわち、グリコール酸ナトリウムデンプン(例えば、パン・ウェスト社(Pan West)の登録商標エクスプロタブ(Exprotab))およびアルファ化コーンスターチ(例えば、登録商標ナショナル(National)1551、登録商標ナショナル(National)1550、および登録商標コロコーン(Colocorn)1550)、粘土(例えば、登録商標ビーガム(Veegum)HV)、精製セルロース、微結晶化セルロース、メチルセルロース、カルボキシメチルセルロースおよびカルボキシメチルセルロースナトリウムなどのセルロース、クロスカルメロースナトリウム(例えば、FMC社の商標登録Ac‐Di‐Sol(Ac-Di-Sol))、アルギン酸、クロスポビドン、ならびに寒天、グアールガム、ローカストビーンガム、カラヤゴム、ペクチンおよびトラガカントガムなどの増粘剤などである。
【0152】
崩壊剤は、組成物を調製する間の適当な工程、特に造粒前の工程、または圧縮処理の前の潤滑処理工程で加えることができる。このような崩壊剤が存在する場合には、全部で、組成物の全重量の約0.2%から30%、好ましくは約0.2%から10%、およびより好ましくは約0.2%から5%を構成する。
【0153】
クロスカルメロースナトリウムは、錠剤またはカプセルを分解するための好適な崩壊剤であり、これがが存在する場合には、好ましくは、全体で、組成物の全重量の約0.2%から30%、より好ましくは約0.2%から7%、およびよりいっそう好ましくは約0.2%から5%を構成する。クロスカルメロースナトリウムは、本発明の顆粒化組成物に優れた顆粒内分解能を与える。
【0154】
1.3.結合剤
本発明に係る組成物は、特に錠剤として投与するために、選択的に、薬学的に許容される一種類以上の結合剤または粘着剤を賦形剤として含む。このような結合剤および粘着剤は、好ましくは、分粒、潤滑、圧縮および包装などの通常の加工作業を可能にするが、摂取されると錠剤が分解して組成物の吸収を可能にするような粘着力を、錠剤処理中の粉末に与える。適切な結合剤および粘着剤には、以下のものを単独または組み合わせたものがあるが、これらに限定されない。すなわち、アラビアゴム;トラガカントガム;ショ糖;ゼラチン;ブドウ糖;アルファ化デンプン(例えば、登録商標ナショナル(National)1551、登録商標ナショナル(National)1550、および登録商標コロコーン(Colocorn)1550)などのデンプン;メチルセルロースおよびカルボキシメチルセルロースナトリウム(例えば、登録商標タイロース(Tylose))などのセルロース;アルギン酸およびアルギン酸塩;ケイ酸マグネシウムアルミニウム;ポリエチレングリコール(PEG);グアールガム;ポリサッカライド酸;ベントナイト;例えば、ポビドンK-15、K-30およびK-29/32のようなポリビニルピロリドン(ポビドンまたはPVP);ポリメタクリル酸;HPMC;ヒドロキシプロピルセルロース(例えば、登録商標クルセル(Klucel));エチルセルロース(例えば、登録商標エトセル(Ethocel))などがあるが、これらに限定されない。このような結合剤および/または粘着剤が存在する場合には、好ましくは、全体で、組成物の全重量の約5.5%から25%、好ましくは、約0.75%から15%、およびより好ましくは、約1%から10%を構成する。
【0155】
HPMCは、エピレレノン処方剤の混合粉末に粘性を与えるために用いるのに好適な結合剤である。HPMCが存在する場合には、好ましくは、全体で、組成物の全重量の約0.15%から10%、好ましくは、約1%から8%、およびより好ましくは、約2%から4%を構成する。粘度が約2 cP(センチポイズ)から6 cP、特に粘度が約2 cPから4 cPが好ましいが、一般的には、約2 cPから8 cPの粘度をもつ低分子量HPMCが用いられる。HPMCの粘度は、20℃で2パーセント水溶液として測定される。HPMCのメトキシ基含有量は、一般的に約15%から約35%であり、一方、ヒドロキシプロピル含有量は、一般的には、最大約15%まで、好ましくは最大約12%である。
【0156】
1.4.湿潤剤
エピレレノンは、水溶液中でおおむね不溶である。したがって、本発明に係る組成物は、選択的にではあるが、好ましくは、一種類以上の薬学的に許容される湿潤剤を賦形剤として含む。このような湿潤剤は、好ましくは、エピレレノンを水になじませておくために、すなわち組成物の相対的生物利用可能性が向上すると考えられている状態を維持するために選択される。
【0157】
本発明に係る組成物において湿潤剤として用いることのできる界面剤の制限的でない例には以下のものがある。例えば、塩化ベンズアルコニウム、塩化ベンズエトニウムおよび塩化セチルピリジニウムなどの第4アンモニア化合物、ジオクチルスルホサクシン酸ナトリウム、例えば、ノンオキシノール9、ノンオキシノール10およびオクトキシノール9などのポリオキシエチレンアルキフェニルエーテル、ポルオキサマー(ポリオキシエチレンおよびポロオキシプロピレンのブロック共重合体)、例えば、ポリオキシエチレン(8)カプリルモノグリセリドおよびジグリセリド(例えば、ガットフォセ社(Gattefosse)のラブラゾル(Labrasol))、ポリオキシエチレン(35)、ひまし油およびポリオキシエチレン(40)硬化ひまし油などのポリオキシエチレン脂肪酸グリセリドおよびポリオキシエチレン脂肪酸グリセリド油;例えば、ポリオキシエチレン(20)セトステアリルエーテルなどのポリオキシエチレンアルキルエーテル、例えば、ステアリン酸ポリオキシエチレン(40)などのポリオキシエチレン脂肪酸エステル、例えば、ポリソルベート20およびポリソルベート80(ICI社の登録商標トゥイーン(Tween))などのポリオキシエチレンソルビタンエステル、例えば、ラウリン酸プロピレングリコール(例えば、ガットフォセ社(Gattefosse)の登録商標ラウログリコール(Lauroglycol))などのプロピレングリコール脂肪酸エステル、ラウリル硫酸ナトリウム、例えば、オレイン酸、オレイン酸ナトリウムおよびオレイン酸トリエタノールアミンなどの脂肪酸およびその塩、例えば、モノステアリン酸グリセリンなどのグリセリル脂肪酸エステル、例えば、ソルビタンモノラウレート、ソルビタンモノオレエート、ソルビタンモノパルミテートおよびソルビタンモノモノステアレートなどのソルビタンエステル、チロキサポールおよびその混合物などである。このような湿潤剤が存在する場合には、好ましくは、全体で、組成物の全重量の約0.25%から15%、好ましくは約0.4%から10%、およびより好ましくは約0.5%から5%を構成する。
【0158】
陰イオン界面活性剤である湿潤剤が好ましい。ラウリル硫酸ナトリウムが特に好ましい湿潤剤である。ラウリル硫酸ナトリウムが存在する場合には、好ましくは、全体で、組成物の全重量の約0.25%から7%、より好ましくは約0.4%から4%、およびよりいっそう好ましくは約0.5%から2%を構成する。
【0159】
1.5.潤滑剤、流動促進剤および固結防止剤
本発明に係る組成物は、選択的に、一種類以上の薬学的に許容される潤滑剤および/または流動促進剤を賦形剤として含む。適当な潤滑剤および/または流動促進剤には、以下のものを単独または組み合わせたものがある。すなわち、グリセリルビハペート(glyceryl behapate)(例えば、登録商標コンプリトール(Compritol)888);ステアリン酸マグネシウム、ステアリン酸カルシウムおよびステアリン酸ナトリウムなどのステアリン酸およびその塩;硬化植物油(例えば、登録商標ステロテックス(Sterotex));コロイド状シリカ;タルク;蝋;ホウ酸;安息香酸ナトリウム;酢酸ナトリウム;フマル酸ナトリウム;塩化ナトリウム;DL-ロイシン;ポリエチレングリコール(登録商標カーボワックス(Carbowax)4000および登録商標カーボワックス(Carbowax)6000);オレイン酸ナトリウム;ラウリル硫酸ナトリウム;ならびにラウリル硫酸マグネシウム。このような潤滑剤および/または流動促進剤が存在する場合には、好ましくは、全体で、組成物の全重量の約0.1%から10%、より好ましくは約0.2%から8%、およびよりいっそう好ましくは約0.25%から5%を構成する。
【0160】
ステアリン酸マグネシウムが、例えば、、錠剤処方剤の圧縮中に生じる、装置と顆粒混合物との間の摩擦を減らすために用いる。好ましい潤滑剤である。
【0161】
適切な固結防止剤には、タルク、DL-ロイシン、コーンスターチ、ラウリル硫酸ナトリウムおよび金属ステアリン酸がある。タルクは、例えば、装置の表面への処方の付着を減らしたり、また、混合物の静電気を減らしたりするのに用いる、好ましい固結防止剤または流動促進剤である。タルクが存在する場合には、好ましくは、全体で、組成物の全重量の約0.1%から10%、より好ましくは約0.2%から5%、およびよりいっそう好ましくは約0.5%から2%を構成する。
【0162】
1.6.他の賦形剤
着色料、香料、甘味料などの他の賦形剤が製薬技術分野において既知であり、本発明の組成物中に使用することができる。錠剤は、例えば、腸溶コーティングなどでコーティングしたり、コーティングしなかったりすることができる。本発明に係る組成物は、さらに、例えば、緩衝剤などを含むことがある。
【0163】
1.7.好適な経口用組成物
一つの実施態様において、本発明に係る組成物は、所望量のエプレレノン、および一種類以上のセルロース賦形剤を含む。「セルロース賦形剤」とは、セルロースまたはそれの誘導体を含む賦形剤を包含し、精製セルロース、微結晶化セルロース、アルキルセルロースおよびそれらの誘導体と塩(例えば、メチルセルロース、エチルセルロース、ヒドロキシプロピルセルロース、HPMC、カルボキシメチルセルロース、クロスカルメロースナトリウムなどのカルボキシメチルセルロースナトリウム)など。好ましくは、このように存在するセルロース賦形剤の少なくとも一種類は、(C1-6アルキル)セルロース、およびそれらの誘導体と塩からなる群より選択される。さらにより好ましくは、このセルロース賦形剤は、ヒドロキシ(C2-4アルキル)-(C1-4アルキル)-セルロース、およびそれらの誘導体と塩からなる群より選択される。
【0164】
本実施態様の組成物は、好ましくは、さらに、希釈剤、崩壊剤、結合剤、湿潤剤、潤滑剤および固結防止剤からなる群より選択される一種類以上の賦形剤を含む。より好ましくは、これらの組成物は、ラクトース、微結晶化セルロース、クロスカルメロースナトリウム、HPMC、ラウリル硫酸ナトリウム、ステアリン酸マグネシウム、およびタルクからなる群より選択される一種類以上の賦形剤を含む。よりいっそう好ましくは、これらの組成物は、ラクトース一水和物、微結晶化セルロース、クロスカルメロースナトリウム、およびHPMCを含み、もっとも好ましくは、さらに、ラウリル硫酸ナトリウム、ステアリン酸マグネシウム、およびタルクからなる群より選択される一種類以上の別の賦形剤を含む。
【0165】
本実施態様において、上記した各賦形剤は、所望であれば、選択的に、他の適当な賦形剤に代えることができる。許容できる代替賦形剤は、エプレレノンともその他の賦形剤とも化学的に親和性のあるものである。これ以外の希釈剤、崩壊剤、結合剤および接着剤、湿潤剤、潤滑剤、および/または固結防止剤、または滑動剤(glindant agent)を用いることができるが、ナノ粒子エプレレノン、ラクトース、微結晶化セルロース、クロスカルメロースナトリウム、およびHPMC、さらに、選択的には、ラウリル硫酸ナトリウム、ステアリン酸マグネシウム、および/またはタルクを含む組成物が、通常、この種の他の組成物に較べて、薬物動態学上、化学的に、および/または物理上優れた特性の組合せである。
【0166】
別の実施態様において、本発明に係る組成物は、
約1%から約95%のエプレレノン、
約5%から約99%の薬学的に許容される希釈剤、
約0.5%から約30%の薬学的に許容される崩壊剤、および
約0.5%から約25%の薬学的に許容される結合剤を含むが、これらの割合はすべて重量単位である。このような組成物は、選択的に、さらに、約0.25%から約15%の薬学的に許容される湿潤剤;約0.1%から約10%の薬学的に許容される潤滑剤;および/または約0.1%から約15%の薬学的に許容される固結防止剤を含むことができる。
【0167】
さらに別の実施態様において、本発明に係る組成物は、好ましくは、錠剤またはカプセルであり、エプレレノン、および上記定義によるセルロース賦形剤を含んだ経口投薬剤形にある。好ましくは、該組成物は、ラクトース一水和物、微結晶化セルロース、クロスカルメロースナトリウム、ヒドロキシプロピルメチルセルロース、ラウリル硫酸ナトリウム、ステアリン酸マグネシウム、およびタルクからなる群より選択される一種類以上の賦形剤を含む。
【0168】
2.非経口用組成物
本発明に係る固体型エプレレノンは、例えば、食塩水、デキストロース溶液または水などの担体液中の固体エプレレノンの懸濁液を、例えば、静脈内、筋肉内、または皮下などの注射によって非経口的に投与することができる。懸濁組成物は、本明細書で経口用組成物について開示したものから選択される適当な賦形剤成分を含むことができる。
【0169】
3.経皮用組成物
例えば、約0.75%から約30%、好ましくは、重量で約0.2%から約20%、より好ましくは、重量で約0.4%から約15%の量の固体エプレレノンが分散している、局所用または経皮用軟膏またはクリームの形にすることができる。このような局所用または経皮用組成物は、望ましくは、エプレレノンが皮膚に吸収または貫通することを促進する組成物を含む。このような皮膚透過促進化合物は、ジメチルスルホキシドおよびその関連化合物を含む。
【0170】
新規の固体型エプレレノンは、貯蔵容器または多孔性メンブレン型または固体マトリックス型のいずれかのパッチを用いて経皮的に投与することができる。どちらの場合にも、エプレレノンは、貯蔵容器から、または微小カプセルから、メンブレンを通って、対象者の皮膚または粘膜に接触しているエプレレノン透過接着剤の中に連続的に輸送される。エプレレノンが皮膚を通って吸収されると、制御されかつ予め決められたエプレレノンの流れがレシピエントに投与される。微小カプセルの場合には、カプセル化剤がメンブレンの働きをすることもできる。
【0171】
治療または予防の方法
本発明は、アルドステロンを媒介とする状態または疾患の治療および/または予防のための方法であって、治療効果を有する量の固体エプレレノンまたは固体エプレレノンを含む医薬組成物を用いて、少なくとも、L型エプレレノンおよび他に一つまたは複数のH型エプレレノン、溶媒和した結晶エプレレノンおよびアモルファスエプレレノンを含む検出可能な割合の固体エプレレノンを用いて、このような状態または疾患を持つまたは生じやすい被検者を治療する工程を含む方法を含む。このような方法は、アルドステロンアンタゴニストの投与を必要とする被検者において、状態または疾患の治療および/または予防のために有用であり、このような治療には、高血圧、心不全を含む心臓疾患、肝硬変、過剰なコラーゲン、線維症、良性前立腺肥大およびうつ病といった高アルドステロン症の状態の治療が含まれるが、それに限らない。
【0172】
ヒトの治療に有用である上に、これらの固体状エプレレノンおよびその医薬組成物は、コンパニオンアニマル、外来性の動物および家畜、例えば、ウマ、イヌおよびネコの獣医学的治療にも有用である。
【0173】
固体状エプレレノンおよびその医薬組成物は、(i)他のアルドステロン受容体アンタゴニストの部分的な、または、完全な代わりとして組み合わせ治療において、および/または、(ii)他の薬剤との組み合わせ治療において用いることもできる。「組み合わせ治療」とは、薬剤の組み合わせの有益な効果を提供する投薬計画において、それぞれの薬剤を順次投与することを含み、同様に、薬剤を実質的に同時に共同して投与すること、例えば、これらの作用物質を固定された比で含む単独のカプセルまたは注射剤において、または、一つにつき一つの物質を含む複数の別々の投与形態または注射剤において投与することも含む。このような併用療法の非限定的な例には、国際公開公報第96/24373号に記載されているような、アルドステロンレセプター拮抗薬とアンギオテンシンIIレセプター拮抗薬を併用して用いる、心臓血管疾患の治療法、国際公開公報第96/40257号に記載されているような、アルドステロンレセプター拮抗薬とアンギオテンシンIIレセプター拮抗薬を併用して用いる、鬱血性心臓疾患の治療法、および、国際公開公報第96/24373号に記載されているような、アルドステロンレセプター拮抗薬、ACEインヒビター、および利尿剤を併用して用いる、心臓疾患の治療法があり、これらの刊行物はすべて、参照として本明細書に組み入れられる。
【0174】
実施例
以下の実施例は、本明細書に記載したエプレレノンの様々な固相状態の調製方法の詳細な説明を含む。これらの詳細な説明は、本発明の範囲に含まれ、その範囲を如何なるようにも制限することなく本発明を説明する。百分率は、特に明記していない限り、全て重量である。以下の実施例のそれぞれにおいて用いられるエプレレノン開始材料は、先に引用した国際公開公報第98/25948号に記載のスキーム1に従って調製した。
【0175】
実施例1:高純度エプレレノン開始材料からのメチルエチルケトン溶媒和化合物の調製と溶媒和化合物からのL型エプレレノンの調製
A. メチルエチルケトン溶媒和化合物の調製
高純度エプレレノン(純度>99%で、ジエポキシドおよび11,12-エポキドの全量が<0.2%)437 mgを、900 rpmで磁石攪拌子によって攪拌しながらホットプレート上で沸騰するまで加熱することによって、メチルエチルケトン10 mlに溶解した。得られた溶液を、磁石攪拌子によって絶えず攪拌しながら室温まで冷却した。室温に達した後、溶液を1℃の水浴に移して1時間攪拌する。冷溶液から固体のメチルエチルケトン溶媒和化合物を真空濾過によって回収した。
【0176】
B. L型エプレレノンの調製
上記のように調製した固体メチルエチルケトン溶媒和化合物を、100℃の炉の中で大気圧で4時間乾燥させた。乾燥した固体は、DSCおよびXRPD分析によって純粋なL型であると決定された。
【0177】
実施例2.高純度エプレレノン開始材料からのさらなる溶媒和化合物の調製
メチルエチルケトンを以下の溶媒のそれぞれに置換することによって、さらなる溶媒和結晶型を実質的に実施例1に記載のように調製した:n-プロパノール、2-ペンタノン、酢酸、アセトン、酢酸ブチル、クロロホルム、エタノール、イソブタノール、酢酸イソブチル、イソプロパノール、酢酸メチル、プロピオン酸エチル、n-ブタノール、n-オクタノール、酢酸プロピル、プロピレングリコール、t-ブタノール、テトラヒドロフラン、およびトルエン。
【0178】
実施例3:気相拡散成長によるメチルエチルケトン溶媒和化合物の調製
エプレレノン(純度>99.9%)400 mgを、ホットプレート上で加温することによってメチルエチルケトン20 mlに溶解して、保存液を調製した。保存液8mlをメチルエチルケトン10 mlで希釈して、得られた溶液を80%希釈試料と呼ぶ。保存液4 mlを、メチルエチルケトンで10 mlで希釈した(40%希釈試料)。保存液2 mlをメチルエチルケトン10 mlで希釈した(20%希釈試料)。20 mlシンチレーションバイアルに入った様々な希釈試料を、抗溶媒として少量のヘキサンを含むデシケータ瓶に移した。デシケータ瓶を密封して、ヘキサン蒸気をメチルエチルケトン溶液に拡散させた。エプレレノンのメチルエチルケトン溶媒和化合物の結晶は、80%希釈試料において24時間以内に成長した。
【0179】
実施例4.ロータリー・エバポレーターによるエプレレノンの溶媒和化合物結晶型の調製
エプレレノン(純度>99.9%)約400 mgを250 ml丸底フラスコに計り取った。メチルエチルケトンおよび実施例2に記載した溶媒から選択される溶媒150 mlをフラスコに加え、必要であれば、エプレレノンが溶解するまで溶液を緩く加熱する。得られた透明な溶液を、85℃の水浴を備えたブッキロータリーエバポレーターに入れて、溶媒を真空で除去した。溶媒約10 mlがフラスコに残った時点で、溶媒除去を停止する。得られた固体を、結晶型の決定のために適当な方法(例えば、XRPD、DSC、TGA、顕微鏡等)によって分析する。
【0180】
実施例5:スラリーの変換
L型エプレレノン約150 mgおよびH型エプレレノン150 mgを酢酸エチル5 mlに加えた。得られたスラリーを300 rpmで磁石攪拌子によって一晩攪拌した。翌日、得られた固体の試料を濾過によって回収した。XRPDによる試料の分析から、試料が完全にL型エプレレノンで構成されていることが示された。
【0181】
実施例6:(a)低純度エプレレノン開始材料からの溶媒和化合物の調製および(b)得られた溶媒和化合物からのH型結晶エプレレノンの調製
本明細書に記載した様々な量のジエポキシド、または11,12-エポキシド不純物を含む試料は、不純物の所望の量を、総試料塊が100 mgとなるために十分なエプレレノンの量と共に7 mlシンチレーションバイアルに加えることによって調製した。それぞれの試料中の不純物の含有量を表6Aおよび6Bに示し、不純物はそれぞれジエポキシドまたは11,12-エポキシドである。それぞれのシンチレーションバイアルに、メチルエチルケトン1 mlと共に微小磁石攪拌子を加えた。バイアルに緩くキャップをして、固体をホットプレート上で磁石攪拌子によって攪拌しながら加熱還流して溶解した。溶解が完了すれば、得られた溶液を絶えず攪拌しながら室温まで冷却した。次に、得られた固体を真空濾過によって回収して、XRPDによって直ちに分析した。次に固体を100℃の炉に入れて、大気圧で1時間乾燥した。乾燥した固体のH型含有量を、約12.1゜2θでのH型回折ピークの面積をモニターすることによって、XRPDによって分析した。XRPD回折パターンは全て、アイネル多目的回折計を用いて記録した。
【0182】
【表6A】

実施例6におけるエプレレノン原料の組成
【表6B】

実施例6におけるエプレレノン開始材料の組成
【0183】
A.ジエポキシドの結果
図13は、(a)0%、(b)1%、(c)3%および(d)5%ジエポキシドを処理したメチルエチルケトン結晶から得られたメチルエチルケトン溶媒和化合物の湿ケークのXRPDパターンを示す。ピーク強度は比較を容易にするために標準化した。H型またはジエポキシドに特徴的なピークは回折パターンに存在しない。パターンは、エプレレノンのメチルエチルケトン溶媒和化合物の特徴を示す。
【0184】
図14は、(a)0%、(b)1%、(c)3%および(d)5%ジエポキシドを処理したメチルエチルケトン結晶から得られた乾燥固体のXRPDパターンを示す。ピーク強度は比較を容易にするために標準化した。ジエポキシド処理レベルが0%または1%である場合、メチルエチルケトン結晶に対応する乾燥試料中にH型は検出されなかった。処理レベルが3%または5%である場合、メチルエチルケトン結晶に対応する乾燥試料中にH型を検出した。各試料について約12.1゜2θでのH型回折ピーク面積およびH型推定含有量を表6Cに示す。
【表6C】

実施例6におけるメチルエチルケトン結晶からのデータ
【0185】
表6Cに報告した結果から、ジエポキシドの存在は溶媒除去の際のH型エプレレノンの形成に影響を及ぼすことが確認される。H型の形成は、ジエポキシドがメチルエチルケトン溶媒和化合物結晶に組み入れられたおよび/または吸着された場合に誘導される。
【0186】
第二の3%ジエポキシド処理実験を行って、溶媒除去の際に形成されたH型の量に及ぼす調製経路の影響を分析した。この実験では、処理した結晶から得られたエチルメチルケトン溶媒和化合物を2つの部分に分けた。第一の部分は無処置のままであり、第二の部分は、乳鉢と乳棒で軽くすりつぶして、より高いレベルの結晶のきずを誘導した。2つの部分はいずれも100℃の大気圧で1時間乾燥させた。乾燥した固体をXRPDによって分析した。乾燥前に溶媒和化合物を(a)すりつぶさない場合および(b)すりつぶした場合のジエポキシドの3%処理による、メチルエチルケトン結晶からの乾燥固体に関して、XRPDパターンを図15に示す。XRPDパターンによって、すりつぶしていない試料と比較してすりつぶした試料ではH型の量がより多いことが示された。これらの結果は、メチルエチルケトン溶媒和化合物を単離して取り扱う条件が、溶媒除去によって得られた結晶型に影響を及ぼしうることを示唆している。
【0187】
B.11,12-エポキシドの結果
図16は、(a)0%、(b)1%、(c)5%および(d)10%11,12-エポキシド処理メチルエチルケトン結晶から得られたメチルエチルケトン溶媒和化合物湿ケークのXRPDパターンを示す。ピーク強度は比較を容易にするために標準化した。H型または11,12-エポキシドに特徴的なピークは回折パターンに存在しない。パターンは、エプレレノンのメチルエチルケトン溶媒和化合物の特徴を示す。
【0188】
図17は、(a)0%、(b)1%、(c)5%および(d)10%11,12-エポキシドを処理したメチルエチルケトン結晶から得られた乾燥固体のXRPDパターンを示す。ピーク強度は比較を容易にするために標準化した。11,12-エポキシド処理レベルが0%、1%または5%である場合、メチルエチルケトン結晶に対応する乾燥試料中にH型は検出されなかった。11,12-エポキシド処理レベルが10%である場合、メチルエチルケトン結晶に対応する乾燥試料中にH型を検出した。各試料について約12.1゜2θでのH型回折ピーク面積およびH型推定含有量を表6Dに示す。
【表6D】

実施例6におけるメチルエチルケトン結晶からのデータ
【0189】
表6Dに報告した結果は、11,12-エポキシドの存在が溶媒除去の際のH型エプレレノンの形成に影響を及ぼすことを確認する。H型エプレレノンの形成を誘導するために必要なメチルエチルケトン結晶中の不純物のレベルは、11,12-エポキシドではジエポキシドの場合より大きいように思われる。
【0190】
実施例7:最終結晶型に及ぼす結晶化と乾燥の影響
最終結晶型に及ぼす結晶化と乾燥の影響を分析する以下の4つの実験を実施した:(i)エプレレノンのメチルエチルケトン結晶(実験の23+3統計デザイン)、(ii)低品質母液残査の結晶化、(iii)H型シード添加による高純度エプレレノンの結晶化、および(iv)L型シード添加による低純度エプレレノンの結晶化。これらの実験における変数には、冷却速度、開始材料純度レベル、および結晶化のエンドポイント温度が含まれた。この実施例の目的に関して、高純度エプレレノンは、超純粋(HPLCによる)粉砕エプレレノンとして定義し、低純度エプレレノンは純度89%のエプレレノンとして定義した。低純度エプレレノンを調製するために、エプレレノンの調製のためのプロセスから得られる結晶除去後の母液を分析して、61.1%エプレレノン、12.8%ジエポキシドおよび7.6%11,12-エポキシドである材料を生成するように混和した。次に、この材料を高純度エプレレノンの十分量と混和すると、89%エプレレノンが得られた。
【0191】
A.メチルエチルケトンの結晶化
メチルエチルケトン結晶化実験において、全ての実験は高純度エプレレノン60 gを用いて実施した。高エンドポイントは45℃として定義し、低エンドポイントは5℃として定義した。高冷却速度は3℃/分として定義し、低冷却速度は0.1℃/分として定義した。中心点は、冷却速度1.5℃/分、エプレレノンの純度94.5%、およびエンドポイント25℃であった。
【0192】
FTIRについてバックグラウンドの読みとりを行った後、メチルエチルケトン250 mlを1LのメトラーRC-1、MP10リアクターに加えて、100 rpmで攪拌した。数回スキャンした後、エプレレノンをリアクターに加えた後、メチルエチルケトン470 mlをさらに加えた。攪拌を500 rpmに増加させて、固体を懸濁させて、バッチ温度を80℃に上昇させた。エプレレノンを確実に溶解させるため、バッチ温度を80℃で保持した。得られた透明な溶液中に、黒または白色の斑点が一般的に見えた。次に、バッチ温度を所望の速度で所望のエンドポイントまで徐々に冷却することによって低下させ、この温度を1時間維持してから、移動用フラスコに入れて濾過すると湿ケークが得られた。次に、リアクター、移動用フラスコおよび湿ケークをメチルエチルケトン120 mlで洗浄した。それぞれの湿ケーク約10 gを、公称条件75℃で軽く窒素を抽気して真空で乾燥させた。湿ケークを高および低条件で流動床乾燥によって乾燥させた。流動層乾燥の高条件は、100℃で送風機の設定を4として定義し、低条件は40℃で送風機の設定を1として定義した。
【0193】
B.低品質母液残査の結晶化
低品質母液残査の結晶化を含む実験において、純度61.1%のエプレレノン60 gおよびメチルエチルケトン720 mlを、1LメトラーRC-1、MP10リアクターに直接加えた。不純物含有エプレレノンは、リアクターに加える前に、高純度エプレレノンと混和しなかった。得られた混合物を80℃に加熱すると、その温度では不透明なスラリーが得られた。結晶化を継続して、混合物を速い冷却条件で45℃で濾過した。
【0194】
C.H型のシード添加
H型シード添加実験において、高純度エプレレノン60 gおよびメチルエチルケトン720 mlを1LメトラーRC-1、MP10リアクターに加えた。混合物を80℃に加熱した後、冷却速度1.5℃/分で25℃に冷却した。溶液が62℃まで冷却されると、相純粋なH型結晶3 gをシード添加して、結晶化を開始させた。H型シード結晶は、下記の実施例9に説明する温浸プロセスによって調製した。
【0195】
D.L型のシード添加
L型シード添加実験において、89.3%エプレレノン66.6 g(高純度エプレレノン48.3 gと61.1%エプレレノン18.3 gの混合によって調製)およびメチルエチルケトン720 mlを1LメトラーRC-1、MP10リアクターに加えた。混合物を80℃に加熱した後、冷却速度1.5℃/分で25℃に冷却した。溶液が63℃に冷却されると、相純粋なL型結晶3 gをシード添加して、結晶化を開始させた。L型シード結晶は、上記の実施例1に説明する結晶化および溶媒除去プロセスによって調製した。
【0196】
E.結果
実験結果を表7Aに報告する。
【0197】
メチルエチルケトン結晶化実験において、H型はジエポキシドを含む低純度エプレレノンを用いた場合に限って検出された。最終産物におけるジエポキシドレベルの上昇も同様に、より高い冷却速度の場合に認められた。
【0198】
低品質母液残査の結晶化を含む実験は、XRPDによって分析するとジエポキシドとH型エプレレノンの混合物であるように思われる低品質材料を生成した。
【0199】
H型シード添加実験(高純度エプレレノンにH型のシードを添加した)は、XRPD分析に基づいてH型77%であるが、DSCに基づくと完全にH型である産物を生じた。しかし、XRPDモデルは、H型が約15%を超えた場合の直線性に関して試験していなかった。この実験は、ジエポキシドの非存在下でH型が形成されたこの実施例の4つの実験の唯一のものであった。
【0200】
L型シード添加実験(低純度エプレレノンにL型のシードを添加した)は、完全にL型である産物を生成した。
【0201】
エプレレノンの高条件流動床乾燥から得られたデータは、真空炉乾燥の場合に得られたデータに対応するように思われた。低条件流動床乾燥は、真空炉乾燥の場合とは異なる結果を生じた。
【0202】
【表7A】

実施例7の結果
1 75℃の真空炉で溶媒和化合物を乾燥後の重量%。
2 XRPDによって分析するとH型とジエポキシドとの混合物であるように思われる。
3 XRPDではH型77%、DSCではH型100%であるように思われる。
ND=検出されない
【0203】
F.材料の純度
表7Aで報告したデータに基づく材料の純度、開始材料の純度、冷却速度およびエンドポイント温度の立方プロットを図18に示す。立方プロットは、結晶化開始時に高純度材料を用いれば、より純度の高い産物を生成することを示唆している。結晶化のエンドポイント温度は、産物の純度に大きい影響を及ぼさないように思われる。しかし、冷却速度は何らかの作用を有するように思われ、冷却速度がより速ければ得られた産物の純度はわずかに低い。実際に、ジエポキシドのレベルは一般的に、冷却速度が速ければ高かった。
【0204】
図19は、変数が、もしあるとすれば産物の純度に統計学的に有意な影響を及ぼすか否かを決定するために、立方プロットの結果を用いて調製した半正常プロットを示す。開始材料の純度は産物の純度に対して最大の統計学的に有意な影響を及ぼしたが、冷却速度の影響と、冷却速度と開始材料純度のあいだの相互作用も同様に統計学的に有意であると見なされた。
【0205】
図20は、これらの結果に基づく相互作用グラフであり、産物の純度に及ぼす開始材料純度と冷却速度との相互作用を示している。エプレレノンの純度が高ければ、冷却速度は最終的な純度にほとんどまたは全く影響を及ぼさないように思われる。しかし、エプレレノンの純度が低ければ(89.3%エプレレノン開始材料)、産物の純度は冷却速度が増加するにつれて減少する。この結果は、結晶化をより速い冷却速度で実施すると、より多くの不純物が結晶化することを示唆している。
【0206】
G.H型の含有量
表7Aにおいて報告したデータに基づくH型重量分画、開始材料産物純度、冷却速度およびエンドポイントデータの立方プロットを図21に示す。立方プロットは、結晶化開始時に高純度のエプレレノンを用いれば、H型の量は少なくなることを示唆している。結晶化のエンドポイント温度は、最終生成物の型に影響を及ぼすように思われる。冷却速度はH型の形成に大きく影響を及ぼさないように思われるが、いくつかのH型は、不純物が存在する場合の低エンドポイント温度でのより速い冷却の結果であるかも知れない。
【0207】
図22は、変数が、もしあるとすれば、最終材料におけるH型の量に統計学的に有意な影響を及ぼすか否かを決定するために、立方プロットの結果を用いて調製した半正常プロットを示す。開始材料の純度、結晶化のエンドポイント温度、およびこれらの2つの変数の相互作用は、統計学的に有意な作用であると見なされた。
【0208】
図23は、これらの結果に基づく相互作用グラフであり、最終的なH型含有量に及ぼす開始材料純度とエンドポイント温度のあいだの相互作用を示す。高純度エプレレノンを用いると、エンドポイント温度はH型含有量にほとんど影響を及ぼさないように思われる。いずれの場合でも純粋なエプレレノンを用いれば、H型は生成されなかった。低純度エプレレノン(89.3%エプレレノン開始材料)では、H型は双方の場合について存在し、より高いエンドポイント温度では有意により多くのH型が存在した。
【0209】
表7Bは、流動床(ラブライン・P.R.L.、高速流動床乾燥器、ラブラインインストルメンツインク)または真空炉(バクスター・サイエンティフィックプロダクツ真空乾燥炉、モデルDP-32)のいずれかを用いて乾燥させた材料において測定したH型の重量分画を報告する。高速流動床または真空炉のいずれにおいても、乾燥させた同等の材料について類似のH型含有量を認めた。しかし、真空炉の場合と比較して低速流動床で乾燥させた同等の材料については差を認めた。
【0210】
【表7B】

H型含有量に及ぼすプロセス変数の影響
ND=検出されない
【0211】
実施例8:溶媒除去の際のメチルエチルケトンからのL型の結晶化
H型エプレレノン10 gをメチルエチルケトン80 mlと混合した。混合物を加熱還流して(79℃)室温で約30分攪拌した。スラリーを65℃、50℃、35℃、および25℃で、それぞれの温度で約90分維持することによる段階的なホールドポイントプロトコールによって、得られたスラリーを冷却した。スラリーを濾過して、メチルエチルケトン約20 mlによってすすいだ。得られた単離固体を濾紙上で乾燥させた後、40〜50℃の真空炉で乾燥させた。乾燥は90〜100℃の真空炉で完了させた。溶媒除去した固体は回収率82%で得られた。XRPD、MIRおよびDSCによって、固体がL型結晶構造を有することを確認した。
【0212】
実施例9:低純度エプレレノン開始材料の溶媒による温浸によりH型を生成する
A.エタノール溶媒による温浸
低純度エプレレノン(HPLCアッセイによって64%)24.6 gをエタノール3A 126 mlと混合した。スラリーを加熱還流して、留出物を除去した。溶媒126 mlを大気圧蒸留によって除去すると同時にエタノール3A 126 mlをさらに加えた。溶媒の交換が終了した後、混合物を25℃に冷却して、1時間攪拌した。得られた固体を濾過してエタノール3Aによってすすぎ、風乾させて、エタノール溶媒和化合物を生成した。溶媒和化合物を90〜100℃の真空炉でさらに6時間乾燥させると、H型エプレレノン14.9 gが得られた。
【0213】
B.メチルエチルケトン溶媒による温浸
もう一つの温浸プロセスにおいて、低純度エプレレノン1 g(約65%アッセイ)をメチルエチルケトン4 ml中で2時間温浸し、その後、混合物を室温に冷却した。冷却後、得られた固体を真空濾過によって回収して、XRPD分析によってメチルエチルケトン溶媒和化合物であると決定した。固体を100℃で30〜60分乾燥させた。乾燥した固体はXRPDによって純粋なH型であると決定された。
【0214】
実施例10:高純度エプレレノンの溶媒による温浸によりL型を調製する
A.エタノール溶媒による温浸
高純度エプレレノン1 gをエタノール8 mlに約2時間温浸した。次に溶液を室温まで冷却して、固体を真空濾過によって回収した。濾過後直ちに固体をXRPDによって分析すると、固体は溶媒和化合物(おそらくエタノール溶媒和化合物)であることが示された。その後固体を、100℃の大気圧で30分乾燥させた。乾燥した固体をXRPDによって分析したところ、L型が多数を占めることが決定された(H型は検出されなかった)。
【0215】
B.メチルエチルケトン溶媒による温浸
高純度エプレレノン1 gをメチルエチルケトン4 mlに2時間温浸し、その後、混合物を室温に冷却して、得られた固体を真空濾過によって回収した。固体を直ちにXRPD分析によって分析して、エプレレノンの溶媒和化合物(おそらくメチルエチルケトン溶媒和化合物)であると決定した。その後溶媒和化合物を100℃の大気圧で30〜60分乾燥させた。乾燥した固体をXRPDによって分析したところ、主にL型であると決定され、H型の回折ピークは存在しなかった。
【0216】
実施例11:溶液から直接L型の結晶化
技法A
エプレレノン2.5 gを、75℃に加熱することによって酢酸エチルに溶解した。溶液を75℃で30分維持して、完全に溶解させた後、冷却速度1℃/分で13℃まで冷却した。得られたスラリーを750 rpmのオーバーヘッド攪拌子によって2時間攪拌した。固体を真空濾過によって回収して、40℃の真空炉で1時間乾燥させた。固体のXRPDパターンおよびDSCサーモグラムは、L型エプレレノンの特徴であった。固体のTGAは200℃まで固体からの重量喪失がないことを示した。
【0217】
技法B
もう一つの技法において、エプレレノン2 gを、ホットプレート上で磁石攪拌子によって攪拌しながら加熱することによって、15%アセトニトリルと85%水の混合液350 mlに溶解した。エプレレノンが溶解した後、溶液を磁石攪拌子で攪拌しながら室温まで一晩冷却した。得られた固体を真空濾過によって回収した。結晶は、複屈折であり、三角形の平板状晶癖を有した。固体にXRPDおよびDSC分析を行うと、L型エプレレノンの特徴を示した。TGAは200℃まで重量の喪失がないことを示した。
【0218】
技法C
さらにもう一つの技法において、エプレレノン640 mgを、エチルベンゼン20 mlを加えた50 mlフラスコに入れた。得られたスラリーを116℃に加熱すると、透明な溶液が得られ、これを30分かけて25℃に冷却した。核生成は、冷却期間のあいだに84℃で始まった。得られた固体を溶液から濾過して、風乾させると、固体530 mgが得られた(収率83%)。温ステージ顕微鏡およびXRPDにより、固体がL型エプレレノン結晶であることを確認した。
【0219】
技法D
さらにもう一つの技法において、エプレレノン1.55 gをニトロベンゼン2.0 mlに加えて、200℃に加熱した。得られたスラリーを200℃で一晩攪拌して、透明な溶液になった後、自然の空気対流によって室温まで冷却して、固体を単離した。固体は、XRPDおよび偏光顕微鏡によってL型エプレレノンであると決定された。
【0220】
技法E
さらにもう一つの技法において、エプレレノン5.0 g(純度>99%)をメタノール82 g(104 ml)に加えた。210 rpmで攪拌しながら、溶液を60℃に加熱して、その温度で20分維持して完全に溶解させた。溶液を攪拌しながら0.16℃/分の速度で−5℃まで冷却した。得られた結晶を濾過して回収して、40℃の真空炉で20時間乾燥させた。乾燥した固体は、DSCおよびXRPD分析によってL型エプレレノンであると決定された。
【0221】
技法F
もう一つの技法において、エプレレノン6.0 g(9%エタノールを含み、補正純度95.2%であるエタノール溶媒和化合物)をメタノール82 g(104 ml)に加えた。210 rpmで攪拌しながら、溶液を60℃に加熱して、その温度で20分維持して完全に溶解させた。次に、溶液を0.14℃/分の速度で50℃に冷却して、その温度を2.5時間維持した。次に、溶液を攪拌しながら0.13℃/分の速度で−5℃まで冷却した。得られた結晶を濾過して回収して、40℃の真空炉で16時間乾燥させた。乾燥した固体は、DSCおよびXRPD分析によってL型エプレレノンであると決定された。
【0222】
実施例12:溶液から直接のH型の結晶化
ジエポキシド150.5 mgおよびエプレレノン2.85 gをニトロベンゼン1.5 mlに加えた。混合物を200℃で数時間磁石攪拌子によって攪拌した。次に、得られたスラリーを自然の空気対流によって室温まで冷却した。試料を乾燥させて、偏光顕微鏡およびXRPDによって分析した。XRPD分析によって、試料がH型とL型の混合物であることが示された。結晶は顕微鏡で見ると半透明であり、溶媒除去(およびH型またはL型への変換)が起こっていないことを示している。
【0223】
実施例13:粉砕によるアモルファスエプレレノンの調製
鋼鉄製のウィグLバグ容器の約半分に、エプレレノン(純度>99.9%)約60 gを加えた。鋼鉄製のボールとキャップを試料容器に入れて、ウィグLバグ装置によって30秒間攪拌した。エプレレノンは、ウィグLバグ容器の表面から剥がれ落ちて、容器をさらに30秒間攪拌した。得られた固体をXRPDおよびDSCによって分析すると、アモルファスエプレレノンとL型結晶エプレレノンの混合物であると決定された。
【0224】
実施例14:凍結乾燥によるアモルファスエプレレノンの調製
粗エプレレノン約100 mgを、水400 mlを含むビーカーに計り取った。得られた混合物を5分間軽く加熱した後、超音波処理して、さらに5分間攪拌しながら加熱すると、分散液が得られた。エプレレノン分散液約350 mlを、HPLC用水50 mlを含む1000 mlの丸底フラスコに濾過した。分散液をドライアイス/アセトン浴中で1〜2分のあいだに急速に凍結した。フラスコをラブコンコフリーゾーン4.5凍結乾燥装置に接続して、内容物を一晩乾燥させた。フラスコ中の固体を小さい褐色瓶に移した。少量を偏光顕微鏡で、カージル(cargille)油(1.404)中で10倍、1.25倍で観察し、少なくとも95%アモルファスエプレレノンであることを観察した。図24および25は、アモルファスエプレレノンについて得られたXRPDパターンおよびDSCサーモグラムを示している。図24において39゜2θで認められたピークは、アルミニウム製の試料容器によるものである。
【0225】
実施例15:L型エプレレノンの溶解度
L型エプレレノンの水に対する溶解度をpH 7(100 mM燐酸緩衝液)で、5、25、および40℃で測定した。L型エプレレノン約30 mgを緩衝液約10 mlと混合すると、5℃および25℃ではいずれもエプレレノンのスラリーを形成した。H型エプレレノン約40 mgを緩衝液10 mlと混合すると、40℃でエプレレノンのスラリーを形成した。試料はそれぞれの条件について2つずつ調製した。スラリーは、振とう水浴中で適当な温度で平衡にして、溶液を1、5、12、19、27および36日間隔で紫外線可視分析(245 nm)によってエプレレノン含有量を分析した。各温度からのデータを適切に平均して、各温度でのエプレレノンの溶解度を決定して、表8に報告する。36日間の平衡終了後、各時点での残留固体をDSCおよびTGAによって分析して、L型エプレレノンであると決定した。
【0226】
【表8】

L型エプレレノンの溶解度
【0227】
実施例16:固有の溶解速度の測定
固有溶解速を、以下の4つのエプレレノン多形試料について測定した:(i)実施例11の技法Bと同じように、抗溶媒として水を用いてアセトニトリルから直接結晶化によって調製したL型エプレレノン、(ii)実施例10の技法Aと同じようにエタノールにおける温浸によって調製したH型エプレレノン、(iii)5%H型と95%L型との混合物、および(iv)粉砕して以下の粒子サイズ分布を提供するL型エプレレノン:9μm未満の粒子の重量が10%、22 μm未満の粒子重量が50%、および41 μm未満の粒子の重量が90%。
【0228】
エプレレノン150 mgを計り取って、ファンケル固有溶解測定腔に入れた。カーバープレスを用いて粉末を8280 kPaで圧縮して、錠剤を生成した。次に試料を固有溶解装置に載せた。用いた溶解培地は、1%ドデシル硫酸ナトリウム(SDS)のHPLC水溶液であった。試験は全て、37℃で2時間実施した。実験の開始前に溶解培地500 mlを溶解水浴チャンバー中で37℃で30分平衡にした。最初の試料を各溶解管から採取して、試験の初回時間(T0)とした。エプレレノン錠剤を溶解培地に沈めた。試料を既定の間隔で採取して溶解度の測定を行った。錠剤表面に気泡を形成しないように注意した。試料を243 nmでのUV吸収検出によって分析した。固有の溶解速度は、容積に関して補正し、溶解錠の表面積(0.5 cm2)に関して標準化した濃度対時間プロフィールの直線部分の勾配から計算した。
【0229】
図26は、4つの試料について測定した固有溶解速度を報告する。これらの試験は、H型エプレレノンはL型エプレレノンより固有の溶解速度が速いことを示している。圧縮および非圧縮エプレレノンを比較するXRPD測定によって、多形が圧縮時または溶解試験の経過中に相互変換しないことを確認した。
【0230】
実施例17:エプレレノン多形組成物
表9に示す組成を有するL型エプレレノン25 mg、50 mg、100 mgおよび200 mgを含む錠剤を調製する。
【表9】

実施例17の錠剤の組成
【0231】
実施例18:エプレレノン多形組成物
エプレレノン100 mg用量を含み、表10に示す組成を有するカプセル(硬ゼラチンカプセル、#0)を調製する。
【表10】

実施例18の100 mgカプセルの組成
【0232】
実施例19:エプレレノン多形組成物
エプレレノン200 mg用量を含み、表11に示す組成を有するカプセル(硬ゼラチンカプセル、サイズ#0)を調製する。
【表11】

実施例19の200 mgカプセルの組成
【0233】
実施例20:粉砕したエプレレノンの調製
エプレレノンの乾燥メチルエチルケトン溶媒和化合物をまず、溶媒和化合物をフィッツミル上の20メッシュスクリーンに通過させることによって塊をほぐす。次に、ほぐした塊を、供給速度約250 kg/時間でアルパインホサカワ・スタッドディスクピンミルを用いて、液体窒素冷却下で操作して、細かく粉砕する。ピンミリング技法は約65〜100 μmのD90粒子径を有する粉砕したエプレレノンを生じる。
【0234】
実施例21:イヌの試験における薬物動態パラメータに及ぼすエプレレノン粒子径の影響
エプレレノン血漿濃度および相対的生物学的利用能に及ぼすL型エプレレノンの粒子径の影響をイヌモデルにおいて調べた。体重8〜12 kgの健康な雌性ビーグル犬4匹に、下記の表12に記載した処方を含む即時放出カプセル(#0、白色半透明)1個を胃内投与して、水約10 mlを与えた。
【表12】


実施例21において用いられたエプレレノンカプセルの組成
【0235】
イヌを15〜20時間絶食してからカプセルを投与して、用量の投与後少なくとも4時間は餌を与えなかった。血液試料(約3ml)を、用量の投与後0、0.5、1、2、3、4、6、8および24時間に、ヘパリンを含む冷試験管に静脈穿刺によって採取した。血液試料を氷中に直ちに入れた。血液試料からの血漿の分離は、遠心を約15分行うことによって完了した。得られた血漿試料は、分析するまで約−20℃で凍結して保存した。分析はLC/MS/MS技法を用いて実施した。
【0236】
同じイヌ4匹を、それぞれが表12に示す組成を有するが、エプレレノン粒子径が異なる3つの製剤の試験に用いた。エプレレノン開始材料のD90粒子径はそれぞれ、約212 μm、約86 μm、および約36 μmであった。一連の製剤の投与のあいだは、少なくとも5日間の薬剤回復期間を設けた。結果の平均値を下記の表13および14に報告する。相対的生物学的利用率はAUCの結果から計算し、D90が86 μmである製剤を標準物質として選択した。
【0237】
【表13】

血液血清エプレレノン濃度(μg/ml)、実施例21
【0238】
【表14】

実施例21のデータから計算した薬物動態(PK)パラメータ
【0239】
実施例22:ヒトの試験における薬物動態パラメータに及ぼすエプレレノン粒子径の影響
エプレレノン血漿濃度および生物学的利用率に及ぼすL型エプレレノンの粒子径の影響を、下記の表15に説明する製剤組成物3つを用いてヒトモデルにおいて調べた。無作為化スケジュールに従って、被験者に1、8、15、22および29日に薬剤としてL型エプレレノン組成物100 mgを1回投与した。薬剤は全て午前8時に水180 mlと共に投与した。エプレレノンの薬物動態分析の血液試料は、−0.5(投与前)、投与後0.5、1、2、3、4、6、8、10、12、16、24、36、および48時間に採取した。
【0240】
エプレレノンの血漿濃度は、MS/MS検出を備えた確認されたHPLC法を用いて決定した。薬物動態データは表16に報告する。組成物の調製において用いたL型エプレレノンの粒子径分布は、レーザー光散乱を用いて乾燥粉末状態で決定した。
【0241】
【表15】

1 7.5%顆粒内、10%顆粒外
実施例22において用いたエプレレノン組成物(重量%)
【0242】
【表16】

実施例22のデータから計算した薬物動態(PK)パラメータ
【0243】
本発明は、特定の態様に関して説明してきたが、これらの態様の詳細は制限すると解釈されない。
【図面の簡単な説明】
【0244】
【図1A】H型エプレレノン溶媒和化合物のX線粉末回折パターンを示す。
【図1B】L型エプレレノン溶媒和化合物のX線粉末回折パターンを示す。
【図1C】エプレレノン溶媒和化合物のメチルエチルケトン溶媒和化合物のX線粉末回折パターンを示す。
【図1D】エプレレノンのn-プロピルアルコール溶媒和化合物のX線粉末回折パターンを示す。
【図1E】エプレレノンのテトラヒドロフラン溶媒和化合物のX線粉末回折パターンを示す。
【図1F】エプレレノンのエチルプロピオン酸溶媒和化合物のX線粉末回折パターンを示す。
【図1G】エプレレノンの酢酸溶媒和化合物のX線粉末回折パターンを示す。
【図1H】エプレレノンのアセトン溶媒和化合物のX線粉末回折パターンを示す。
【図1I】エプレレノンのトルエン溶媒和化合物のX線粉末回折パターンを示す。
【図1J】エプレレノンのイソプロパノール溶媒和化合物のX線粉末回折パターンを示す。
【図1K】エプレレノンのエタノール溶媒和化合物のX線粉末回折パターンを示す。
【図1L】エプレレノンの酢酸イソブチル溶媒和化合物のX線粉末回折パターンを示す。
【図1M】エプレレノンの酢酸ブチル溶媒和化合物のX線粉末回折パターンを示す。
【図1N】エプレレノンの酢酸メチル溶媒和化合物のX線粉末回折パターンを示す。
【図1O】エプレレノンの酢酸プロピル溶媒和化合物のX線粉末回折パターンを示す。
【図2A】メチルエチルケトンから直接結晶化した未粉末化L型エプレレノンの示差走査熱量測定(DSC)熱記録を示す。
【図2B】メチルエチルケトンから高純度エプレレノンを結晶化して得られた溶媒和物の脱溶媒化によって調製した未粉末化L型エプレレノンのDSC熱記録を示す。
【図2C】メチルエチルケトンから高純度エプレレノンを結晶化して得られた溶媒和化合物の脱溶媒化による産物を粉末化して調製したL型エプレレノンのDSC熱記録を示す。
【図2D】適当な溶媒から低純度エプレレノンを温浸して得られた溶媒和物の脱溶媒化によって調製した未粉末化H型エプレレノンのDSC熱記録を示す。
【図2E】エプレレノンのn-プロピルアルコール溶媒和化合物のDSC熱記録を示す。
【図2F】エプレレノンのテトラヒドロフラン溶媒和化合物のDSC熱記録を示す。
【図2G】エプレレノンのエチルプロピオン酸溶媒和化合物のDSC熱記録を示す。
【図2H】エプレレノンの酢酸溶媒和化合物のDSC熱記録を示す。
【図2I】エプレレノンのクロロホルム溶媒和化合物のDSC熱記録を示す。
【図2J】エプレレノンのアセトン溶媒和化合物のDSC熱記録を示す。
【図2K】エプレレノンのトルエン溶媒和化合物のDSC熱記録を示す。
【図2L】エプレレノンのイソプロパノール溶媒和化合物のDSC熱記録を示す。
【図2M】エプレレノンのエタノール溶媒和化合物のDSC熱記録を示す。
【図2N】エプレレノンの酢酸t-ブチル溶媒和化合物のDSC熱記録を示す。
【図2O】エプレレノンの酢酸イソブチル溶媒和化合物のDSC熱記録を示す。
【図2P】エプレレノンの酢酸ブチル溶媒和化合物のDSC熱記録を示す。
【図2Q】エプレレノンの酢酸メチル溶媒和化合物のDSC熱記録を示す。
【図2R】エプレレノンの酢酸プロピル溶媒和化合物のDSC熱記録を示す。
【図2S】エプレレノンのn-ブタノール溶媒和化合物のDSC熱記録を示す。
【図2T】エプレレノンのn-オクタノール溶媒和化合物のDSC熱記録を示す。
【図3A】H型エプレレノンの赤外線(IR)スペクトル(拡散反射率、DRIFT)を示す。
【図3B】L型エプレレノンのIRスペクトル(拡散反射率、DRIFT)を示す。
【図3C】エプレレノンのメチルエチルケトン溶媒和化合物のIRスペクトル(拡散反射率、DRIFT)を示す。
【図3D】クロロホルム溶液中のエプレレノンのIRスペクトル(拡散反射率、DRIFT)を示す。
【図3E】エプレレノンのn-プロピルアルコール溶媒和化合物のIRスペクトルを示す。
【図3F】エプレレノンのテトラヒドロフラン溶媒和化合物のIRスペクトルを示す。
【図3G】エプレレノンのエチルプロピオン酸溶媒和化合物のIRスペクトルを示す。
【図3H】エプレレノンの酢酸溶媒和化合物のIRスペクトルを示す。
【図3I】エプレレノンのアセトン溶媒和化合物のIRスペクトルを示す。
【図3J】エプレレノンのトルエン溶媒和化合物のIRスペクトルを示す。
【図3K】エプレレノンのイソプロパノール溶媒和化合物のIRスペクトルを示す。
【図3L】エプレレノンのエタノール溶媒和化合物のIRスペクトルを示す。
【図3M】エプレレノンの酢酸イソブチル溶媒和化合物のIRスペクトルを示す。
【図3N】エプレレノンの酢酸ブチル溶媒和化合物のIRスペクトルを示す。
【図3O】エプレレノンの酢酸プロピル溶媒和化合物のIRスペクトルを示す。
【図3P】エプレレノンの酢酸メチル溶媒和化合物のIRスペクトルを示す。
【図3Q】エプレレノンのプロピレングリコール溶媒和化合物のIRスペクトルを示す。
【図3R】エプレレノンの酢酸t-ブチル溶媒和化合物のIRスペクトルを示す。
【図4】H型エプレレノンの13C NMRスペクトルを示す。
【図5】L型エプレレノンの13C NMRスペクトルを示す。
【図6A】エプレレノンのメチルエチルケトン溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6B】エプレレノンのn-プロピルアルコール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6C】エプレレノンのテトラヒドロフラン溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6D】エプレレノンのエチルプロピオン酸溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6E】エプレレノンの酢酸溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6F】エプレレノンのクロロホルム溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6G】エプレレノンのアセトン溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6H】エプレレノンのトルエン溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6I】エプレレノンのイソプロパノール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6J】エプレレノンのエタノール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6K】エプレレノンの酢酸イソブチル溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6L】エプレレノンの酢酸ブチル溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6M】エプレレノンの酢酸メチル溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6N】エプレレノンの酢酸プロピル溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6O】エプレレノンのプロピレングリコール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6P】エプレレノンのn-ブタノール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6Q】エプレレノンのn-オクタノール溶媒和化合物の熱重量測定分析プロフィールを示す。
【図6R】エプレレノンの酢酸t-ブチル溶媒和化合物の熱重量測定分析プロフィールを示す。
【図7】エプレレノンのメチルエチルケトンの溶媒和化合物を脱溶媒化して調製したL型エプレレノンの走査型電子顕微鏡写真。
【図8】酢酸エチルから直接結晶化して調製したL型エプレレノンの走査型電子顕微鏡写真。
【図9】メチルエチルケトンから単離された7-メチル水素4α,5α;9α,11α-ジエポキシ-17ヒドロキシ-3-オキソ-17α-プレグナン-7α,21-ジカルボン酸であるγラクトン(「ジエポキシド」)の結晶形のX線粉末回折パターンを示す。
【図10】イソプロパノールから単離された7-メチル11α,12α-エポキシ-17ヒドロキシ-3-オキソ-17α-プレグン-4-エン-7α,21-ジカルボン酸であるγ-ラクトン(「11,12-エポキシド」)の結晶形のX線粉末回折パターンを示す。
【図11】n-ブタノールから単離された7-メチル水素-17ヒドロキシ-3-オキソ-17α-プレグナ-4,9(11)-ジエン-7α,21-ジカルボン酸であるγ-ラクトン(「9,11-オレフィン」)の結晶形のX線粉末回折パターンを示す。
【図12】互変的な関係にある多形についての、ギブス自由エネルギーと温度との関係を図示する。n-ブタノールから単離された7-メチル水素-17ヒドロキシ-3-オキソ-17α-プレグナ-4,9(11)-ジエン-7α,21-ジカルボン酸であるγ-ラクトン(「9,11-オレフィン」)の結晶形のX線粉末回折パターンを示す。
【図13】(a) 0%, (b) 1%, (c) 3%、および(d) 5%のジエポキシ不純物添加処理によるメチルエチルケトン結晶化により得られたメチルエチルケトン溶媒和化合物の湿塊のX線粉末回折パターンを示す。
【図14】(a) 0%, (b) 1%, (c) 3%、および(d) 5%のジエポキシ・不純物添加処理によるメチルエチルケトン結晶化により得られた乾燥固体のX線粉末回折パターンを示す。
【図15】乾燥する前に溶媒和化合物を(a) 磨砕せず、また (b) 磨砕して、 3%ジエポキシ不純物添加処理によるメチルエチルケトン結晶化により得られた乾燥固体のX線粉末回折パターンを示す。
【図16】(a) 0%, (b) 1%, (c) 5%、および(d) 10%の11,12-エポキシ・不純物添加処理によるメチルエチルケトン結晶化により得られたメチルエチルケトン溶媒和化合物の湿塊のX線粉末回折パターンを示す。
【図17】(a) 0%, (b) 1%, (c) 5%、および(d) 10%の11,12-エポキシ・不純物添加処理によるメチルエチルケトン結晶化により得られた乾燥固体のX線粉末回折パターンを示す。
【図18】本明細書の実施例7の表7Aで報告されているデータに基づく、産物の純度、出発物質の純度、冷却速度、および終点温度の立体プロットを示す。
【図19】最終物質の純度に対して統計的に有意な効果をもつ変数を決定するために、図18の立体プロットを用いて作成された半定位プロットを示す。
【図20】最終物質の純度に対する効果について、出発物質の純度と冷却速度の間の相互作用を示す、本明細書の実施例7の表7Aで報告されているデータに基づいた相互作用グラフ。
【図21】本明細書の実施例7の表7Aで報告されているデータに基づく、H型重量画分、出発物質の純度、冷却速度、および終点温度の立体プロットを示す。
【図22】最終物質の純度に対して統計的に有意な効果をもつ変数を決定するために、図21の立体プロットを用いて作成された半定位プロットを示す。
【図23】最終物質の純度に対する効果について、出発物質の純度と終点温度の間の相互作用を示す、本明細書の実施例7の表7Aで報告されているデータに基づいた相互作用グラフ。
【図24】無定形エプレレノンのX線回折パターンを示す。
【図25】無定形エプレレノンのDSC熱記録を示す。
【図26】4種類のエプレレノン多形試料について測定した溶解速度を示す。
【特許請求の範囲】
【請求項1】
単斜晶系をもち、および8.0±0.2という2θ度(degree)にピークをもつX線粉末回折パターンを示すL型結晶エプレレノン。
【請求項2】
約223℃から約242℃の範囲内に融点をもつ、請求項1記載の結晶エプレレノン。
【請求項3】
約400μm未満のD90粒子サイズをもつ粒子状態にある、請求項1記載の結晶エプレレノン。
【請求項4】
約25から約400μmのD90粒子サイズをもつ粒子状態にある、請求項1記載の結晶エプレレノン。
【請求項5】
約0.01から約15μmのD90粒子サイズをもつ粒子状態にある、請求項1記載の結晶エプレレノン。
【請求項6】
L型結晶エプレレノンを検出可能量含むエプレレノン薬剤物質。
【請求項7】
約90%から約100%のL型結晶エプレレノンを含む、請求項6記載のエプレレノン薬剤物質。
【請求項8】
実質的に位相が純粋なL型結晶エプレレノンである、請求項6記載のエプレレノン薬剤物質。
【請求項9】
残り(balance)のエプレレノンが、(i)斜方晶系をもつH型結晶エプレレノン、(ii)溶媒和させた結晶形エプレレノン、および(iii)無定形エプレレノンの一種類以上からなるものである、請求項6記載のエプレレノン薬剤物質。
【請求項10】
請求項1から9いずれか一項記載のL型エプレレノンまたはエプレレノン薬剤物質を、治療上の有効量である約10から約1000 mg、および一種類以上の薬学的に許容される賦形剤を含む薬学的組成物。
【請求項11】
アルドステロンが関与する症状または疾患を予防または治療する方法において、このような症状または疾患に対して感受性の対象者に、治療上または予防上有効な量の請求項10記載の組成物を投与することを含む方法。
【請求項12】
アルドステロンが関与する症状または疾患を予防または治療するのに有用な薬物の製造における、請求項1から9いずれか一項記載のL型エプレレノンまたはエプレレノン薬剤物質の使用。
【請求項13】
請求項1から9いずれか一項記載のL型エプレレノンまたはエプレレノン薬剤物質を調製する方法において、溶媒または溶媒の混合液からエプレレノンを結晶化することを含む方法。
【請求項14】
溶媒または溶媒の混合液が、メタノール、酢酸エチル、酢酸イソプロピル、アセトニトリル、ニトロベンゼン、水、およびエチルベンゼンからなる群より選択される溶媒を含む、請求項13記載の方法。
【請求項15】
エプレレノンを結晶化する前に、L型エプレレノンの結晶を溶媒または溶媒の混合液に播種する、請求項13記載の方法。
【請求項16】
請求項1から9いずれか一項記載のL型エプレレノンまたはエプレレノン薬剤物質を調製する方法において、
(a)溶媒水和化合物を作製するために、溶媒または溶媒の混合液からエプレレノンを結晶化する段階、および
(b)該溶媒和化合物を脱溶媒する段階
を含む方法。
【請求項17】
溶媒または溶媒の混合液が、メチルエチルケトン、2-ペンタノン、酢酸、アセトン、酢酸ブチル、クロロホルム、エタノール、イソブタノール、酢酸イソブチル、酢酸メチル、プロピオン酸エチル、n-ブタノール、n-オクタノール、n-プロパノール、イソプロパノール、酢酸プロピル、プロピレングリコール、t-ブタノール、テトラヒドロフラン、トルエン、および酢酸t-ブチルからなる群より選択される溶媒を含む、請求項16記載の方法。
【請求項18】
溶媒または溶媒の混合液が、メチルエチルケトン、またはエタノールを含む、請求項16記載の方法。
【請求項1】
単斜晶系をもち、および8.0±0.2という2θ度(degree)にピークをもつX線粉末回折パターンを示すL型結晶エプレレノン。
【請求項2】
約223℃から約242℃の範囲内に融点をもつ、請求項1記載の結晶エプレレノン。
【請求項3】
約400μm未満のD90粒子サイズをもつ粒子状態にある、請求項1記載の結晶エプレレノン。
【請求項4】
約25から約400μmのD90粒子サイズをもつ粒子状態にある、請求項1記載の結晶エプレレノン。
【請求項5】
約0.01から約15μmのD90粒子サイズをもつ粒子状態にある、請求項1記載の結晶エプレレノン。
【請求項6】
L型結晶エプレレノンを検出可能量含むエプレレノン薬剤物質。
【請求項7】
約90%から約100%のL型結晶エプレレノンを含む、請求項6記載のエプレレノン薬剤物質。
【請求項8】
実質的に位相が純粋なL型結晶エプレレノンである、請求項6記載のエプレレノン薬剤物質。
【請求項9】
残り(balance)のエプレレノンが、(i)斜方晶系をもつH型結晶エプレレノン、(ii)溶媒和させた結晶形エプレレノン、および(iii)無定形エプレレノンの一種類以上からなるものである、請求項6記載のエプレレノン薬剤物質。
【請求項10】
請求項1から9いずれか一項記載のL型エプレレノンまたはエプレレノン薬剤物質を、治療上の有効量である約10から約1000 mg、および一種類以上の薬学的に許容される賦形剤を含む薬学的組成物。
【請求項11】
アルドステロンが関与する症状または疾患を予防または治療する方法において、このような症状または疾患に対して感受性の対象者に、治療上または予防上有効な量の請求項10記載の組成物を投与することを含む方法。
【請求項12】
アルドステロンが関与する症状または疾患を予防または治療するのに有用な薬物の製造における、請求項1から9いずれか一項記載のL型エプレレノンまたはエプレレノン薬剤物質の使用。
【請求項13】
請求項1から9いずれか一項記載のL型エプレレノンまたはエプレレノン薬剤物質を調製する方法において、溶媒または溶媒の混合液からエプレレノンを結晶化することを含む方法。
【請求項14】
溶媒または溶媒の混合液が、メタノール、酢酸エチル、酢酸イソプロピル、アセトニトリル、ニトロベンゼン、水、およびエチルベンゼンからなる群より選択される溶媒を含む、請求項13記載の方法。
【請求項15】
エプレレノンを結晶化する前に、L型エプレレノンの結晶を溶媒または溶媒の混合液に播種する、請求項13記載の方法。
【請求項16】
請求項1から9いずれか一項記載のL型エプレレノンまたはエプレレノン薬剤物質を調製する方法において、
(a)溶媒水和化合物を作製するために、溶媒または溶媒の混合液からエプレレノンを結晶化する段階、および
(b)該溶媒和化合物を脱溶媒する段階
を含む方法。
【請求項17】
溶媒または溶媒の混合液が、メチルエチルケトン、2-ペンタノン、酢酸、アセトン、酢酸ブチル、クロロホルム、エタノール、イソブタノール、酢酸イソブチル、酢酸メチル、プロピオン酸エチル、n-ブタノール、n-オクタノール、n-プロパノール、イソプロパノール、酢酸プロピル、プロピレングリコール、t-ブタノール、テトラヒドロフラン、トルエン、および酢酸t-ブチルからなる群より選択される溶媒を含む、請求項16記載の方法。
【請求項18】
溶媒または溶媒の混合液が、メチルエチルケトン、またはエタノールを含む、請求項16記載の方法。
【図1A】


【図1B】


【図1C】


【図1D】


【図1E】


【図1F】


【図1G】


【図1H】


【図1I】


【図1J】


【図1K】


【図1L】


【図1M】


【図1N】


【図1O】


【図2A】


【図2B】


【図2C】


【図2D】


【図2E】


【図2F】


【図2G】


【図2H】


【図2I】


【図2J】


【図2K】


【図2L】


【図2M】


【図2N】


【図2O】


【図2P】


【図2Q】


【図2R】


【図2S】


【図2T】


【図3A】


【図3B】


【図3C】


【図3D】


【図3E】


【図3F】


【図3G】


【図3H】


【図3I】


【図3J】


【図3K】


【図3L】


【図3M】


【図3N】


【図3O】


【図3P】


【図3Q】


【図3R】


【図4】


【図5】


【図6A】


【図6B】


【図6C】


【図6D】


【図6E】


【図6F】


【図6G】


【図6H】


【図6I】


【図6J】


【図6K】


【図6L】


【図6M】


【図6N】


【図6O】


【図6P】


【図6Q】


【図6R】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】




【図1B】


【図1C】


【図1D】


【図1E】


【図1F】


【図1G】


【図1H】


【図1I】


【図1J】


【図1K】


【図1L】


【図1M】


【図1N】


【図1O】


【図2A】


【図2B】


【図2C】


【図2D】


【図2E】


【図2F】


【図2G】


【図2H】


【図2I】


【図2J】


【図2K】


【図2L】


【図2M】


【図2N】


【図2O】


【図2P】


【図2Q】


【図2R】


【図2S】


【図2T】


【図3A】


【図3B】


【図3C】


【図3D】


【図3E】


【図3F】


【図3G】


【図3H】


【図3I】


【図3J】


【図3K】


【図3L】


【図3M】


【図3N】


【図3O】


【図3P】


【図3Q】


【図3R】


【図4】


【図5】


【図6A】


【図6B】


【図6C】


【図6D】


【図6E】


【図6F】


【図6G】


【図6H】


【図6I】


【図6J】


【図6K】


【図6L】


【図6M】


【図6N】


【図6O】


【図6P】


【図6Q】


【図6R】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【公開番号】特開2007−16043(P2007−16043A)
【公開日】平成19年1月25日(2007.1.25)
【国際特許分類】
【出願番号】特願2006−238694(P2006−238694)
【出願日】平成18年9月4日(2006.9.4)
【分割の表示】特願2001−542722(P2001−542722)の分割
【原出願日】平成12年12月4日(2000.12.4)
【出願人】(501315278)ファルマシア コーポレイション (1)
【Fターム(参考)】
【公開日】平成19年1月25日(2007.1.25)
【国際特許分類】
【出願日】平成18年9月4日(2006.9.4)
【分割の表示】特願2001−542722(P2001−542722)の分割
【原出願日】平成12年12月4日(2000.12.4)
【出願人】(501315278)ファルマシア コーポレイション (1)
【Fターム(参考)】
[ Back to top ]

