国際特許分類[C07D213/803]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | 複素環式化合物 (108,186) | 異項原子として1個の窒素原子のみをもち,環原子相互間または環原子と非環原子間に3個またはそれ以上の二重結合を有し,他の環と縮合していない6員環からなる複素環式化合物 (5,861) | 環原子相互間または環原子と非環原子間に3個の二重結合を有するもの (5,859) | 環の窒素原子と非環原子間に結合をもたないもの,または環の窒素原子に直接結合する水素原子または炭素原子のみをもつもの (5,713) | 異種原子,または異種原子に対する3個の結合をもち,そのうち多くても1個がハロゲンに対する結合である炭素原子,例.エステルまたはニトリル基,が環の炭素原子に直接結合したもの (3,690) | 異種原子に対する3個の結合をもち,そのうち多くても1個がハロゲンに対する結合である炭素原子,例.エステルまたはニトリル基 (1,391) | 酸;エステル (402) | 製造方法 (50)
国際特許分類[C07D213/803]の下位に属する分類
国際特許分類[C07D213/803]に分類される特許
31 - 40 / 47
6−メチルニコチン酸フェニルエステル類およびその製造方法
【課題】 医薬等の重要な中間体として使用される1−(6−メチルピリジン−3−イル)−2−[(4−メチルスルホニル)−フェニル]エタノンを、より安全で容易に製造するための有用な原料である6−メチルニコチン酸フェニルエステル類およびその製造方法を提供すること。
【解決手段】 式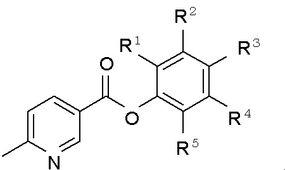
(式中、R1〜R5はそれぞれ独立して、水素原子、ハロゲン原子、ニトロ基、炭素数1〜4のアルキル基、または炭素数1〜4のアルコキシル基を示す。)で表される6−メチルニコチン酸フェニルエステル類およびその製造方法。
(もっと読む)
ニコチン酸誘導体又はその塩の製造方法
【課題】 特定のニコチン酸誘導体又はその塩の製造方法を提供する。
【解決手段】 式(I):
【化1】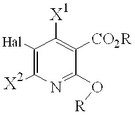
(式中、X1及びX2は各々独立に、水素原子、ハロゲン原子、アルキル基、アルコキシ基、ハロアルキル基及びハロアルコキシ基であり;Rはアルキル基であり;Halは塩素原子又は臭素原子である)で表されるニコチン酸誘導体又はその塩の製造方法であって、式(II):
【化2】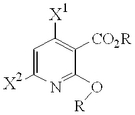
(式中、X1、X2及びRは前述の通りである)で表される化合物又はその塩と、塩素原子又は臭素原子を含むハロゲン化剤とを反応させることを特徴とする前記ニコチン酸誘導体又はその塩の製造方法を提供する。
(もっと読む)
置換されたニコチン酸エステルの製造方法
本発明は、プロトン源が存在する不活性溶媒中で、式(II)の化合物(式中R3はC1-C8アルキル又はC3-C6シクロアルキルであり、そしてR4及びR05は式(I)の定義の通りである)と式(III )の化合物(式中、R、R1、R2及びX1は請求項1の式(I)の定義の通りである)を反応させることによる、式(I)の化合物(式中の置換基は請求項1の定義の通りである)の調製方法に関する。 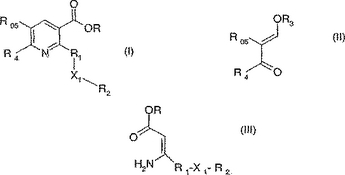 (もっと読む)
(もっと読む)
4,4’−ジカルボキシ−2,2’−ビピリジンの製造方法
【課題】 工業的に優位な高純度の4,4’−ジカルボキシ−2,2’−ビピリジンの製造方法及び精製方法を提供すること。
【解決手段】 塩基性条件下で式(1):
【化1】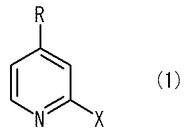
で示される2−ハロゲノピリジン類をカップリング反応せしめ、得られた反応混合物を、酸でpH4〜6の範囲に調整して4,4’−ジカルボキシ−2,2’−ビピリジンを析出させることを特徴とする4,4’−ジカルボキシ−2,2’−ビピリジンの製造方法、及びイソニコチン酸を含有する4,4’−ジカルボキシ−2,2’−ビピリジンを精製するにあたり、当該4,4’−ジカルボキシ−2,2’−ビピリジンの塩基性水溶液を調製し、次いでその塩基性水溶液を酸でpH4〜6の範囲に調製して4,4’−ジカルボキシ−2,2’−ビピリジンを析出させることを特徴とする4,4’−ジカルボキシ−2,2’−ビピリジンの精製方法。
【図面】 なし
(もっと読む)
N−アリールカルバミン酸エステルとハロ−ヘテロアリールとを反応させることによるN−ヘテロアリール−N−アリール−アミンの調製のためのプロセスおよび類似のプロセス
本発明は、式(I)のジアリールアミン化合物またはその塩を生成するためのプロセスに関する。このプロセスは、アルカリ金属塩または遷移金属触媒の存在下で、式(II)の化合物と式(III)のアミンとを結合させる工程を包含し、ここで:Ar1およびAr2は、独立してQであり;各Qは、0〜4個のヘテロ原子を有する飽和または不飽和の5〜8員環に必要に応じて縮合されたアリール環系またはヘテロアリール環系であり;Qは、請求項1で定義されるように必要に応じて置換され、ここで:Xは脱離基であり;そしてYは、−C(O)−O−Zであり;そしてZは、C1〜C6脂肪族、ベンジル、Fmoc、−SO2R’およびQから選択され、ただし、Qは、Xまたはアルキンで置換されず;ここでR’は、請求項1で定義されるものである。
【化51】
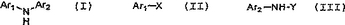 (もっと読む)
(もっと読む)
2−クロロ−5−フルオロ−3−置換ピリジンまたはその塩の製造方法
入手容易な原料から、反応操作が簡便で取扱いの容易な試薬を用いて、短い工程で、かつ温和な反応条件で、2−クロロ−5−フルオロ−3−置換−ピリジンまたはその塩を高収率で製造する方法を提供する。すなわち、下記化合物(1)またはその塩の6位の塩素原子を選択的に還元する下記化合物(2)またはその塩の製造方法を提供する。また、該還元反応によって得た下記化合物(2)またはその塩のZ1基をZ2基に置換することによる、下記化合物(4)またはその塩の製造方法を提供する。ただし、Z1は、−CO2R1等であり、R1は、水素原子、アルキル基、アルケニル基、アリール基、アルアルキル基またはシクロアルキル基を示す。Z2はZ1と異なる基であり、−CO2R5等であり、R5はアルキル基、アルケニル基、アリール基、アルアルキル基またはシクロアルキル基を示す。
 (もっと読む)
(もっと読む)
ピリジン誘導体の製造方法
【課題】 医薬中間体として有用な6−クロロアセチルピリジン−2−カルボン酸誘導体を工程数が少なく、工業的に効率良く製造し得る法を提供する。
【解決手段】 式(II)の6−アセチルピリジン−2−カルボン酸エステル誘導体をブロム化し、式(III)の6−ブロモアセチルピリジン−2−カルボン酸エスル誘導体とし、
次いで、該化合物と塩酸とを反応させることを特徴とする式(I)で表される6−クロロアセチルピリジン−2−カルボン酸誘導体の製造方法。
【化1】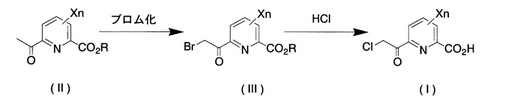
(式中、Xはハロゲン、NO2、アルキル、ハロアルキル、アルコキシ又はハロアルコキシ
、nは0〜3。Rはアルキル。)
(もっと読む)
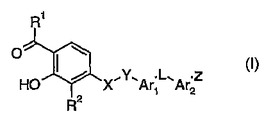
グルタミン酸受容体の増強剤
本発明は、式Iの化合物、その医薬組成物、並びにそれを使用する方法、その処理又は調製、及びその化合物の中間体を提供する。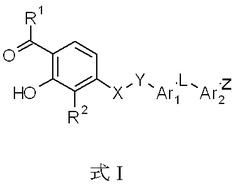
 (もっと読む)
(もっと読む)
複素環式芳香族カルボン酸を生成するための方法
複素環式芳香族カルボン酸の生成のための方法であって、触媒の存在下で、前記カルボン酸の前駆体を酸化剤と接触させる工程であって、かかる接触が、超臨界条件または超臨界点に近い近超臨界条件下の水を含む水性溶媒中にある前記前駆体および酸化剤を用いて行われる工程を含む、方法。 (もっと読む)
他元素ドープルチル型酸化チタンとその製造法、光触媒、及び該触媒を用いた有機化合物の酸化方法
【課題】 長波長側の可視光でも高い触媒活性を発現しうる他元素ドープ酸化チタンとその製造法及び活性の高い光触媒を提供する。
【解決手段】 本発明の他元素ドープルチル型酸化チタンはルチル型酸化チタンに炭素原子及び硫黄原子からなる群より選択された少なくとも1種の原子がドープされている。炭素原子はC4+としてドープされていてもよい。また、硫黄原子はS4+としてドープされていてもよい。このような他元素ドープルチル型酸化チタンは、ルチル型酸化チタンと炭素源及び硫黄源との混合物を焼成処理することにより得ることができる。
(もっと読む)
31 - 40 / 47
[ Back to top ]

