国際特許分類[C07K1/04]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | ペプチド (29,849) | ペプチドの製造のための一般方法 (1,853) | 担体上で (78)
国際特許分類[C07K1/04]に分類される特許
21 - 30 / 78
血液由来インター−アルファ−阻害タンパク質の調製及び組成物。
本発明は概ね、血液からインター−アルファ−阻害タンパク質(IαIp)を精製する方法及びその組成物を提供する。 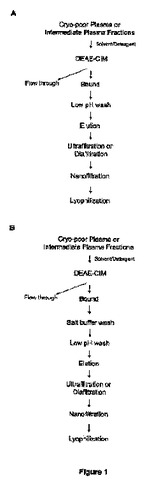 (もっと読む)
(もっと読む)
試薬再循環を用いてオリゴマー、特に、ペプトイドを合成するための装置
【課題】固相合成技術を用いてペプトイドオリゴマーを合成する方法および装置であって、従来のシステムに付随した無駄をなくした方法および装置などの提供。
【解決手段】ペプトイドオリゴマー合成方法であって、以下を包含する方法:(a)保護したアミノ基を有する固相を提供する工程;(b)該固相上にて該アミノ基を脱保護して、反応性アミンを提供する工程;(c)該反応性アミンをアシルサブモノマーと接触させることにより、該アミンをアシル化して脱離基を含むアシル化アミンを提供する工程;(d)該アシル化アミンをアミン試薬と接触させることにより該アシル化アミンに由来の該脱離基をアミンで置き換えてN置換モノマーおよび脱離基副生成物を提供する工程;および(e)該脱離基副生成物と共に未使用アミン試薬を閉じ込め手段に再循環させるこにより引き続いた置換反応で使用するのに適切な再生アミン試薬を提供する工程。
(もっと読む)
アミノ酸のα−N−メチル化
【課題】Fmoc/tBuSPPSと適合性があるアミノ酸のN−メチル化法の提供。
【解決手段】式I: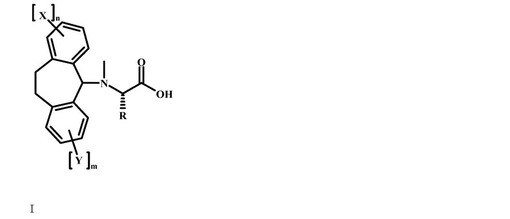
で表される化合物、該化合物を利用した樹脂上メチル化に適切なアミノ酸のαN−保護方法。
(もっと読む)
治療効果の改善のための新規の光学的に純粋な化合物
本発明は、既知の立体異性体の複雑な混合物と比較して改善した抗癌活性を示す、新規の光学的に純粋な化合物に関する。そのような化合物は、式(I)のものであって、式中、各Xは任意のアミノ酸を独立に表し;nは0又は1であり;mは0から3の間の整数であり;kは少なくとも3の整数であり;PsiはLysとProの間のペプチドアミド結合に代わる還元された結合であり;式(I)の化合物の偽ペプチド単位中のLys残基は、全てL立体配置又は全てD立体配置のいずれかである。そのような化合物の製造方法及びその治療的使用も提供する。合成方法は、ボランを使用する、ジペプチド中間体におけるLysとProとの間のペプチド結合の選択的還元を伴う。前記治療的使用は、癌、炎症、及び創傷治癒のためのものである。 (もっと読む)
新規な二重標的化抗腫瘍複合体
本発明は、式(I)の2重標的化細胞毒性化合物と、それらの調製とに関する。記述される化合物には、腫瘍特異的作用が与えられており3つの機能的単位:スペーサと、それによって1つに接続されている腫瘍認識部分及び腫瘍選択的酵素基質配列とが組み込まれている。これらの複合体は、血清安定性及びそれと同時に酵素切断性の結果としての腫瘍細胞内での所望の作用が保証されるよう設計されている。
[(L-D)nE]m-F-D-PI-SI-CT (式I)
(もっと読む)
固相及び溶液相の組み合わせ技術を使用したインシュリン分泌性ペプチド合成
本発明は、固相及び溶液相(「ハイブリッド」)アプローチを使用して合成されるインシュリン分泌性ペプチドの調製に関する。一般的に、アプローチは、固相化学を使用して3つの異なるペプチド中間体フラグメントを合成することを含む。溶液相化学を次に使用して、追加のアミノ酸材料を第3のフラグメントに加えて、それを次に第2のフラグメントに、そして次に第1のフラグメントに溶液中で結合させる。あるいは、異なる第2のフラグメントを、第1のフラグメントに固相中で結合させる。次に、溶液相化学を次に使用して、追加のアミノ酸材料を異なる第3のフラグメントに加える。後に、この異なる第3のフラグメントを、結合した第1の及び異なる第2のフラグメントに溶液相中で結合させる。フラグメントの1つにおける疑似プロリンの使用によって、そのフラグメントの固相合成が容易になり、また、このフラグメントの他のフラグメントへの後の溶液相結合が容易になる。本発明は、インシュリン分泌性ペプチド、例えばGLP−1(7−36)並びにその天然及び非天然対応物などを形成するために非常に有用である。 (もっと読む)
固相および溶液相の組み合わせ技法を使用するインスリン分泌性ペプチドの合成
本発明は、固相および溶液相(「ハイブリッド型」)アプローチを使用して合成される、直接配列の少なくとも2つのグルタミン酸残基(Glu−Glu)を含むインスリン分泌性ペプチドの調製に関する。一般に、そのアプローチは、固相化学反応を使用して三つの異なるペプチド中間体フラグメントを合成することを含む。次に、溶液相化学反応を使用して、フラグメントの一つに追加のアミノ酸物質を付加する。次に、溶液相中でフラグメントを一緒にカップリングする。フラグメントの一つにシュードプロリンを使用することで、そのフラグメントの固相合成が容易になり、このフラグメントと他のフラグメントとのその後の溶液相カップリングもまた容易になる。本発明は、エキセナチド(1−39)などのインスリン分泌性ペプチドおよびその対応物を形成させるために非常に有用である。 (もっと読む)
治療的抗ウイルス性ペプチドの新規合成方法
ペプチドの合成方法が、本明細書で提供される。詳細には、治療的抗ウイルス性ペプチドの合成方法が、本明細書で提供される。 (もっと読む)
ポリペプチドおよび蛋白質の化学的合成のための方法および中間体
本発明はポリペプチドおよび蛋白質の化学合成のための方法および中間体、さらにとりわけ、N−末端β(ベータ)−メチル−システイン(SEQ ID NO:1)を含むペプチドフラグメントをC−末端チオエステルを有する別のペプチドフラグメントと化学的に連結して、自発的に再配列してアミド結合を形成するβ(ベータ)−アミノ−チオエステル中間体を生み出すための方法および中間体に関する。また、本発明はβ(ベータ)−メチル−システイン(SEQ ID NO:1)およびその保護された型を合成する方法に冠する。そのうえ、本発明はポリペプチドおよび蛋白質のβ(ベータ)−メチル−チアゾリジン残基をβ(ベータ)−メチル−システイン(SEQ ID NO:1)残基に変換することに関する。
(もっと読む)
タンパク質の製造方法
【課題】 効率よく不活性タンパク質から活性タンパク質にタンパク質をリフォールディングすることが求められていた。
【解決手段】 タンパク質の製造方法であって、不活性タンパク質をメソ孔中に担持した多孔体を用意する工程と、前記不活性タンパク質を担持した前記多孔体に変性剤を付与する工程と、前記多孔体より変性剤を除去し、前記不活性タンパク質を活性タンパク質に変化させる工程とを備えるタンパク質の製造方法により解決することが可能になった。
(もっと読む)
21 - 30 / 78
[ Back to top ]



