Fターム[4C063EE05]の内容
Fターム[4C063EE05]に分類される特許
361 - 380 / 645
アクリル酸エステル及びヒドロキシ化合物、該アクリル酸エステルの(共)重合体、それを用いた電子写真感光体、画像形成方法、画像形成装置及び画像形成装置用プロセスカートリッジ
【課題】良好なラジカル重合性と電荷輸送性を有し、成膜性や他のモノマーとの相溶性、耐摩耗特性に優れ且つ電気的特性が良好で且つ白斑点等による画像欠陥が少ない長寿命な電子写真感光体を提供する。
【解決手段】下記一般式(1)で表される連鎖重合性化合物。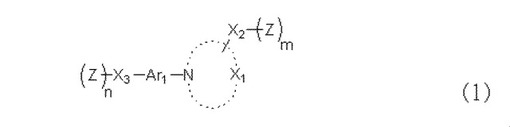 (もっと読む)
(もっと読む)
ヒンバシン類似体の合成において使用される{[5−(3−フルオロフェニル)−ピリジン−2−イル]メチル}ホスホン酸ジエチルの合成
本願は、それら自体トロンビン受容体アンタゴニストとして有用なヒンバシン類似体の調製において中間体として有用であるホスホン酸エステルの新規調製方法を開示する。本明細書で教示される化学反応は、以下のスキーム:
によって例示することができる。式中、R9は、1〜10個の炭素原子を有するアルキル基、アリール基、ヘテロアリール基、およびアリールアルキル基から選択され、R11は、出現する毎に独立に、1〜10個の炭素原子を有するアルキル基、アリール基、ヘテロアリール基およびアリールアルキル基、ならびに水素から選択され、X2は、Cl、Br、またはIであり、X3は、ClおよびBrから選択され、PdLnは、パラジウム金属担持触媒または可溶性不均一パラジウム触媒である。L−誘導体化試薬は、化合物137Dのアルコール官能基を、任意の脱離基に変換する部分である。  (もっと読む)
(もっと読む)
3R−アミノピロリジン誘導体の製造方法
【課題】本発明の課題は、比較的安価でかつ工業的スケールで入手容易な3R−ヒドロキシプロリン誘導体を製造原料とし、収率よく、かつ高い立体選択性で3R−アミノピロリジン誘導体を、工業的な見地から効率よく製造する方法を提供することを目的とする。
【解決手段】 一般式(1)
(式中、R1は置換または無置換のアルキル基、置換または無置換のベンジル基、−CO−O−X、−CO−Yを示し、Xは置換または無置換の炭素数アルキル基、置換または無置換のベンジル基、置換または無置換のフルオレニルメチル基、置換または無置換のアリール基を示し、Yは、置換または無置換のアルキル基、置換または無置換のアリール基を示す。)で表される化合物から、一般式(5)、一般式(6)で表される化合物を経由して、一般式(9)
【化9】
(式中、R1は前記と同義である。)で表される化合物の製造方法。
(もっと読む)
グリコーゲン・シンターゼ・キナーゼ(GSK3)に関連する疾患の治療のためのイミダゾール−ピリミジン誘導体
本発明は、遊離塩基としての式(I)の化合物、又は薬学的に許容されるその塩に関する。本発明は、また該化合物を含む医薬処方、及び治療における該化合物の使用に関する。本発明は、更に、式(I)の化合物の製造方法、及びその中で使用される新しい中間体に関する。
【化1】
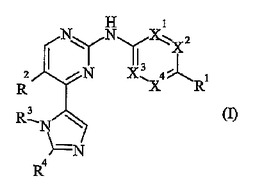 (もっと読む)
(もっと読む)
非ステロイド性グルココルチコイド受容体リガンドとしてのフェニルピラゾール誘導体
本発明は、式(I)で表される化合物、その製造方法、本化合物を含む医薬組成物および前記組成物の製造、中間体、治療用(特に炎症疾患、アレルギー疾患および/または自己免疫疾患の治療用)医薬を製造するための本化合物に使用を提供する。
【化1】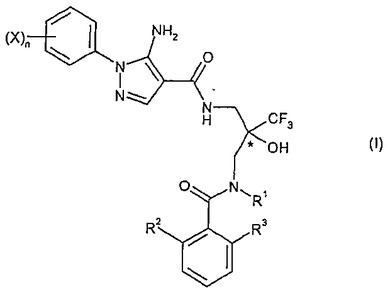 (もっと読む)
(もっと読む)
チオエポキシ系重合性組成物
【課題】チオエポキシ系化合物からなる樹脂の屈折率、色相、光学歪みなどのばらつきの少ない重合性組成物及びその製造方法を提供。
【解決手段】式(1)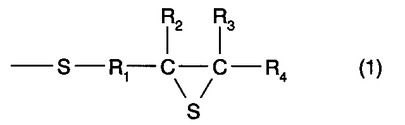
(式中、R1は炭素数1〜10の炭化水素、R2、R3、R4はそれぞれ炭素数1〜10の炭化水素基または水素原子を表す。)で表される構造を1個以上有する化合物を含有する重合性組成物において、ジチオエポキシ構造を少なくとも一つ有し、かつ、チオエポキシ構造を少なくとも一つ有するチオエポキシ化合物A、及びエポキシ構造を少なくとも一つ有し、かつ、チオエポキシで表される構造を少なくとも一つ有するチオエポキシ化合物Bの合計が、重合性組成物総質量に対して4質量%以下であることを特徴とする重合性組成物。
(もっと読む)
メルカプト官能性の高μβEO発色団、及び、高Tg低光学損失の共有結合性の高μβEO発色団を含むポリマー、及びEO材料の合成方法
本発明は、一般に、メルカプト官能性の高μβEO発色団及びEOポリマーに関し、特に、電気光学装置およびシステムの製造に有用なメルカプト官能性の高μβEO発色団及びEOポリマーに関する。メルカプト官能性の高μβEO発色団は、ポリ(硫化イミド)ポリマーに共有結合して、Tgが高く光学損失の少ない共有結合性の高μβEO発色団含有ポリマーを生じる。穏やかな重合条件を用いて、これらのEO材料を合成する方法についても説明する。 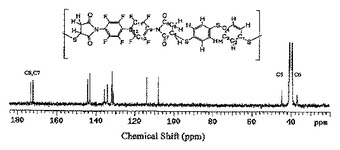 (もっと読む)
(もっと読む)
N−(2,3−エポキシ−2−メチルプロピル)フタルイミドの製造法
【課題】N−(2,3−エポキシ−2−メチルプロピル)フタルイミドの効率的な製造法を提供する。
【解決手段】2−メチル−エピハロヒドリンをアルコール類、エーテル類等の有機溶媒中で、アルカリ金属炭酸塩、アルカリ金属炭酸水素塩、または特定の第4級アンモニウム塩の存在下、反応させてN−(3−ハロゲノ−2−ヒドロキシ−2−メチルプロピル)フタルイミドを得、次いで、アルカリ金属アルコキシドにより閉環反応させることを特徴とする。
(もっと読む)
tert−ブチル(E)−(6−[2−[4−(4−フルオロフェニル)−6−イソプロピル−2−[メチル(メチルスルホニル)アミノ]ピリミジン−5−イル]ビニル](4R,6S)−2,2−ジメチル[1,3]ジオキサン−4−イル)アセテートの製造法
【課題】高コレステロール血症、高リポ蛋白血症、及びアテローム性動脈硬化症等の治療に有用な医薬を製造する上での中間体の製造法の提供。
【解決手段】ジフェニル[4-(4-フルオロフェニル)-6-イソプロピル-2-[メチル(メチルスルホニル)アミノ]ピリミジン-5-イルメチル]ホスフィンオキシドとtert-ブチル 2-[(4R,6S)-6-ホルミル-2,2-ジメチル-1,3-ジオキサン-4-イル]アセテートとを強塩基の存在下で反応させることにより、tert-ブチル (E)-(6-[2-[4-(4-フルオロフェニル)-6-イソプロピル-2-[メチル(メチルスルホニル)アミノ]ピリミジン-5-イル]ビニル]-(4R,6S)-2,2-ジメチル[1,3]ジオキサン-4-イル)アセテートを製造する。
(もっと読む)
4−アルコキシピリジン−1−オキシド誘導体の製造方法
【課題】胃酸分泌抑制剤、抗潰瘍剤として有用なベンズイミダゾール誘導体の製造中間体である4−アルコキシピリジン−1−オキシド誘導体の、爆発の危険性がなく、作業性および操作性に優れる製造方法を提供する。
【解決手段】下記式(I)で表される化合物の製造方法であって、
(式中、RaおよびRcは、水素原子等を、Wは、単結合等を、Rbは、C1−C6アルキル基等を示す。)トルエン中、水酸化カリウムを用いて、ピリジンNオキシドの誘導体とHO−W−Rb化合物とを反応させる工程を含む製造方法。
(もっと読む)
光学活性なピペラジン化合物の製造方法
【課題】光学活性なミルタザピン等の医薬品の製造に有用な、新規な光学活性な1−メチル−3−フェニルピペラジンおよびその塩、その製造方法、並びにその中間体を提供する。
【解決手段】以下の方法により、光学活性な1−メチル−3−フェニルピペラジンおよびその塩を製造する。
(式中の各記号は明細書に記載の通りである)。
(もっと読む)
光学活性なピペラジン化合物の製造方法
【課題】光学活性なミルタザピン等の医薬品の製造に有用な光学活性な1−メチル−3−フェニルピペラジン、ならびに光学活性な1−(3−ヒドロキシメチル−2−ピリジル)−4−メチル−2−フェニルピペラジンの製造方法を提供すること。
【解決手段】光学活性なフェニルグリシン誘導体を原料とし、N−クロルアセチルフェニルグリシン、N−メチルアミノアセチルフェニルグリジン、そのメチルエステル、1−メチル−3−フェニルピペラジン−2,5−ジオン、1−メチル−3−フェニルピペラジン、1−(3−シアノ−2−ピリジル)−4−メチル−2−フェニルピペラジン、1−(3−ホルミル−2−ピリジル)−4−メチル−2−フェニルピペラジンを経て製造する。
(もっと読む)
ベンゾイソインドール系化合物およびその製造法
【課題】新規な骨格の機能材料とその有機エレクトロルミネッセンス素子への応用。
【解決手段】下記一般式(1)で表される化合物。一般式(1)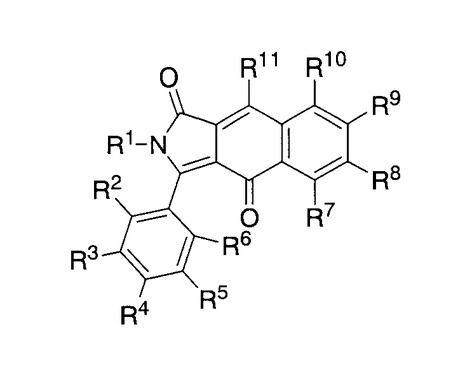
[式中、Rは、互いに独立に、水素原子、アルキル基、フェニル基などである。]
(もっと読む)
複素環式誘導体の製造方法
本発明は、様々な化合物、とりわけD3受容体の強力で特異的なアンタゴニストである化合物の合成において、式(I)[式中、Xは、窒素または硫黄であってよく;Hetは、アリールまたはヘテロアリールを意味し;その各々は、ハロゲン、C1−C6アルキル、C1−C6アルコキシ、ハロC1−C6アルキル、C2−C6アルケニル、C2−C6アルキニル、ハロC1−C6アルコキシ、−C(O)R1、ニトロ、ヒドロキシ、−NR2R3、シアノまたはZ基から選択される1個〜4個のJ基により置換されていてもよく;R1は、C1−C4アルキル、−OR3または−NR3R4であり;R2は、水素またはC1−C6アルキルであり;R3は、水素またはC1−C6アルキルであり;Rは、H、C1−C6アルキル、アリール、ベンジルであり;その各々は1個〜4個のJ基により置換されていてもよい]で示される重要な中間体を調製するのに有用な新規の方法であって、以下のスキームI[ここで、工程aは、式(II)で示される化合物を得るための、化合物(IIA)の塩基性条件下での3−チオセミカルバジド誘導体との反応、次に無機塩基およびn−プロパンホスホン酸環状無水物を用いた処理、そして最後に無機酸を用いたpH調節を意味する]
に従う方法に関する。
 (もっと読む)
(もっと読む)
鏡像異性的に富化した環式β−アリール又はヘテロアリールカルボン酸の調製方法
本発明は、下記スキーム(式I,II)[式中、Xは、−C(R)(R’)−、−N(R”)−、−O−、−S(O)o−、C(O)N(R”)、−N(R”)C(O)−又は−C(O)−であり;R及びR’は、互いに独立して、水素、C1−7−アルキル、C1−7−アルキル(ハロゲン、C1−7−アルコキシ、ヒドロキシ又は−(CH2)p−Arで置換されている)であり;R”は、水素、C1−7−アルキル、ハロゲンで置換されているC1−7−アルキル、−S(O)o−C1−7−アルキル、−S(O)o−Ar、−S(O)o−NRR’、−(CH2)p−Ar、−C(O)−C1−7−アルキル、−C(O)−Ar、−C(O)−NRR’又は−C(O)O−C1−7−アルキルであり;Arは、アリール1又はヘテロアリール1であり;nは、0、1、2又は3であり;mは、0、1、2又は3であり;oは、0、1又は2であり;pは、0、1又は2である]に従うエナンチオ選択的水素化による高いジアステレオ選択性及び高いエナンチオ選択性のシス置換環式β−アリール又はヘテロアリールカルボン酸誘導体ならびにそれらの対応する塩を調製する方法に関する。  (もっと読む)
(もっと読む)
キノロン中間体調製のためのカップリング方法
式Iの7−シクロアミノ−1−シクロプロピル−1,4−ジヒドロ−8−メトキシ−4−オキソ−3−キノリンカルボン酸の製造方法。そのような製法の用途に好適な式(IV)のホウ酸エステル化合物。 (もっと読む)
炭酸ジメチルを用いたインドール化合物のメチル化
【課題】インドール化合物のN-メチル化。
【解決手段】塩基および/または触媒の存在下で、周囲圧にて、メチル化されていない前躯体を炭酸ジメチルと反応させて一般式(I)で表わされるメチル化されたインドール化合物(ただしR1とR2はこの明細書と請求の範囲に定義してある)を製造する方法。
(もっと読む)
ジオキサジニルピラゾール化合物の製造方法および中間体
【課題】 ジオキサジニルピラゾール化合物の製造方法を提供する。
【解決手段】公知のスルファモイルピラゾールカルボン酸エステル化合物または公知のスルファモイルピラゾールカルボン酸化合物より、新規なスルファモイルカーバメートピラゾールカルボン酸化合物、スルファモイルピラゾールヒドロキサム酸化合物、スルファモイルピラゾールカルボン酸混合酸無水物、スルファモイルピラゾールカルボン酸クロリド化合物、ピラゾロイソチアゾール化合物およびスルファモイルピラゾールヒドロキサム酸−O−(2−ヒドロキシエチル)化合物を中間体として製造し、スルファモイルピラゾールヒドロキサム酸−O−(2−ヒドロキシエチル)化合物を脱水反応させることにより4−(5,6−ジヒドロ−1,4,2−ジオキサジン−3−イル)スルファモイルピラゾール化合物を製造する。
(もっと読む)
1−ハロ−2,7−ナフチリジニル誘導体を調製する方法
1−ハロ−2,7−ナフチリジニル誘導体(I)(式中、Xは、Cl又はBrである)を調製する方法であって、(i)式(A)の3−シアノ−4−メチルピリジン誘導体と、式(II)の化合物との、N,N−ジメチルホルムアミドジC1〜6アルキルアセタールの存在下での反応により、式(III)のエナミン誘導体を得るステップと、(ii)式(III)のエナミンの環化によって、式(IV)の化合物を得るステップと、(iii)式(IV)の化合物とハロゲン化剤との反応によって、式(I)の化合物を得るステップとを含む方法が記載される。  (もっと読む)
(もっと読む)
置換ピラゾールの製造方法
本発明は、一般に置換ピラゾール、置換ピラゾールの互変異性体、ならびに置換ピラゾールおよび互変異性体の塩類を製造する方法に関する。置換ピラゾールの構造は式(I)
に対応し、式中のR3A、R3B、R3C、Y1、Y2、Y3、Y4、およびY5は、明細書中に定めたもの
である: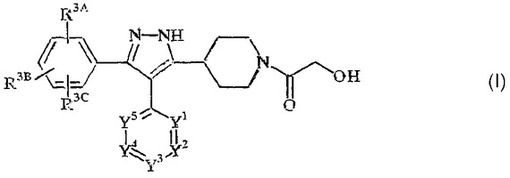 (もっと読む)
(もっと読む)
361 - 380 / 645
[ Back to top ]