Fターム[4G169CB68]の内容
触媒 (289,788) | 化学合成用(C1化学を除く) (9,462) | 生成する置換基からみた有機合成反応 (2,941) | ハロゲン化 (124)
Fターム[4G169CB68]の下位に属するFターム
フッ素化 (35)
Fターム[4G169CB68]に分類される特許
41 - 60 / 89
2−アミノ−5−シアノ安息香酸誘導体を調製するための方法
式2の化合物と、少なくとも1種の式3のアルカリ金属シアン化物および式4の化合物とを接触させる工程を含む式1の化合物を調製する方法が開示されている。
【化1】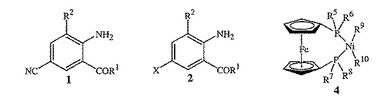
式中、R1はNHR3またはOR4であり;R2はCH3またはClであり;R3は、H、C1〜C4アルキル、シクロプロピル、シクロプロピルシクロプロピル、シクロプロピルメチルまたはメチルシクロプロピルであり;R4はHまたはC1〜C4アルキルであり;Xは、Br、ClまたはIであり;ならびに、R5、R6、R7、R8、R9およびR10は本開示中に定義されているとおりである。
また、YがCl、BrまたはIである式5の化合物と、シクロアルカジエン二座リガンド、少なくとも1種の金属還元剤およびニトリル溶剤とを接触させる工程を含む、R9およびR10が一緒になってシクロアルカジエン二座リガンドである式4の化合物を調製する方法もまた開示されている。
また、式5の化合物と、シクロアルカジエン二座リガンドおよび少なくとも1種の金属還元剤とを接触させることにより式4の化合物を調製する工程、次いで、式4の化合物を含むこの反応混合物と式2の化合物および式3の少なくとも1種のアルカリ金属シアン化物とを接触させる工程を含む式1の化合物を調製する方法も開示されており;ならびに、式1の化合物を上記に開示の方法により調製することを特徴とする、R15、R16、R17およびZが式1の化合物を用いて本開示中に定義されているとおりである式6の化合物を調製する方法がさらに開示されている。
【化2】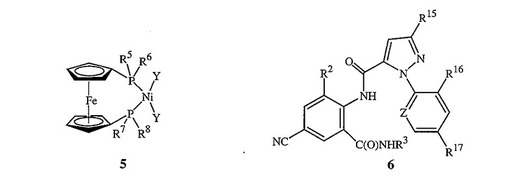
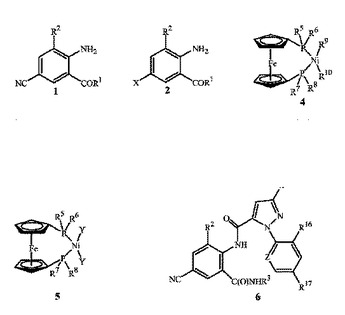 (もっと読む)
(もっと読む)
ヨード化芳香族化合物の製造方法
本発明は、ヨード化芳香族化合物の製造方法を開示する。さらに詳しくは、ゼオライト触媒を用いて酸素雰囲気下で芳香族化合物をヨード化反応させる方法において、原料としての芳香族化合物およびそのモノヨード化合物をヨウ素と反応させることによりヨード化芳香族化合物を製造する方法を開示する。モノヨード化合物の添加なしで芳香族化合物のみを原料として使用する方法と比較すると、本発明の方法はジヨード化合物の生産性およびとp−ジヨード化合物の選択性を高めると同時に、副反応を抑制することにより、触媒の使用周期を延長することができる。 (もっと読む)
置換クロルメタン化合物の製造方法
【課題】アルコキシカルボニル基、アルキルカルボニル基またはアリールカルボニル基で置換されたクロルメタン化合物を工業的により有利に製造できる方法の提供。
【解決手段】第6族元素金属または第6族元素化合物と、過酸化水素とを反応させて第6族元素酸化物を調製し、次いで、該第6族元素酸化物およびリン酸塩の存在下、置換メタン化合物(例えばアセチルアセトン)と過酸化水素と金属塩素化物とを反応させる式(2)で示される置換クロルメタン化合物(例えば2−クロロ−3,5−オエンタンジオン)の製造方法。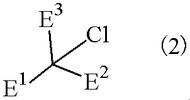
(式中、E1〜E3は、置換されていてもよいアルコキシカルボニル基、置換されていてもよいアルキルカルボニル基、置換されていてもよいアリールカルボニル基または水素原子を表す。)
(もっと読む)
アルファ、ベータ−不飽和カルボニルハロゲン化物を形成するプロセス
マイクロリアクター中でα,β−不飽和カルボニルハロゲン化物を形成するプロセスが記述される。この反応物質は、α,β−不飽和カルボン酸、ハロゲン化剤、及び触媒を含む。第1の流入ストリーム、第2の流入ストリーム、及び任意選択の第3の流入ストリームが貫流マイクロリアクターの反応チャンバに流入し、α,β−不飽和カルボニルハロゲン化物を含む反応生成物を生成する。 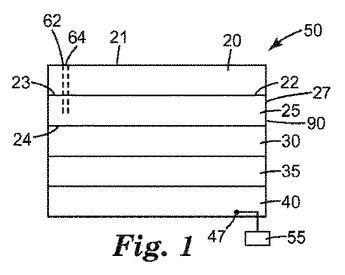 (もっと読む)
(もっと読む)
新規なキラルサレン触媒とこれを利用したラセミ体エポキシ化合物からのキラル化合物の製造方法
本発明は新規なキラルサレン触媒とこれを利用してラセミ体エポキシドからキラル化合物を製造する方法に関する。より詳しくは、新しい分子構造を有しているため触媒活性に優れており、反応が終わった後にも生成された目的キラル化合物のラセミ化が起きなくまたは非常に少なく起こるという長所があり、触媒再生処理なしに繰り返して再使用が可能な新規なキラルサレン触媒とこのような新規なキラルサレン触媒を利用してキラル食品添加剤、キラル医薬品またはキラル農薬などを製造するための原料として使われることができる高光学純度のキラル化合物を大量生産が可能に経済的に製造する方法に関する。 (もっと読む)
可逆的なハロゲン化水素の捕捉及び放出を組み込んだ領域反応器
炭化水素原料を高級炭化水素に転換する改良された方法及び領域反応器が提供される。反応器の第一のゾーンはハロゲン化水素(HX)を放出することができる物質及び炭素−炭素カップリング触媒を含み、第二のゾーンは最初は空であるか又はハロゲン化触媒及び/又はオキシハロゲン化触媒を含み、かつ第三のゾーンは炭素−炭素カップリング触媒及びHXを捕捉することができる物質を含む。空気又は酸素は第一のゾーンに導入され、原料は第二のゾーンに導入され、また第三のゾーンで生成物が生産される。反応時に生産されたHXは、ゾーン1及び3で可逆的に捕捉され放出される。 (もっと読む)
ビニル芳香族重合体のクロロメチル化からの流出液を処理する方法
ビニル芳香族重合体のクロロメチル化からの流出液を処理する方法であって、流出液は触媒および揮発性有機物を含み、その方法は、1)触媒の少なくとも一部を不活性化する工程、2)流出液を蒸留する工程、3)流出液にカセイアルカリを添加する工程、および4)流出液を蒸留する工程を含む。 (もっと読む)
CF3IおよびCF3CF2Iを合成するための触媒
【課題】フルオロヨードアルカン化合物の工業的に有利な製造方法を提供する。
【解決手段】式:CF3(CF2)n−Y(式中、nは、0または1であり、Yは、H、Cl、BrおよびCOOHからなる群より選択される。)で示される化合物とヨウ素源を、d1s1配置を有する元素、および、ランタニド元素を含む触媒、および酸素源の存在下反応させる。
(もっと読む)
高含有率デカブロモジフェニルエタンの調製および提供
高含有率反応由来デカブロモジフェニルエタン生成物が、(i)ジフェニルエタンまたは(ii)平均臭素数約2つ未満の部分臭素化ジフェニルエタン、または(iii)(i)および(ii)の両方を反応混合物の液体領域に供給することにより調製される。前記反応混合物は、(a)過剰な液体臭素とアルミニウム系ルイス酸臭素化触媒を含む成分から形成され、(b)約45°−90℃の高い反応温度の1つまた複数の温度に保持され、少なくとも、圧力の上昇が使用温度で反応混合物の液状を保つのに必要である場合、反応混合物は芳香族臭素化反応が起こるような、高圧下に置く。ここで、効果的な難燃剤である、高含有率反応由来デカブロモジフェニルエタン生成物を形成するのに十分な低速で、供給を実施する。  (もっと読む)
(もっと読む)
触媒活性物質の製造方法、並びに、モノクロロアルカン及び/又はモノクロロシクロアルカンの製造方法
【課題】所定の鉄化合物から、アルケン等と塩化水素との反応に対する触媒活性を有する物質を製造すること。また、この触媒活性物質を、アルケン等と塩化水素との反応に用いて、モノクロロアルカン等を製造すること。
【解決手段】アルケン、シクロアルケン及び塩化水素の不存在下で塩化第二鉄をモノクロロアルカン及び/又はモノクロロシクロアルカンと混合することにより得られ、アルケン及び/又はシクロアルケンと塩化水素との反応に対する触媒活性を実質的に示さない鉄化合物に、アルケン及びシクロアルケンの不存在下で塩化水素を接触させることによる触媒活性物質の製造方法。また、この方法により得られる触媒活性物質の存在下に、アルケン及び/又はシクロアルケンと塩化水素とを反応させるモノクロロアルカン及び/又はモノクロロシクロアルカンの製造方法。
(もっと読む)
オキシ塩素化反応の触媒組成物
【課題】エチレンと塩化水素の転化を増大させ、1,2−ジクロロエタンの形成の選択率が減少することなく、移動床として使用されたときに触媒が互いに固着することのない、エチレンのオキシ塩素化反応の触媒組成物の提供。
【解決手段】触媒組成物が、a)銅塩として、3〜12質量%の銅、b)アルカリ土類金属塩として、0〜3質量%のアルカリ土類金属塩、c)アルカリ金属塩として、0〜3質量%のアルカリ金属塩、d)対応する金属塩又はテトラクロロ金酸として、0.001〜0.1質量%、好ましくは0.005〜0.05質量%の、ルテニウム、ロジウム、オスミウム、イリジウム、及び白金からなる群より選択された1種以上の金属、及び/又は0.0001〜0.1質量%、好ましくは0.001〜0.05質量%の金を含むような割合で、担体に施されることを特徴とする触媒組成物に関する。
(もっと読む)
相間移動反応用触媒
【課題】磁気による分離回収が可能な新規な相関移動反応用触媒を提供する。
【解決手段】 下記一般式(1)
【化1】
(式中、Aはアルキル基、Bはメチレン基又はNH基を表す。R1、R2は炭化水素基、R3、R4、R5は炭化水素基又は水素原子を表し、それぞれが結合して環を形成していてもよい。R6は炭素数1から3のアルキル基を表す。mは0から1までの数字、nは1から3までの数字を表す。)で表されるクラウンエーテルを含有する相関移動反応用触媒。該相関移動反応用触媒に磁性微粒子(M)を担持させ、下記構造で表される磁石により分離回収可能な相関移動反応用触媒。
【化2】 (もっと読む)
(もっと読む)
トリフルオロヨードメタンとペンタフルオロヨードエタンを製造するための触媒プロモーター
【課題】式CF3(CF2)n−I[式中、nは0又は1である]によって表されるフルオロヨードアルカン化合物の製造方法の提供。
【解決手段】(i)式CF3(CF2)n−Yによって表される化合物[式中、YはH、Cl、Br及びCOOHから選択され、そしてnは0又は1である];(ii)ヨウ素の供給源;(iii)担体に支持されたアルカリ又はアルカリ土類金属塩触媒;及び、(iv)アルカリ又はアルカリ土類金属塩触媒のための触媒プロモーター、を接触させる工程を含む。触媒プロモーターは、遷移金属元素、希土類金属元素、アルカリ又はアルカリ土類金属元素以外の典型元素、いずれものこれらの塩、及び、いずれものこれらの組合せから選択される少なくとも一つの元素を含む。接触は、フルオロヨードアルカン化合物を製造するための温度及び圧力で、そして十分な長さの時間で行われる。
(もっと読む)
ゼオライト触媒の活性回復方法
【課題】ゼオライト触媒を使用して、液相で芳香族化合物を反応する際に、簡便な処理により、ゼオライト触媒の活性を回復する方法を提供する。また、燃焼などの発熱反応を行わず、活性回復操作の管理が容易であり、熱、スチーミング等によるゼオライトの結晶構造の破壊を回避できる方法を提供する。
【解決手段】液相で芳香族化合物を反応させたゼオライト触媒の活性回復方法であって、50℃以下で前記ゼオライト触媒に水を吸着させた後、反応温度以下でエージング運転することを特徴とするゼオライト触媒の活性回復方法。
(もっと読む)
モノ−ヨードベンゼンの製造方法
本発明はトランスヨード化反応を用いたモノ−ヨードベンゼンの製造方法に関し、より詳しくは、Si/Alのモル比が5乃至100のHYゼオライト触媒を利用するトランスヨード化反応によって、ジ−ヨードベンゼン及びトリ−ヨードベンゼンからなる群より選択される1種以上のマルチヨードベンゼンとベンゼンとを含む反応物からモノ−ヨードベンゼンを製造する方法に関する。
本発明の製造方法は、一般的なp−ジ−ヨードベンゼンの製造工程中に生成される副生成物であるm−ジ−ヨードベンゼン、o−ジ−ヨードベンゼン、及びトリ−ヨードベンゼンからヨウ素を回収して、ヨウ素の損失を最小化することができる長所がある。  (もっと読む)
(もっと読む)
1,1,1,3,3−ペンタクロロプロパンの製造方法
【課題】ハロアルカンを製造する方法、より詳細には1,1,1,3,3−ペンタクロロプロパン(HCC−240fa)及び/又は1,1,1,3−テトラクロロプロパン(HCC−250fb)の製造方法を提供する。
【解決手段】 この方法は(a)均質な混合物を生成するのに適切な条件下で、触媒、共触媒、及びハロアルカン出発物質を混合すること;(b)ハロアルカン生成物流れを生成するのに適切な条件下で、該均質な混合物をハロアルケン及び/又はアルケン出発物質と反応させること;及び(c)前記生成物流れからハロアルカン生成物を回収することを含む。
(もっと読む)
ハイドロハロプロパンおよびハイドロフルオロブタンの接触製造方法
ハイドロハロプロパンまたはハイドロフルオロブタンの製造方法が開示される。本方法は、改質塩化アルミニウム触媒または改質臭化アルミニウム触媒の存在下にハイドロフルオロメタンをフルオロオレフィンと反応させてハイドロハロプロパンまたはハイドロフルオロブタンを生成する工程を含む。ハイドロフルオロメタンはCH2F2またはCH3Fである。フルオロオレフィンはCF2=CF2、ClFC=CF2またはCF3CF=CF2である。 (もっと読む)
オキシクロリネーション用触媒およびその製造方法
【課題】 流動性、流動性の低下抑制、耐摩耗性等に優れると共に活性、EDCの選択性、エチレン燃焼抑制等に優れる。
【解決手段】 オキシクロリネーション用触媒は、シリカ、ボリアおよび五酸化リンから選ばれる1種または2種以上の酸化物(A)とアルミナと銅とを含んでなり、酸化物(A)の含有量が酸化物として1〜8重量%の範囲にあり、銅の含有量が酸化物(CuO)として5〜20重量%の範囲にある。さらに、アルカリ、アルカリ土類、希土類等の助触媒成分を含有しても良い。
(もっと読む)
複数帯域の固定床反応器における、アルキルメルカプタンの製造方法
本発明は、反応を少なくとも2の連続する反応帯域で実施し、触媒が異なる活性と選択性を含む、アルカリタングステン酸塩を用いたアルカノールと硫化水素との触媒気相反応によるアルキルメルカプタンの製造方法に関する。 (もっと読む)
置換ビフェニルの製造法
本発明は、式(I)の構造を有する置換ビフェニルの製造法であって、式(II)の構造を有する化合物を、塩基および以下:
a) パラジウムが酸化状態ゼロであるパラジウム−トリアリールホスフィンもしくは−トリアルキルホスフィン錯体、
b) 錯体リガンドとしてトリアリールホスフィンもしくはトリアルキルホスフィン存在下であるパラジウム塩、または
c) 担体に保持されていてもよい金属パラジウム
の群より選択されるパラジウム触媒の存在下において、トリアリールホスフィンまたはトリアルキルホスフィン存在下、溶媒中で式(III)の構造を有するジフェニルボリン酸と反応させることを含み、ここで、使用するトリアリールホスフィンまたはトリアルキルホスフィンが置換されていてもよい、前記製造法に関する。
〔式(I)中、置換基が以下:
Xはフッ素または塩素であり、
R1はニトロ、アミノまたはNHR3であり、
R2はシアノ、ニトロ、ハロゲン、C1〜C6-アルキル、C1〜C6-アルケニル、C1〜C6-アルキニル、C1〜C6-アルコキシ、C1〜C6-ハロアルキル、(C1〜C6-アルキル)カルボニルまたはフェニルであり、
R3はC1〜C4-アルキル、C1〜C4-アルケニルまたはC1〜C4-アルキニルであり、
nは1、2または3であるが、nが2または3の場合には、該R2基は互いに異なっていてもよい、
として定義される〕
〔式(II)中、Halはハロゲンであり、かつXおよびR1は上記に定義されたものである〕
〔式(III)中、R2およびnは上記に定義されたものである〕
(もっと読む)
41 - 60 / 89
[ Back to top ]



