国際特許分類[A61P19/08]の内容
生活必需品 (1,310,238) | 医学または獣医学;衛生学 (978,171) | 化合物または医薬製剤の特殊な治療活性 (401,658) | 骨格系疾患の治療剤 (18,007) | 骨疾患のためのもの,例.くる病,ページェット病 (5,534)
国際特許分類[A61P19/08]の下位に属する分類
骨粗しょう症のためのもの (3,265)
国際特許分類[A61P19/08]に分類される特許
1,081 - 1,090 / 2,269
化学化合物
細胞周期阻害活性を保有する式(I)の化合物について記載する。 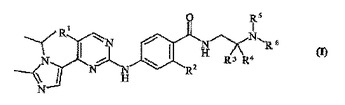 (もっと読む)
(もっと読む)
縮合[d]ピリダジン−7−オン類
【解決手段】 本発明は、式(I)の縮合[d]ピリダジン−7−オン類を対象とする。この発明はまた、該縮合[d]ピリダジン−7−オン類を生成および使用するための方法を対象とする。特に、本発明の化合物は、例えば血管新生障害および神経変成疾患を含む、VEGFR2、CDK5およびMLK1酵素の活性に関連する疾患の治療に有用であり得る。
(もっと読む)
ピラゾロピリミジン類及びそれらの塩類、それらを含んで成る医薬組成物類、それらの調製方法及びそれらの使用
本発明は、一般式(I)のピラゾロピリミジン化合物類及びそれらの塩、前記ピラゾロピリミジン化合物類を含んで成る医薬組成物、前記ピラゾロピリミジン化合物類の調製方法、及び異常調節された血管増殖、又は異常調節された血管増殖に付随する疾病の処理又は予防のための医薬組成物の製造のためへのそれらの使用に関する。 (もっと読む)
ヒトIL−17に対する抗体分子
インターロイキン17(IL-17)に対する、結合メンバー、特に、抗体分子。この結合メンバーは、関節リウマチなどのインターロイキン17に関連する障害の治療にとって有用である。 (もっと読む)
骨形成用徐放性医薬組成物
【課題】各種ゼラチンハイドロゲルの中からヘパリン結合能の亢進した改変型BMPとの組み合わせに最も適したキャリアを選択し、改変型BMPおよび最適のゼラチンハイドロゲルを含む骨形成用徐放性医薬組成物を提供する
【解決手段】大腸菌を宿主として生産され、ヘパリン結合能の亢進した改変型BMPと、塩基性ゼラチンハイドロゲルとを含む構成の骨形成用徐放性医薬組成物とする。当該骨形成用徐放性医薬組成物は低コストで製造できるとともに、低用量の投与でも十分な骨形成効果を発揮できる。
(もっと読む)
プテリジン誘導体およびカテプシン阻害剤としてのそれらの使用
本発明は、システインプロテアーゼ活性と関連する疾患の処置のための化合物および組成物に関する。本化合物は、システインプロテアーゼS、K、F、LおよびBの可逆性阻害剤である。特に興味深いのは、カテプシンKと関連する疾患である。 (もっと読む)
カルシウム粉体及び骨強化剤
【課題】従来よりも優れた骨強化効果が得られる骨強化剤を提供すること。また、その原料となるカルシウム粉体を提供すること。
【解決手段】 本発明のカルシウム粉体は、粒径が20〜650nmであり、(長径/短径)が1.5以下である粒子からなるを特徴とする。骨強化剤は、カルシウム粉体とビタミンD3とを含有することを特徴とする。
(もっと読む)
キノリン化合物および使用方法
式(I)の化合物と、その立体異性体、幾何異性体、互変異性体、溶媒和物、代謝産物、塩、および薬学的に許容されるプロドラッグは、受容体チロシンキナーゼの阻害、およびそれによって媒介される過剰増殖性の障害の治療に有用である。哺乳動物細胞のそのような障害、または関連する病理学的症状のインビトロ、インサイチュ、およびインビボでの診断、予防、または治療のために、式(I)の化合物ならびに、その立体異性体、幾何異性体、互変異性体、溶媒和物、および薬学的に許容される塩を使用する方法が開示される。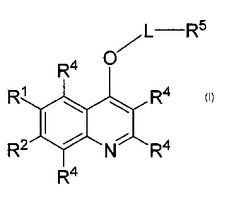
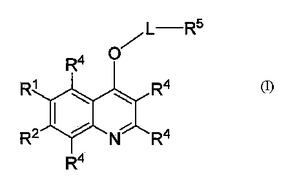 (もっと読む)
(もっと読む)
マクロファージ転位阻害因子阻害剤としてのオキシム誘導体
式(I)の化合物および他の化合物が、与えられている。これらの化合物を含んでいる医薬組成物も、与えられている。加え、哺乳類におけるマクロファージ転位阻害因子(MIF)活性を阻害していくとの方法も、与えられており、哺乳類における炎症を処置もしくは予防していくとの方法、ならびに、敗血症(sepsis)、敗血症(septicemia)、および/または内毒素(エンドトキシン)ショックを持っている哺乳類を処置していくとの方法もである。
【化1】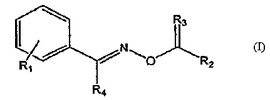
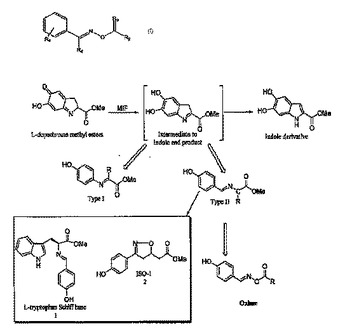 (もっと読む)
(もっと読む)
安定化されたインスリン様増殖因子ポリペプチド
本発明は、IGF−1またはIGF−2配列およびE−ペプチド配列を有し、IGFからのE−ペプチドの生理学的自然開裂が阻止されている、安定化されたポリペプチドに関するものである。 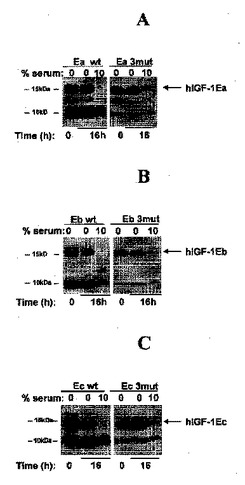 (もっと読む)
(もっと読む)
1,081 - 1,090 / 2,269
[ Back to top ]

