国際特許分類[C07D215/22]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | 複素環式化合物 (108,186) | キノリン環系または水素添加したキノリン環系を含有する複素環式化合物 (1,797) | 環の窒素原子と非環原子間に結合をもたないもの,または環の窒素原子に直接結合する水素原子または炭素原子のみをもつもの (1,761) | 異種原子,または異種原子に対する3個の結合をもち,そのうち多くても1個がハロゲンに対する結合である炭素原子,例.エステルまたはニトリル基,が環の炭素原子に直接結合したもの (1,324) | 酸素原子 (478) | 2位または4位に結合しているもの (249)
国際特許分類[C07D215/22]の下位に属する分類
2位に1個の酸素原子のみが結合するもの
4位に1個の酸素原子のみが結合するもの
国際特許分類[C07D215/22]に分類される特許
51 - 60 / 249
CNS障害の治療に有用なキノリノン誘導体
本発明は、CNS障害の動物モデルにおいて有効であり、したがって、CNS(中枢神経系)疾患又は障害の予防又は治療用の貴重な候補である、新規なキノリノン誘導体(I)に関する。本発明は、他の態様において、本発明のキノリノン誘導体を含む医薬組成物及び治療用途のためのこれらの化合物の使用に関する。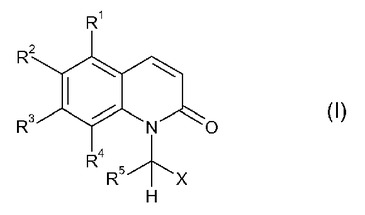
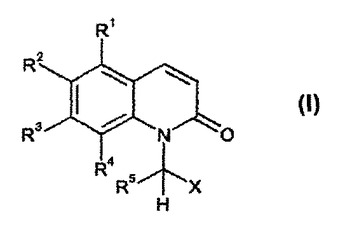 (もっと読む)
(もっと読む)
医薬
【課題】パーキンソン病の慢性進行性を阻止もしくはドパミン神経細胞をその病因から保護することにより神経機能障害の進行を抑制し、L-ドーパ服用時期までの期間を延長すると共に機能改善効果を有する医薬を提供することを課題とする。
【解決手段】本発明は、一般式(1)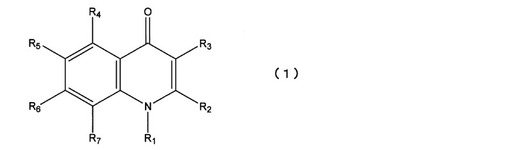
[式中、R1は、水素等を示す。R2は、水素等を示す。R3は、置換基を有していてもよいフェニル基等を示す。R4は、ハロゲンを示す。R5は水素またはハロゲンを示す。R6は、水素を示す。R7は、ヒドロキシ基等を示す。]
で表されるキノロン化合物またはその塩からなる医薬を提供する。
(もっと読む)
フッ素含有化合物およびその使用法
フッ素化化合物およびフッ素化化合物の製造法が本明細書に記載されている。例えば、フッ素化ベンラファキシン、フッ素化デュロキセチン、フッ素化バレニクリン、フッ素化アトモキセチン、フッ素化セルトラリン、フッ素化トラゾドン、フッ素化ミルタザピン、フッ素化アミトリプチリン、フッ素化アモキサピン、フッ素化クロミプラミン、フッ素化イミプラミン、フッ素化ノルトリプチリン、フッ素化トリミプラミン、フッ素化マプロチリン、フッ素化ネファゾドン、フッ素化シブトラミン、18F置換ブプロピオンなどが提供される。 (もっと読む)
AKTの選択的阻害剤およびその使用方法
本発明は、プロテインキナーゼBとしても公知であり、アポトーシスの阻害において、ならびに従って、癌および、神経変性疾患を含めた他の状態の病因において鍵となる役割を担っていると考えられる、酵素Akt1プロテインキナーゼの酵素活性を阻害する活性について、化合物をスクリーニングするための改善された方法を記載する。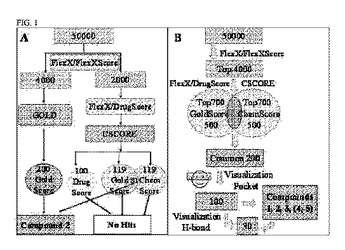 (もっと読む)
(もっと読む)
アルツハイマー病および癌の治療のためのクマリン系化合物
神経変性疾患及び癌に対するさらなる治療薬の必要性が存在する。本発明は、クマリン系化合物、それらの医薬組成物、及びそれらを用いた疾患の治療方法に関する。γ−セクレターゼ阻害薬として有用な式I(X、R1、R2及び添字tは、本明細書に定義されている通りである)の化合物を含む化合物を提供し、該化合物を含む組成物、並びに例えばアルツハイマー病などの神経変性疾患を治療又は予防するための該化合物の使用方法を提供する。 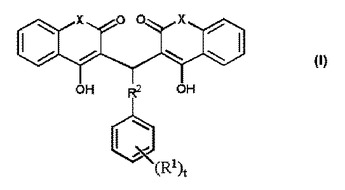 (もっと読む)
(もっと読む)
癌ならびに免疫および自己免疫疾患の治療のためのアポトーシス誘発剤
抗アポトーシスBcl−2タンパク質の活性を阻害する化合物、これらを含む組成物、および、その間に抗アポトーシスBcl−2タンパク質を発現する疾患の治療方法を開示する。 (もっと読む)
キノリン誘導体の調製方法
遺伝性および孤発性の腎乳頭腫および扁平上皮癌で、c-Metのキナーゼ領域の活性化が確認されている。従って、c-Metの調節は癌および癌関連疾患の治療手段として望ましい。本明細書はプロテインキナーゼの酵素活性の調節に役立つ化合物の調製方法に関する。より具体的には、本明細書は増殖、分化、プログラム細胞死、遊走、浸潤などの細胞活動の調節に役立つ化合物の調製方法に関する。
式i(1) の化合物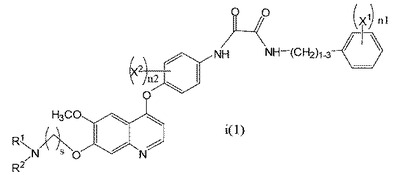
またはその薬学的に許容される塩を調製する方法。
式中、R1およびR2は、それらが結合する窒素原子と共に、6員のヘテロシクロアルキル基を形成する。
X1はH、Br、Cl、Fのいずれかである。
X2はH、Br、Cl、Fのいずれかである。
sは2〜6である。
n1は0〜2である。
n2は0〜2である。 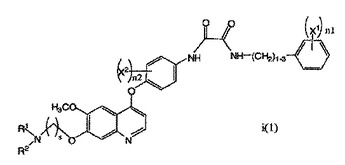 (もっと読む)
(もっと読む)
キノリン誘導体の調製方法
式i(1)の化合物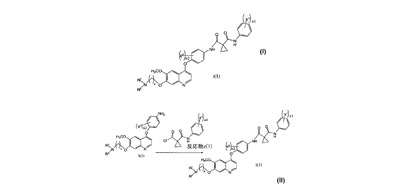
またはその薬学的に許容される塩を調製する方法。
式中、R1およびR2は、それらが結合する窒素原子と共に、6員のヘテロシクロアルキル基を形成する。
X1はH、Br、Cl、Fのいずれかである。
X2はH、Br、Cl、Fのいずれかである。
sは2〜6である。
n1は1〜2である。
n2は1〜2である。 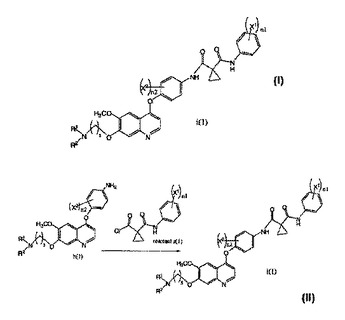 (もっと読む)
(もっと読む)
化合物及び使用方法
本発明は、タンパク質チロシンキナーゼ活性の調節、並びに細胞間及び/又は細胞内シグナル伝達の調節において有用な新規化合物を提供する。本発明は、そのような化合物を含有する医薬として許容し得る組成物、並びに哺乳動物、特にヒトにおける過増殖性疾患の治療における該組成物の使用方法も提供している。 (もっと読む)
骨欠損関連疾患の処置および/または予防に有用な化合物の新規な同定方法
本発明は、DOCK5タンパク質によるRAC GTPアーゼの活性化を阻害する化合物を同定するための方法であって、(i)細胞においてDOCK5とRACタンパク質を同時発現させる工程(ここで、該DOCK5タンパク質は不活性RAC(この不活性RACはGDPに結合されている)の、活性RAC(この活性RACはGTPに結合されている)への変換を誘導する)、(ii)該細胞を該化合物と接触させる、または接触させない工程、(iii)該化合物の存在下または不在下で、不活性RACの活性RACへの変換を判定する工程、および(iv)不活性RACの活性RACへの変換を阻害する化合物を選択する工程を含んでなる方法に関する。該化合物は骨欠損関連疾患の処置に有用である。 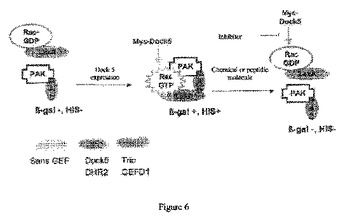 (もっと読む)
(もっと読む)
51 - 60 / 249
[ Back to top ]