Fターム[4C057LL19]の内容
糖類化合物 (12,552) | 1個の異項原子を糖類基と共有する複素環 (1,626) | Nを共有 (1,610) | 異項原子としてNのみを含有する複素環 (1,586) | ピリミジン (666) | 糖が2−デオキシリボシル (95)
Fターム[4C057LL19]に分類される特許
61 - 80 / 95
ヌクレオシド誘導体及びその製造方法
【課題】 核酸の糖部に芳香族置換基が導入された新規ヌクレオシド誘導体を容易に製造することのできる方法を提供すること。
【解決手段】 本発明のヌクレオシド誘導体の製造方法は、下記工程(a)及び(b)を含む。
(a)一般式(1)で表わされるヌクレオシド誘導体を、一般式(2)で表わされる芳香族ハロゲン化物と塩基の存在下で反応させて、一般式(3)で表わされる化合物を得る工程;及び
(b)一般式(3)で表わされる化合物を脱保護剤で処理することにより、保護基R1を脱保護して、一般式(4)で表わされるヌクレオシド誘導体を得る工程。
【化1】
R3−X (2)
【化2】
【化3】 (もっと読む)
(もっと読む)
ウィルス感染を治療するための脂質アナログ
【課題】ウィルス感染、特に HIV−1、肝炎B型ウィルス、及びヘルペスウィルスを治療する方法の提供。
【解決手段】治療の必要な患者に、感染と戦う量のリン脂質又はリン脂質誘導体を投与することを含む方法。
(もっと読む)
抗ウイルス4′−置換プロヌクレオチドホスホルアミダート
本発明は、C型肝炎ウイルス(HCV)が媒介する疾患の治療に有用である、式Iの新規ヌクレオシド化合物を提供するもので、式中、R1、R2a、R2b、R3、R4、R5、R6、R8a、R9、およびR10は本明細書に定義する通りである。本発明はさらに、式Iの化合物、およびこれら化合物を含む医薬組成物によって、HCVが媒介する疾患を治療しまたは予防するための方法を提供する。 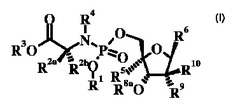 (もっと読む)
(もっと読む)
塩基部無保護ホスホロアミダイト化合物の製造方法
【課題】 水酸基選択的な反応等の複雑な反応を必要としない簡素な方法により、塩基部無保護ホスホロアミダイト化合物を製造する方法を得る。
【解決手段】 塩基部保護ホスホロアミダイト化合物の塩基部を、アンモニア/メタノール溶液またはメチルアミン/THF溶液を用いて脱保護する。塩基部保護ホスホロアミダイト化合物としては、ヌクレオシドの塩基部を保護した後に5’−OH基を保護し、さらに3’−OH基をホスホロアミダイト化したものが好ましい。本発明によれば、水酸基選択的な反応等の複雑な反応を必要としない簡素な方法により、塩基部無保護ホスホロアミダイト化合物を製造する方法を得ることができ、塩基部無保護ホスホロアミダイト化合物を大量に生産できる。
(もっと読む)
ヌクレオチド誘導体及びその利用
【課題】塩基特異的なシグナル変化を利用するヌクレオチド配列における塩基種の特定に際して、識別性の高い蛍光発光特性を備えるヌクレオチド誘導体を提供する。
【解決手段】以下の一般式(2)で表されるヌクレオチド誘導体等を用いる。
(Aはアントラセン化合物,R1〜R9はH又は置換基,R10はH又はOH,Aはエステル,アミド等の連結基,Yはメチレン基,エチレン基等,mは1〜3の整数,n1〜3は5以下の整数を表す。)
(もっと読む)
抗ウイルスヌクレオシド類似体およびウイルス感染特にHIV感染の処置方法
この発明は一般的構造式(I、II、III、IVまたはV)の新規な化合物に関するものであり、ここでBは構造式(VI)のヌクレオシド塩基であり、RはH、F、Cl、Br、I、C1−C4アルキル(好ましくはCH3)、−C≡N、−C≡C−Ra、構造式(VII)であり、XはH、C1−C4アルキル(好ましくはCH3)、F、Cl、BrまたはIであり、化合物が構造式IIであるときにZがCH2でありOではないとの条件付きでZはOまたはCH2であり、R3は−C≡C−Hであり、R2はHまたはリン酸、二リン酸、三リン酸またはホスホトリエステル基であり、R1はH、アシル基、C1−C20アルキルまたはエーテル基であり、R2はH、アシル基、CI−C20アルキルまたはエーテル基、リン酸、二リン酸、三リン酸、ホスホジエステル基または構造式(VIII)または構造式(IX)基であり、生物学的に活性な抗ウイルス化合物からのアミノ基またはヒドロキシル基がリン酸、ホスホラミデート、炭酸塩または隣接部分を具えたウレタン基を形成するようにNuは生物学的に活性な抗ウイルス化合物の遊離基であり、R8はHまたはC1−C20アルキルまたはエーテル基、好ましくはC1−C12アルキル基であり、kは0−12、好ましくは0−2であり、R3はC1−C4アルキル(好ましくはCH3)、−(CH2)n−C≡C−Ra、構造式(X)または(XI)から選ばれ、R3aとR3bとは独立にH、F、Cl、BrまたはIから選ばれ、R4とR5がともにHではないという条件付きでR4とR5は独立にH、F、Cl、Br、I、OH、C1−C4アルキル(好ましくはCH3)、−(CH2)n−C≡C−Ra、構造式(XII)または(XIII)から選ばれ、RaはH、F、Cl、Br、Iまたは−C1−C4アルキル、好ましくはHまたはCH3であり、YはH、F、Cl、Br、IまたはC1−C4アルキル、好ましくはHまたはCH3であり、nは0,1,2,3,4、または5、好ましくは0,1または2であり、かつこれらのアノマー、薬学的に受容可能な塩、溶媒和物またはそれらの多形体である。
 (もっと読む)
(もっと読む)
LFMAUおよびLDTを用いる癌および他の症状または病状の処置方法
本発明は、腫瘍、癌および過剰増殖性疾患、取分けその症状または病状を処置するための、以下の式(I)で示される化合物および医薬的に許容されるその塩の使用に関する[式中、XはHまたはFである;R1およびR2は独立してH、アシル基、C1−C20アルキルもしくはエーテル基、リン酸、二リン酸、三リン酸もしくはホスホジエステル基、基(A)または(B)(式中、Nuは抗癌性、抗ウイルス性または抗過剰増殖性化合物などの生物学的に活性な化合物の遊離基であって、当該生物学的に活性な化合物からのアミノ基またはヒドロキシル基が隣接部位とホスフェート、ホスホルアミデート、カーボネートまたはウレタン基を形成するような基である;各R8は独立してH、またはC1−C20アルキルもしくはエーテル基、好ましくはC1−C12アルキル基である;kは0〜12、好ましくは0〜2である)で示される基である]。  (もっと読む)
(もっと読む)
堅いリンカーを有するヌクレオチド化合物
【課題】プライマー伸長反応において、非標識の伸長可能なヌクレオチドに対して大過剰を必要とせず、そしてSanger型配列決定反応において、均一なピーク高さ分布を生成する標識ヌクレオチドターミネーター化合物の提供。
【解決手段】以下の構造:NUC−L−S−LB/LGを有するヌクレオシド/ヌクレオチド化合物であって、ここで:NUCは、核酸塩基部分Bを有するヌクレオシド/ヌクレオチドであり;Lは、堅い結合であり;Sは、スペーサーであり;LB/LGは、結合対または標識のメンバーであり;ここで、NUCは、Bを介してLに付加され、その結果、Bがプリンである場合、Lはプリンの8位に付加され、Bが7−デアザプリンである場合、Lは7−デアザプリンの7位に付加され、そしてBがピリミジンである場合、Lはピリミジンの5位に付加される、ヌクレオシド/ヌクレオチド化合物。
(もっと読む)
スルフリルフルオリドを用いるフッ素化反応
【課題】大量規模での製造に適したフッ素化反応を提供する。
【解決手段】ヒドロキシ誘導体を有機塩基の存在下に、または有機塩基と「有機塩基とフッ化水素からなる塩または錯体」の存在下にスルフリルフルオリド(SO2F2)と反応させることによりフルオロ誘導体が製造できることを見出した。本製造方法は、工業的な使用が好ましくないパーフルオロアルカンスルホニルフルオリドを用いる必要がなく、医農薬および光学材料の重要中間体である光学活性フルオロ誘導体、具体的には4−フルオロプロリン誘導体、2'−デオキシ−2'−フルオロウリジン誘導体および光学活性α−フルオロカルボン酸エステル誘導体等を大量規模でも有利に製造できる。
(もっと読む)
トリチル型化合物
【課題】 同一分子内に存在する二つの水酸基を同時に保護でき、なおかつ適切な条件で処理することで一方の水酸基のみを選択的に脱保護可能な保護基を提供する。
【解決手段】 一般式(I):
【化1】
〔式中、X1、X2、X3、X4、X5、Y1、Y2、Y3、Y4、Y5、Z1、Z2、Z3、Z4、及びZ5は水素原子などを表し、R1は塩素原子などを表し、R2は保護基を有していてもよい水酸基を表す。〕
などで表される化合物。
(もっと読む)
ゲムシタビン誘導体の経口投薬形態
本発明は、2’,2’−ジフルオロデオキシシチジン(ゲムシタビン)のある特定の長鎖飽和脂肪酸誘導体及び長鎖モノ不飽和脂肪酸誘導体の経口投薬形態に関する。特に、本発明は、癌の治療コンプライアンスを改善させる経口投薬形態を製造するための上記ゲムシタビン誘導体又はそれらの医薬的に許容可能な塩の使用に関する。  (もっと読む)
(もっと読む)
ヌクレオシド誘導体、ヌクレオチド誘導体及びそれらの製造方法
【課題】立体構造が制御されたヌクレオシド誘導体及びヌクレオチド誘導体の提供。
【解決手段】
不斉リン原子に由来する立体配置が制御された下記各一般式に示されるヌクレオシド誘導体及びヌクレオチド誘導体。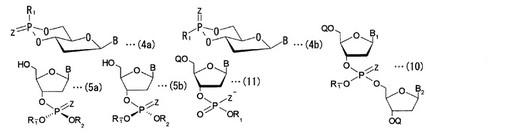
(式中、B、B1及びB2は水素、OH基、核酸塩基又はその誘導体から選択され;ZはS又はSeであり;R1及びR2は互いに異なる一部水素が置換されていても良い炭化水素基から選択される;QはOH基の保護基である。)
(もっと読む)
ゲムシタビン誘導体ナノ粒子
本発明は、一般式(I)の2',2'-ジフルオロ-2'-デオキシシチジン誘導体であって、式中、R1、R2、およびR3が、同一または異なっており、互いに独立に、水素原子、または少なくともC18の炭化水素アシル基を表し、かつ、極性溶媒媒質中において前記一般式(I)の化合物にコンパクト化された形態をもたらすことが可能である立体配座のものであり、基R1、R2、およびR3の少なくとも1つが、水素原子以外のものである誘導体に関する。 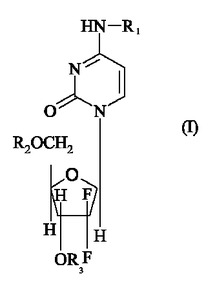 (もっと読む)
(もっと読む)
チオヌクレオシド−S−ニトロシル誘導体
本発明は、次式I:
〔式中、R1はリボース、2−デオキシリボース又はこれらの誘導体を表し、R2は水素原子、アミノ基、ヒドロキシル基、ハロゲン原子、R3−オキシ基又はR3−アミノ基(R3は、置換されてもよい炭素数1〜15のアルキル基又は置換されてもよい炭素数1〜15のアシル基を表す。)を表す。〕
で示されるチオヌクレオシド−S−ニトロシル誘導体又はその塩を提供する。  (もっと読む)
(もっと読む)
耐性HBV菌株の治療のためのβ−L−2’−デオキシヌクレオシド及び併用療法
β−L−2’−デオキシヌクレオシドは、突然変異を有する薬剤耐性B型肝炎ウイルスに対して活性であることが発見された。β−L−2’−デオキシヌクレオシド又は医薬適合性のその塩、エステルもしくはプロドラッグを投与することを含む、宿主においてラミブジン耐性HBV(M552V)を治療するための方法を提供する。さらに、β−L−2’−デオキシヌクレオシド又は医薬適合性のその塩、エステルもしくはプロドラッグを投与することを含む、ナイーブ宿主においてラミブジン耐性HBV(M552V)突然変異が起こることを予防するための方法を提供する。(3−L−2’−デオキシヌクレオシド又は医薬適合性のその塩、エステルもしくはプロドラッグを投与することを含む、宿主においてHBV二重突然変異株(L528M/M552V)の出現を予防する及び/又は抑制するための方法も提供する。 (もっと読む)
可逆的ヌクレオチドターミネーターおよびその使用
本発明は、1つ以上のDNA配列決定技術に有用であるヌクレオチドアナログを提供する。1つの態様によれば、本発明は、ヌクレオチドアナログが、成長する核酸鎖、例えば、DNA鎖に取り込まれた後に、ヌクレオチドアナログを検出することによって核酸の配列を決定するための方法を提供する。キットであって、(a)本発明の式I、II、IIIまたはIVの個別のヌクレオチドアナログ;および(b)DNAポリメラーゼ、(c)反応緩衝液、(d)天然2’デオキシヌクレオシド三リン酸および必要であれば、(e)切断試薬を備える、キットもまた提供される。 (もっと読む)
プロダン含有ヌクレオチド及びその利用
【課題】簡便かつ正確に核酸塩基を同定できるポリヌクレオチド誘導体を提供する。
【解決手段】式(1)で表される化合物を塩基とするヌクレオチド誘導体を含むポリヌクレオチド誘導体。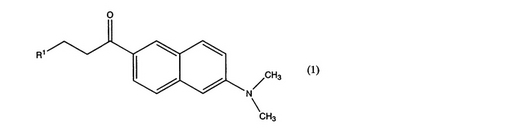
(式中、R1は、置換ピリミジン環又は置換プリン環を示す。)
(もっと読む)
アルコール溶媒中での有機フルオロ化合物の調製方法
本発明は、放射性同位元素フッ素18を含んだ有機フルオロ化合物の調製方法に関するもので、より詳細には、放射性同位元素フッ素18を含んだフッ素塩とアルキルハライドまたはアルキルスルホナートとを反応させて有機フルオロ化合物を調製する方法において、下記の化学式1で表わされるアルコールを溶媒に使用することによって、有機フルオロ化合物を高収率で調製する有機フルオロ化合物の調製方法に関するものであり、本発明による合成は、穏和な反応条件下で行うことができ、反応時間を短縮させるだけではなくその収率を顕著に向上させることにより、有機フルオロ化合物の大量生成に好適である。 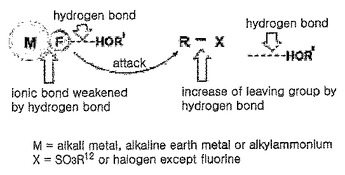 (もっと読む)
(もっと読む)
シチジンアナログ及びシチジン誘導体の医薬配合物
本発明は、5-アザシチジン、5-アザ-2'-デオキシ-2',2'-ジフルオロシチジン、5-アザ-2'-デオキシ-2'-フルオロシチジン、2'-デオキシ-2',2'-ジフルオロシチジン、及び、シトシン1-β-D-アラビノフラノシドのようなシチジンアナログ、並びに、シチジン誘導体の医薬配合物と共に、当該配合物の製造方法を提供する。とりわけ、当該シチジンアナログ、又は、シチジン誘導体は、安定化するため、及び/又は、当該薬剤の溶解性を高めるために、シクロデキストリン化合物と共に処方される。当該医薬配合物の使用のためのキット、及び、方法もまた提供され、これには、癌、及び、血液疾患のような、状態、又は、疾患の治療をするための当該シチジンアナログ、又は、シチジン誘導体の投与方法が含まれる。 (もっと読む)
N4−アセチル−2’−デオキシ−2’−フルオロ−シチジン誘導体の製造法
【課題】高純度なN4−アセチル−2’−デオキシ−2’−フルオロ−シチジン誘導体の製造法を提供すること
【解決手段】一般式(1)
(式中、R1は水素、炭素数1〜4のアルキル基、炭素数2〜4のアルケニル基、炭素数2〜4のアルキニル基、炭素数1〜4のペルフルオロアルキル基、またはハロゲン原子を表す。)で表される化合物に、包接用溶媒Qを含む溶媒中で該包接用溶媒を包接させる、一般式(2)
(式中、R1は前記の通りであり、m及びnはそれぞれ1〜100の整数であり、Qはエーテル系化合物、ケトン系化合物、またはエステル系化合物を表す。)で表される包接化合物の結晶の製造法。
(もっと読む)
61 - 80 / 95
[ Back to top ]

