国際特許分類[C07D209/34]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | 複素環式化合物 (108,186) | 異項原子として1個の窒素原子のみを含有し,他の環と縮合している5員環からなる複素環式化合物 (3,383) | 1個の炭素環と縮合しているもの (2,455) | インドール;水素添加したインドール (1,835) | 異種原子,または異種原子に対する3個の結合をもち,そのうち多くても1個がハロゲンに対する結合である炭素原子が複素環の炭素原子に直接結合したもの (558) | 酸素原子 (168) | 2位において (117)
国際特許分類[C07D209/34]に分類される特許
71 - 80 / 117
ジプラシドンを用いて認知を増強する方法
本発明は、一態様においては、例えば精神病、自閉症、痴呆または精神発達遅滞等に悩むヒトを含む哺乳動物における認知を増強するために、明細書中の定義に従う式(I)のピペラジニル−複素環化合物を使用する方法であって、当該哺乳動物に対し式(I)の化合物(例えば、ジプラシドン)の有効量を投与することを含む方法に関する。別の態様においては、本発明は、自閉症、精神発達遅滞、強迫性障害、および痴呆から選択される障害または状態に悩むヒトを含む哺乳動物において、当該哺乳動物に対し式(I)の化合物(例えば、ジプラシドン)の有効量を投与することを含む、前記障害または状態に随伴する陽性症状(例:過剰な攻撃性、性行動の脱抑制、不適切な性行動、激越の他、例えば頭部強打、咬唇癖、自傷、常同行為などの強迫性行動)を軽減または改善する方法を指向する。別の態様においては、本発明は、哺乳動物に対し式(I)の化合物(例えば、ジプラシドン)の有効量を投与することを含む、ヒトを含む哺乳動物における小児双極性障害を治療する方法を指向する。式(I)の化合物という化合物類は、明細書中に定義される。あるいは式中Ar、n、X、およびYが明細書中の定義に従う、その薬学的に許容できる酸付加塩である。 (もっと読む)
(もっと読む)
VR1アンタゴニストとしての置換アリールオキシ−N−ビシクロメチルアセトアミド化合物
本発明は式(I)の化合物または薬学的に許容できるその塩を提供する[式中、
【化1】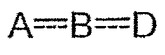
は、NR10−C(O)−NR9、S−C(O)−NR9、NR9−C(O)−S、NR9−C(O)−O、CR10−C(O)−NR9、O−C(O)−NR9、NR10−C(O)−CR9、NR10−NR9−C(O)、C(O)−NR9−NR10、NR10−N=CR9、N=N−CR9、NR10−CR9=N、N=CR9−NR10、NR10−N=N、N=N−NR10、S−CR9=NまたはN=CR9−Sを表し、X1は、CR1またはNを表し、X2およびX3はそれぞれ独立に、CR8またはNを表し、R1、R6、R8、R9およびR10はそれぞれ独立に、水素、ハロゲン、ヒドロキシ、(C1〜C6)アルキル、(C1〜C6)アルコキシ、ヒドロキシ(C1〜C6)アルコキシ、(C1〜C6)アルコキシ−(C1〜C6)アルキル、(C1〜C6)アルコキシ−(C1〜C6)アルコキシ、ハロ(C1〜C6)アルキル、(C1〜C6)アルキルチオ、(C1〜C6)アルキルスルフィニルまたは(C1〜C6)アルキルスルホニルを表し、R2、R3、R4およびR5はそれぞれ独立に、水素、(C1〜C6)アルキル、ハロゲン、ハロ(C1〜C6)アルキルまたはヒドロキシ(C1〜C6)アルキルを表し、R7は、ハロゲン、(C1〜C6)アルキル、ハロ(C1〜C6)アルキル、(C1〜C6)アルコキシ、ヒドロキシ(C1〜C6)アルコキシ、(C1〜C6)アルコキシ−(C1〜C6)アルキル、(C1〜C6)アルコキシ−(C1〜C6)アルコキシ、[(C1〜C6)アルキル]NH−または[(C1〜C6)アルキル]2N−を表すが、ただし、(i)
【化2】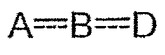
がNR10−N=NまたはN=N−NR10を表す場合、R2は(C1〜C6)アルキル、ハロゲン、ハロ(C1〜C6)アルキルまたはヒドロキシ(C1〜C6)アルキルを表すか、または(ii)
【化3】
がNR10−N=NまたはN=N−NR10を表し、R2が(C1〜C6)アルキルを表す場合、R7は、ハロゲン、(C1〜C6)アルキル、(C1〜C6)アルコキシ、ヒドロキシ(C1〜C6)アルコキシ、(C1〜C6)アルコキシ−(C1〜C6)アルキル、(C1〜C6)アルコキシ(C1〜C6)アルコキシ、[(C1〜C6)アルキル]NH−または[(C1〜C6)アルキル]2N−を表す]。これらの化合物は、哺乳動物における疼痛などのVR1受容体の過活性により誘発される疾患状態を治療するために有用である。さらに本発明は、前記化合物を含む医薬組成物を提供する。
【化4】
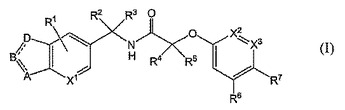 (もっと読む)
(もっと読む)
インドール誘導体の製造方法
式(I)の4−[2−(ジ−n−プロピルアミノ)エチル]−2,3−ジヒドロ−1H−インドール−2−オン、その医薬的に許容される塩、および溶媒和物、並びに式(A)および(B)の化合物の新規な中間体[式中、Rは(i)フッ素、塩素原子、臭素原子およびヨウ素原子から選択されるハロゲン原子;(ii)メタンスルホニルオキシ、エタンスルホニルオキシ、イソプロパンスルホニルオキシ、プロパンスルホニルオキシ、ブタンスルホニルオキシ、tert−ブタンスルホニルオキシ、ペンタンスルホニルオキシ、ヘキサンスルホニルオキシから選択される低級アルカンスルホニルオキシ基;(iii)フェニルスルホニルオキシ、4−メチルフェニルスルホニルオキシ、2−メチルフェニルスルホニルオキシ、4−ニトロフェニルスルホニルオキシ、4−メトキシフェニルスルホニルオキシ、3−クロロフェニルスルホニルオキシから選択される置換または無置換アリールスルホニルオキシ基;(iv)ベンジルスルホニルオキシ、2−フェニルエチルスルホニルオキシ、4−フェニルブチルスルホニルオキシ、4−メチルベンジルスルホニルオキシ、2−メチルベンジルスルホニルオキシ、4−ニトロベンジルスルホニルオキシ、4−メトキシベンジルスルホニルオキシ、3−クロロベンジルスルホニルオキシから選択されるアリールアルキルスルホニルオキシ基を表す]の製造方法。
 (もっと読む)
(もっと読む)
3,3−二置換オキシインドールおよびチオ−オキシインドールを調製する方法
オキシインドールおよびチオ−オキシインドール化合物を調製する方法が提供され、こうした化合物は、有用な医薬品の前駆体として有用である。具体的には、5−ピロール−3,3−オキシインドール化合物および5−(7−フルオロ−3,3−ジメチル−2−オキソ−2,3−ジヒドロ−1H−インドール−5−イル)−1−メチル−1H−ピロール−2−カルボニトリルを調製する方法が提供される。また、イミノベンゾ[b]チオフェンおよびベンゾ[b]チオフェノン化合物を調製する方法も提供される。 (もっと読む)
炎症性疾患の治療用の新規化合物
本発明は式1
【化1】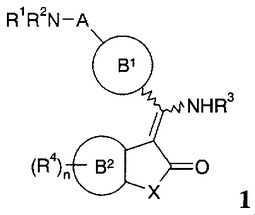
の新規化合物、これらのヘテロ誘導体、及びこれらの薬理学上適合性の塩、ジアステレオマー、鏡像体、ラセミ体、水和物又は溶媒和物(これらは呼吸器又は胃腸の病気又は疾患、関節、皮膚又は眼の炎症性疾患、末梢神経系もしくは中枢神経系に関する疾患、又は癌疾患を治療するのに適している)に関する。また、本発明は前記化合物を含む医薬組成物に関する。 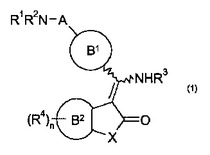 (もっと読む)
(もっと読む)
光学活性塩素化合物の製造方法
【課題】光学純度が高い光学括性α-塩素化合物を製造する方法を提供する。
【解決手段】一般式(1)
R1-Xn-CO-CHR2W(式中Rl及びR2は,鎖状または環状の炭化水素基などを表し,Xはアルキレン基などを示し,Wは電子吸引基を示す。nは0または1を示す。)で表される化合物を,一般式(2)MLrAsDc(式中,Lは不斉配位子を示し,Mは遷移金属を示し,Aは水または中性配位子を示し,Dはアニオン性配位子または対アニオンを示し,rは1または2,Sは0,1,2,4,または6,Cは0,1,または2である。)で表される不斉遷移金属錯体触媒の存在下に一般式(3)RfSO2Cl(式中Rfはペルフルオロアルキル基を示す)で表されるペルフルオロアルキルスルホニルクロリド類を反応させ、一般式(4)R1-Xn-CO-C*ClR2W(式中R1,R2,Wは前記定義と同じ,C*は不斉炭素)で表される光学活性塩素化合物誘導体を製造する。
(もっと読む)
置換オキシインドール誘導体、前記誘導体を含む医薬およびそれの使用
本発明は、一般式(I)
(式中、置換基R1、R2、A、BおよびYは請求項1で定義のものなどである)の新規なオキシインドール誘導体に関するものである。その薬剤を含む医薬およびバソプレッシン依存性および/またはオキシトシン依存性疾患の予防および/または治療のためのそれの使用も開示されている。  (もっと読む)
(もっと読む)
5−HT2C受容体活性を有する化合物およびその使用
本発明は、式(I):
の化合物およびその製薬上許容される塩に関する。
[式中、R1は、ハロゲン、シアノ、C1-6アルキル、C3-7シクロアルキル、C3-7シクロアルキルオキシ、C1-6アルコキシ、C1-6アルキルチオ、ヒドロキシ、アミノ、モノ-もしくはジ-C1-6アルキルアミノ、N結合4〜7員ヘテロ環式基、ニトロ、ハロC1-6アルキル、ハロC1-6アルコキシ、アリール、-COOR3、-COR4(ここでR3およびR4は独立して、水素またはC1-6アルキルである)、または-COR5(ここでR5は、アミノ、モノ-もしくはジ-C1-6アルキルアミノまたはN結合4〜7員ヘテロ環式基である)であり; pは、0、1、2または3であり; Qは、6員の芳香族基または6員の複素環式芳香族基であり; Aは、-(CH2-CH2)-、-(CH=CH)-、または基-(CHR7)-(ここでR7は、水素、ハロゲン、ヒドロキシ、シアノ、ニトロ、C1-6アルキル、C3-7シクロアルキル、C3-7シクロアルキルオキシ、ハロC1-6アルキル、C1-6アルコキシ、ハロC1-6アルコキシまたはC1-6アルキルチオである)であり; R2は、水素、ハロゲン、ヒドロキシ、シアノ、ニトロ、C1-6アルキル、C1-6アルカノイル、C3-7シクロアルキル、C3-7シクロアルキルオキシ、ハロC1-6アルキル、C1-6アルコキシ、ハロC1-6アルコキシ、C1-6アルキルチオ、アミノ、モノ-もしくはジ-C1-6アルキルアミノまたはN結合4〜7員ヘテロ環式基であり; Xは、酸素、硫黄、-CH2-またはNR8(ここでR8は、水素またはC1-6アルキルである)であり; Yは、単結合、-CH2-、-(CH2)2-または-CH=CH-であり; Zは、場合によっては置換されていてもよいN結合ヘテロ環式基またはC結合4〜7員ヘテロ環式基(少なくとも1個の窒素含有)、または-NR9R10(ここで、R9およびR10は独立して、水素またはC1-6アルキル)である。]本発明はまた、当該化合物およびその製薬上許容される塩の製造方法、鬱病または不安などの治療におけるそれらの使用に関する。  (もっと読む)
(もっと読む)
6,7,8,9−テトラヒドロ−5−アミノ−5H−ベンゾシクロヘプテン−6−オール誘導体類及び抗炎症剤として使用される関連する化合物類
本発明は、下記式I:[式中、R3は、1〜3個のヒドロキシ基、ハロゲン原子、又は1〜3個の(C1-C5)-アルコキシ基から選択された基により任意に置換さえ得るC1-C10-アルキル基、任意に置換された(C3-C7)−シクロアルキル基、任意に置換されたヘテロシクリル基、任意に置換されたアリール基、又は他の置換基を表し、Aは、-CR6R7-CH2-基又は-CH2-CR6R7-基を表し、Dは、-CR4R5-CH2-基又は-CH2-CR4R5-基を表し、R4は、ヒドロキシ基、OR10基又はO(CO)R10基を表し、R5は、(C1-C5)-アルキル基又は任意には部分的に又は完全に弗素化された(C1-C5)-アルキル基、(C3-C7)シクロアルキル基、(C1-C8)アルキレン(C3-C7)シクロアルキル基、(C2-C8)アルキレン(C3-C7)シクロアルキル基、ヘテロシクリル基、(C1-C8)アルキレンへテロシクリル基、(C2-C8)アルケニレンヘテロシクリル基、アリール基、(C1-C8)アルキレンアリール基、(C2-C8)アルケニレンアリール基、(C2-C8)アルキニレンアリール基、又は他の置換基を表す]で表される、多置換された5Hベンゾシクロヘプテン誘導体に関する。前記他の置換基は請求項に特定される。本発明はまた、前記誘導体の生成方法、及び抗炎症剤へのそれらの使用にも関する。
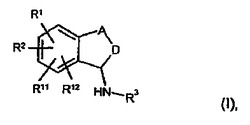 (もっと読む)
(もっと読む)
2−オキシインドール類の製造方法
【課題】 イサチン類を原料とし、中間体であるヒドラゾン体を経由して2−オキシインドール類を製造する方法において、ヒドラゾン体の分離、精製の必要がなく、温和な温度域で2−オキシインドール類を収率よく得る方法を提供する。
【解決手段】 置換または非置換のイサチンを、芳香族炭化水素又はハロゲン化芳香族炭化水素からなる溶媒中でヒドラジンと反応させて得られる反応混合物を共沸脱水し、次いでアルカリ金属アルコキシドのような強塩基を加えて反応させ、2−オキシインドール類を製造する。
(もっと読む)
71 - 80 / 117
[ Back to top ]

