国際特許分類[C07H1/00]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | 糖類;その誘導体;ヌクレオシド;ヌクレオチド;核酸 (3,852) | 糖誘導体の製造方法 (142)
国際特許分類[C07H1/00]の下位に属する分類
国際特許分類[C07H1/00]に分類される特許
61 - 66 / 66
3−フルオロ−2,3−ジデオキシ−β−D−リボフラノシル型ヌクレオシド誘導体の製造方法
【課題】3−フルオロ−2,3−ジデオキシ−β−D−リボフラノシル型ヌクレオシド誘導体、特に3’−フルオロ−2’,3’−ジデオキシグアノシンを工業的に低コストで製造することができる方法を提供する。
【解決手段】3−ハロゲノ−3−デオキシ−β−D−キシロフラノシル型ヌクレオシド誘導体をサルファーテトラフルオリド(SF4)と反応させることにより、高い位置選択性で2−ハロゲノ−2,3−ジデオキシ−3−フルオロ−β−D−アラビノフラノシル型ヌクレオシド誘導体に変換し、引き続いて(1)2'位ハロゲン原子を脱ハロゲン化する工程、(2)5'位水酸基の保護基を脱保護する工程、および、必要に応じて(3)核酸塩基またはその誘導体の保護、脱保護または修飾の内、少なくとも何れか一つを行う工程を順不同に行うことにより、3−フルオロ−2,3−ジデオキシ−β−D−リボフラノシル型ヌクレオシド誘導体を製造する。
(もっと読む)
粘膜送達のための方法および製品
本発明は、多糖類製剤の非侵襲性送達に関連した方法および製品を特徴とする。 (もっと読む)
9−β−アノマー性ヌクレオシド類似体の調製方法
9−β−アノマー性ヌクレオシド類似体の位置選択的及び立体選択的合成を十分に増進させるための方法を説明する。6−置換プリン塩基への糖部分の導入は、9−β−D−又はL−プリンヌクレオシド類似体のみが得られるように実施された。糖部分のこの位置選択的及び立体選択的導入により、実質上7位―位置異性体の形成なしに高収率でヌクレオシド類似体、特に2’−デオキシ、3’−デオキシ、2’−デオキシ2’−β−フルオロ及び2’,3’−ジデオキシ−2’−β−フルオロプリンヌクレオシド類似体を合成できるようになる。該化合物は薬剤又は薬剤に対する中間体である。 (もっと読む)
2−デヒドロ−3−デオキシ−D−グルコネートからの2’−デオキシヌクレオシド及び2’−デオキシヌクレオシド前駆体の製造
この発明は、2’−デオキシヌクレオシド化合物又は2’−デオキシヌクレオシド前駆体を、2−デヒドロ−3−デオキシ−D−グルコン酸(通常、KDGと略記)又はその塩を出発物質として利用して製造する方法に関係する。様々な2’−デオキシヌクレオシド及びそれらの類似体が、抗ウイルス剤、抗癌剤又はアンチセンス剤の製造における合成又は薬物配合のための出発物質として用いられる。 (もっと読む)
二糖モノマー及びそのオリゴマーとオリゴマーの製造方法
【目的】 分子内にN−アセチルグルコサミンユニットを有し、キチンおよびその加水分解物と同様の特性を備えるオリゴマー及びその製造方法並びにその原料として有用な2糖モノマーを提供する。
【構成】 二糖モノマーであるフッ化4−O−(2−アセトアミド−2−デオキシ−β−D−グルコピラノシル)−β−D−グルコピラノシルを開発した。該二糖モノマーにアセトニトリルと緩衝液との混合液中でセルラーゼを作用させることによってオリゴマーを得る。
(もっと読む)
エスクレチン誘導体、その製造方法及びマトリックスメタロプロテアーゼ阻害剤
【目的】 エスクレチン誘導体、その製造方法及びマトリックスメタロプロテアーゼ阻害剤を提供する。
【構成】 エスクレチン誘導体は下記一般式(I)で表される。
【化1】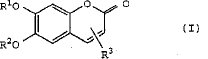
R1 及びR2 は−CON(R4 )R5 、単糖類残基、アシル化単糖類残基;R1又はR2 の少なくとも1方は−CON(R4 )R5 ;R4 及びR5 はH、OH、アルキル、アリール若しくはアラルキル、又はR4 とR5 とは3〜7員の飽和脂肪族環状アミノ基を形成でき;R3 は−COOR8 、H、OH、アルキル、アリール又はアラルキル;R3 は3位又は4位;R8 はH又はアルキル。
(もっと読む)
61 - 66 / 66
[ Back to top ]



