国際特許分類[C07K1/20]の内容
化学;冶金 (1,075,549) | 有機化学 (230,229) | ペプチド (29,849) | ペプチドの製造のための一般方法 (1,853) | 抽出;分離;精製 (1,152) | クロマトグラフィーによるもの (651) | 分配,逆相または疎水性相互作用クロマトグラフィー (78)
国際特許分類[C07K1/20]に分類される特許
31 - 40 / 78
単一ドメイン抗原結合分子の精製方法
プロテインAに基づくアフィニティークロマトグラフィーを用いた、相補的抗体ドメインと免疫グロブリン定常領域を実質的に欠く1つまたは複数の単一結合ドメイン(たとえば1つまたは複数のナノボディ分子)とが含まれる単一ドメイン抗原結合(SDAB)分子を精製または分離するプロセスおよび方法を開示する。 (もっと読む)
IL−18に結合する抗体およびそれを精製する方法
本明細書において、抗IL−18抗体が開示され、これは、この抗原結合部分を包含する。試料母体から抗IL−18抗体を単離および精製するための1つ以上の方法が示される。これらの単離された抗IL−18抗体は、臨床現場および研究開発に使用することができる。単離された抗IL−18抗体を含む医薬組成物も記載される。 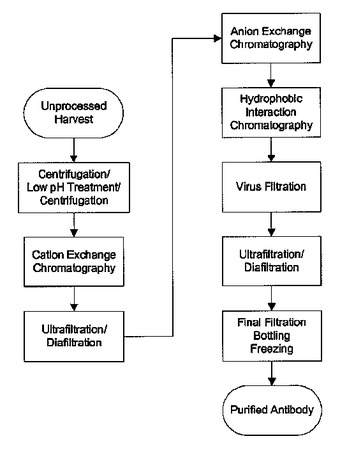 (もっと読む)
(もっと読む)
抗体精製中におけるウイルスの不活性化
本明細書において、試料マトリックスから抗体を単離および精製する方法が記載される。本開示の1つの態様は、抗体精製の様々なステップにおいて生み出される試料のウイルス減少/不活性化に関する。1つの具体的な態様では、本明細書の方法は酸性化ステップとこれに続く1つまたは複数のクロマトグラフィーステップを採用する。当該クロマトグラフィーステップは、1つまたは複数の下記クロマトグラフィー手順を含み得る:イオン交換クロマトグラフィー、アフィニティークロマトグラフィーおよび疎水性相互作用クロマトグラフィー。  (もっと読む)
(もっと読む)
クロストリジウムヒストリチカム液体培養物由来のコラゲナーゼの改良された精製
【課題】クロストリジウム・ヒストリチカムコラゲナーゼI型およびII型タンパク質を、複合混合物から精製するための方法を提供する。
【解決手段】硫酸アンモニウムによる沈殿、疎水性相互作用クロマトグラフィー、陽イオン交換クロマトグラフィー、および陰イオンクロマトグラフィーを行うことにより精製する方法、安定化された部分精製調製物、なおかつ沈殿工程を導く条件。調製物は、格別に純粋で完全な酵素的に活性であるコラゲナーゼI型およびII型タンパク質であり、また、2つの単離されたタンパク質のブレンド。さらに、インビトロにおける組織試料を処理するための精製されたコラゲナーゼタンパク質またはそれらのブレンドの使用。
(もっと読む)
精製免疫グロブリン融合タンパク質およびその精製方法
本発明は、免疫グロブリン(Ig)融合タンパク質の製造中に不純物を分離するための方法および組成物を提供する。本発明の方法に従って除去され得る不純物の例としては、不活性形態のIg融合タンパク質および/または凝集体が挙げられる。本発明はまた、抗体ベースの生物製剤、すなわち、免疫グロブリン(Ig)融合タンパク質の精製中に、複数の生成物関連の不純物を除去することが可能な高分解能の疎水性相互作用クロマトグラフィー(HIC)工程を提供する。 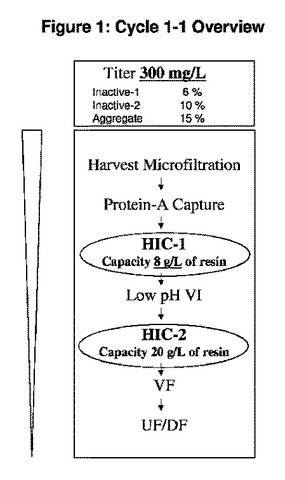 (もっと読む)
(もっと読む)
Fc融合タンパク質を精製する方法
本発明は、青色色素アフィニティ・クロマトグラフィを介してFc融合タンパク質を精製する方法、具体的には、Fc融合タンパク質製剤中の遊離Fc部分の量を低減する方法に関する。 (もっと読む)
ニューロトロフィンの精製
【課題】治療用途に適した、成熟NGFを含むニューロトロフィンの大規模な精製方法が提供される。
【解決手段】ニューロトロフィンを、様々なあまり望ましくない誤って加工され、誤って折り畳まれた、サイズ、グリコシル化もしくは荷電型から、逆相液体クロマトグラフィー、カチオン交換クロマトグラフィーカラム等によって分離する手段を使用する。また、これらの変種が実質的に含まれない成熟NGFを含むニューロトロフィンの組成物も製造することができる。
(もっと読む)
α−1−抗トリプシンおよびアポリポタンパク質A−Iを精製する方法
本発明は、例えばヒト血漿画分からの、α−1−抗トリプシン(AAT、またα−1プロテイナーゼ阻害剤、APIおよびA1−PIとしても知られている)およびアポリポタンパク質A−I(ApoA−I)の双方のタンパク質の分離方法および精製方法に関する。特定の実施態様では、本発明は、双方のタンパク質の原料として同一の出発原料が使用できるように、精製の初期段階でApoA−IからAATを分離する方法を提供する。本方法は、医薬用途に適するAATおよびApoA−Iの組成物の提供にさらに関連し、大規模精製に適する。 (もっと読む)
トランスジェニック哺乳動物の乳中に外因性タンパク質を産生させるための方法
本発明は、哺乳動物に対して毒性であり得る目的のタンパク質の産生に有用な、非ヒトトランスジェニック哺乳動物に関連する。この哺乳動物は、目的のタンパク質、好ましくは組換えヒトインスリンの不活性形態の乳中における産生に関してトランスジェニックであるという事実によって特徴付けられる。組換えヒトインスリンは哺乳動物においてある程度の生物学的活性を有し、そして哺乳動物に対して毒性であり得るので、この分子をトランスジェニック哺乳動物において産生することは不可能である。従って、本発明は、発現ベクターにおいてβカゼインプロモーターのコントロール下にある、修飾ヒトインスリン前駆体をコードする配列を含む遺伝的構築物をクローニングすることを含む。また、発現プラスミドを、線維芽細胞のような、胎仔ウシ体細胞にトランスフェクトすること、および核移植によってウシ卵母細胞を除核してトランスジェニック胚を産生することを含む。 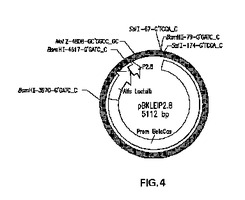 (もっと読む)
(もっと読む)
ポリペプチドコンジュゲートの精製方法
本発明は、ポリペプチドコンジュゲートを製造するための方法を提供する。特に本発明は、ポリ(アルキレンオキシド)部分などの少なくとも1つのポリマー修飾基を含むポリペプチドコンジュゲートを精製するための方法を提供する。例示的なポリ(アルキレンオキシド)部分としては、ポリ(エチレングリコール)(PEG)およびポリ(プロピレングリコール)が挙げられる。例示的な方法において、グリコPEG化ポリペプチドの種々のグリコフォームを分離するために、疎水性相互作用クロマトグラフィー(HIC)が用いられる。 (もっと読む)
31 - 40 / 78
[ Back to top ]