ミオシンの発現及び筋線維の同一性を制御するマイクロRNA
【課題】心臓及び骨格筋におけるマイクロRNAの関与について詳述する。
【解決手段】 本発明は、速骨格筋収縮タンパク質遺伝子を抑制する2種のマイクロRNA、miR−499及びmiR−208bの特定に関する。miR−499及び/又はmiR−208bの発現を使用して、筋骨格系障害の治療において速筋線維遺伝子を抑制し、遅筋線維遺伝子を活性化することができる。miR−499及び/又はmiR−208bの阻害は、心臓肥大、心筋梗塞、及び/又は心不全の治療として提示される。miR−499及びmiR−208b機能の拮抗薬及び作動薬を含む医薬品組成物も開示される。
【解決手段】 本発明は、速骨格筋収縮タンパク質遺伝子を抑制する2種のマイクロRNA、miR−499及びmiR−208bの特定に関する。miR−499及び/又はmiR−208bの発現を使用して、筋骨格系障害の治療において速筋線維遺伝子を抑制し、遅筋線維遺伝子を活性化することができる。miR−499及び/又はmiR−208bの阻害は、心臓肥大、心筋梗塞、及び/又は心不全の治療として提示される。miR−499及びmiR−208b機能の拮抗薬及び作動薬を含む医薬品組成物も開示される。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
(a)心臓肥大、心不全、又は心筋梗塞を有する対象を特定する工程と、
(b)前記対象の心臓細胞でmiR−499又はmiR−208bの発現又は活性を阻害する工程と
を含む、その必要がある対象の、病的な心臓肥大、心不全、又は心筋梗塞を治療する方法。
【請求項2】
阻害する工程が、miR−499又はmiR−208bの阻害薬を前記対象に投与する工程を含む、請求項1に記載の方法。
【請求項3】
miR−499又はmiR−208bの阻害薬が、アンタゴmir、アンチセンスオリゴヌクレオチド、又は阻害性RNA分子である、請求項2に記載の方法。
【請求項4】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、成熟miR−499又はmiR−208b配列に相補的な配列を含む、請求項3に記載の方法。
【請求項5】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、配列番号26又は配列番号27に相補的な配列を含む、請求項4に記載の方法。
【請求項6】
阻害性RNA分子が二本鎖領域を含み、前記二本鎖領域が、成熟miR−499又はmiR−208b配列と実質的に同一な配列を含む、請求項3に記載の方法。
【請求項7】
二本鎖領域が、配列番号26又は配列番号27と実質的に同一な配列を含む、請求項6に記載の方法。
【請求項8】
miR−499又はmiR−208bの阻害薬が、非経口投与又は直接注射によって心臓組織に投与される、請求項2に記載の方法。
【請求項9】
非経口投与が静脈内又は皮下投与である、請求項8に記載の方法。
【請求項10】
miR−499又はmiR−208bの阻害薬が、経口、経皮、持続放出、制御放出、遅延放出、坐薬、カテーテル、又は舌下投与によって投与される、請求項2に記載の方法。
【請求項11】
miR−499及びmiR−208bの両方の発現又は活性が阻害される、請求項1に記載の方法。
【請求項12】
第2の心臓肥大治療薬を前記対象に投与する工程をさらに含む、請求項1に記載の方法。
【請求項13】
前記第2の治療薬が、β遮断薬、イオノトロープ、利尿薬、ACE−I、AII拮抗薬、BNP、Ca++遮断薬、エンドセリン受容体拮抗薬、及びHDAC阻害薬からなる群から選択される、請求項12に記載の方法。
【請求項14】
前記第2の治療薬が、miR−499又はmiR−208bの阻害薬と同時に投与される、請求項12に記載の方法。
【請求項15】
前記第2の治療薬が、miR−499又はmiR−208bの阻害薬の前又は後に投与される、請求項12に記載の方法。
【請求項16】
病的な心臓肥大、心不全、又は心筋梗塞の1つ又は複数の症状が、miR−499又はmiR−208bの阻害薬の投与の後に対象内で改善される、請求項1に記載の方法。
【請求項17】
前記1つ又は複数の症状が、高い運動能力、高い心臓駆出容積、低い左心室拡張末期圧、低い肺毛細血管楔入圧、高い心拍出量、高い心係数、低い肺動脈圧、低い左心室収縮末期及び拡張末期径、低い左心室及び右心室壁応力、低い壁張力、高い生活の質、低い疾患関連罹患率又は死亡率、又はこれらの組合せである、請求項16に記載の方法。
【請求項18】
miR−499又はmiR−208bの阻害薬の投与が、対象での心臓肥大から心不全への移行を遅延させる、請求項2に記載の方法。
【請求項19】
(a)病的な心臓肥大又は心不全を発症する危険性がある対象を特定する工程と、
(b)前記対象の心臓細胞でのmiR−499又はmiR−208bの発現又は活性を阻害する工程と
を含む、その必要がある対象で病的な肥大又は心不全を予防する方法。
【請求項20】
阻害する工程が、miR−499又はmiR−208bの阻害薬を心臓細胞に送達する工程を含む、請求項19に記載の方法。
【請求項21】
miR−499又はmiR−208bの阻害薬が、アンタゴmir、アンチセンスオリゴヌクレオチド、又は阻害性RNA分子である、請求項20に記載の方法。
【請求項22】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、成熟miR−499又はmiR−208b配列に相補的な配列を含む、請求項21に記載の方法。
【請求項23】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、配列番号26又は配列番号27に相補的な配列を含む、請求項22に記載の方法。
【請求項24】
阻害性RNA分子が二本鎖領域を含み、前記二本鎖領域が、成熟miR−499又はmiR−208b配列と実質的に同一な配列を含む、請求項21に記載の方法。
【請求項25】
二本鎖領域が、配列番号26又は配列番号27と実質的に同一な配列を含む、請求項24に記載の方法。
【請求項26】
危険性のある対象が、長期にわたって管理されていない高血圧、矯正されていない弁膜症、慢性アンギナ、最近の心筋梗塞、心疾患に対する先天的素因、及び病的な肥大からなる群から選択された1つ又は複数の危険因子を示す可能性がある、請求項19に記載の方法。
【請求項27】
危険性のある対象が、心臓肥大に対する遺伝的素因を有すると診断された、請求項19に記載の方法。
【請求項28】
危険性のある対象が、心臓肥大の家族歴を有する、請求項19に記載の方法。
【請求項29】
トランスジェニック非ヒト哺乳類であって、その細胞が、機能性miR−499又はmiR−208bを発現することができない哺乳類。
【請求項30】
マウスである、請求項29に記載のトランスジェニック哺乳類。
【請求項31】
トランスジェニック非ヒト哺乳類であって、その細胞が、前記非ヒト哺乳類の細胞で活性な異種プロモーターの制御下にあるMiR−499又はmiR−208bコード領域を含む哺乳類。
【請求項32】
マウスである、請求項31に記載のトランスジェニック哺乳類。
【請求項33】
前記プロモーターが組織特異的プロモーターである、請求項31に記載のトランスジェニック哺乳類。
【請求項34】
組織特異的プロモーターが筋特異的プロモーターである、請求項33に記載のトランスジェニック哺乳類。
【請求項35】
組織特異的プロモーターが心筋特異的プロモーターである、請求項33に記載のトランスジェニック哺乳類。
【請求項36】
天然のmiR−499対立遺伝子の一方又は両方、及び/又は天然のmiR−208b対立遺伝子の一方又は両方を欠くトランスジェニック非ヒト哺乳類細胞。
【請求項37】
前記天然のmiR−499対立遺伝子の両方、及び/又は前記天然のmiR−208b対立遺伝子の両方を欠く、請求項36に記載の細胞。
【請求項38】
対象の心臓細胞でのmiR−499又はmiR−208bの発現又は活性を阻害する工程を含む、その必要がある対象の心臓肥大及び拡張型心筋症を予防する方法。
【請求項39】
対象の心臓細胞でのmiR−499又はmiR−208bの発現又は活性を阻害する工程を含む、その必要がある対象での心臓肥大の進行を阻害する方法。
【請求項40】
(a)筋骨格系障害の危険性を有し、あるいは危険性がある対象を特定する工程と、
(b)前記対象の骨格筋細胞でのmiR−499及び/又はmiR−208bの発現及び/又は活性を増大させる工程と
を含む、その必要がある対象の筋骨格系障害を治療又は予防する方法。
【請求項41】
前記筋骨格障害が、筋萎縮症、抗重力に応答した筋肉疲労、及び除神経からなる群から選択される、請求項40に記載の方法。
【請求項42】
miR−499又はmiR−208bの発現及び/又は活性を増大させる工程が、成熟miR−499又は成熟miR−208b配列を含むポリヌクレオチドを前記対象に投与する工程を含む、請求項40に記載の方法。
【請求項43】
ポリヌクレオチドが配列番号26又は配列番号27の配列を含む、請求項42に記載の方法。
【請求項44】
miR−499及び/又はmiR−208bの発現及び/又は活性を増大させる工程が、miR−499及び/又はmiR−208bをコードする発現ベクターを前記対象に投与する工程を含む、請求項40に記載の方法。
【請求項45】
発現ベクターがウイルス発現ベクターである、請求項44に記載の方法。
【請求項46】
ウイルス発現ベクターがアデノウイルス発現ベクターである、請求項45に記載の方法。
【請求項47】
発現ベクターが非ウイルス発現ベクターである、請求項44に記載の方法。
【請求項48】
非ウイルス発現ベクターが脂質ビヒクル内に含まれる、請求項47に記載の方法。
【請求項49】
ポリヌクレオチドが脂質ビヒクル内に含まれる、請求項42に記載の方法。
【請求項50】
miR−499及びmiR−208bの両方の発現及び/又は活性を、前記対象の骨格筋細胞で増大させる、請求項40に記載の方法。
【請求項51】
前記骨格筋細胞の1つ又は複数の速骨格筋遺伝子の発現を、miR−499又はmiR−208bの発現又は活性を増大させた後に低下させる、請求項40に記載の方法。
【請求項52】
1つ又は複数の速骨格筋遺伝子が、トロポニンI2、トロポニンT3、速骨格ミオシン軽鎖、及びα骨格アクチンからなる群から選択される、請求項51に記載の方法。
【請求項53】
非miR−499又はmiR−208b治療薬を対象に投与する工程をさらに含む、請求項40に記載の方法。
【請求項54】
miR−499及び/又はmiR−208bのモジュレーターを特定するための方法であって、
(a)細胞を候補物質に接触させる工程と、
(b)miR−499及び/又はmiR−208bの活性又は発現を評価する工程と、
(c)工程(b)の活性又は発現を、候補物質の不在下での活性又は発現と比較する工程と
を含み、測定した活性又は発現の間の差から、前記候補物質がmiR−499及び/又はmiR−208bのモジュレーターであることが示される方法。
【請求項55】
細胞を、in vitroで候補物質に接触させる、請求項54に記載の方法。
【請求項56】
細胞を、in vivoで候補物質に接触させる、請求項54に記載の方法。
【請求項57】
miR−499及び/又はmiR−208bのモジュレーターが、miR−499及び/又はmiR−208bの作動薬である、請求項54に記載の方法。
【請求項58】
miR−499及び/又はmiR−208bのモジュレーターが、miR−499及び/又はmiR−208bの拮抗薬である、請求項54に記載の方法。
【請求項59】
候補物質が、タンパク質、ペプチド、ポリペプチド、ポリヌクレオチド、オリゴヌクレオチド、又は小分子である、請求項54に記載の方法。
【請求項60】
miR−499及び/又はmiR−208bの活性又は発現を評価する工程が、miR−499及び/又はmiR−208bの発現を評価する工程を含む、請求項54に記載の方法。
【請求項61】
miR−499及び/又はmiR−208bの発現を評価する工程が、ノーザンブロット又はRT−PCRを含む、請求項60に記載の方法。
【請求項62】
miR−499及び/又はmiR−208bの活性又は発現を評価する工程が、miR−499及び/又はmiR−208bの活性を評価する工程を含む、請求項54に記載の方法。
【請求項63】
miR−499又はmiR−208bの活性を評価する工程が、miR−499又はmiR−208bによって調節された遺伝子の発現又は活性を評価する工程を含む、請求項62に記載の方法。
【請求項64】
miR−499によって調節された遺伝子が、β−ミオシン重鎖又は速骨格筋タンパク質遺伝子である、請求項63に記載の方法。
【請求項65】
miR−208bによって調節された遺伝子が、Sp3、ミオスタチン、PURβ、THRAP1、又は速骨格筋タンパク質遺伝子である、請求項63に記載の方法。
【請求項66】
速骨格筋タンパク質遺伝子が、トロポニンI2、トロポニンT3、速骨格筋ミオシン軽鎖、又はα骨格アクチンである、請求項64又は請求項65に記載の方法。
【請求項67】
miR−499又はmiR−208bの活性を評価する工程が、α−ミオシン重鎖発現レベルとβ−ミオシン重鎖発現レベルとの比を評価する工程を含む、請求項62に記載の方法。
【請求項68】
miR−499及び/又はmiR−208bの阻害薬を含む医薬品組成物。
【請求項69】
前記阻害薬が、アンタゴmir、アンチセンスオリゴヌクレオチド、又は阻害性RNA分子である、請求項68に記載の医薬品組成物。
【請求項70】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、成熟miR−499又はmiR−208b配列に相補的な配列を含む、請求項69に記載の医薬品組成物。
【請求項71】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、配列番号26又は配列番号27に相補的な配列を含む、請求項70に記載の医薬品組成物。
【請求項72】
阻害性RNA分子が二本鎖領域を含み、前記二本鎖領域が、成熟miR−499又はmiR−208b配列と実質的に同一な配列を含む、請求項69に記載の医薬品組成物。
【請求項73】
二本鎖領域が、配列番号26又は配列番号27と実質的に同一な配列を含む、請求項72に記載の医薬品組成物。
【請求項74】
miR−499の阻害薬及びmiR−208bの阻害薬を含む、請求項68に記載の医薬品組成物。
【請求項75】
注射用に配合される、請求項68に記載の医薬品組成物。
【請求項76】
非経口投与用のキットと組み合わせた、請求項68に記載の医薬品組成物。
【請求項77】
非経口投与が静脈内又は皮下投与である、請求項76に記載の医薬品組成物。
【請求項78】
カテーテル投与用のキットと組み合わせた、請求項68に記載の医薬品組成物。
【請求項79】
miR−499又はmiR−208bの成熟配列を含有するポリヌクレオチドを含む、医薬品組成物。
【請求項80】
前記ポリヌクレオチドが発現ベクター内に含有される、請求項79に記載の医薬品組成物。
【請求項81】
前記ポリヌクレオチドが配列番号26又は配列番号27の配列を含む、請求項79に記載の医薬品組成物。
【請求項82】
前記ポリヌクレオチドが脂質送達ビヒクルに含まれる、請求項79に記載の医薬品組成物。
【請求項83】
miR−499及びmiR−208bの両方の成熟配列を含有するポリヌクレオチドを含む、請求項79に記載の医薬品組成物。
【請求項1】
(a)心臓肥大、心不全、又は心筋梗塞を有する対象を特定する工程と、
(b)前記対象の心臓細胞でmiR−499又はmiR−208bの発現又は活性を阻害する工程と
を含む、その必要がある対象の、病的な心臓肥大、心不全、又は心筋梗塞を治療する方法。
【請求項2】
阻害する工程が、miR−499又はmiR−208bの阻害薬を前記対象に投与する工程を含む、請求項1に記載の方法。
【請求項3】
miR−499又はmiR−208bの阻害薬が、アンタゴmir、アンチセンスオリゴヌクレオチド、又は阻害性RNA分子である、請求項2に記載の方法。
【請求項4】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、成熟miR−499又はmiR−208b配列に相補的な配列を含む、請求項3に記載の方法。
【請求項5】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、配列番号26又は配列番号27に相補的な配列を含む、請求項4に記載の方法。
【請求項6】
阻害性RNA分子が二本鎖領域を含み、前記二本鎖領域が、成熟miR−499又はmiR−208b配列と実質的に同一な配列を含む、請求項3に記載の方法。
【請求項7】
二本鎖領域が、配列番号26又は配列番号27と実質的に同一な配列を含む、請求項6に記載の方法。
【請求項8】
miR−499又はmiR−208bの阻害薬が、非経口投与又は直接注射によって心臓組織に投与される、請求項2に記載の方法。
【請求項9】
非経口投与が静脈内又は皮下投与である、請求項8に記載の方法。
【請求項10】
miR−499又はmiR−208bの阻害薬が、経口、経皮、持続放出、制御放出、遅延放出、坐薬、カテーテル、又は舌下投与によって投与される、請求項2に記載の方法。
【請求項11】
miR−499及びmiR−208bの両方の発現又は活性が阻害される、請求項1に記載の方法。
【請求項12】
第2の心臓肥大治療薬を前記対象に投与する工程をさらに含む、請求項1に記載の方法。
【請求項13】
前記第2の治療薬が、β遮断薬、イオノトロープ、利尿薬、ACE−I、AII拮抗薬、BNP、Ca++遮断薬、エンドセリン受容体拮抗薬、及びHDAC阻害薬からなる群から選択される、請求項12に記載の方法。
【請求項14】
前記第2の治療薬が、miR−499又はmiR−208bの阻害薬と同時に投与される、請求項12に記載の方法。
【請求項15】
前記第2の治療薬が、miR−499又はmiR−208bの阻害薬の前又は後に投与される、請求項12に記載の方法。
【請求項16】
病的な心臓肥大、心不全、又は心筋梗塞の1つ又は複数の症状が、miR−499又はmiR−208bの阻害薬の投与の後に対象内で改善される、請求項1に記載の方法。
【請求項17】
前記1つ又は複数の症状が、高い運動能力、高い心臓駆出容積、低い左心室拡張末期圧、低い肺毛細血管楔入圧、高い心拍出量、高い心係数、低い肺動脈圧、低い左心室収縮末期及び拡張末期径、低い左心室及び右心室壁応力、低い壁張力、高い生活の質、低い疾患関連罹患率又は死亡率、又はこれらの組合せである、請求項16に記載の方法。
【請求項18】
miR−499又はmiR−208bの阻害薬の投与が、対象での心臓肥大から心不全への移行を遅延させる、請求項2に記載の方法。
【請求項19】
(a)病的な心臓肥大又は心不全を発症する危険性がある対象を特定する工程と、
(b)前記対象の心臓細胞でのmiR−499又はmiR−208bの発現又は活性を阻害する工程と
を含む、その必要がある対象で病的な肥大又は心不全を予防する方法。
【請求項20】
阻害する工程が、miR−499又はmiR−208bの阻害薬を心臓細胞に送達する工程を含む、請求項19に記載の方法。
【請求項21】
miR−499又はmiR−208bの阻害薬が、アンタゴmir、アンチセンスオリゴヌクレオチド、又は阻害性RNA分子である、請求項20に記載の方法。
【請求項22】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、成熟miR−499又はmiR−208b配列に相補的な配列を含む、請求項21に記載の方法。
【請求項23】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、配列番号26又は配列番号27に相補的な配列を含む、請求項22に記載の方法。
【請求項24】
阻害性RNA分子が二本鎖領域を含み、前記二本鎖領域が、成熟miR−499又はmiR−208b配列と実質的に同一な配列を含む、請求項21に記載の方法。
【請求項25】
二本鎖領域が、配列番号26又は配列番号27と実質的に同一な配列を含む、請求項24に記載の方法。
【請求項26】
危険性のある対象が、長期にわたって管理されていない高血圧、矯正されていない弁膜症、慢性アンギナ、最近の心筋梗塞、心疾患に対する先天的素因、及び病的な肥大からなる群から選択された1つ又は複数の危険因子を示す可能性がある、請求項19に記載の方法。
【請求項27】
危険性のある対象が、心臓肥大に対する遺伝的素因を有すると診断された、請求項19に記載の方法。
【請求項28】
危険性のある対象が、心臓肥大の家族歴を有する、請求項19に記載の方法。
【請求項29】
トランスジェニック非ヒト哺乳類であって、その細胞が、機能性miR−499又はmiR−208bを発現することができない哺乳類。
【請求項30】
マウスである、請求項29に記載のトランスジェニック哺乳類。
【請求項31】
トランスジェニック非ヒト哺乳類であって、その細胞が、前記非ヒト哺乳類の細胞で活性な異種プロモーターの制御下にあるMiR−499又はmiR−208bコード領域を含む哺乳類。
【請求項32】
マウスである、請求項31に記載のトランスジェニック哺乳類。
【請求項33】
前記プロモーターが組織特異的プロモーターである、請求項31に記載のトランスジェニック哺乳類。
【請求項34】
組織特異的プロモーターが筋特異的プロモーターである、請求項33に記載のトランスジェニック哺乳類。
【請求項35】
組織特異的プロモーターが心筋特異的プロモーターである、請求項33に記載のトランスジェニック哺乳類。
【請求項36】
天然のmiR−499対立遺伝子の一方又は両方、及び/又は天然のmiR−208b対立遺伝子の一方又は両方を欠くトランスジェニック非ヒト哺乳類細胞。
【請求項37】
前記天然のmiR−499対立遺伝子の両方、及び/又は前記天然のmiR−208b対立遺伝子の両方を欠く、請求項36に記載の細胞。
【請求項38】
対象の心臓細胞でのmiR−499又はmiR−208bの発現又は活性を阻害する工程を含む、その必要がある対象の心臓肥大及び拡張型心筋症を予防する方法。
【請求項39】
対象の心臓細胞でのmiR−499又はmiR−208bの発現又は活性を阻害する工程を含む、その必要がある対象での心臓肥大の進行を阻害する方法。
【請求項40】
(a)筋骨格系障害の危険性を有し、あるいは危険性がある対象を特定する工程と、
(b)前記対象の骨格筋細胞でのmiR−499及び/又はmiR−208bの発現及び/又は活性を増大させる工程と
を含む、その必要がある対象の筋骨格系障害を治療又は予防する方法。
【請求項41】
前記筋骨格障害が、筋萎縮症、抗重力に応答した筋肉疲労、及び除神経からなる群から選択される、請求項40に記載の方法。
【請求項42】
miR−499又はmiR−208bの発現及び/又は活性を増大させる工程が、成熟miR−499又は成熟miR−208b配列を含むポリヌクレオチドを前記対象に投与する工程を含む、請求項40に記載の方法。
【請求項43】
ポリヌクレオチドが配列番号26又は配列番号27の配列を含む、請求項42に記載の方法。
【請求項44】
miR−499及び/又はmiR−208bの発現及び/又は活性を増大させる工程が、miR−499及び/又はmiR−208bをコードする発現ベクターを前記対象に投与する工程を含む、請求項40に記載の方法。
【請求項45】
発現ベクターがウイルス発現ベクターである、請求項44に記載の方法。
【請求項46】
ウイルス発現ベクターがアデノウイルス発現ベクターである、請求項45に記載の方法。
【請求項47】
発現ベクターが非ウイルス発現ベクターである、請求項44に記載の方法。
【請求項48】
非ウイルス発現ベクターが脂質ビヒクル内に含まれる、請求項47に記載の方法。
【請求項49】
ポリヌクレオチドが脂質ビヒクル内に含まれる、請求項42に記載の方法。
【請求項50】
miR−499及びmiR−208bの両方の発現及び/又は活性を、前記対象の骨格筋細胞で増大させる、請求項40に記載の方法。
【請求項51】
前記骨格筋細胞の1つ又は複数の速骨格筋遺伝子の発現を、miR−499又はmiR−208bの発現又は活性を増大させた後に低下させる、請求項40に記載の方法。
【請求項52】
1つ又は複数の速骨格筋遺伝子が、トロポニンI2、トロポニンT3、速骨格ミオシン軽鎖、及びα骨格アクチンからなる群から選択される、請求項51に記載の方法。
【請求項53】
非miR−499又はmiR−208b治療薬を対象に投与する工程をさらに含む、請求項40に記載の方法。
【請求項54】
miR−499及び/又はmiR−208bのモジュレーターを特定するための方法であって、
(a)細胞を候補物質に接触させる工程と、
(b)miR−499及び/又はmiR−208bの活性又は発現を評価する工程と、
(c)工程(b)の活性又は発現を、候補物質の不在下での活性又は発現と比較する工程と
を含み、測定した活性又は発現の間の差から、前記候補物質がmiR−499及び/又はmiR−208bのモジュレーターであることが示される方法。
【請求項55】
細胞を、in vitroで候補物質に接触させる、請求項54に記載の方法。
【請求項56】
細胞を、in vivoで候補物質に接触させる、請求項54に記載の方法。
【請求項57】
miR−499及び/又はmiR−208bのモジュレーターが、miR−499及び/又はmiR−208bの作動薬である、請求項54に記載の方法。
【請求項58】
miR−499及び/又はmiR−208bのモジュレーターが、miR−499及び/又はmiR−208bの拮抗薬である、請求項54に記載の方法。
【請求項59】
候補物質が、タンパク質、ペプチド、ポリペプチド、ポリヌクレオチド、オリゴヌクレオチド、又は小分子である、請求項54に記載の方法。
【請求項60】
miR−499及び/又はmiR−208bの活性又は発現を評価する工程が、miR−499及び/又はmiR−208bの発現を評価する工程を含む、請求項54に記載の方法。
【請求項61】
miR−499及び/又はmiR−208bの発現を評価する工程が、ノーザンブロット又はRT−PCRを含む、請求項60に記載の方法。
【請求項62】
miR−499及び/又はmiR−208bの活性又は発現を評価する工程が、miR−499及び/又はmiR−208bの活性を評価する工程を含む、請求項54に記載の方法。
【請求項63】
miR−499又はmiR−208bの活性を評価する工程が、miR−499又はmiR−208bによって調節された遺伝子の発現又は活性を評価する工程を含む、請求項62に記載の方法。
【請求項64】
miR−499によって調節された遺伝子が、β−ミオシン重鎖又は速骨格筋タンパク質遺伝子である、請求項63に記載の方法。
【請求項65】
miR−208bによって調節された遺伝子が、Sp3、ミオスタチン、PURβ、THRAP1、又は速骨格筋タンパク質遺伝子である、請求項63に記載の方法。
【請求項66】
速骨格筋タンパク質遺伝子が、トロポニンI2、トロポニンT3、速骨格筋ミオシン軽鎖、又はα骨格アクチンである、請求項64又は請求項65に記載の方法。
【請求項67】
miR−499又はmiR−208bの活性を評価する工程が、α−ミオシン重鎖発現レベルとβ−ミオシン重鎖発現レベルとの比を評価する工程を含む、請求項62に記載の方法。
【請求項68】
miR−499及び/又はmiR−208bの阻害薬を含む医薬品組成物。
【請求項69】
前記阻害薬が、アンタゴmir、アンチセンスオリゴヌクレオチド、又は阻害性RNA分子である、請求項68に記載の医薬品組成物。
【請求項70】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、成熟miR−499又はmiR−208b配列に相補的な配列を含む、請求項69に記載の医薬品組成物。
【請求項71】
アンタゴmir又はアンチセンスオリゴヌクレオチドが、配列番号26又は配列番号27に相補的な配列を含む、請求項70に記載の医薬品組成物。
【請求項72】
阻害性RNA分子が二本鎖領域を含み、前記二本鎖領域が、成熟miR−499又はmiR−208b配列と実質的に同一な配列を含む、請求項69に記載の医薬品組成物。
【請求項73】
二本鎖領域が、配列番号26又は配列番号27と実質的に同一な配列を含む、請求項72に記載の医薬品組成物。
【請求項74】
miR−499の阻害薬及びmiR−208bの阻害薬を含む、請求項68に記載の医薬品組成物。
【請求項75】
注射用に配合される、請求項68に記載の医薬品組成物。
【請求項76】
非経口投与用のキットと組み合わせた、請求項68に記載の医薬品組成物。
【請求項77】
非経口投与が静脈内又は皮下投与である、請求項76に記載の医薬品組成物。
【請求項78】
カテーテル投与用のキットと組み合わせた、請求項68に記載の医薬品組成物。
【請求項79】
miR−499又はmiR−208bの成熟配列を含有するポリヌクレオチドを含む、医薬品組成物。
【請求項80】
前記ポリヌクレオチドが発現ベクター内に含有される、請求項79に記載の医薬品組成物。
【請求項81】
前記ポリヌクレオチドが配列番号26又は配列番号27の配列を含む、請求項79に記載の医薬品組成物。
【請求項82】
前記ポリヌクレオチドが脂質送達ビヒクルに含まれる、請求項79に記載の医薬品組成物。
【請求項83】
miR−499及びmiR−208bの両方の成熟配列を含有するポリヌクレオチドを含む、請求項79に記載の医薬品組成物。
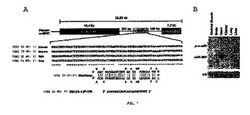
【図1】


【図2A】


【図2B】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21A】


【図21B】


【図21C】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】




【図2A】


【図2B】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21A】


【図21B】


【図21C】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【公表番号】特表2010−535246(P2010−535246A)
【公表日】平成22年11月18日(2010.11.18)
【国際特許分類】
【出願番号】特願2010−520205(P2010−520205)
【出願日】平成20年7月31日(2008.7.31)
【国際出願番号】PCT/US2008/071837
【国際公開番号】WO2009/018492
【国際公開日】平成21年2月5日(2009.2.5)
【出願人】(501100582)ボード オブ リージェンツ, ザ ユニバーシティー オブ テキサス システム (19)
【Fターム(参考)】
【公表日】平成22年11月18日(2010.11.18)
【国際特許分類】
【出願日】平成20年7月31日(2008.7.31)
【国際出願番号】PCT/US2008/071837
【国際公開番号】WO2009/018492
【国際公開日】平成21年2月5日(2009.2.5)
【出願人】(501100582)ボード オブ リージェンツ, ザ ユニバーシティー オブ テキサス システム (19)
【Fターム(参考)】
[ Back to top ]

