Fターム[4B050CC03]の内容
Fターム[4B050CC03]の下位に属するFターム
人為的に変えられた配列のもの (930)
2種以上の蛋白質が融合したもの (356)
Fターム[4B050CC03]に分類される特許
281 - 300 / 2,040
カテナ:漿液性癌幹細胞
本発明は、漿液性癌幹細胞(CSC)のクローン的に純粋な集団、CSCを製造及び培養する方法、並びにその使用に関する。CSCは、ヒアルロン酸とプロテオグリカンとのグリコカリックス被覆を有するカテナ(浮遊性細胞鎖)を形成する。この発見が、グリコカリックス形成の除去又は抑制を標的とすることにより漿液性癌及び卵巣癌を治療する方法であって、グリコカリックス阻害剤との併用による化学療法を用いた併用療法を含む上記方法の開発に至った。また、本発明は、これらのCSC、並びにその他漿液性癌細胞に対する効果的な化合物を同定するための薬物スクリーニングアッセイを提供する。カテナ遺伝子特性、タンパク質、及び表面抗原を使用する方法が、漿液性癌幹細胞の存在について患者試料を監視するために提供される。  (もっと読む)
(もっと読む)
トランスジェニック生物における多不飽和脂肪酸の製造方法
【課題】Δ5-エロンガーゼ活性を有するポリペプチドをコードする核酸を導入した生物において多不飽和脂肪酸を製造する方法の提供。
【解決手段】Thalassiosira、EuglenaまたはOstreococcusに由来するΔ6-デサチュラーゼ、Δ5-デサチュラーゼ、Δ4-デサチュラーゼおよび/またはΔ6-エロンガーゼ活性をコードする核酸配列、当該核酸配列を含んでなる遺伝子構築物。
(もっと読む)
グルカナーゼ、それらをコードする核酸並びにそれらを製造及び使用する方法
【課題】グルカナーゼ(例えばエンドグルカナーゼ)、マンナナーゼ、キシラナーゼ活性またはこれら活性の組合せを有する新規なポリペプチド、およびそれらをコードするポリヌクレオチド、新規な酵素を設計する方法およびそれらを使用する方法を提供する。
【解決手段】特定の塩基配列配列少なくとも約20、25、30、35、40、45、50、55、60、75または100残基にわたって少なくとも約50%の配列同一性を有するポリヌクレオチドまたはポリペプチド。
(もっと読む)
ラッカーゼ活性を有するタンパク質、当該タンパク質をコードするポリヌクレオチド、当該タンパク質を産生する方法、および、当該ポリヌクレオチドの取得方法
【課題】耐熱性および耐久性に優れたラッカーゼ活性を有するタンパク質、当該タンパク質をコードするポリヌクレオチド、当該タンパク質を産生する方法および当該ポリヌクレオチドを簡便に取得する方法を提供する。
【解決手段】ラッカーゼ活性を有し、特定のアミノ酸配列および前記アミノ酸配列において1又は複数のアミノ酸の欠失、置換、挿入および付加から選択される1以上の改変が生じたアミノ酸配列を有するタンパク質、および堆肥試料から抽出したメタゲノムDNA由来であって、ラッカーゼ活性を有するタンパク質をコードするポリヌクレオチド。
(もっと読む)
酸性ホスホリパーゼのクローニング、発現および用途
本発明は、本質的にリパーゼ活性を持たず、ホスホリパーゼ活性を有するポリペプチドをコードするDNA配列であって、このDNA配列は、a)SEQ ID NO:1によるヌクレオチド配列を有するDNA配列、b)SEQ ID NO:1によるコード化配列を有するDNA配列、c)SEQ ID NO:2による蛋白質配列をコードするDNA配列、d)図7による制限マップを持ち、受託番号DSM22741で寄託されている、プラスミドpPL3940−Topo2.5によってコードされるDNA配列、e)a)、b)、c)またはd)によるDNA配列の1つとストリンジェント条件下で交雑するDNA配列、f)遺伝子コードの減成によりa)、b)、c)、d)またはe)のDNA配列と関係するDNA配列、およびg)a)〜f)による配列に対する相補鎖
から選択され、ここでDNA配列は好ましくはアスペルギルス、さらに好ましくはアスペルギルス フミガタスから誘導される、ことを特徴とする、上記DNA配列、ならびにa)上記の1つによるDNA配列のコードする部分によってコードされるポリペプチド、b)SEQ ID NO:2による配列または1つもしくはそれ以上のアミノ酸の置換、附加もしくは除去によって得られうる、それから誘導された配列を有するポリペプチド、c)SEQ ID NO:2のアミノ酸1〜299と少なくとも83%同一性を有する配列を有するポリペプチド、
d)(i)SEQ ID NO:1のヌクレオチド55〜1106、(ii)SEQ ID NO:1のヌクレオチド55〜1106に含有されるcDNA配列、(iii)少なくとも100ヌクレオチドの(i)または(ii)の部分配列、または(iv)(i)、(ii)もしくは(iii)の相補鎖とストリンジェント条件下で交雑する核酸配列によってコードされるポリペプチド、e)1つもしくはそれ以上のアミノ酸の置換、除去および/または挿入を含む、SEQ ID NO:2を有するポリペプチドの変異型、f)アミノ酸配列a)〜e)に対するアレリック変異型、から選ばれる、本質的にリパーゼ活性を有さず、ホスホリパーゼ活性を有するポリペプチドに関する。
(もっと読む)
変異型ルシフェラーゼ
【課題】ルシフェラーゼ酵素が、対応する野生型ルシフェラーゼと比較して異なる波長の光を発することができ、および/または対応する野生型ルシフェラーゼと比較して熱安定性が向上している組換えタンパク質を提供する。
【解決手段】野生型ルシフェラーゼと少なくとも60%の類似性を有する組換えタンパク質であって、この酵素の配列中、Photinus pyralisのルシフェラーゼ中の残基357に対応するアミノ酸残基が対応する野生型ルシフェラーゼと比較して変異させられている。変異型ルシフェラーゼは、発せられる光の大きな(50nm)波長のシフトを生み出すことができ、優れた熱安定性を有し、その結果生、カラーシフトは、補酵素Aを加えることによって逆転させることができる。これらの性質によって、この変異体はさまざまなアッセイにおいて非常に有用である。
(もっと読む)
キノプロテイングルコース脱水素酵素およびその製造方法
【課題】耐熱性および耐pH性に優れ、温度安定性およびpH安定性に優れたキノプロテイングルコース脱水素酵素の提供。
【解決手段】ピロバキュラム由来の、下記の性質を有するキノプロテイングルコース脱水素酵素。(1)分子量(SDS−PAGE法):33±6kDa(2)一量体タンパク質(3)最適pH:pH7〜9(4)最適温度:75℃以上(5)温度安定性:80℃以下(6)pH安定性:pH4〜11および、該酵素の製造方法、この酵素と補酵素との複合体、グルコース測定キット、前記酵素遺伝子、前記酵素遺伝子を含むベクター、前記ベクターを含む形質転換体。
(もっと読む)
グリコサミノグリカン分解促進剤
【課題】 微生物により産生されるコンドロイチナーゼに代わり、タンパク質分解酵素などの混入のおそれの少ないヒト由来のグリコサミノグリカン分解活性を有するタンパク質を、医薬などとして提供し、またこのタンパク質を用いた機能性オリゴ糖の製造方法を提供する。
【解決手段】 配列番号1に示されるアミノ酸配列からなるタンパク質、または配列番号1に示されるアミノ酸配列において1個もしくは数十個のアミノ酸が置換され、欠失され、または付加されたアミノ酸配列からなり、かつD−グルクロン酸に結合した硫酸化N−アセチル−DーガラクトサミンのN−アセチル−D−ガラクトサミニド結合を加水分解する活性を有するタンパク質を有効成分とする。
(もっと読む)
アメフラシ由来マンナナーゼ
【課題】酸性条件においても安定して高い酵素活性を示す新規なマンナナーゼを提供すること。
【解決手段】
アメフラシに由来し、下記の(a)〜(c)の理化学的性質を有するマンナナーゼ。
(a) 作用:ガラクトマンナン及びグルコマンナンを分解して、還元糖を遊離する
(b) 基質特異性:ロカストビーンガム、タラガム、グアガム及びグルコマンナンを分解する
(c) 至適pH:pH2.0〜7.5(最適pH:pH3.0〜7.0)
(もっと読む)
スタチンおよびスタチン中間体の合成のための酵素化学的方法
【課題】アトルバスタチン、LIPITOR(登録商標)、ロスバスタチン(CRESTOR(登録商標))、フルバスタチン(LESCOL(登録商標))、等のスタチン、関連化合物およびそれらの中間体を製造する方法を提供する。
【解決手段】新規なアルドラーゼおよび前記アルドラーゼをコードする核酸、たとえば、特定な配列からなる遺伝子配列の核酸、または特定な配列のアミノ酸配列からなるポリペプチドまたはそれらの酵素的に活性な断片、およびそれらの使用。
(もっと読む)
テトラヒメナから得られるΔ−6−デサチュラーゼをコードする核酸、その産生と使用
【課題】テトラヒメナから得られ、商業的に価値ある多不飽和脂肪酸(いわゆるPUFA:多不飽和脂肪酸)の生合成に関与する繊毛虫特異的Δ−6−デサチュラーゼをコードする、核酸(群)の提供。
【解決手段】Δ−6−不飽和脂肪酸、特に、γ−リノレン酸(GLA)の産生増加を目的とした、繊毛虫、好ましくはテトラヒメナ、特にテトラヒメナ・サーモフィラでの過度に発現するための核酸。
(もっと読む)
カルバミン酸(R)−1−アリール−2−テトラゾリル−エチルエステルの製造方法
対応するアリールケトンのエナンチオ選択的酵素的還元及びその結果生じるアルコールのカルバメート化を含む、カルバミン酸(R)−1−アリール−2−テトラゾリル−エチルエステルの製造方法を開示する。 (もっと読む)
タンパク質欠損性障害の治療のための併用療法
【課題】タンパク質補充療法を活性部位特異的シャペロン(ASSC)と組み合わせることによって、投与されるタンパク質の安定性及び有効性を高め、タンパク質補充療法を改善する方法を提供する。
【解決手段】精製タンパク質と前記ASSCとを含有する組成物。前記精製タンパク質がα-ガラクトシダーゼAまたはβ-グルコセレブロシダーゼであり、前記ASSCが前記酵素の可逆的競争阻害剤である前記組成物を投与することによって治療する方法。
(もっと読む)
ホスホ−6−マンノースへのマンノース−1−ホスホ−6−マンノース結合の加水分解
マンノース−1−ホスホ−6−マンノース結合をホスホ−6−マンノースに加水分解することのできるマンノシダーゼを用いることにより、オリゴ糖におけるマンノース−6−リン酸残基をキャップ除去するのに有用な方法および遺伝的に操作されている細胞が本明細書に記載されている。本発明により、例えば、オリゴ糖におけるマンノース−6−リン酸残基をキャップ除去するための方法であって、a)マンノース−1−ホスホ−6−マンノース結合を有する該オリゴ糖を提供するステップと、b)該オリゴ糖を、該マンノース−1−ホスホ−6−マンノース結合をホスホ−6−マンノースに加水分解することのできるマンノシダーゼと接触させるステップと、を含む、方法が提供される。 (もっと読む)
グルクロン酸転移酵素の製造方法
【課題】酵母を用いたグルクロン酸転移酵素の発現系において、従来の方法では酵母内での発現量の低かった分子種について、発現量を向上させることができるグルクロン酸転移酵素の製造方法を提供する。
【解決手段】グルクロン酸転移酵素遺伝子を導入した酵母形質転換体を用いるグルクロン酸転移酵素の製造方法。前記グルクロン酸転移酵素遺伝子は、発現量がUGT1A7の50%以下である低発現量グルクロン酸転移酵素遺伝子である。前記低発現量グルクロン酸転移酵素遺伝子は、シグナル配列遺伝子を、発現量がUGT1A7の80%以上である高発現グルクロン酸転移酵素のシグナル配列遺伝子と置換したものである。酵母形質転換体によるグルクロン酸転移酵素の発現量がシグナル配列遺伝子未置換の形質転換体に比べて強化されている。
(もっと読む)
微生物由来アルデヒドデヒドロゲナーゼによる不飽和脂肪族アルデヒドの分解方法
【課題】微生物酵素を用いることにより毒性の高いアクロレインを酵素反応で分解し除去する方法を提供する。
【解決手段】本発明は、微生物由来のアルデヒドデヒドロゲナーゼによる不飽和脂肪族アルデヒドの分解方法を提供する。
(もっと読む)
一分子型プローブ及びその利用
【課題】発光輝度が高く、容易に設計可能な一分子型プローブを提供する。
【解決手段】本発明に係る融合タンパク質は、標的物質を検出するプローブとして使用されるものであり、前記標的物質が結合する結合部位を有する一次結合タンパク質と、前記一次結合タンパク質に前記標的物質が結合したことを認識する二次結合タンパク質と、前記一次結合タンパク質と前記二次結合タンパク質との間に位置する、活性型の酵素又はその前駆体とを有し、前記一次結合タンパク質に前記標的物質が結合したことを前記二次結合タンパク質が認識した場合に、酵素活性度を増加するものである。
(もっと読む)
新規ベンズアルデヒドデヒドロゲナーゼ遺伝子及び芳香族カルボン酸の製造法
【課題】シリンガアルデヒド、パニリン、p−ヒドロキシベンズアルデヒド等のリグニン由来の芳香族アルデヒドを効率よく酸化して対応する合成繊維やプラスチックの原料である芳香族カルボン酸に変換する新規遺伝子、新規タンパク質、及び該芳香族カルボン酸の製造法を提供する。
【解決手段】以下の(a)又は(b)のタンパク質:(a)特定のアミノ酸配列からなるタンパク質;(b)(a)のアミノ酸配列において、1個もしくは2個以上のアミノ酸が欠失、置換もしくは付加されたアミノ酸配列からなり、かつベンズアルデヒドデヒドロゲナーゼ活性を有するタンパク質。;該タンパク質をコードする遺伝子;及び、芳香族カルボン酸の製造法。
(もっと読む)
遺伝子増幅によるリジン産生の増加
【課題】本発明は、宿主細胞染色体におけるアミノ酸生合成経路遺伝子の増幅によって、Corynebacterium種からのアミノ酸の産生を増加する方法を提供する。
【解決手段】
好ましい実施形態において、本発明は、宿主細胞染色体におけるL−リジンの産生を増加するための方法を提供する。本発明はまた、宿主細胞染色体におけるアミノ酸生合成経路遺伝子の増幅によって、および/またはプロモーター強度の増加によって、アミノ酸の酸の産生のための新規なプロセスを提供する。好ましい実施形態において、本発明は、宿主細胞染色体におけるL−リジン生合成経路遺伝子の増幅によって、Corynebacterium glutamicumにおけるL−リジンの産生を増加するためのプロセスを提供する。本発明は、Corynebacterium glutamicumのL−リジン生合成経路遺伝子についての新規な単離された核酸分子を提供する。
(もっと読む)
アミダーゼおよび3−アミノカルボン酸エステルを製造するためのその使用
本発明は、一般式(I)(式中、R1はアルキル、アルコキシアルキル、アルケニル、シクロアルキル、ヘテロシクロアルキル、アリール、またはヘタリールを表し、R2はアルキル、シクロアルキルまたはアリールを表す)の光学活性な3-アミノカルボン酸エステル化合物およびそのアンモニウム塩の製造方法に関し、該方法では、一般式(I.b)(式中、R1およびR2は上記で定義した通りであり、R3は水素、アルキル、シクロアルキル、またはアリールである)の単純N-アシル化3-アミノカルボン酸エステルのエナンチオマー混合物を、請求項1に記載のポリペプチドを添加することによりエナンチオ選択的脱アシル化に供する。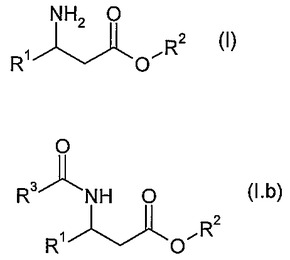 (もっと読む)
(もっと読む)
281 - 300 / 2,040
[ Back to top ]



