Fターム[4C096DC22]の内容
磁気共鳴イメージング装置 (34,967) | 画像処理 (5,620) | 画像からの計測又は解析 (747)
Fターム[4C096DC22]の下位に属するFターム
Fターム[4C096DC22]に分類される特許
201 - 220 / 225
手術支援システム
【課題】動的な画像を表示することが可能であって、バーチャルな手術の支援をすることが容易であり、手術の支援を効率的に実施する。
【解決手段】被検体の断層画像に対応する画像データを記憶する画像記憶部11と、手術器具を操作する手術器具操作部12と、手術器具操作部12により操作される手術器具の位置に対応する手術器具画像の画像データを手術器具画像生成部13と、画像記憶部11が記憶する断層画像の画像データと、手術器具画像生成部13が生成する手術器具画像の画像データとに基づいて、被検体の断層画像と手術器具画像とを重ね合わせて表示する画像表示部14とを有する。ここで、画像記憶部11は、断層画像の画像データを時間に対応して記憶しており、画像表示部14は、断層画像を時間に対応させて表示する。
(もっと読む)
磁気共鳴画像診断システム、磁気共鳴画像診断方法及びコンピュータプログラム
本発明による磁気共鳴画像診断システム(1)は、内部に撮像空間(図示せず)を有する主磁石(12)を有するデータ取得システム11を具えている。磁界傾斜Gx(14)、Gy(16)及びGz(17)を生成すべく構成された傾斜システム(G)が設けられている。整列したスピンをXY平面のような横断平面内に転向させるか、あるいはXY平面の成分を持たせるための無線周波数(RF)パルスを発生するRF励磁システム(10)が設けられている。スピンを転向させるためのシステム(10)は、磁石(12)内のRFコイル(図示せず)及びパルス送信機(15)を具えている。パルス送信周波数はシンセサイザ(19)によって供給することができ、そして制御システム(21)によって制御することができる。制御システム(21)は、磁気共鳴装置を構成する種々の構成部品の出力の時間及び振幅を制御すべく構成されている。送信されるパルスは、送信機(15)から送信機−受信機選択スイッチ(22)を通って磁石内のRFコイルに供給される。第2送信機−受信機スイッチ(23)によってシステムが送信モードである際には、シンセサイザの信号は送信機(15)に結合される。受信モードでは、磁石内のRFコイルが、例えばエコー信号を含む自由誘導減衰信号の形の、検査物体のRFパルスに対する応答を検出する。スイッチ(22)が制御システム(21)によってRFコイルを受信機に接続する受信モードに切り換えられている際には、RFコイルで受信した信号はスイッチ(22)を通して供給される。そしてこの受信信号はアナログ−ディジタル変換器(25)を通る。変換器(25)のディジタル出力は、好適には関連するメモリ(27)を有する画像再構成装置(26)に供給される。画像再構成装置(26)は、温度測定データ及び長手方向の緩和時間データをMR信号から抽出して、対応する再構成画像を表示ユニット(28)に転送すべく構成されている。本発明はさらに、磁気共鳴画像診断の方法及びコンピュータプログラムに関するものである。  (もっと読む)
(もっと読む)
歯科インプラントの位置を検出する方法とマーカエレメント
例えば歯科インプラントのような人の顎(13)に固定される補綴要素(2)の位置を検出し、それによって顎の、あるいは補綴要素(2)を設けているこの顎の再生モデルの像がX線あるいは磁気共鳴によって形成される方法とマーカエレメントである。少なくとも1個のマーカエレメント(3)が前記補綴要素に設けられ、形像技術において強力なコントラストを発生させる。顎に対する前記マーカエレメント(3)の位置がX線によってあるいは磁気共鳴を介して形成される像に基づいて検出され、次いで、前記補綴要素(2)の位置が前記マーカエレメント(3)の観察された位置から検出される。  (もっと読む)
(もっと読む)
軟組織を同時に画像化しながら等角放射線治療を送達するためのシステム
増殖性の組織異常によって引き起こされる疾病の治療において、患者へと投与される高度に原体照射的な電離放射線の線量を直接測定して制御するため、強度変調放射線治療(IMRT)の最中に患者の体構造について、高い時間および空間分解能でのMR画像化を実行するための装置およびプロセス。本発明は、オープンMRI(0015)、マルチリーフ・コリメータ(125)または補償フィルタをベースとするIMRT(020)投与、およびコバルト遠隔治療の技術を、位置合わせされてガントリー(025)へと取り付けられた単一のシステムへと組み合わせている。 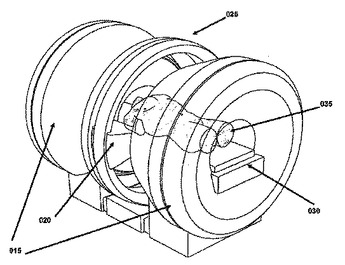 (もっと読む)
(もっと読む)
インターベンションデバイスの空間的ロードマップ生成方法、システム、及びその空間的精度を監視する品質管理システム
本発明は、インターベンションデバイスの空間的ロードマップ生成方法、システム、及びその空間的精度を監視する品質管理システムに関する。本発明を実施するシステム100の一実施形態では、X線画像化器100aを用いて、カテーテル182a、182bを含む検査対象のボリュームを示す好適な画像Di+1、Di、...、DNを取得する。これらのX線画像は、次に、それ自体既知の再構成方法により処理され、動き補正された3次元検査ボリュームを生成する。このボリュームは、次に、ディスプレイ部183上の好適なユーザインターフェイスにより、検出可能マーカを備えたカテーテル182a、182bの遠位部とともに表示される(簡単のため、1カテーテルにつき1つの検出可能マーカのみを示した)。対象臓器184の動き補正した3次元画像を用いて、動き補正された対象臓器指向3次元座標系を構成する。この座標系は、空間的ロードマップ183を描くために用いられ、さらに別の検出可能マーカ185′を有する置換可能カテーテルの空間的位置を位置決めするために用いられる。これらの計算は計算手段160を用いて実行する。計算手段160は、可視化された空間的ロードマップ183と置換可能カテーテル185の位置の間の空間的食い違いの計算を含むさらなる計算を実行するように構成されている。大幅な不一致が通知され、カテーテルが制御可能ナビゲーションシステム190により対象臓器内に位置づけられている場合、計算手段は、ナビゲーションシステム190に適用すべき制御信号Sを計算し、空間的ロードマップ183と置換可能カテーテル185の位置との間の不一致を補正する。制御部は、次に、ナビゲーションシステム190に補正信号Sを送る。インターベンションプロシージャが続く。
 (もっと読む)
(もっと読む)
非侵襲的イメージングのグローバル組織特性を用いた組織評価および画像のグローバル組織特性を決定するシステム
心臓の正常なミオサイトおよび線維組織の量の変化などの自然組織要素の比率の変化や損傷組織の特定を含む組織特性の評価、細胞外液要素または流体(水腫または細胞外液マトリクスタンパク質)の量の増大の識別、あるいは、腫瘍細胞または人間等の患者の対象組織への炎症の媒介物の侵入の検出は、例えば、患者に対する造影剤の投与後に第1の取得物から関心領域を含む組織の第1の画像を得ることにより、また、例えば患者に対する造影剤の投与後におけるその後の第2の取得中に関心領域を含む組織の第2の画像を得ることにより行なわれる。その後の取得物は所定期間後に得られてもよく、それにより、その所定期間中に損傷が生じたかどうかが決定されてもよい。関心領域としては、心臓、血液、筋肉、脳、神経、骨格、骨格筋、肝臓、腎臓、肺、膵臓、内分泌腺、胃腸及び/又は性尿器組織を挙げることができる。第1の画像および第2の画像の関心領域のグローバル特性は、グローバルな組織特性の変化を招く可能性を決定するため、第1の画像および第2の画像グローバル特性の比較を行なえるように決定される。そのような比較は、平均値、平均特性、スキューおよび尖度等のヒストグラム形状、またはヒストグラム内の強度の分布の比較を含んでいてもよい。
 (もっと読む)
(もっと読む)
手術中の2次元画像および手術前の3次元画像をアフィン重ね合わせするための方法およびシステム
手術中のターゲットフィーチャの2次元(2D)医学画像を手術前のターゲットフィーチャの3次元(3D)医学画像と重ね合わせるためのシステムおよび方法が開示される。ターゲットフィーチャの3D画像は第1スケルトングラフに変換される。ターゲットフィーチャの2D画像は第2スケルトングラフに変換される。第1スケルトングラフと第2スケルトングラフのグラフマッチングがグラフの荒いアライメントを得るために実行され、第1スケルトングラフト第2スケルトングラフが重ね合わされる。 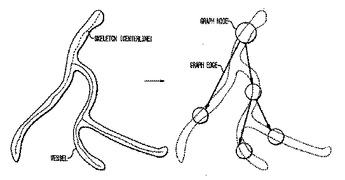 (もっと読む)
(もっと読む)
カテーテルをナビゲートする装置及び方法
本発明は、心拍及び/又は呼吸のための自発運動の影響を受ける患者の器官内のインターベンションニードル又は脈管系内のカテーテルをナビゲートする装置及び方法に関する。これに関連して、前記自発運動の基準位相(E0)を基準にして前記脈管系内のポイントの変位を記述する運動モデル(11)が、データ処理装置(10)のメモリ内に準備しておかれる。位置決め装置(2)によって測定される前記患者(3)の前記脈管系内の前記機器(4)の空間的位置及び向き、並びにそれと並行して記録されるECG値(E)は、前記データ処理装置(10)によって前記運動モデル(11)を利用して前記機器の動き補償位置(r+Δ)に変換され、前記動き補償位置(r+Δ)は、次いで、静止脈管又は器官マップ(12)内に表示され得る。前記運動モデル(11)は、前記脈管系の一連の三次元記録から得られ得る。更に、又は他の例においては、前記機器が前方に移動しない時間中の前記機器(4)の測定位置及び測定向きが用いられ得る。 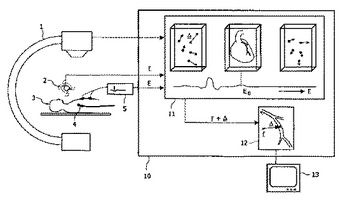 (もっと読む)
(もっと読む)
心臓機能の確率的解析
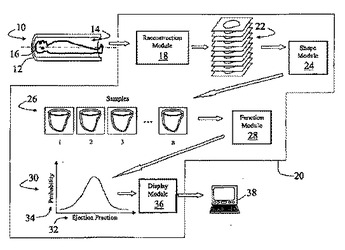
診断イメージング装置(10)は確率論的モデルに基づいて被検体の診断画像の区分化を行う。複数の断層画像の束(22)が、各々の束が遅れずに置換されるようにして生成される。断層画像の束から器官形状の複数解が複数の形状サンプル(26)の形態で計算される。画像を仮定した下での形状の条件付き分布を記述するベイズモデルに従ってサンプル群(24)が生成され、サンプル群の各々について、少なくとも1つの機能パラメータ(32)が導出される。各パラメータについて確率値(30)が導出され、表示(36、38)される。
 (もっと読む)
(もっと読む)
弾力的な画像位置合わせ
画像位置合わせは、従来、非常にしばしば手動で実行する必要のある面倒な仕事であった。本発明のある例示的な実施形態によれば、目印と類似性値との組み合わせに基づく逐次精製プロセスによる非剛体的な画像位置合わせが提案される。有利なことに、非常に高速かつ堅牢な方法が提供されうる。 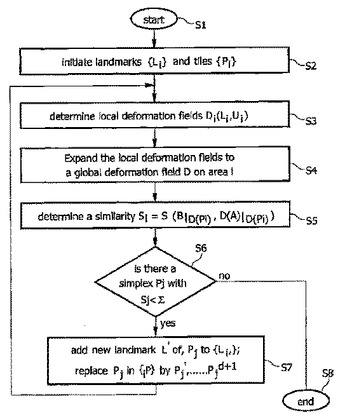 (もっと読む)
(もっと読む)
血液中のトレーサの濃度を決定する装置及び方法
本発明は、患者(1)の血液中のPETトレーサの濃度を決定するための装置及び方法に関する。X線CT(5、6)を用いて、まず最初に、血液で満たされるボリューム要素(2)の空間的な位置(r)が決定される。血液で満たされるボリューム要素(2)は、例えば心臓の左心室又は大動脈の一部でありえる。その後、2つの検出器素子(3a、3b)を有するTOF−PETユニットは、それが、このボリューム要素(2)中、ゆえに血液中のトレーサの濃度を確立するように設定される。この値は、例えば、3次元PETユニット(4)を用いて、患者(1)について実行される薬物動力学的検査のフレームワーク内で使用されることができる。 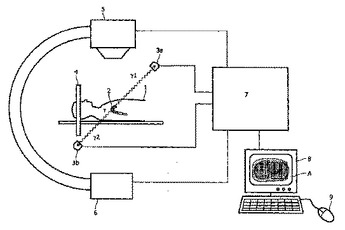 (もっと読む)
(もっと読む)
治療支援用画像処理装置
治療の目標となる治療範囲を予め設定しておいて、治療中に既に治療が完了したと考えられる既治療領域の画像を取得し、この既治療領域に基づいて目的治療領域全体の治療が終了するまでの時間を推定する。また、治療中の部位の変化を色で表現させて表示する。また、複数の治療時間について治療の完了したイメージをシミュレートすることでよりわかりやすく治療が終了するまでの時間を決定する。以上の特徴により、治療精度を向上させ、治療に要する総時間や被曝の低減を図ることができる。 (もっと読む)
脈管構造の局部画像を自動的に配向する方法及びシステム
D次元空間内の複数の点から成るドメインに対応する複数の輝度から成るディジタル画像中の管状構造を配向する方法を提供する。この方法は画像ドメイン内の1つの点を選択し(101)、選択された点の近傍において画像の勾配を計算し(102)、選択された点における基本構造を計算し(102)、選択された点の構造テンソルを求め(103)、構造テンソルの固有値を見つける(104)ステップを含む。最小固有値(105)に対応する固有ベクトルは管状構造と整列する。管状構造と整列する固有ベクトルによって画定される軸を中心とするカートホイール投影を計算(106)すればよい。 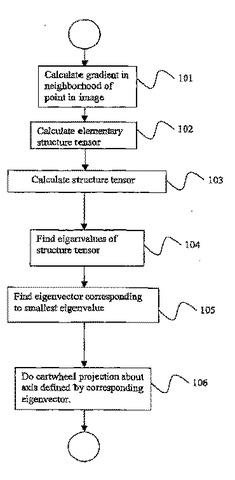 (もっと読む)
(もっと読む)
放射線治療の計画および実施のための目標追跡の方法および装置
被験体(140)内のある目標領域(130)を治療するための目標治療装置が提供される。当該装置は、検査領域(110)内に配置されている被験体のMRスキャンの間にMR画像を生成するためのMRI装置(100)を含んでいる。当該装置はさらに、MRI装置から画像データを受信し、目標(130)を定位するMRI定位器(150)と、目標の近傍に配置された複数の参照点からの参照データを非侵襲的に受信し、参照点を定位する参照マーカー定位器(160、160′)とを含んでいる。当該装置にはまた、該定位されたデータを前記MRI定位器から受信し、参照マーカーと目標領域との間の関係を生成する追跡プロセッサ(300)も含まれる。 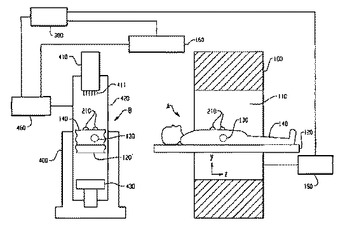 (もっと読む)
(もっと読む)
心臓における電気生理学的カテーテル療法の視覚的支援方法および装置
本発明は、心臓の治療すべき範囲の準備された電気解剖学的3Dマッピングデータがカテーテル療法実施中に可視化される心臓における電気生理学的カテーテル療法の視覚的支援方法および装置に関する。カテーテル療法の実施前に断層撮影による3D画像化法により治療すべき範囲を含んでいる身体部位の3D画像データが検出される。これらの3D画像データから治療すべき範囲またはその重要部分の3D画像データが抽出されて、選択された画像3D画像データが得られる。準備された電気解剖学的3Dマッピングデータおよび選択された3D画像データが最終的に位置正しくかつ寸法正しく関連付けされ、例えばカテーテルアブレーションの実施中に並べて可視化される。方法および装置は心臓におけるカテーテル療法の実施時における操作者の方位決めを改善する。  (もっと読む)
(もっと読む)
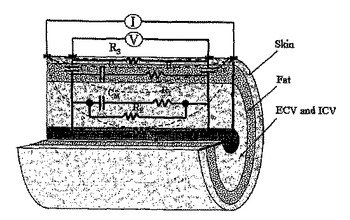
生体インピーダンス方法及び装置
生体インピーダンス分析を与えるための方法及び装置が提供される。いくつかの態様において、MRIデータとの改善された相関をもたらす等価回路周波数応答モデルが提供される。周波数応答モデルには、身体分区の脂肪成分を含む、身体組成を考慮にいれている。被験者の腓に関して生体インピーダンススペクトロスコピー(BIS)及びMRIを実施することによって得られたデータは、50kHzにおける単一周波数分析及び通常のコール−コールモデルを用いて実施された分析に比較して改善された相関が得られることを示す。
 (もっと読む)
(もっと読む)
心臓における電気生理学的カテーテル療法の視覚的支援方法および装置
本発明は、心臓の治療すべき範囲の準備された電気解剖学的3Dマッピングデータがカテーテル療法の実施中に可視化される心臓における電気生理学的カテーテル療法の視覚的支援方法および装置に関する。カテーテル療法の実施前に断層撮影による3D画像化法により治療すべき範囲の3D画像データが検出され、3D画像データからセグメンテーションによって治療すべき範囲における対象の3D表面形状が抽出され、電気解剖学的3Dマッピングデータと少なくとも3D表面形状を形成する3D画像データとがレジストレーションによって位置正しくかつ寸法正しく関連付けられ、例えばカテーテル療法の実施中に互いに重ね合わされた可視化される。本発明による方法および装置は、心臓における電気生理学的カテーテル療法の実施時における操作者の改善された方位決めを可能にする。  (もっと読む)
(もっと読む)
構造テンソルを利用して肺小結節及び大腸ポリープを検知する方法及びシステム
ディジタル画像中の球形対象を識別する方法を提案する。画像は複数の3D空間点を含む。この方法は画像ドメイン内の各点において画像の勾配を計算し(100);画像ドメイン内の各点において基本構造テンソルを計算し(102);画像ドメイン内の各点の構造テンソルを求め(103);構造テンソルの固有値を求め(104);各構造テンソルについて、前記構造テンソルの最小固有値と前記構造テンソルの最大固有値の比で表される等方性値を計算し(105)、球形対象であることを示す等方性度=1を見出すステップから成る。  (もっと読む)
(もっと読む)
解剖学的なターゲットの場所を特定するための磁気共鳴画像の使用
放射線治療を計画するためにMR画像を使用する新しいMR方法及びシステムが記述されている。画像は、磁気中心(アイソセンタ)を有する磁界を生成するスキャナによって得られる。まず、少なくとも1つの基準のマーカ(4;5)が、アイソセンタから予め決められた距離離れた患者の身体(1)に適用される。患者は、解剖学的なターゲット(2)が前記アイソセンタの近くに位置するように、前記スキャナの範囲内で配置しなおされる。前記ターゲット(2)の第1の画像が得られ、そののち、患者(1)は、基準マーカ(4;5)がアイソセンタの近くにくるようにシフトされる。第2の画像が、基準マーカが前記第1の画像にマージされる正確な幾何学的位置を有するシフトされた位置において得られる。  (もっと読む)
(もっと読む)
画像処理のための方法および装置
本発明は、例えばMRI画像撮影といったような画像処理のための方法および装置を開示するものである。本発明による方法および装置を使用すれば、撮影対象をなす容積(例えば、傷害部位)内における選択されたポイントのコントラスト変化/輝度変化が、対象物の移動の影響であるかどうかを、決定することができる。本発明においては、撮影対象容積の位置合わせ品質(時系列をなす複数の画像に関しての位置合わせ品質)を高速で視覚的に評価し得るような方法および装置が提供される。また、本発明においては、この方法の効果的な使用を可能とし得るよう、対話型のディスプレイツールが提供される。  (もっと読む)
(もっと読む)
201 - 220 / 225
[ Back to top ]


