国際特許分類[G01N27/62]の内容
物理学 (1,541,580) | 測定;試験 (294,940) | 材料の化学的または物理的性質の決定による材料の調査または分析 (128,275) | 電気的,電気化学的,または磁気的手段の利用による材料の調査または分析 (17,622) | ガスのイオン化の調査によるもの;放電の調査によるもの,例.陰極の放射 (3,117)
国際特許分類[G01N27/62]の下位に属する分類
国際特許分類[G01N27/62]に分類される特許
2,661 - 2,670 / 2,683
心臓血管障害に関連する分泌ポリペプチド種
本発明は心臓血管障害を有する患者の血漿において高レベルで循環するヒト分泌ポリペプチドを開示する。本発明はまた診断、予後診断および薬剤開発のためのポリペプチド、これらをコードするポリヌクレオチド、およびこれらのポリペプチドに特異的な抗体をも提供する。 (もっと読む)
メタボノミクスにおいてLC−MSまたはLC−MS/MSデータの処理を行うための方法およびデバイス
真のクロマトグラフィおよびMSピークがメタボノミクスで使用するために識別されるように、収集されたLC−MSまたはLC−MS/MSデータの集合を縮小する方法が開示されている。識別されたピークは、マスタエンティティリストに表示される1バッチの試料に対するLC/MS、GC/MS、DIOS−MS、またはMALDI−MS信号および応答のリストを作成するために使用される。試料はマスタエンティティリスト内にある。その後、マスタエンティティリストに載っている試料は、バイオマーカーを自動的に識別するためにケモメトリクスを適用するのに先立って同位体クラスタ分離および付加体除去を受ける。PLS−DAまたはPCA分離に関与するものとして識別された信号についてLC−MS/MSまたはLC/MS、GC/MS、DIOS−MSまたはMALDI−MS収集リストが生成される。LCまたはGC保持時間、正確な質量およびMS/MSスペクトルを知られている化合物のデータベースと比較し、生物学的指標に関連する識別された化合物を新しい化合物データベースに格納することができる。 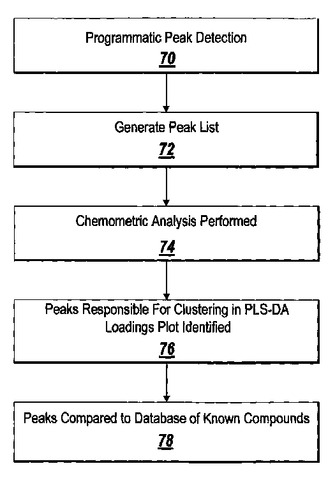 (もっと読む)
(もっと読む)
死亡率を予想する独立したリスク因子としてのリラキシン
リラキシンレベルの測定をベースとするヒト個体の余命の同定方法を開示する。本発明のある態様では、ヒト個体は、末期の腎臓病患者である。 (もっと読む)
空気中に存在し、または堆積した、痕跡量の低分子量化合物の検出
空気中にある、または堆積した、痕跡量の低分子量化合物の検出。
空気中にある、または堆積した、痕跡量の低分子量化合物、例えば麻薬または爆薬、を検出する機構および方法であって、帯電したコレクタ表面(該コレクタ表面は、該コレクタ表面の電荷と反対の電荷で空気中にある粒子をイオン化するイオナイザに接続されている)、所望により使用する空気攪拌手段、採集された材料を該コレクタ表面から抽出するための抽出手段、および該抽出された、採集された材料から該化合物を化学的および/または生物化学的に検出する装置を備えてなる機構および方法を開示する。さらに、該コレクタが、該装置の本体から伸びており、好ましくは取り外し可能な、帯電させることができる採集表面を備えており、所望により、装置の空気をイオン化する部分もイオナイザ/コレクタ装置の本体から、該伸びているコレクタアームと共に、またはそれとは別に、延長されている、変形されたイオナイザ/コレクタ装置を開示する。この装置は、バッテリー駆動および持ち運び可能であり、税関、空港警備および警察による、例えば麻薬または爆薬の検出に、あるいは地雷の検出に使用するのに好適である。  (もっと読む)
(もっと読む)
質量に基づく毒素アッセイおよびそのための基質
メタロプロテアーゼについてのアッセイは、(i)試験化合物を基質と混合する工程であって、ここで該プロテアーゼが該基質と反応して生成物を形成する、工程;および(ii)該メタロプロテアーゼの存在を該生成物の質量を測定することにより検出する工程を含む。 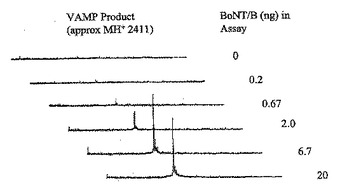 (もっと読む)
(もっと読む)
IMSシステム
IMSシステムは、端部に吸気口(2)を有するセル(1,101)を含む。解析すべきガス又は蒸気は、吸気口(2)からセル(1,101)に供給される。セル(1,101)における選択的障壁(6)は、選択した分子がイオン化領域(7)内を透過し、生成したイオンがゲート(8)を介してドリフト領域(9)に至る。前記イオンはセル(1,101)に沿ってコレクター(11)までドリフトし、電気的出力を生成する。システム(40,140)は、清浄かつ乾燥した空気をセル(1,101)の反対側の端部(30)に供給し、前記イオンの流れに抗してセル内を流す。システム(40)は、ドープされたモレキュラーシーブ(41)を含み、第1の試薬を連続して前記空気に付加し、セル中で選択したイオンと結合させる。システム(40)は、付加的な異なる試薬の追加の貯蔵室(42,43,44)を含む。この追加の試薬は、セル出力が示された際に前記第1の試薬に加えて前記空気に供給され、妨害イオンと結合する。 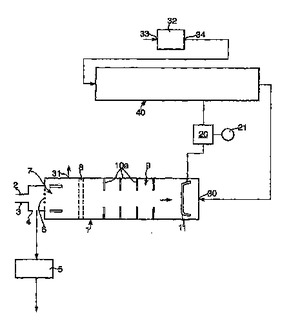 (もっと読む)
(もっと読む)
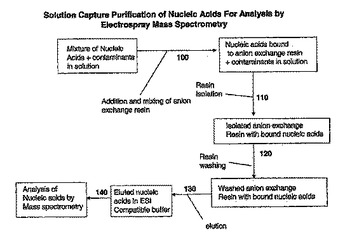
後の質量分析法を用いた分析のために、溶液捕獲によって核酸を迅速に精製する方法
本発明は、既存の方法と比較して効率的で費用効果的であるエレクトロスプレー質量分析法による後の分析のための、核酸の迅速な溶液捕獲精製法を提供する。精製された試料がエレクトロスプレー質量分析法による分析に良好な状態になるように、本発明は、核酸の迅速な溶液捕獲を実践するために有効なキットも提供する。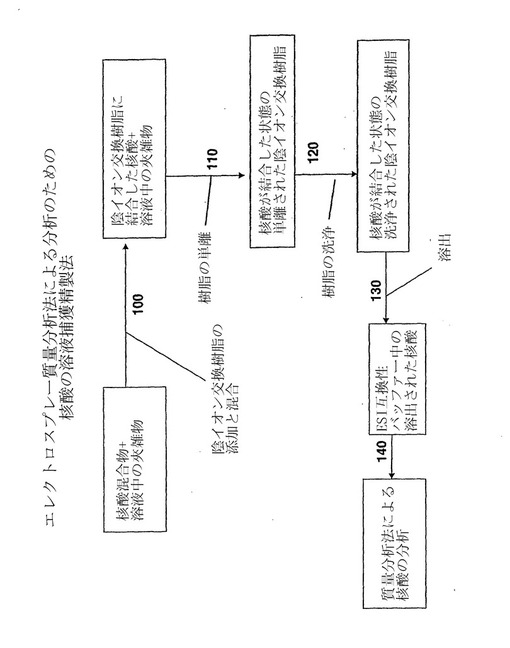
 (もっと読む)
(もっと読む)
質量分析法
方法は、
(a) 質量スペクトルの第1ピークを選択する、
(b) 前記第1ピークを生じることが可能な第1荷電状態を有する第1モノアイソトピック参照イオンを選択する、
(c) 前記第1参照イオンの1つ以上の他の同位体形態に対して前記質量スペクトル中で1つ以上の更なる予想ピークを決定する、
(d) 前記1つ以上の決定された更なる予想ピークに合致する1つ以上のピークが前記質量スペクトル中に存在するかどうかを決定するために、前記1つ以上の決定された更なる予想ピークを前記質量スペクトルと比較する、
(e) 前記1つ以上の決定された更なる予想ピークが前記質量スペクトル中の1つ以上のピークと合致すれば、前記第1ピークをデータピークとして指定し、及び任意で前記質量スペクトルに存在する前記1つ以上の決定された更なる予想ピークに合致する1つ以上のピークをデータピークとして指定する、
(f) 前記決定された更なる予想ピークが前記質量スペクトル中のピークに合致しなければ、1つ以上の更なる参照イオンを1つ以上の更なる荷電状態で、前記工程(b)から前記工程(e)を繰り返す、
(g) 任意で、前記第1荷電状態にある参照イオンあるいは更なる荷電状態にある更なる参照イオンについて、前記第1ピークがデータピークとして指定可能でなければ、前記第1ピークを非データピークとして指定する、
(h) 任意で、前記質量スペクトル中の1つ以上の更なるピークのために前記工程(a)から前記工程(g)を繰り返す、
工程を含むことを特徴とする試料から作成される質量スペクトルデータを処理する方法。
(もっと読む)
増大表面積用ナノファイバー表面
本発明は新規ナノファイバー増大表面積基板と前記基板を含む構造、及び前記基板の方法と使用を提供する。 (もっと読む)
リン酸化ペプチドおよび/またはタンパク質のアフィニティに基づく濃縮
本発明は、少なくとも2つの規定の基を含むスペーサーへリンカーによって結合した固相担体を含む物質に関する。前記物質は、リン酸化ペプチドおよび/またはタンパク質を濃縮および/または単離するためのアフィニティ材料としての使用に適している。本発明の物質は特に、チロシン−リン酸化ペプチドおよび/またはタンパク質を濃縮および/または単離することを可能にする。 (もっと読む)
2,661 - 2,670 / 2,683
[ Back to top ]

