マイクロリアクタ
【課題】 マイクロポンプによって複数の試薬をそれぞれの試薬収容部から下流側へ送出し、これらの試薬を合流させて混合し、得られた混合試薬をそのさらに下流において試料と合流させて反応部で反応を行う際に、混合比率が安定した混合試薬のみを後続する工程へ送出可能なマイクロリアクタを提供する。
【解決手段】 本発明のマイクロリアクタは、初期混合試薬を反応部に送出することを防止する送出防止機構を備えている。好ましい態様では、複数の試薬を混合する流路であって混合試薬7cの流れが停止される下流末端8が設けられた混合流路5cと、混合流路5cの中間部において分岐され、反応部へ混合試薬7cを送出する送出流路5dと、から前記送出防止機構が構成されており、初期混合試薬7dは、混合流路5cの中間部と下流末端8との間に収容されて送出流路5dから反応部への送出が防止される。
【解決手段】 本発明のマイクロリアクタは、初期混合試薬を反応部に送出することを防止する送出防止機構を備えている。好ましい態様では、複数の試薬を混合する流路であって混合試薬7cの流れが停止される下流末端8が設けられた混合流路5cと、混合流路5cの中間部において分岐され、反応部へ混合試薬7cを送出する送出流路5dと、から前記送出防止機構が構成されており、初期混合試薬7dは、混合流路5cの中間部と下流末端8との間に収容されて送出流路5dから反応部への送出が防止される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、例えば、遺伝子増幅反応、抗原抗体反応などによる生体物質の検査・分析、その他の化学物質の検査・分析、有機合成等による目的化合物の化学合成などに用いられるマイクロリアクタに関するものであり、特に、複数の試薬を混合した混合試薬と試料とを混合して反応させる際に、安定した混合比率の混合試薬を後続する工程へ送出する技術の改良に関する。
【背景技術】
【0002】
近年、マイクロマシン技術および超微細加工技術を駆使することにより、従来の試料調製、化学分析、化学合成などを行うための装置、手段(例えばポンプ、バルブ、流路、セ
ンサーなど)を微細化して1チップ上に集積化したシステムが開発されている(特許文献
1)。これは、μ−TAS(Micro total Analysis System)、バイオリアクタ、ラブ・
オン・チップ(Lab-on-chips)、バイオチップとも呼ばれ、医療検査・診断分野、環境測定分野、農産製造分野でその応用が期待されている。現実には遺伝子検査に見られるように、煩雑な工程、熟練した手技、機器類の操作が必要とされる場合には、自動化、高速化および簡便化されたミクロ化分析システムは、コスト、必要試料量、所要時間のみならず、時間および場所を選ばない分析を可能とすることによる恩恵は多大と言える。
【0003】
各種の分析、検査ではこれらの分析用チップにおける分析の定量性、解析の精度、経済性などが重要視される。そのためにはシンプルな構成で、高い信頼性の送液システムを確立することが課題である。精度が高く、信頼性に優れるマイクロ流体制御素子が求められている。これに好適なマイクロポンプシステムおよびその制御方法を本発明者らはすでに提案している(特許文献2〜4)。
【0004】
微細流路内で各成分の反応を行う上記のような分析用チップでは、微細流路内でこれらの成分を合流させて混合する工程が必要となる(特許文献5)。例えば、分析対象の試料と反応させる試薬が複数である場合には、予め複数の試薬を微細流路内で合流させて混合試薬を得る必要がある。
【特許文献1】特開2004−28589号公報
【特許文献2】特開2001−322099号公報
【特許文献3】特開2004−108285号公報
【特許文献4】特開2004−270537号公報
【特許文献5】特開2005−66400号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかし、複数の試薬を合流させて混合する際に、マイクロポンプによって各試薬を合流部へ同じタイミングで送り出したとしても、タイミングが高精度に合っていない限り、液の先頭部分では各試薬の混合比率を安定させることが難しい。この先頭部分の初期混合試薬を下流において試料と合流させて反応を行うと、この先頭部分では混合比率が安定していないので不具合が生じる場合が多い。
【0006】
本発明は、マイクロポンプによって複数の試薬をそれぞれの試薬収容部から下流側へ送出し、これらの試薬を合流させて混合し、得られた混合試薬をそのさらに下流において試料と合流させて反応部で反応を行う際に、混合比率が安定した混合試薬のみを後続する工程へ送出可能なマイクロリアクタを提供することを目的としている。
【課題を解決するための手段】
【0007】
本発明のマイクロリアクタは、板状のチップと、
複数の試薬が個別に収容される収容室からなる複数の試薬収容部と、
前記複数の試薬収容部から送出される複数の試薬を混合して混合試薬を生成する試薬混合部と、
外部から試料を注入するための注入口を有する試料受容部と、
前記試薬混合部から送出される混合試薬と、前記試料受容部から送出される試料とを混合して反応させる反応部と、を備え、
前記複数の試薬収容部、試薬混合部、試料受容部および反応部は、前記チップ内に組み込まれて流路により互いに連通され、
前記試薬混合部において生成された混合試薬のうち、初期に混合された初期混合試薬を前記反応部に送出することを防止する送出防止機構を備えることを特徴とする。
【0008】
上記の発明における好ましい態様では、前記試薬混合部は、前記複数の試薬を混合する流路であって混合試薬の流れが停止される下流末端が設けられた混合流路からなり、
該混合流路の中間部において、前記反応部へ混合試薬を送出する送出流路が分岐され、
前記送出防止機構は、前記混合流路と送出流路とから構成されており、
前記初期混合試薬は、前記混合流路の中間部と下流末端との間に収容されて前記送出流路から前記反応部への送出が防止される。
【0009】
この場合、前記送出防止機構は、前記混合流路と送出流路との接続部に、混合流路内の圧力が所定圧以上となった際に送出流路へ混合試薬を送出する送液制御部を備えることが好ましい。
【0010】
このような送液制御部は、前記混合流路と送出流路との接続部における送出流路側に設けられた、送出流路の断面積よりも小さい断面積を有する細流路で構成することができる。
【0011】
上記の発明では、混合当初の初期混合試薬を混合流路の下流末端側へトラップして切り捨てるようにしたので、試薬同士の合流のタイミングが多少ずれていても、混合比率が安定した混合試薬のみを後続する工程へ送り出すことができる。
【発明の効果】
【0012】
本発明によれば、試薬同士の合流のタイミングが多少ずれていても、混合比率が安定した混合試薬のみを後続する工程へ送り出すことができる。
【発明を実施するための最良の形態】
【0013】
以下、図面を参照しながら本発明について詳細に説明する。本発明のマイクロリアクタは、板状のチップ内に設けられた微細流路または構造部において、各種の検査、化学分析、化学合成、試料の処理・分離などの目的で試料と試薬との反応を行うものである。
【0014】
本発明のマイクロリアクタの用途には、例えば、遺伝子増幅反応、抗原抗体反応などによる生体物質の検査・分析、その他の化学物質の検査・分析、有機合成などによる目的化合物の化学合成、薬効スクリーニング、薬品抽出、金属錯体の形成・分離などが含まれる。
【0015】
本発明のマイクロリアクタは、板状のチップ内に、
(i)複数の試薬が個別に収容される収容室からなる複数の試薬収容部
(ii)前記複数の試薬収容部から送出される複数の試薬を混合して混合試薬を生成する試薬混合部
(iii)外部から試料を注入するための注入口を有する試料受容部
(iv)前記試薬混合部から送出される混合試薬と、前記試薬受容部から送出される試料とを混合して反応させる反応部
を備えている。
【0016】
前記複数の試薬収容部、試薬混合部、試料受容部および反応部は、前記チップ内に組み込まれて流路により互いに連通されている。
上記の各部の他、チップ内には、必要に応じて、各種の機能をもつ構造部が設けられる。このような構造部の具体例としては、送液を制御するための部位、試料および試薬以外の処理液を収容するための収容部、生体試料等に含まれる不要成分を除去するために試薬との反応に先立って前処理を行うための前処理部、反応後の液に含まれる標的物質等を検出するための検出部、廃液を貯留するための廃液貯留部、液を送出するためのマイクロポンプなどが挙げられる。
【0017】
送液を制御するための部位の具体例としては、逆止弁、能動弁のような弁部などが挙げられる。
各処理液を収容するための収容部の具体例としては、流路壁、ビーズ等の担体などに必要物質を吸着させた状態で洗浄を行うための洗浄液の収容部、試薬と試料との反応を停止させる反応停止液の収容部、反応生成物を検出に適するように変性させるための変性処理液の収容部、光学的検出のために反応生成物を蛍光物質等で標識するための標識用試薬の収容部、その他、抽出液、溶離液、溶菌試薬、溶血試薬等の収容部などが挙げられる。
【0018】
検出部は、マイクロリアクタ内における反応生成物を光学的に検出する場合には、例えば、光透過性の部材を用いて形成された流路部位または液溜状の部位から構成される。
前処理部は、試料に含まれる分析対象物の濃縮、分離、溶菌等を行う部位であり、例えば、生体試料に含まれるタンパク質やイオン性物質等の除去が行われる。このような処理は、例えば、フィルター、ビーズ、ゲル、メンブレンなどの担体を流路内に配置し、この担体に生体物質等を吸着させて該流路内に溶菌試薬、溶血試薬等を流し、次いで洗浄液を流すことにより行うことができる。
【0019】
廃液貯留部は、例えば、所要の大きさをもつ凹部が形成された基材を、流路用の基材の下部側に貼り合わせることによって設けられた、流路と連通する空間により構成される。必要に応じて、該空間にはスポンジ等の廃液吸収用の多孔体が収納される。
【0020】
マイクロポンプは、試薬収容部に収容された各試薬、他の収容部に収容された液などの各液を流路下流側へ送出する。マイクロポンプは通常、送出すべき液に対応して複数個が設置され、それぞれのマイクロポンプは水性または油性の駆動液を下流側へ送出し、試料や試薬等の液を駆動液で下流側へ押し出して送液を行う。
【0021】
マイクロポンプは、マイクロリアクタに直接形成する場合もあるが、マイクロリアクタとは別途に、すなわち板状のチップとは独立して設置することができる。例えば、マイクロポンプおよびその制御装置、反応検出用の光学検出装置、温度制御装置、駆動液を収容した駆動液タンクなどを備えた装置本体と、予め試薬を封入したマイクロリアクタと、から試料検査装置を構成する場合が挙げられる。
【0022】
この場合、マイクロリアクタの試料受容部に試料を注入した後、このマイクロリアクタを装置本体に装着して、装置本体側の複数のマイクロポンプと、これらのマイクロポンプに対応するマイクロリアクタの各流路とを連通させる。この状態で、駆動液タンクからの駆動液をマイクロポンプによりマイクロリアクタの流路へ送り出し、これによって流路内の液、例えば試薬収容部の試薬、試料受容部の試料などを下流側へ押し出して試薬同士の
混合、試薬と試料との混合などを行う。
【0023】
マイクロポンプは、フォトリソグラフィ技術などにより作製され、特開2001−322099号公報、特開2004−108285号公報に記載されたピエゾ素子により駆動するマイクロポンプ、アクチュエータを設けた弁室の流出入孔に逆止弁を設けた逆止弁型のマイクロポンプなど各種のものが使用できる。なお、上記のピエゾ素子により駆動するマイクロポンプは、流路抵抗が差圧に応じて変化する第1流路と、差圧の変化に対する流路抵抗の変化割合が第1流路よりも小さい第2流路と、第1流路および第2流路に接続された加圧室と、該加圧室の内部圧力を変化させるピエゾアクチュエータとを備えており、このアクチュエータを別途の制御装置により電圧で駆動することにより正逆方向への送液ができるようになっている。
【0024】
マイクロリアクタは、板状の基材を用いて、フォトリソグラフィ技術などの微細加工技術を適用して作製される。通常は、流路および構造部となる凹部を1または2以上の基材に形成した後、複数枚の基材を貼り合わせることによってマイクロリアクタを作製する。
【0025】
マイクロリアクタを構成する基材の材料には、目的に応じて各種のものが使用される。その具体例としては、ポリスチレンなどのプラスチック樹脂、ポリジメチルシロキサンなどのゴム系材料、各種の無機ガラス、シリコン、セラミックス、金属などが挙げられる。また、流路壁面に対して、目的に応じて疎水化処理、親水化処理などの各種の表面処理を行ってもよい。
【0026】
マイクロリアクタにおける流路幅のサイズは、マイクロスケール空間の利点、流路抵抗などを考慮して適宜に設計されるが、例えば、幅が数十〜数百μm、好ましくは50〜200μmであり、深さが25〜300μm、好ましくは50〜100μmである。マイクロリアクタのチップ全体の縦横サイズは、用途等にもよるが、典型的には数十mm、その高さは典型的には数mm程度である。
【0027】
本発明のマイクロリアクタにおける試料受容部は、試料を一時収容する収容室と、外部から収容室へ試料を注入するための注入口とを備えている。この収容室は、流路形状、液溜形状など各種の形状であってよい。
【0028】
試料受容部の注入口は、例えば、チップ上面から微量試料を注入できるように構成されている。外部への漏失、汚染、生体試料を使用する場合の感染などを防ぎ、密封性を確保するために、ゴム状材質などの弾性体からなる栓が注入口に形成されているか、あるいはポリジメチルシロキサンなどのゴム材、強化フィルム等で注入口が覆われていることが望ましい。例えば、ゴム材質の栓に突き刺したニードルまたは蓋付き細孔に通したニードルでシリンジ内の試料を注入する。前者の場合、ニードルを抜くとその針穴が直ちに塞がることが好ましい。また、これら以外の試料注入機構を設置してもよい。
【0029】
試料受容部の上流側は、マイクロポンプに連通される流路に連通し、その下流側は、試薬との混合部に連通している。試料受容部に注入された試料は、マイクロポンプによって供給された駆動液により下流側へ押し出され、必要に応じて前処理された後、試薬と混合される。
【0030】
試料受容部に注入される試料は、目的に応じて各種のものが対象となる。例えば、生体物質の検査・分析を行う場合には、生体由来のアナライト含有試料、例えば全血、血漿、血清、バフィーコート、尿、糞便、唾液、喀痰などが挙げられる。遺伝子検査の場合、増幅反応の鋳型となる核酸として遺伝子、DNAまたはRNAがアナライトである。また、このような核酸を含む可能性のある試料から調製または単離したものを試料としてもよい
。他のアナライトとしては、各種の代謝物質、ホルモン、タンパク質(酵素、抗原なども含む)などが挙げられる。
【0031】
その他、化学合成を目的とする場合には、試薬と反応させる原料化合物が試料となり、薬効スクリーニング、薬品抽出、金属錯体の形成・分離などを目的とする場合には、それらを行うために試薬と反応させる対象が試料となる。
【0032】
本発明のマイクロリアクタにおける試薬収容部は、試薬を収容する収容室から構成されている。この収容室は、流路形状、液溜形状など各種の形状であってよい。試薬収容部の上流側は、マイクロポンプに連通される流路に連通し、その下流側は、他の試薬との混合部に連通している。試薬収容部に収容された試薬は、マイクロポンプによって供給された駆動液により下流側へ押し出され、他の試薬と合流して混合される。
【0033】
試薬は、目的に応じて各種のものが対象となる。例えば、PCR法により検体中に含まれる遺伝子を増幅する場合における試薬には、少なくとも2'−デオキシヌクレオシド5'−三リン酸のほか、Taq DNAポリメラーゼ、Vent DNAポリメラーゼまたはPfu DN
Aポリメラーゼが含まれる。
【0034】
また、特許第3433929号に記載されたICAN(Isothermal chimera primer initiated nucleic acid amplification )法により検体中に含まれる遺伝子を増幅する場
合における試薬には、少なくとも2'−デオキシヌクレオシド5'−三リン酸、検出したい遺伝子に特異的にハイブリダイゼーションできるキメラプライマー、鎖置換活性を有するDNAポリメラーゼ、エンドヌクレアーゼのRNaseが含まれる。
【0035】
その他、化学合成を目的とする場合には、試料と反応させる原料化合物などが試薬となり、薬効スクリーニング、薬品抽出、金属錯体の形成・分離などを目的とする場合には、それらを行うために試料と反応させる物質などが試薬となる。
【0036】
遺伝子検査などの用途では、場所や時間を問わず迅速に検査ができるように、試薬収容部に予め試薬が収容されていることが望ましい。この場合、内蔵される試薬の蒸発、漏失、気泡の混入、汚染、変性などを防止するため、試薬収容部の上流側および下流側を封止することが好ましい。
【0037】
試薬収容部の封止は、封止剤により行うことができる。この封止剤は、使用前にマイクロリアクタが保管される冷蔵条件下では、固化もしくはゲル化しており、使用時、室温にすると融解し流動状態となるものである。例えば、油脂、ゼラチンの水溶液などを使用することができる。
【0038】
また、試薬収容部の収容室の上流側端部または下流側端部、あるいはこれらの両方に、後述する図4の撥水バルブを設けてもよい。これによって、マイクロリアクタの保管時における試薬の外部への流出を有効に防止できると共に、使用時には、マイクロポンプによって容易に試薬を外部へ押し出すことができる。
【0039】
反応部では、試料と混合試薬との混合液が導入された後、例えば、昇温などにより反応が開始される。反応部は、液溜形状、流路形状など各種の形状であってよく、例えば試料と混合試薬とを液溜に貯留して反応を行う態様、試料と混合試薬とを微細流路内に合流させて、合流液の送液方向をマイクロポンプにより切り替えて、合流液を微細流路内で繰り返し前後動させながら反応させる態様など、試料と試薬の種類等に応じて適宜の反応形態とすることができる。
【0040】
以上に説明したマイクロリアクタにおいて、マイクロポンプによって複数の試薬をそれぞれの試薬収容部から下流側へ送出し、これらの試薬を合流させて混合し、得られた混合試薬をそのさらに下流において試料と合流させて反応部で反応を行うのであるが、複数の試薬を合流させて混合する際に、各試薬を合流部へ同じタイミングで送り出したとしても、タイミングが高精度に合っていない限り、液の先頭部分では各試薬の混合比率を安定させることが難しい。この先頭部分の初期混合試薬を下流において試料と合流させて反応を行うと、この先頭部分では混合比率が安定していないので不具合が生じる場合が多い。そのため、混合比率が安定してから混合試薬を次工程へ送り出すことが望ましい。
【0041】
そこで本発明では、複数の試薬収容部から送出される複数の試薬を混合して混合試薬を生成する試薬混合部において生成された混合試薬のうち、初期に混合された初期混合試薬を前記反応部に送出することを防止する送出防止機構を備えている。以下、図1〜図3および図5〜図7を参照しながら初期混合試薬の送出防止機構について説明する。
【0042】
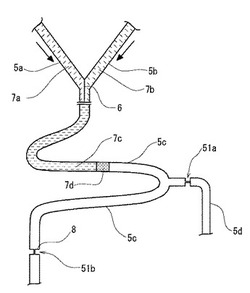
図1は、本発明の一実施例におけるマイクロリアクタが備える、初期混合試薬の送出防止機構の構成を示した図である。本実施例では、試薬7aと試薬7bとの2種類の試薬により混合試薬7cを得る場合を示している。
【0043】
同図において、5aは試薬7aが送出される流路であり、その上流側は、試薬7aが収容される試薬収容部(図示せず)に連通している。
5bは、試薬7bが送出される流路であり、その上流側は、試薬7bが収容される試薬収容部(図示せず)に連通している。
【0044】
5cは、試薬7aと試薬7bとを混合して混合試薬7cを生成する混合流路(試薬混合部)であり、流路5aと流路5bとの合流部6から、混合試薬7cの流れが停止される下流末端8までの流路で構成されている。
【0045】
混合流路5cの中間部では、下流の反応部(図示せず)へ混合試薬7cを送出する送出流路5dが分岐されている。送出流路5dは、混合流路5cとの分岐点から先の流路で構成されている。
【0046】
混合流路5cと送出流路5dとの接続部における送出流路5d側には、撥水バルブ51aが設けられている。この撥水バルブ(送液制御部)は、図4に示した構造を備えている。同図の撥水バルブ51は、細径の送液制御通路52を備えている。送液制御通路52は、その断面積(流路に対して垂直な断面の断面積)が、上流側の流路53aおよび下流側の流路53bの断面積よりも小さい細流路である。
【0047】
流路壁がプラスチック樹脂などの疎水性の材質で形成されている場合には、送液制御通路52に接する液54は、流路壁との表面張力の差によって、下流側の流路53bへ通過することが規制される。
【0048】
下流側の流路53bへ液54を流出させる際には、マイクロポンプによって所定圧以上の送液圧力を加え、これによって表面張力に抗して液54を送液制御通路52から下流側の流路53bへ押し出す。液54が流路53bへ流出した後は、液54の先端部を下流側の流路53bへ押し出すのに要する送液圧力を維持せずとも液が下流側の流路53bへ流れていく。すなわち、上流側から下流側への正方向への送液圧力が所定圧力に達するまで送液制御通路52から先への液の通過が遮断され、所定圧以上の送液圧力が加わることにより液54は送液制御通路52を通過する。
【0049】
流路壁がガラスなどの親水性の材質で形成されている場合には、少なくとも送液制御通
路52の内面に、撥水性のコーティング、例えばフッ素系のコーティングを施す必要がある。
【0050】
図1において、初期混合試薬7dは、以下に説明する作用により、混合流路5cの送出流路5dとの分岐点において、下流末端8側へ選択的に送り出され、混合流路5cの下流側にトラップされる。これにより、初期混合試薬7dが送出流路5d側へ流出することが防止される。
【0051】
図1に示したように、マイクロポンプにより試薬収容部から流路5aへ送り出された試薬7aと、別途のマイクロポンプにより他の試薬収容部から流路5bへ送り出された試薬7bとは、合流部6で合流し、混合流路5cで混合される。
【0052】
この際、マイクロポンプによる混合試薬7cの送液圧力を、初期混合試薬7dおよび混合試薬7cが撥水バルブ51aを通過可能な圧力よりも小さな圧力として混合流路5c内の混合試薬7cを送液する。これにより、図2に示したように、混合流路5cと送出流路5dとの接続部において、初期混合試薬7dは送出流路5d側には流出せずに混合流路5cの下流末端8側へ送り出される。
【0053】
そして、初期混合試薬7dが混合流路5cの下流末端8に達した後、マイクロポンプによる混合試薬7cの送液圧力を、混合試薬7cが撥水バルブ51aを通過可能な圧力以上の圧力とする。これにより、図3に示したように、混合流路5c内の混合試薬7cは、撥水バルブ51aを通過し、混合試薬7cは送出流路5dに流出する。
【0054】
以上のようにマイクロポンプによる送液圧力を制御することで、初期混合試薬7dは混合流路5cの中間部と下流末端8との間に収容され、送出流路5dには、初期混合試薬7dが切り捨てられた混合試薬7cのみが送出される。すなわち、混合比率が安定した混合試薬だけを後続する工程へ供給することができる。
【0055】
なお、本実施例では、混合流路5cの下流末端8にも撥水バルブ51bを設けている。この撥水バルブ51bは、初期混合試薬7dが下流側の流路へ通過可能な送液圧力が、撥水バルブ51aにおいて混合試薬7cが送出流路5d側へ通過可能な送液圧力よりも大きい撥水バルブである。
【0056】
したがって、初期混合試薬7dが混合流路5cの下流末端8に達した後、マイクロポンプによる混合試薬7cの送液圧力を、混合試薬7cが撥水バルブ51aを通過可能であり、且つ、初期混合試薬7dが撥水バルブ51bを通過できない圧力とすることで、図3に示したように、混合試薬7cを撥水バルブ51aの先へ通過させると共に、混合流路5cの下流末端8において初期混合試薬7dが撥水バルブ51bの先へ通過することを防止できる。
【0057】
例えば、撥水バルブ51aにおける送液制御通路(図4の符号52)の断面積を、撥水バルブ51bにおける送液制御通路の断面積よりも大きくすることによって、これらの送液制御通路を液が通過可能な送液圧力に差をもたせることができる。この他、場合によっては、撥水バルブ51aと撥水バルブ51bとの間で、液と送液制御通路の流路壁との表面張力差を相違させることで、液が通過可能な送液圧力に差をもたせることも考えられる。
【0058】
例えば、撥水バルブ51bよりも先の流路は、廃液貯留部に連通される。この場合、全ての反応、検出工程を終えた後などの適切な時期に、混合流路5cの中間部と下流末端8との間に収容された初期混合試薬7dおよび混合試薬7cを、マイクロポンプの送液圧力
を上げることによって撥水バルブ51bよりも先の流路へ押し出し、その先の廃液貯留部に収容する。
【0059】
なお、本実施例では混合流路5cの下流末端8にこのような撥水バルブ51bを設けたが、下流末端8に撥水バルブ51bを設けずに、下流末端8完全に封止する構造としてもよい。
【0060】
図5は、本発明の他の実施例におけるマイクロリアクタが備える、初期混合試薬の送出防止機構の構成を示した図である。なお、図1〜図3と対応する構成要素は同一の符号で示しその詳細な説明を省略する。
【0061】
本実施例では、基本的な構成は上述した実施例と同様であるが、混合流路5cと送出流路5dとの接続部における送出流路5d側に、能動弁9が設けられている。初期混合試薬7dは、以下に説明する作用によって、混合流路5cの送出流路5dとの分岐点において、選択的に下流末端8側へ送り出され、混合流路5cの下流側にトラップされる。これにより、初期混合試薬7dが送出流路5d側へ流出することが防止される。
【0062】
図5に示したように、マイクロポンプにより試薬収容部から流路5aへ送り出された試薬7aと、別途のマイクロポンプにより他の試薬収容部から流路5bへ送り出された試薬7bとは、合流部6で合流し、混合流路5cで混合される。
【0063】
この際、能動弁9は閉止した状態になっており、図6に示したように、混合流路5cと送出流路5dとの接続部において、初期混合試薬7dは送出流路5d側には流出せずに混合流路5cの下流末端8側へ送り出される。
【0064】
そして、初期混合試薬7dが混合流路5cと送出流路5dとの分岐点を通過した後、能動弁9を開放する。これにより、図7に示したように、混合流路5c内の混合試薬7cは、能動弁9を通過し、混合試薬7cは送出流路5dに流出する。
【0065】
以上のように能動弁9を制御することで、初期混合試薬7dは混合流路5cの中間部と下流末端8との間に収容され、送出流路5dには、初期混合試薬7dが切り捨てられた混合試薬7cのみが送出される。すなわち、混合比率が安定した混合試薬だけを後続する工程へ供給することができる。
【0066】
なお、能動弁9として、公知である各種の構造のものをマイクロリアクタに形成することができる。例えば、空気圧ピストン、油圧ピストン、水圧ピストン、圧電アクチュエータ、形状記憶合金アクチュエータなどにより、柔軟な材質からなる基材を上方から押圧して、この基材の下方に配置された開口を覆って流路を塞ぐ構造の能動弁、弁体としてバイメタルを使用し、通電加熱により弁体を変形させて流路を塞ぐ構造の能動弁、弁体として形状記憶合金を使用し、通電加熱により弁体を変形させて流路を塞ぐ構造の能動弁などが使用できる。弁の開閉制御は、外部の制御装置による電圧駆動などによって行う。
【0067】
以上に説明した、本発明のマイクロリアクタが備える初期混合試薬の送出防止機構は、混合流路と送出流路とから構成されており、初期混合試薬は、混合流路の中間部と下流末端との間に収容されて送出流路から反応部への送出が防止される。
【0068】
このような初期混合試薬の送出防止機構を備えた2つの実施例について説明したが、この他、例えば混合流路の断面積と、送出流路の断面積とを相違させることにより、毛細管力によって初期混合試薬を選択的に混合流路の流路末端側へ導くことで、初期混合試薬の送出流路側への送出を防止できる。
【0069】
あるいは、混合流路の流路壁の表面張力と、送出流路の流路壁の表面張力とを、流路材質または流路壁の表面処理等により相違させ、表面張力によって初期混合試薬を選択的に混合流路の流路末端側へ導くことで、初期混合試薬の送出流路側への送出を防止できる。
【0070】
図8は、本発明の他の実施例におけるマイクロリアクタの流路構成を示した図であり、試料との混合部よりも上流側の流路構成を示している。
3種類の各試薬は、試薬収容部33h、33i、33jのそれぞれに収容され、各試薬収容部の上流側には、マイクロリアクタとは別途の装置に内蔵されたマイクロポンプ12h,12i,12jがポンプ接続部31で接続され、各試薬収容部から下流側の混合流路5cへこれらのマイクロポンプにより試薬が送液される。
【0071】
混合流路5cと、混合流路5cから分岐した送出流路5dと、撥水バルブ51a、51bは、図1と同様な初期混合試薬の送出防止機構を構成しており、試薬収容部33h、33i、33jから送出され混合流路5cで合流した各試薬の混合液の先端部を切り捨て、混合状態が安定した後に混合試薬を次工程へ送出するようにしている。
【0072】
図9は、本発明のマイクロリアクタの他の実施例を示した平面図である。本実施例のマイクロリアクタ1には、試薬の収容室である流路状の試薬収容部33a、33b、33cのそれぞれに3種類の試薬が収容されている。これらの試薬収容部の両端部(試薬収容部33aでは上流側の端部34aおよび下流側の端部34b)には、図4に示した構造の撥水バルブが設けられ、これらの撥水バルブの間の流路に試薬が封入されている。
【0073】
なお、詳細な説明は省略するが、図9のマイクロリアクタ1の微細流路には、試薬収容部33a〜33cの両端部以外の位置にも図4の撥水バルブが設けられており、例えば、混合試薬と試料との合流部38における混合試薬の入口と試料の入口などにも上記の撥水バルブが設けられており、この撥水バルブによってその先の流路への送液開始のタイミングが制御される。
【0074】
図9の試薬収容部33a〜33cの上流側には、マイクロリアクタ1の一方の面から外部へ開放された開口32c〜32eが設けられている。これらの開口32c〜32eは、マイクロリアクタ1を後述するマイクロポンプユニットに重ね合わせて接続した際に、マイクロポンプユニットの接続面に設けられた流路開口と位置合わせされてマイクロポンプに連通される。
【0075】
なお、開口32a,32bおよび32f〜32kも同様に、マイクロリアクタ1とマイクロポンプユニットとの接続によってマイクロポンプに連通される。これらの開口32a〜32kを含むチップ面によってポンプ接続部が構成され、ポンプ接続部をマイクロポンプユニットの接続面に密着させることによってマイクロリアクタ1とマイクロポンプユニットとが接続される。
【0076】
このポンプ接続部は、必要なシール性を確保して駆動液の漏出を防止するために、ポリテトラフルオロエチレン、シリコーン樹脂などの柔軟性(弾性、形状追随性)をもつ樹脂によって密着面が形成されることが好ましい。このような柔軟性を有する密着面は、例えばマイクロリアクタの構成基材自体によるものであってもよく、また、ポンプ接続部における流路開口の周囲に貼着された柔軟性を有する別途の部材によるものであってもよい。
【0077】
試薬収容部33a〜33cに収容された試薬は、開口32c〜32eに連通するそれぞれ別途のマイクロポンプによって、試薬収容部33a〜33cの下流側端部に設けられた撥水バルブ(図示せず)を通過して合流部35へ流れ込み、その先に続く流路である混合
流路5c(試薬混合部36)で3種類の各試薬が混合される。
【0078】
なお、この混合流路5cと、送出流路5dとを含む流路系によって、図1または図5の実施例に示したような初期混合試薬の送出防止機構が構成されており、初期混合試薬を混合流路5cの流路末端8にトラップするようにしている。
【0079】
混合流路5cで混合され送出流路5dに送り出された混合試薬は、試料受容部37に収容された試料と合流部38で合流する。なお、混合試薬は開口32bに連通したマイクロポンプによって駆動液で下流へ押し出され、試料は開口32aに連通したマイクロポンプによって駆動液で下流へ押し出される。混合試薬と試料との混合液は、反応部39へ収容され加熱等によって反応が開始される。
【0080】
反応後の液は、検出部40へ送液され、例えば光学的な検出方法などによって標的物質が検出される。なお、開口32f〜32jに連通するそれぞれ別途のマイクロポンプによって、これらの開口から先の流路に予め収容された各試薬(例えば混合試薬と試料との反応を停止させる液、検出対象の物質に対して標識などの必要な処理を行うための液、洗浄液など)を所定のタイミングで下流へ押し出して送液するようにしている。
【0081】
図10は、図9のマイクロリアクタに使用されるマイクロポンプユニットの斜視図、図11は、その断面図である。このマイクロポンプユニット11は、シリコン製の基板17と、その上のガラス製の基板18と、その上のガラス製の基板19との3つの基板から構成されている。基板17と基板18、および基板18と基板19はそれぞれ、陽極接合によって接合されている。
【0082】
シリコン製の基板17と、その上に陽極接合によって貼り合わされたガラス製の基板18との間の内部空間によってマイクロポンプ12(ピエゾポンプ)が構成されている。
基板17は、シリコンウエハをフォトリソグラフィ技術により所定の形状に加工したものである。例えば、シリコン基板面への酸化膜の形成、レジスト塗布、レジストの露光および現像、酸化膜のエッチング、ICP(高周波誘導結合型プラズマ、Inductively Coupled Plasma)などによるシリコンのエッチング等を含む微細加工によって、加圧室22、第1流路23、第1液室25、第2流路24、および第2液室26が形成されている。
【0083】
加圧室22の位置では、シリコン基板がダイヤフラムに加工され、その外側表面には、チタン酸ジルコン酸鉛(PZT)セラミックスなどからなる圧電素子21が貼着されている。
【0084】
このマイクロポンプ12は、圧電素子21への制御電圧によって次のように駆動される。印加された所定波形の電圧により圧電素子21が振動すると共に、加圧室22の位置におけるシリコンダイヤフラムが振動し、これによって加圧室22の体積が増減する。第1流路23と第2流路24とは、幅および深さが同じで、長さが第1流路23よりも第2流路24の方が長くなっている。第1流路23では、差圧が大きくなると、流路内で乱流が発生し、流路抵抗が増加する。一方、第2流路24では、流路幅が長いので差圧が大きくなっても層流になり易く、第1流路23に比べて差圧の変化に対する流路抵抗の変化割合が小さくなる。
【0085】
例えば、圧電素子21に対する制御電圧を調整することにより、加圧室22の内部へ向かう方向へ素早くシリコンダイヤフラムを変位させて大きい差圧を与えながら加圧室22の体積を減少させ、次いで加圧室22からその外側へ向かう方向へゆっくりシリコンダイヤフラムを変位させて小さい差圧を与えながら加圧室22の体積を増加させると、駆動液は図11において左から右へ向かう方向へ正方向に送液される。
【0086】
これとは反対に、加圧室22からその外側へ向かう方向へ素早くシリコンダイヤフラムを変位させて大きい差圧を与えながら加圧室22の体積を増加させ、次いで加圧室22の内部へ向かう方向へゆっくりシリコンダイヤフラムを変位させて小さい差圧を与えながら加圧室22の体積を減少させると、駆動液は図11の右から左へ逆方向に送液される。
【0087】
なお、第1流路23と第2流路24における、差圧の変化に対する流路抵抗の変化割合の相違は、必ずしも流路の長さの違いによる必要はなく、他の形状的な相違に基づくものであってもよい。
【0088】
マイクロポンプ12による流量の制御は、圧電素子21に印加する電圧を調整することにより行うことができる。
基板19には、流路20がパターニングされている。一例として、流路20の寸法および形状は、幅が150μm程度、深さが300μm程度の断面矩形状である。流路20の下流側には、図9のマイクロリアクタの開口32a〜32kに位置合わせすることによりマイクロポンプ12を検査チップの微細流路に連通させるための開口15が設けられている。
【0089】
流路20の上流側は、基板18の貫通孔16bを介して、基板17に設けられた流路を通りマイクロポンプ12に連通されている。また、マイクロポンプ12の上流側は、基板17に設けられた流路から基板18の貫通孔16aを介して、ガラス製の基板19に設けられた開口14に連通されている。この開口14は不図示の駆動液タンクに接続されている。開口14は、例えば、PDMS(ポリジメチルシロキサン)のパッキンを介して駆動液タンクに接続される。
【0090】
開口15a,15b,15cはそれぞれ、図9のマイクロリアクタの開口32c,32d,32eと連通される(なお、図10ではマイクロポンプユニット全体のうち一部分のみ示している)。マイクロポンプ12によって、流路20、開口15a、開口32cを通じて駆動液を送液して試薬収容部33aに収容された試薬を下流へ押し出し、流路20、開口15b、開口32dを通じて駆動液を送液して試薬収容部33bに収容された試薬を下流へ押し出し、流路20、開口15c、開口32eを通じて駆動液を送液して試薬収容部33cに収容された試薬を下流へ押し出す。
【0091】
マイクロリアクタは、例えば、別途のシステム本体に装着することにより反応と分析が行われる。このシステム本体とマイクロリアクタとによりマイクロ総合分析システムが構成される。このマイクロ総合分析システムの一例を以下に説明する。図12は、マイクロ総合分析システムの一例を示した斜視図、図13は、このマイクロ総合分析システムにおけるシステム本体の内部構成を示した図である。
【0092】
このマイクロ総合分析システム2のシステム本体3は、分析のための各装置を収納する筺体状の収納体62を備えている。この収納体62の内部には、マイクロリアクタ1に連通させるための流路開口を有するチップ接続部13と、複数のマイクロポンプ(図示せず)とが設けられたマイクロポンプユニット11が配置されている。
【0093】
さらに収納体62の内部には、マイクロリアクタ1における反応を検出するための検出処理装置(LED、光電子増倍菅、CCDカメラ等の光源68および、可視分光法、蛍光測光法などによる光学的な検出を行う検出器69)と、この検出処理装置とマイクロポンプユニット11とを制御する制御装置(図示せず)とが設けられている。この制御装置によって、マイクロポンプによる送液の制御、光学的手段等によりマイクロリアクタ1における反応を検出する検出処理装置の制御の他、後述する加熱・冷却ユニットによるマイク
ロリアクタ1の温度制御、マイクロリアクタ1における反応の制御、データの収集(測定)および処理等を行う。マイクロポンプの制御は、予め送液順序、流量、タイミングなどに関する諸条件が設定されたプログラムに従って、それに応じた駆動電圧をマイクロポンプに印加することによって行う。
【0094】
このマイクロ総合分析システム2では、マイクロリアクタ1の微細流路の上流側(例えば試薬収容部、試料受容部などの上流側)に設けられた流路開口およびその周囲のチップ面からなるポンプ接続部31と、マイクロポンプユニット11のチップ接続部13とを液密に密着させた状態でマイクロリアクタ1を収納体62の内部に装着した後、マイクロリアクタ1において検体中の標的物質が分析される。マイクロリアクタ1は、搬送トレイ65に載置されて挿入口63から収納体62の内部に導入される。しかし、マイクロリアクタがマイクロポンプユニットに対して加圧された状態でマイクロリアクタを収納体62の内部に固定できるのであれば、必ずしも搬送トレイを用いる必要はない。
【0095】
収納体62の内部には、所定位置に装着されたマイクロリアクタ1を局所的に加熱もしくは冷却するための加熱・冷却ユニット(ペルチェ素子66、ヒーター67)が設けられている。例えば、マイクロリアクタ1における試薬収容部の領域にペルチェ素子66を圧接することにより試薬収容部を選択的に冷却し、これによって試薬の変質等を防止するとともに、反応部を構成する流路の領域にヒーター67を圧接することにより反応部を選択的に加熱し、これによって反応部を反応に適した温度にする。
【0096】
マイクロポンプユニット11は1つの駆動液タンク61に接続され、マイクロポンプの上流側はこの駆動液タンク61に連通している。一方、マイクロポンプの下流側は、マイクロポンプユニット11の片面に設けられた流路開口に連通されており、それぞれのマイクロポンプに連通したそれぞれの流路開口と、マイクロリアクタ1のポンプ接続部31に設けられたそれぞれの流路開口とが連結するようにマイクロリアクタ1がマイクロポンプユニット11に対して接続される。
【0097】
マイクロポンプによって、駆動液タンク61に収容された鉱物油などのオイル系あるいは水系の駆動液を、ポンプ接続部31を経由してマイクロリアクタ1における各液の収容部に送り出し、駆動液によって各収容部の液をマイクロリアクタ1の下流側へ押し出して送液する。
【0098】
測定試料である検体の前処理、反応および検出の一連の分析工程は、マイクロポンプ、検出処理装置および制御装置が一体化されたシステム本体2に、マイクロリアクタ1を装着した状態で行なわれる。好ましくは、試料および試薬の送液、前処理、混合に基づく所定の反応および光学的測定が、一連の連続的工程として自動的に実施され、測定データが、必要な条件、記録事項とともにファイル内に格納される。図12では、分析の結果が収納体62の表示部64に表示されるようになっている。
【0099】
以下に、本発明のマイクロリアクタを用いた試料(検体)と試薬との反応およびその検出の具体的な例を示す。マイクロリアクタの好ましい一態様では、一つのチップ内において、
検体もしくは検体から抽出したアナライト(例えば、DNA、RNA、遺伝子)が注入される試料受容部と、
検体の前処理を行う検体前処理部と、
プローブ結合反応、検出反応(遺伝子増幅反応または抗原抗体反応なども含む)などに用いる試薬が収容される試薬収容部と、
ポジティブコントロールが収容されるポジティブコントロール収容部と、
ネガティブコントロールが収容されるネガティブコントロール収容部と、
プローブ(例えば、遺伝子増幅反応により増幅された検出対象の遺伝子にハイブリダイズさせるプローブ)が収容されるプローブ収容部と、
これらの各収容部に連通する微細流路と、
前記各収容部および流路内の液体を送液する別途のマイクロポンプに接続可能なポンプ接続部と、が設けられている。
【0100】
このマイクロリアクタには、ポンプ接続部を介してマイクロポンプが接続され、試料受容部に注入された検体もしくは検体から抽出した生体物質(例えばDNAまたはそれ以外の生体物質)と、試薬収容部に収容された試薬とを下流の流路へ送液し、微細流路の反応部、例えば遺伝子増幅反応(タンパク質の場合、抗原抗体反応など)を行う反応部で混合して反応させる。次いで、その下流側流路にある検出部へ、この反応液を処理した処理液と、プローブ収容部に収容されたプローブとを送液し、流路内で混合してプローブと結合(またはハイブリダイゼーション)させ、この反応生成物に基づいて生体物質の検出を行う。
【0101】
また、ポジティブコントロール収容部に収容されたポジティブコントロールおよびネガティブコントロールに収容されたネガティブコントロールについても同様に上記反応および検出を行う。
【0102】
試料受容部に注入された検体は、必要に応じて、試薬との混合前に、予め流路に設けられた検体前処理部にて、例えば検体と処理液とを混合することによって前処理される。この検体前処理部は、分離フィルター、吸着用樹脂、ビーズなどを含んでいてもよい。好ましい検体前処理としては、アナライトの分離または濃縮、除タンパクなどが挙げられる。例えば、1%SDS混合液などの溶菌剤を用いて溶菌処理・DNA抽出処理を行なう。この過程では、細胞内部からDNAが放出され、ビーズまたはフィルターの膜面に吸着する。
【0103】
マイクロリアクタの試薬収容部には、必要な試薬が予め所定の量だけ封入されている。したがって使用時にその都度試薬を必要量充填する必要はなく、即使用可能の状態になっている。検体中の生体物質を分析する場合、測定に必要な試薬類は、通常それぞれ公知である。例えば、検体に存在する抗原を分析する場合、それに対する抗体、好ましくはモノクローナル抗体を含有する試薬が使用される。抗体は、好ましくはビオチンおよびFITCで標識されている。
【0104】
遺伝子検査用のマイクロリアクタに予め収容される試薬類には、遺伝子増幅に用いられる各種試薬の他、検出に使用されるプローブ類、発色試薬、前記の検体前処理に使用する前処理試薬などがある。
【0105】
マイクロポンプから駆動液を供給することにより、各試薬収容部から試薬を押し出してこれらを合流させることによって、混合試薬を生成する。この際、図1〜図3などに示した初期混合試薬の送出機構によって初期混合試薬を切り捨て、混合比率が安定した混合試薬のみを下流へ送り出す。
【0106】
その後、マイクロポンプから駆動液を供給することにより、試料受容部から検体を押し出し、混合比率が安定した混合試薬と合流させることによって、反応部にて、遺伝子増幅反応、アナライトのトラップまたは抗原抗体反応といった分析に必要な反応が開始される。
【0107】
DNA増幅方法としては、改良点も含めて各種文献などに記載され、多方面で盛んに利用されているPCR増幅法を使用することができる。PCR増幅法においては、3つの温
度間で昇降させる温度管理が必要になるが、マイクロチップに好適な温度制御を可能とする流路デバイスが、すでに本発明者らにより提案されている(特開2004−108285号)。このデバイスシステムを本発明のチップの増幅用流路に適用すればよい。これにより、熱サイクルが高速に切り替えられ、微細流路を熱容量の小さいマイクロ反応セルとしているため、DNA増幅は、手作業で行う従来の方式よりはるかに短時間で行うことができる。
【0108】
最近開発されたICAN(Isothermal chimera primer initiated nucleic acid
amplification)法は、50〜65℃における任意の一定温度の下にDNA増幅を短時間で実施できるため(特許第3433929号)、本発明システムにおいても好適な増幅技術である。手作業では、1時間かかる本法は、本発明のシステムにおいては、10〜20分、好ましくは15分で解析まで終わる。
【0109】
マイクロリアクタの微細流路における反応部よりも下流側には、アナライト、例えば増幅された遺伝子を検出するための検出部が設けられている。少なくともその検出部分は、光学的測定を可能とするために透明な材質、好ましくは透明なプラスチックとなっている。
【0110】
微細流路上の検出部に吸着されたビオチン親和性タンパク質(アビジン、ストレプトアビジン)は、プローブ物質に標識されたビオチン、または遺伝子増幅反応に使用されるプライマーの5’末端に標識されたビオチンと特異的に結合する。これにより、ビオチンで標識されたプローブまたは増幅された遺伝子が本検出部位でトラップされる。
【0111】
分離されたアナライトまたは増幅された目的遺伝子のDNAを検出する方法は特に限定されないが、好ましい態様として基本的には以下の工程で行われる。
(1a) 検体もしくは検体から抽出したDNA、あるいは検体もしくは検体から抽出したRNAから逆転写反応により合成したcDNAと、5’位置でビオチン修飾したプライマーとを、これらの収容部から下流の微細流路へ送液する。
【0112】
反応部の微細流路内で遺伝子増幅反応を行った後、微細流路内で増幅された遺伝子を含む増幅反応液と変性液とを混合して、増幅された遺伝子を変性処理により一本鎖にし、これと末端をFITC(fluorescein isothiocyanate)で蛍光標識したプローブDNAと
をハイブリダイズさせる。
【0113】
次いで、ビオチン親和性タンパク質を吸着させた微細流路内の検出部位に送液し、前記増幅遺伝子を微細流路内の検出部位にトラップする(増幅遺伝子を検出部位でトラップした後に蛍光標識したプローブDNAとをハイブリダイズさせてもよい。)。
(1b) 検体に存在する抗原、代謝物質、ホルモンなどのアナライトに対する特異的な抗体、好ましくはモノクローナル抗体を含有する試薬を検体と混合する。その場合、抗体は、ビオチンおよびFITCで標識されている。したがって抗原抗体反応により得られる生成物は、ビオチンおよびFITCを有する。これをビオチン親和性タンパク質(好ましくはストレプトアビジン)を吸着させた微細流路内の検出部位に送液し、ビオチン親和性タンパク質とビオチンとの結合を介して該検出部位に固定化する。
(2) 上記微細流路内にFITCに特異的に結合する抗FITC抗体で表面を修飾した金コロイド液を流し、これにより固定化したアナライト・抗体反応物のFITCに、あるいは遺伝子にハイブリダイズしたFITC修飾プローブに、その金コロイドを吸着させる。
(3) 上記微細流路の金コロイドの濃度を光学的に測定する。
【0114】
以上、本発明の実施形態について説明したが、本発明はこれらの実施形態に限定される
ことはなく、その要旨を逸脱しない範囲内において各種の変形、変更が可能である。
【図面の簡単な説明】
【0115】
【図1】図1は、本発明の一実施例におけるマイクロリアクタが備える、初期混合試薬の送出防止機構の構成を示した図であり、2つの試薬が合流して混合流路5cで混合された状態を示している。
【図2】図2は、図1の送出防止機構において、混合試薬の先端部が混合流路の下流末端側へ通過した状態を示した図である。
【図3】図3は、図1の送出防止機構において、混合試薬の先端部が混合流路の下流末端に達した後、混合試薬が送出流路へ流出した状態を示した図である。
【図4】図4は、撥水バルブを示した図である。
【図5】図5は、本発明の他の実施例におけるマイクロリアクタが備える、初期混合試薬の送出防止機構の構成を示した図であり、2つの試薬が合流して混合流路5cで混合された状態を示している。
【図6】図6は、図5の送出防止機構において、混合試薬の先端部が混合流路の下流末端側へ通過した状態を示した図である。
【図7】図7は、図5の送出防止機構において、混合試薬の先端部が混合流路の下流末端に達した後、混合試薬が送出流路へ流出した状態を示した図である。
【図8】図8は、本発明の他の実施例におけるマイクロリアクタの流路構成を示した図であり、試料との混合部よりも上流側の流路構成を示している。
【図9】図9は、本発明のマイクロリアクタの他の実施例を示した平面図である。
【図10】図10は、図9のマイクロリアクタに使用されるマイクロポンプユニットの斜視図である。
【図11】図11は、図10のマイクロポンプユニットの断面図である。
【図12】図12は、マイクロ総合分析システムの一例を示した斜視図である。
【図13】図13は、このマイクロ総合分析システムにおけるシステム本体の内部構成を示した図である。
【符号の説明】
【0116】
1 マイクロリアクタ
2 マイクロ総合分析システム
3 システム本体
5a 流路
5b 流路
5c 混合流路
5d 送出流路
6 合流部
7a 試薬
7b 試薬
7c 混合試薬
7d 初期混合試薬
8 下流末端
9 能動弁
11 マイクロポンプユニット
12,12h〜12j マイクロポンプ
13 チップ接続部
14 開口
15,15a〜15c 開口
16a 貫通孔
16b 貫通孔
17 基板
18 基板
19 基板
20 流路
21 圧電素子
22 加圧室
23 第1流路
24 第2流路
25 第1液室
26 第2液室
31 ポンプ接続部
32a〜32k 開口
33a〜33c,33h〜33j 試薬収容部
34a,34b 端部
35 合流部
36 試薬混合部
37 試料受容部
38 合流部
39 反応部
40 検出部
51,51a〜51e 撥水バルブ
52 送液制御通路
53a,53b 流路
54 液
61 駆動液タンク
62 収納体
63 挿入口
64 表示部
65 搬送トレイ
66 ペルチェ素子
67 ヒーター
68 光源
69 検出器
【技術分野】
【0001】
本発明は、例えば、遺伝子増幅反応、抗原抗体反応などによる生体物質の検査・分析、その他の化学物質の検査・分析、有機合成等による目的化合物の化学合成などに用いられるマイクロリアクタに関するものであり、特に、複数の試薬を混合した混合試薬と試料とを混合して反応させる際に、安定した混合比率の混合試薬を後続する工程へ送出する技術の改良に関する。
【背景技術】
【0002】
近年、マイクロマシン技術および超微細加工技術を駆使することにより、従来の試料調製、化学分析、化学合成などを行うための装置、手段(例えばポンプ、バルブ、流路、セ
ンサーなど)を微細化して1チップ上に集積化したシステムが開発されている(特許文献
1)。これは、μ−TAS(Micro total Analysis System)、バイオリアクタ、ラブ・
オン・チップ(Lab-on-chips)、バイオチップとも呼ばれ、医療検査・診断分野、環境測定分野、農産製造分野でその応用が期待されている。現実には遺伝子検査に見られるように、煩雑な工程、熟練した手技、機器類の操作が必要とされる場合には、自動化、高速化および簡便化されたミクロ化分析システムは、コスト、必要試料量、所要時間のみならず、時間および場所を選ばない分析を可能とすることによる恩恵は多大と言える。
【0003】
各種の分析、検査ではこれらの分析用チップにおける分析の定量性、解析の精度、経済性などが重要視される。そのためにはシンプルな構成で、高い信頼性の送液システムを確立することが課題である。精度が高く、信頼性に優れるマイクロ流体制御素子が求められている。これに好適なマイクロポンプシステムおよびその制御方法を本発明者らはすでに提案している(特許文献2〜4)。
【0004】
微細流路内で各成分の反応を行う上記のような分析用チップでは、微細流路内でこれらの成分を合流させて混合する工程が必要となる(特許文献5)。例えば、分析対象の試料と反応させる試薬が複数である場合には、予め複数の試薬を微細流路内で合流させて混合試薬を得る必要がある。
【特許文献1】特開2004−28589号公報
【特許文献2】特開2001−322099号公報
【特許文献3】特開2004−108285号公報
【特許文献4】特開2004−270537号公報
【特許文献5】特開2005−66400号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかし、複数の試薬を合流させて混合する際に、マイクロポンプによって各試薬を合流部へ同じタイミングで送り出したとしても、タイミングが高精度に合っていない限り、液の先頭部分では各試薬の混合比率を安定させることが難しい。この先頭部分の初期混合試薬を下流において試料と合流させて反応を行うと、この先頭部分では混合比率が安定していないので不具合が生じる場合が多い。
【0006】
本発明は、マイクロポンプによって複数の試薬をそれぞれの試薬収容部から下流側へ送出し、これらの試薬を合流させて混合し、得られた混合試薬をそのさらに下流において試料と合流させて反応部で反応を行う際に、混合比率が安定した混合試薬のみを後続する工程へ送出可能なマイクロリアクタを提供することを目的としている。
【課題を解決するための手段】
【0007】
本発明のマイクロリアクタは、板状のチップと、
複数の試薬が個別に収容される収容室からなる複数の試薬収容部と、
前記複数の試薬収容部から送出される複数の試薬を混合して混合試薬を生成する試薬混合部と、
外部から試料を注入するための注入口を有する試料受容部と、
前記試薬混合部から送出される混合試薬と、前記試料受容部から送出される試料とを混合して反応させる反応部と、を備え、
前記複数の試薬収容部、試薬混合部、試料受容部および反応部は、前記チップ内に組み込まれて流路により互いに連通され、
前記試薬混合部において生成された混合試薬のうち、初期に混合された初期混合試薬を前記反応部に送出することを防止する送出防止機構を備えることを特徴とする。
【0008】
上記の発明における好ましい態様では、前記試薬混合部は、前記複数の試薬を混合する流路であって混合試薬の流れが停止される下流末端が設けられた混合流路からなり、
該混合流路の中間部において、前記反応部へ混合試薬を送出する送出流路が分岐され、
前記送出防止機構は、前記混合流路と送出流路とから構成されており、
前記初期混合試薬は、前記混合流路の中間部と下流末端との間に収容されて前記送出流路から前記反応部への送出が防止される。
【0009】
この場合、前記送出防止機構は、前記混合流路と送出流路との接続部に、混合流路内の圧力が所定圧以上となった際に送出流路へ混合試薬を送出する送液制御部を備えることが好ましい。
【0010】
このような送液制御部は、前記混合流路と送出流路との接続部における送出流路側に設けられた、送出流路の断面積よりも小さい断面積を有する細流路で構成することができる。
【0011】
上記の発明では、混合当初の初期混合試薬を混合流路の下流末端側へトラップして切り捨てるようにしたので、試薬同士の合流のタイミングが多少ずれていても、混合比率が安定した混合試薬のみを後続する工程へ送り出すことができる。
【発明の効果】
【0012】
本発明によれば、試薬同士の合流のタイミングが多少ずれていても、混合比率が安定した混合試薬のみを後続する工程へ送り出すことができる。
【発明を実施するための最良の形態】
【0013】
以下、図面を参照しながら本発明について詳細に説明する。本発明のマイクロリアクタは、板状のチップ内に設けられた微細流路または構造部において、各種の検査、化学分析、化学合成、試料の処理・分離などの目的で試料と試薬との反応を行うものである。
【0014】
本発明のマイクロリアクタの用途には、例えば、遺伝子増幅反応、抗原抗体反応などによる生体物質の検査・分析、その他の化学物質の検査・分析、有機合成などによる目的化合物の化学合成、薬効スクリーニング、薬品抽出、金属錯体の形成・分離などが含まれる。
【0015】
本発明のマイクロリアクタは、板状のチップ内に、
(i)複数の試薬が個別に収容される収容室からなる複数の試薬収容部
(ii)前記複数の試薬収容部から送出される複数の試薬を混合して混合試薬を生成する試薬混合部
(iii)外部から試料を注入するための注入口を有する試料受容部
(iv)前記試薬混合部から送出される混合試薬と、前記試薬受容部から送出される試料とを混合して反応させる反応部
を備えている。
【0016】
前記複数の試薬収容部、試薬混合部、試料受容部および反応部は、前記チップ内に組み込まれて流路により互いに連通されている。
上記の各部の他、チップ内には、必要に応じて、各種の機能をもつ構造部が設けられる。このような構造部の具体例としては、送液を制御するための部位、試料および試薬以外の処理液を収容するための収容部、生体試料等に含まれる不要成分を除去するために試薬との反応に先立って前処理を行うための前処理部、反応後の液に含まれる標的物質等を検出するための検出部、廃液を貯留するための廃液貯留部、液を送出するためのマイクロポンプなどが挙げられる。
【0017】
送液を制御するための部位の具体例としては、逆止弁、能動弁のような弁部などが挙げられる。
各処理液を収容するための収容部の具体例としては、流路壁、ビーズ等の担体などに必要物質を吸着させた状態で洗浄を行うための洗浄液の収容部、試薬と試料との反応を停止させる反応停止液の収容部、反応生成物を検出に適するように変性させるための変性処理液の収容部、光学的検出のために反応生成物を蛍光物質等で標識するための標識用試薬の収容部、その他、抽出液、溶離液、溶菌試薬、溶血試薬等の収容部などが挙げられる。
【0018】
検出部は、マイクロリアクタ内における反応生成物を光学的に検出する場合には、例えば、光透過性の部材を用いて形成された流路部位または液溜状の部位から構成される。
前処理部は、試料に含まれる分析対象物の濃縮、分離、溶菌等を行う部位であり、例えば、生体試料に含まれるタンパク質やイオン性物質等の除去が行われる。このような処理は、例えば、フィルター、ビーズ、ゲル、メンブレンなどの担体を流路内に配置し、この担体に生体物質等を吸着させて該流路内に溶菌試薬、溶血試薬等を流し、次いで洗浄液を流すことにより行うことができる。
【0019】
廃液貯留部は、例えば、所要の大きさをもつ凹部が形成された基材を、流路用の基材の下部側に貼り合わせることによって設けられた、流路と連通する空間により構成される。必要に応じて、該空間にはスポンジ等の廃液吸収用の多孔体が収納される。
【0020】
マイクロポンプは、試薬収容部に収容された各試薬、他の収容部に収容された液などの各液を流路下流側へ送出する。マイクロポンプは通常、送出すべき液に対応して複数個が設置され、それぞれのマイクロポンプは水性または油性の駆動液を下流側へ送出し、試料や試薬等の液を駆動液で下流側へ押し出して送液を行う。
【0021】
マイクロポンプは、マイクロリアクタに直接形成する場合もあるが、マイクロリアクタとは別途に、すなわち板状のチップとは独立して設置することができる。例えば、マイクロポンプおよびその制御装置、反応検出用の光学検出装置、温度制御装置、駆動液を収容した駆動液タンクなどを備えた装置本体と、予め試薬を封入したマイクロリアクタと、から試料検査装置を構成する場合が挙げられる。
【0022】
この場合、マイクロリアクタの試料受容部に試料を注入した後、このマイクロリアクタを装置本体に装着して、装置本体側の複数のマイクロポンプと、これらのマイクロポンプに対応するマイクロリアクタの各流路とを連通させる。この状態で、駆動液タンクからの駆動液をマイクロポンプによりマイクロリアクタの流路へ送り出し、これによって流路内の液、例えば試薬収容部の試薬、試料受容部の試料などを下流側へ押し出して試薬同士の
混合、試薬と試料との混合などを行う。
【0023】
マイクロポンプは、フォトリソグラフィ技術などにより作製され、特開2001−322099号公報、特開2004−108285号公報に記載されたピエゾ素子により駆動するマイクロポンプ、アクチュエータを設けた弁室の流出入孔に逆止弁を設けた逆止弁型のマイクロポンプなど各種のものが使用できる。なお、上記のピエゾ素子により駆動するマイクロポンプは、流路抵抗が差圧に応じて変化する第1流路と、差圧の変化に対する流路抵抗の変化割合が第1流路よりも小さい第2流路と、第1流路および第2流路に接続された加圧室と、該加圧室の内部圧力を変化させるピエゾアクチュエータとを備えており、このアクチュエータを別途の制御装置により電圧で駆動することにより正逆方向への送液ができるようになっている。
【0024】
マイクロリアクタは、板状の基材を用いて、フォトリソグラフィ技術などの微細加工技術を適用して作製される。通常は、流路および構造部となる凹部を1または2以上の基材に形成した後、複数枚の基材を貼り合わせることによってマイクロリアクタを作製する。
【0025】
マイクロリアクタを構成する基材の材料には、目的に応じて各種のものが使用される。その具体例としては、ポリスチレンなどのプラスチック樹脂、ポリジメチルシロキサンなどのゴム系材料、各種の無機ガラス、シリコン、セラミックス、金属などが挙げられる。また、流路壁面に対して、目的に応じて疎水化処理、親水化処理などの各種の表面処理を行ってもよい。
【0026】
マイクロリアクタにおける流路幅のサイズは、マイクロスケール空間の利点、流路抵抗などを考慮して適宜に設計されるが、例えば、幅が数十〜数百μm、好ましくは50〜200μmであり、深さが25〜300μm、好ましくは50〜100μmである。マイクロリアクタのチップ全体の縦横サイズは、用途等にもよるが、典型的には数十mm、その高さは典型的には数mm程度である。
【0027】
本発明のマイクロリアクタにおける試料受容部は、試料を一時収容する収容室と、外部から収容室へ試料を注入するための注入口とを備えている。この収容室は、流路形状、液溜形状など各種の形状であってよい。
【0028】
試料受容部の注入口は、例えば、チップ上面から微量試料を注入できるように構成されている。外部への漏失、汚染、生体試料を使用する場合の感染などを防ぎ、密封性を確保するために、ゴム状材質などの弾性体からなる栓が注入口に形成されているか、あるいはポリジメチルシロキサンなどのゴム材、強化フィルム等で注入口が覆われていることが望ましい。例えば、ゴム材質の栓に突き刺したニードルまたは蓋付き細孔に通したニードルでシリンジ内の試料を注入する。前者の場合、ニードルを抜くとその針穴が直ちに塞がることが好ましい。また、これら以外の試料注入機構を設置してもよい。
【0029】
試料受容部の上流側は、マイクロポンプに連通される流路に連通し、その下流側は、試薬との混合部に連通している。試料受容部に注入された試料は、マイクロポンプによって供給された駆動液により下流側へ押し出され、必要に応じて前処理された後、試薬と混合される。
【0030】
試料受容部に注入される試料は、目的に応じて各種のものが対象となる。例えば、生体物質の検査・分析を行う場合には、生体由来のアナライト含有試料、例えば全血、血漿、血清、バフィーコート、尿、糞便、唾液、喀痰などが挙げられる。遺伝子検査の場合、増幅反応の鋳型となる核酸として遺伝子、DNAまたはRNAがアナライトである。また、このような核酸を含む可能性のある試料から調製または単離したものを試料としてもよい
。他のアナライトとしては、各種の代謝物質、ホルモン、タンパク質(酵素、抗原なども含む)などが挙げられる。
【0031】
その他、化学合成を目的とする場合には、試薬と反応させる原料化合物が試料となり、薬効スクリーニング、薬品抽出、金属錯体の形成・分離などを目的とする場合には、それらを行うために試薬と反応させる対象が試料となる。
【0032】
本発明のマイクロリアクタにおける試薬収容部は、試薬を収容する収容室から構成されている。この収容室は、流路形状、液溜形状など各種の形状であってよい。試薬収容部の上流側は、マイクロポンプに連通される流路に連通し、その下流側は、他の試薬との混合部に連通している。試薬収容部に収容された試薬は、マイクロポンプによって供給された駆動液により下流側へ押し出され、他の試薬と合流して混合される。
【0033】
試薬は、目的に応じて各種のものが対象となる。例えば、PCR法により検体中に含まれる遺伝子を増幅する場合における試薬には、少なくとも2'−デオキシヌクレオシド5'−三リン酸のほか、Taq DNAポリメラーゼ、Vent DNAポリメラーゼまたはPfu DN
Aポリメラーゼが含まれる。
【0034】
また、特許第3433929号に記載されたICAN(Isothermal chimera primer initiated nucleic acid amplification )法により検体中に含まれる遺伝子を増幅する場
合における試薬には、少なくとも2'−デオキシヌクレオシド5'−三リン酸、検出したい遺伝子に特異的にハイブリダイゼーションできるキメラプライマー、鎖置換活性を有するDNAポリメラーゼ、エンドヌクレアーゼのRNaseが含まれる。
【0035】
その他、化学合成を目的とする場合には、試料と反応させる原料化合物などが試薬となり、薬効スクリーニング、薬品抽出、金属錯体の形成・分離などを目的とする場合には、それらを行うために試料と反応させる物質などが試薬となる。
【0036】
遺伝子検査などの用途では、場所や時間を問わず迅速に検査ができるように、試薬収容部に予め試薬が収容されていることが望ましい。この場合、内蔵される試薬の蒸発、漏失、気泡の混入、汚染、変性などを防止するため、試薬収容部の上流側および下流側を封止することが好ましい。
【0037】
試薬収容部の封止は、封止剤により行うことができる。この封止剤は、使用前にマイクロリアクタが保管される冷蔵条件下では、固化もしくはゲル化しており、使用時、室温にすると融解し流動状態となるものである。例えば、油脂、ゼラチンの水溶液などを使用することができる。
【0038】
また、試薬収容部の収容室の上流側端部または下流側端部、あるいはこれらの両方に、後述する図4の撥水バルブを設けてもよい。これによって、マイクロリアクタの保管時における試薬の外部への流出を有効に防止できると共に、使用時には、マイクロポンプによって容易に試薬を外部へ押し出すことができる。
【0039】
反応部では、試料と混合試薬との混合液が導入された後、例えば、昇温などにより反応が開始される。反応部は、液溜形状、流路形状など各種の形状であってよく、例えば試料と混合試薬とを液溜に貯留して反応を行う態様、試料と混合試薬とを微細流路内に合流させて、合流液の送液方向をマイクロポンプにより切り替えて、合流液を微細流路内で繰り返し前後動させながら反応させる態様など、試料と試薬の種類等に応じて適宜の反応形態とすることができる。
【0040】
以上に説明したマイクロリアクタにおいて、マイクロポンプによって複数の試薬をそれぞれの試薬収容部から下流側へ送出し、これらの試薬を合流させて混合し、得られた混合試薬をそのさらに下流において試料と合流させて反応部で反応を行うのであるが、複数の試薬を合流させて混合する際に、各試薬を合流部へ同じタイミングで送り出したとしても、タイミングが高精度に合っていない限り、液の先頭部分では各試薬の混合比率を安定させることが難しい。この先頭部分の初期混合試薬を下流において試料と合流させて反応を行うと、この先頭部分では混合比率が安定していないので不具合が生じる場合が多い。そのため、混合比率が安定してから混合試薬を次工程へ送り出すことが望ましい。
【0041】
そこで本発明では、複数の試薬収容部から送出される複数の試薬を混合して混合試薬を生成する試薬混合部において生成された混合試薬のうち、初期に混合された初期混合試薬を前記反応部に送出することを防止する送出防止機構を備えている。以下、図1〜図3および図5〜図7を参照しながら初期混合試薬の送出防止機構について説明する。
【0042】
図1は、本発明の一実施例におけるマイクロリアクタが備える、初期混合試薬の送出防止機構の構成を示した図である。本実施例では、試薬7aと試薬7bとの2種類の試薬により混合試薬7cを得る場合を示している。
【0043】
同図において、5aは試薬7aが送出される流路であり、その上流側は、試薬7aが収容される試薬収容部(図示せず)に連通している。
5bは、試薬7bが送出される流路であり、その上流側は、試薬7bが収容される試薬収容部(図示せず)に連通している。
【0044】
5cは、試薬7aと試薬7bとを混合して混合試薬7cを生成する混合流路(試薬混合部)であり、流路5aと流路5bとの合流部6から、混合試薬7cの流れが停止される下流末端8までの流路で構成されている。
【0045】
混合流路5cの中間部では、下流の反応部(図示せず)へ混合試薬7cを送出する送出流路5dが分岐されている。送出流路5dは、混合流路5cとの分岐点から先の流路で構成されている。
【0046】
混合流路5cと送出流路5dとの接続部における送出流路5d側には、撥水バルブ51aが設けられている。この撥水バルブ(送液制御部)は、図4に示した構造を備えている。同図の撥水バルブ51は、細径の送液制御通路52を備えている。送液制御通路52は、その断面積(流路に対して垂直な断面の断面積)が、上流側の流路53aおよび下流側の流路53bの断面積よりも小さい細流路である。
【0047】
流路壁がプラスチック樹脂などの疎水性の材質で形成されている場合には、送液制御通路52に接する液54は、流路壁との表面張力の差によって、下流側の流路53bへ通過することが規制される。
【0048】
下流側の流路53bへ液54を流出させる際には、マイクロポンプによって所定圧以上の送液圧力を加え、これによって表面張力に抗して液54を送液制御通路52から下流側の流路53bへ押し出す。液54が流路53bへ流出した後は、液54の先端部を下流側の流路53bへ押し出すのに要する送液圧力を維持せずとも液が下流側の流路53bへ流れていく。すなわち、上流側から下流側への正方向への送液圧力が所定圧力に達するまで送液制御通路52から先への液の通過が遮断され、所定圧以上の送液圧力が加わることにより液54は送液制御通路52を通過する。
【0049】
流路壁がガラスなどの親水性の材質で形成されている場合には、少なくとも送液制御通
路52の内面に、撥水性のコーティング、例えばフッ素系のコーティングを施す必要がある。
【0050】
図1において、初期混合試薬7dは、以下に説明する作用により、混合流路5cの送出流路5dとの分岐点において、下流末端8側へ選択的に送り出され、混合流路5cの下流側にトラップされる。これにより、初期混合試薬7dが送出流路5d側へ流出することが防止される。
【0051】
図1に示したように、マイクロポンプにより試薬収容部から流路5aへ送り出された試薬7aと、別途のマイクロポンプにより他の試薬収容部から流路5bへ送り出された試薬7bとは、合流部6で合流し、混合流路5cで混合される。
【0052】
この際、マイクロポンプによる混合試薬7cの送液圧力を、初期混合試薬7dおよび混合試薬7cが撥水バルブ51aを通過可能な圧力よりも小さな圧力として混合流路5c内の混合試薬7cを送液する。これにより、図2に示したように、混合流路5cと送出流路5dとの接続部において、初期混合試薬7dは送出流路5d側には流出せずに混合流路5cの下流末端8側へ送り出される。
【0053】
そして、初期混合試薬7dが混合流路5cの下流末端8に達した後、マイクロポンプによる混合試薬7cの送液圧力を、混合試薬7cが撥水バルブ51aを通過可能な圧力以上の圧力とする。これにより、図3に示したように、混合流路5c内の混合試薬7cは、撥水バルブ51aを通過し、混合試薬7cは送出流路5dに流出する。
【0054】
以上のようにマイクロポンプによる送液圧力を制御することで、初期混合試薬7dは混合流路5cの中間部と下流末端8との間に収容され、送出流路5dには、初期混合試薬7dが切り捨てられた混合試薬7cのみが送出される。すなわち、混合比率が安定した混合試薬だけを後続する工程へ供給することができる。
【0055】
なお、本実施例では、混合流路5cの下流末端8にも撥水バルブ51bを設けている。この撥水バルブ51bは、初期混合試薬7dが下流側の流路へ通過可能な送液圧力が、撥水バルブ51aにおいて混合試薬7cが送出流路5d側へ通過可能な送液圧力よりも大きい撥水バルブである。
【0056】
したがって、初期混合試薬7dが混合流路5cの下流末端8に達した後、マイクロポンプによる混合試薬7cの送液圧力を、混合試薬7cが撥水バルブ51aを通過可能であり、且つ、初期混合試薬7dが撥水バルブ51bを通過できない圧力とすることで、図3に示したように、混合試薬7cを撥水バルブ51aの先へ通過させると共に、混合流路5cの下流末端8において初期混合試薬7dが撥水バルブ51bの先へ通過することを防止できる。
【0057】
例えば、撥水バルブ51aにおける送液制御通路(図4の符号52)の断面積を、撥水バルブ51bにおける送液制御通路の断面積よりも大きくすることによって、これらの送液制御通路を液が通過可能な送液圧力に差をもたせることができる。この他、場合によっては、撥水バルブ51aと撥水バルブ51bとの間で、液と送液制御通路の流路壁との表面張力差を相違させることで、液が通過可能な送液圧力に差をもたせることも考えられる。
【0058】
例えば、撥水バルブ51bよりも先の流路は、廃液貯留部に連通される。この場合、全ての反応、検出工程を終えた後などの適切な時期に、混合流路5cの中間部と下流末端8との間に収容された初期混合試薬7dおよび混合試薬7cを、マイクロポンプの送液圧力
を上げることによって撥水バルブ51bよりも先の流路へ押し出し、その先の廃液貯留部に収容する。
【0059】
なお、本実施例では混合流路5cの下流末端8にこのような撥水バルブ51bを設けたが、下流末端8に撥水バルブ51bを設けずに、下流末端8完全に封止する構造としてもよい。
【0060】
図5は、本発明の他の実施例におけるマイクロリアクタが備える、初期混合試薬の送出防止機構の構成を示した図である。なお、図1〜図3と対応する構成要素は同一の符号で示しその詳細な説明を省略する。
【0061】
本実施例では、基本的な構成は上述した実施例と同様であるが、混合流路5cと送出流路5dとの接続部における送出流路5d側に、能動弁9が設けられている。初期混合試薬7dは、以下に説明する作用によって、混合流路5cの送出流路5dとの分岐点において、選択的に下流末端8側へ送り出され、混合流路5cの下流側にトラップされる。これにより、初期混合試薬7dが送出流路5d側へ流出することが防止される。
【0062】
図5に示したように、マイクロポンプにより試薬収容部から流路5aへ送り出された試薬7aと、別途のマイクロポンプにより他の試薬収容部から流路5bへ送り出された試薬7bとは、合流部6で合流し、混合流路5cで混合される。
【0063】
この際、能動弁9は閉止した状態になっており、図6に示したように、混合流路5cと送出流路5dとの接続部において、初期混合試薬7dは送出流路5d側には流出せずに混合流路5cの下流末端8側へ送り出される。
【0064】
そして、初期混合試薬7dが混合流路5cと送出流路5dとの分岐点を通過した後、能動弁9を開放する。これにより、図7に示したように、混合流路5c内の混合試薬7cは、能動弁9を通過し、混合試薬7cは送出流路5dに流出する。
【0065】
以上のように能動弁9を制御することで、初期混合試薬7dは混合流路5cの中間部と下流末端8との間に収容され、送出流路5dには、初期混合試薬7dが切り捨てられた混合試薬7cのみが送出される。すなわち、混合比率が安定した混合試薬だけを後続する工程へ供給することができる。
【0066】
なお、能動弁9として、公知である各種の構造のものをマイクロリアクタに形成することができる。例えば、空気圧ピストン、油圧ピストン、水圧ピストン、圧電アクチュエータ、形状記憶合金アクチュエータなどにより、柔軟な材質からなる基材を上方から押圧して、この基材の下方に配置された開口を覆って流路を塞ぐ構造の能動弁、弁体としてバイメタルを使用し、通電加熱により弁体を変形させて流路を塞ぐ構造の能動弁、弁体として形状記憶合金を使用し、通電加熱により弁体を変形させて流路を塞ぐ構造の能動弁などが使用できる。弁の開閉制御は、外部の制御装置による電圧駆動などによって行う。
【0067】
以上に説明した、本発明のマイクロリアクタが備える初期混合試薬の送出防止機構は、混合流路と送出流路とから構成されており、初期混合試薬は、混合流路の中間部と下流末端との間に収容されて送出流路から反応部への送出が防止される。
【0068】
このような初期混合試薬の送出防止機構を備えた2つの実施例について説明したが、この他、例えば混合流路の断面積と、送出流路の断面積とを相違させることにより、毛細管力によって初期混合試薬を選択的に混合流路の流路末端側へ導くことで、初期混合試薬の送出流路側への送出を防止できる。
【0069】
あるいは、混合流路の流路壁の表面張力と、送出流路の流路壁の表面張力とを、流路材質または流路壁の表面処理等により相違させ、表面張力によって初期混合試薬を選択的に混合流路の流路末端側へ導くことで、初期混合試薬の送出流路側への送出を防止できる。
【0070】
図8は、本発明の他の実施例におけるマイクロリアクタの流路構成を示した図であり、試料との混合部よりも上流側の流路構成を示している。
3種類の各試薬は、試薬収容部33h、33i、33jのそれぞれに収容され、各試薬収容部の上流側には、マイクロリアクタとは別途の装置に内蔵されたマイクロポンプ12h,12i,12jがポンプ接続部31で接続され、各試薬収容部から下流側の混合流路5cへこれらのマイクロポンプにより試薬が送液される。
【0071】
混合流路5cと、混合流路5cから分岐した送出流路5dと、撥水バルブ51a、51bは、図1と同様な初期混合試薬の送出防止機構を構成しており、試薬収容部33h、33i、33jから送出され混合流路5cで合流した各試薬の混合液の先端部を切り捨て、混合状態が安定した後に混合試薬を次工程へ送出するようにしている。
【0072】
図9は、本発明のマイクロリアクタの他の実施例を示した平面図である。本実施例のマイクロリアクタ1には、試薬の収容室である流路状の試薬収容部33a、33b、33cのそれぞれに3種類の試薬が収容されている。これらの試薬収容部の両端部(試薬収容部33aでは上流側の端部34aおよび下流側の端部34b)には、図4に示した構造の撥水バルブが設けられ、これらの撥水バルブの間の流路に試薬が封入されている。
【0073】
なお、詳細な説明は省略するが、図9のマイクロリアクタ1の微細流路には、試薬収容部33a〜33cの両端部以外の位置にも図4の撥水バルブが設けられており、例えば、混合試薬と試料との合流部38における混合試薬の入口と試料の入口などにも上記の撥水バルブが設けられており、この撥水バルブによってその先の流路への送液開始のタイミングが制御される。
【0074】
図9の試薬収容部33a〜33cの上流側には、マイクロリアクタ1の一方の面から外部へ開放された開口32c〜32eが設けられている。これらの開口32c〜32eは、マイクロリアクタ1を後述するマイクロポンプユニットに重ね合わせて接続した際に、マイクロポンプユニットの接続面に設けられた流路開口と位置合わせされてマイクロポンプに連通される。
【0075】
なお、開口32a,32bおよび32f〜32kも同様に、マイクロリアクタ1とマイクロポンプユニットとの接続によってマイクロポンプに連通される。これらの開口32a〜32kを含むチップ面によってポンプ接続部が構成され、ポンプ接続部をマイクロポンプユニットの接続面に密着させることによってマイクロリアクタ1とマイクロポンプユニットとが接続される。
【0076】
このポンプ接続部は、必要なシール性を確保して駆動液の漏出を防止するために、ポリテトラフルオロエチレン、シリコーン樹脂などの柔軟性(弾性、形状追随性)をもつ樹脂によって密着面が形成されることが好ましい。このような柔軟性を有する密着面は、例えばマイクロリアクタの構成基材自体によるものであってもよく、また、ポンプ接続部における流路開口の周囲に貼着された柔軟性を有する別途の部材によるものであってもよい。
【0077】
試薬収容部33a〜33cに収容された試薬は、開口32c〜32eに連通するそれぞれ別途のマイクロポンプによって、試薬収容部33a〜33cの下流側端部に設けられた撥水バルブ(図示せず)を通過して合流部35へ流れ込み、その先に続く流路である混合
流路5c(試薬混合部36)で3種類の各試薬が混合される。
【0078】
なお、この混合流路5cと、送出流路5dとを含む流路系によって、図1または図5の実施例に示したような初期混合試薬の送出防止機構が構成されており、初期混合試薬を混合流路5cの流路末端8にトラップするようにしている。
【0079】
混合流路5cで混合され送出流路5dに送り出された混合試薬は、試料受容部37に収容された試料と合流部38で合流する。なお、混合試薬は開口32bに連通したマイクロポンプによって駆動液で下流へ押し出され、試料は開口32aに連通したマイクロポンプによって駆動液で下流へ押し出される。混合試薬と試料との混合液は、反応部39へ収容され加熱等によって反応が開始される。
【0080】
反応後の液は、検出部40へ送液され、例えば光学的な検出方法などによって標的物質が検出される。なお、開口32f〜32jに連通するそれぞれ別途のマイクロポンプによって、これらの開口から先の流路に予め収容された各試薬(例えば混合試薬と試料との反応を停止させる液、検出対象の物質に対して標識などの必要な処理を行うための液、洗浄液など)を所定のタイミングで下流へ押し出して送液するようにしている。
【0081】
図10は、図9のマイクロリアクタに使用されるマイクロポンプユニットの斜視図、図11は、その断面図である。このマイクロポンプユニット11は、シリコン製の基板17と、その上のガラス製の基板18と、その上のガラス製の基板19との3つの基板から構成されている。基板17と基板18、および基板18と基板19はそれぞれ、陽極接合によって接合されている。
【0082】
シリコン製の基板17と、その上に陽極接合によって貼り合わされたガラス製の基板18との間の内部空間によってマイクロポンプ12(ピエゾポンプ)が構成されている。
基板17は、シリコンウエハをフォトリソグラフィ技術により所定の形状に加工したものである。例えば、シリコン基板面への酸化膜の形成、レジスト塗布、レジストの露光および現像、酸化膜のエッチング、ICP(高周波誘導結合型プラズマ、Inductively Coupled Plasma)などによるシリコンのエッチング等を含む微細加工によって、加圧室22、第1流路23、第1液室25、第2流路24、および第2液室26が形成されている。
【0083】
加圧室22の位置では、シリコン基板がダイヤフラムに加工され、その外側表面には、チタン酸ジルコン酸鉛(PZT)セラミックスなどからなる圧電素子21が貼着されている。
【0084】
このマイクロポンプ12は、圧電素子21への制御電圧によって次のように駆動される。印加された所定波形の電圧により圧電素子21が振動すると共に、加圧室22の位置におけるシリコンダイヤフラムが振動し、これによって加圧室22の体積が増減する。第1流路23と第2流路24とは、幅および深さが同じで、長さが第1流路23よりも第2流路24の方が長くなっている。第1流路23では、差圧が大きくなると、流路内で乱流が発生し、流路抵抗が増加する。一方、第2流路24では、流路幅が長いので差圧が大きくなっても層流になり易く、第1流路23に比べて差圧の変化に対する流路抵抗の変化割合が小さくなる。
【0085】
例えば、圧電素子21に対する制御電圧を調整することにより、加圧室22の内部へ向かう方向へ素早くシリコンダイヤフラムを変位させて大きい差圧を与えながら加圧室22の体積を減少させ、次いで加圧室22からその外側へ向かう方向へゆっくりシリコンダイヤフラムを変位させて小さい差圧を与えながら加圧室22の体積を増加させると、駆動液は図11において左から右へ向かう方向へ正方向に送液される。
【0086】
これとは反対に、加圧室22からその外側へ向かう方向へ素早くシリコンダイヤフラムを変位させて大きい差圧を与えながら加圧室22の体積を増加させ、次いで加圧室22の内部へ向かう方向へゆっくりシリコンダイヤフラムを変位させて小さい差圧を与えながら加圧室22の体積を減少させると、駆動液は図11の右から左へ逆方向に送液される。
【0087】
なお、第1流路23と第2流路24における、差圧の変化に対する流路抵抗の変化割合の相違は、必ずしも流路の長さの違いによる必要はなく、他の形状的な相違に基づくものであってもよい。
【0088】
マイクロポンプ12による流量の制御は、圧電素子21に印加する電圧を調整することにより行うことができる。
基板19には、流路20がパターニングされている。一例として、流路20の寸法および形状は、幅が150μm程度、深さが300μm程度の断面矩形状である。流路20の下流側には、図9のマイクロリアクタの開口32a〜32kに位置合わせすることによりマイクロポンプ12を検査チップの微細流路に連通させるための開口15が設けられている。
【0089】
流路20の上流側は、基板18の貫通孔16bを介して、基板17に設けられた流路を通りマイクロポンプ12に連通されている。また、マイクロポンプ12の上流側は、基板17に設けられた流路から基板18の貫通孔16aを介して、ガラス製の基板19に設けられた開口14に連通されている。この開口14は不図示の駆動液タンクに接続されている。開口14は、例えば、PDMS(ポリジメチルシロキサン)のパッキンを介して駆動液タンクに接続される。
【0090】
開口15a,15b,15cはそれぞれ、図9のマイクロリアクタの開口32c,32d,32eと連通される(なお、図10ではマイクロポンプユニット全体のうち一部分のみ示している)。マイクロポンプ12によって、流路20、開口15a、開口32cを通じて駆動液を送液して試薬収容部33aに収容された試薬を下流へ押し出し、流路20、開口15b、開口32dを通じて駆動液を送液して試薬収容部33bに収容された試薬を下流へ押し出し、流路20、開口15c、開口32eを通じて駆動液を送液して試薬収容部33cに収容された試薬を下流へ押し出す。
【0091】
マイクロリアクタは、例えば、別途のシステム本体に装着することにより反応と分析が行われる。このシステム本体とマイクロリアクタとによりマイクロ総合分析システムが構成される。このマイクロ総合分析システムの一例を以下に説明する。図12は、マイクロ総合分析システムの一例を示した斜視図、図13は、このマイクロ総合分析システムにおけるシステム本体の内部構成を示した図である。
【0092】
このマイクロ総合分析システム2のシステム本体3は、分析のための各装置を収納する筺体状の収納体62を備えている。この収納体62の内部には、マイクロリアクタ1に連通させるための流路開口を有するチップ接続部13と、複数のマイクロポンプ(図示せず)とが設けられたマイクロポンプユニット11が配置されている。
【0093】
さらに収納体62の内部には、マイクロリアクタ1における反応を検出するための検出処理装置(LED、光電子増倍菅、CCDカメラ等の光源68および、可視分光法、蛍光測光法などによる光学的な検出を行う検出器69)と、この検出処理装置とマイクロポンプユニット11とを制御する制御装置(図示せず)とが設けられている。この制御装置によって、マイクロポンプによる送液の制御、光学的手段等によりマイクロリアクタ1における反応を検出する検出処理装置の制御の他、後述する加熱・冷却ユニットによるマイク
ロリアクタ1の温度制御、マイクロリアクタ1における反応の制御、データの収集(測定)および処理等を行う。マイクロポンプの制御は、予め送液順序、流量、タイミングなどに関する諸条件が設定されたプログラムに従って、それに応じた駆動電圧をマイクロポンプに印加することによって行う。
【0094】
このマイクロ総合分析システム2では、マイクロリアクタ1の微細流路の上流側(例えば試薬収容部、試料受容部などの上流側)に設けられた流路開口およびその周囲のチップ面からなるポンプ接続部31と、マイクロポンプユニット11のチップ接続部13とを液密に密着させた状態でマイクロリアクタ1を収納体62の内部に装着した後、マイクロリアクタ1において検体中の標的物質が分析される。マイクロリアクタ1は、搬送トレイ65に載置されて挿入口63から収納体62の内部に導入される。しかし、マイクロリアクタがマイクロポンプユニットに対して加圧された状態でマイクロリアクタを収納体62の内部に固定できるのであれば、必ずしも搬送トレイを用いる必要はない。
【0095】
収納体62の内部には、所定位置に装着されたマイクロリアクタ1を局所的に加熱もしくは冷却するための加熱・冷却ユニット(ペルチェ素子66、ヒーター67)が設けられている。例えば、マイクロリアクタ1における試薬収容部の領域にペルチェ素子66を圧接することにより試薬収容部を選択的に冷却し、これによって試薬の変質等を防止するとともに、反応部を構成する流路の領域にヒーター67を圧接することにより反応部を選択的に加熱し、これによって反応部を反応に適した温度にする。
【0096】
マイクロポンプユニット11は1つの駆動液タンク61に接続され、マイクロポンプの上流側はこの駆動液タンク61に連通している。一方、マイクロポンプの下流側は、マイクロポンプユニット11の片面に設けられた流路開口に連通されており、それぞれのマイクロポンプに連通したそれぞれの流路開口と、マイクロリアクタ1のポンプ接続部31に設けられたそれぞれの流路開口とが連結するようにマイクロリアクタ1がマイクロポンプユニット11に対して接続される。
【0097】
マイクロポンプによって、駆動液タンク61に収容された鉱物油などのオイル系あるいは水系の駆動液を、ポンプ接続部31を経由してマイクロリアクタ1における各液の収容部に送り出し、駆動液によって各収容部の液をマイクロリアクタ1の下流側へ押し出して送液する。
【0098】
測定試料である検体の前処理、反応および検出の一連の分析工程は、マイクロポンプ、検出処理装置および制御装置が一体化されたシステム本体2に、マイクロリアクタ1を装着した状態で行なわれる。好ましくは、試料および試薬の送液、前処理、混合に基づく所定の反応および光学的測定が、一連の連続的工程として自動的に実施され、測定データが、必要な条件、記録事項とともにファイル内に格納される。図12では、分析の結果が収納体62の表示部64に表示されるようになっている。
【0099】
以下に、本発明のマイクロリアクタを用いた試料(検体)と試薬との反応およびその検出の具体的な例を示す。マイクロリアクタの好ましい一態様では、一つのチップ内において、
検体もしくは検体から抽出したアナライト(例えば、DNA、RNA、遺伝子)が注入される試料受容部と、
検体の前処理を行う検体前処理部と、
プローブ結合反応、検出反応(遺伝子増幅反応または抗原抗体反応なども含む)などに用いる試薬が収容される試薬収容部と、
ポジティブコントロールが収容されるポジティブコントロール収容部と、
ネガティブコントロールが収容されるネガティブコントロール収容部と、
プローブ(例えば、遺伝子増幅反応により増幅された検出対象の遺伝子にハイブリダイズさせるプローブ)が収容されるプローブ収容部と、
これらの各収容部に連通する微細流路と、
前記各収容部および流路内の液体を送液する別途のマイクロポンプに接続可能なポンプ接続部と、が設けられている。
【0100】
このマイクロリアクタには、ポンプ接続部を介してマイクロポンプが接続され、試料受容部に注入された検体もしくは検体から抽出した生体物質(例えばDNAまたはそれ以外の生体物質)と、試薬収容部に収容された試薬とを下流の流路へ送液し、微細流路の反応部、例えば遺伝子増幅反応(タンパク質の場合、抗原抗体反応など)を行う反応部で混合して反応させる。次いで、その下流側流路にある検出部へ、この反応液を処理した処理液と、プローブ収容部に収容されたプローブとを送液し、流路内で混合してプローブと結合(またはハイブリダイゼーション)させ、この反応生成物に基づいて生体物質の検出を行う。
【0101】
また、ポジティブコントロール収容部に収容されたポジティブコントロールおよびネガティブコントロールに収容されたネガティブコントロールについても同様に上記反応および検出を行う。
【0102】
試料受容部に注入された検体は、必要に応じて、試薬との混合前に、予め流路に設けられた検体前処理部にて、例えば検体と処理液とを混合することによって前処理される。この検体前処理部は、分離フィルター、吸着用樹脂、ビーズなどを含んでいてもよい。好ましい検体前処理としては、アナライトの分離または濃縮、除タンパクなどが挙げられる。例えば、1%SDS混合液などの溶菌剤を用いて溶菌処理・DNA抽出処理を行なう。この過程では、細胞内部からDNAが放出され、ビーズまたはフィルターの膜面に吸着する。
【0103】
マイクロリアクタの試薬収容部には、必要な試薬が予め所定の量だけ封入されている。したがって使用時にその都度試薬を必要量充填する必要はなく、即使用可能の状態になっている。検体中の生体物質を分析する場合、測定に必要な試薬類は、通常それぞれ公知である。例えば、検体に存在する抗原を分析する場合、それに対する抗体、好ましくはモノクローナル抗体を含有する試薬が使用される。抗体は、好ましくはビオチンおよびFITCで標識されている。
【0104】
遺伝子検査用のマイクロリアクタに予め収容される試薬類には、遺伝子増幅に用いられる各種試薬の他、検出に使用されるプローブ類、発色試薬、前記の検体前処理に使用する前処理試薬などがある。
【0105】
マイクロポンプから駆動液を供給することにより、各試薬収容部から試薬を押し出してこれらを合流させることによって、混合試薬を生成する。この際、図1〜図3などに示した初期混合試薬の送出機構によって初期混合試薬を切り捨て、混合比率が安定した混合試薬のみを下流へ送り出す。
【0106】
その後、マイクロポンプから駆動液を供給することにより、試料受容部から検体を押し出し、混合比率が安定した混合試薬と合流させることによって、反応部にて、遺伝子増幅反応、アナライトのトラップまたは抗原抗体反応といった分析に必要な反応が開始される。
【0107】
DNA増幅方法としては、改良点も含めて各種文献などに記載され、多方面で盛んに利用されているPCR増幅法を使用することができる。PCR増幅法においては、3つの温
度間で昇降させる温度管理が必要になるが、マイクロチップに好適な温度制御を可能とする流路デバイスが、すでに本発明者らにより提案されている(特開2004−108285号)。このデバイスシステムを本発明のチップの増幅用流路に適用すればよい。これにより、熱サイクルが高速に切り替えられ、微細流路を熱容量の小さいマイクロ反応セルとしているため、DNA増幅は、手作業で行う従来の方式よりはるかに短時間で行うことができる。
【0108】
最近開発されたICAN(Isothermal chimera primer initiated nucleic acid
amplification)法は、50〜65℃における任意の一定温度の下にDNA増幅を短時間で実施できるため(特許第3433929号)、本発明システムにおいても好適な増幅技術である。手作業では、1時間かかる本法は、本発明のシステムにおいては、10〜20分、好ましくは15分で解析まで終わる。
【0109】
マイクロリアクタの微細流路における反応部よりも下流側には、アナライト、例えば増幅された遺伝子を検出するための検出部が設けられている。少なくともその検出部分は、光学的測定を可能とするために透明な材質、好ましくは透明なプラスチックとなっている。
【0110】
微細流路上の検出部に吸着されたビオチン親和性タンパク質(アビジン、ストレプトアビジン)は、プローブ物質に標識されたビオチン、または遺伝子増幅反応に使用されるプライマーの5’末端に標識されたビオチンと特異的に結合する。これにより、ビオチンで標識されたプローブまたは増幅された遺伝子が本検出部位でトラップされる。
【0111】
分離されたアナライトまたは増幅された目的遺伝子のDNAを検出する方法は特に限定されないが、好ましい態様として基本的には以下の工程で行われる。
(1a) 検体もしくは検体から抽出したDNA、あるいは検体もしくは検体から抽出したRNAから逆転写反応により合成したcDNAと、5’位置でビオチン修飾したプライマーとを、これらの収容部から下流の微細流路へ送液する。
【0112】
反応部の微細流路内で遺伝子増幅反応を行った後、微細流路内で増幅された遺伝子を含む増幅反応液と変性液とを混合して、増幅された遺伝子を変性処理により一本鎖にし、これと末端をFITC(fluorescein isothiocyanate)で蛍光標識したプローブDNAと
をハイブリダイズさせる。
【0113】
次いで、ビオチン親和性タンパク質を吸着させた微細流路内の検出部位に送液し、前記増幅遺伝子を微細流路内の検出部位にトラップする(増幅遺伝子を検出部位でトラップした後に蛍光標識したプローブDNAとをハイブリダイズさせてもよい。)。
(1b) 検体に存在する抗原、代謝物質、ホルモンなどのアナライトに対する特異的な抗体、好ましくはモノクローナル抗体を含有する試薬を検体と混合する。その場合、抗体は、ビオチンおよびFITCで標識されている。したがって抗原抗体反応により得られる生成物は、ビオチンおよびFITCを有する。これをビオチン親和性タンパク質(好ましくはストレプトアビジン)を吸着させた微細流路内の検出部位に送液し、ビオチン親和性タンパク質とビオチンとの結合を介して該検出部位に固定化する。
(2) 上記微細流路内にFITCに特異的に結合する抗FITC抗体で表面を修飾した金コロイド液を流し、これにより固定化したアナライト・抗体反応物のFITCに、あるいは遺伝子にハイブリダイズしたFITC修飾プローブに、その金コロイドを吸着させる。
(3) 上記微細流路の金コロイドの濃度を光学的に測定する。
【0114】
以上、本発明の実施形態について説明したが、本発明はこれらの実施形態に限定される
ことはなく、その要旨を逸脱しない範囲内において各種の変形、変更が可能である。
【図面の簡単な説明】
【0115】
【図1】図1は、本発明の一実施例におけるマイクロリアクタが備える、初期混合試薬の送出防止機構の構成を示した図であり、2つの試薬が合流して混合流路5cで混合された状態を示している。
【図2】図2は、図1の送出防止機構において、混合試薬の先端部が混合流路の下流末端側へ通過した状態を示した図である。
【図3】図3は、図1の送出防止機構において、混合試薬の先端部が混合流路の下流末端に達した後、混合試薬が送出流路へ流出した状態を示した図である。
【図4】図4は、撥水バルブを示した図である。
【図5】図5は、本発明の他の実施例におけるマイクロリアクタが備える、初期混合試薬の送出防止機構の構成を示した図であり、2つの試薬が合流して混合流路5cで混合された状態を示している。
【図6】図6は、図5の送出防止機構において、混合試薬の先端部が混合流路の下流末端側へ通過した状態を示した図である。
【図7】図7は、図5の送出防止機構において、混合試薬の先端部が混合流路の下流末端に達した後、混合試薬が送出流路へ流出した状態を示した図である。
【図8】図8は、本発明の他の実施例におけるマイクロリアクタの流路構成を示した図であり、試料との混合部よりも上流側の流路構成を示している。
【図9】図9は、本発明のマイクロリアクタの他の実施例を示した平面図である。
【図10】図10は、図9のマイクロリアクタに使用されるマイクロポンプユニットの斜視図である。
【図11】図11は、図10のマイクロポンプユニットの断面図である。
【図12】図12は、マイクロ総合分析システムの一例を示した斜視図である。
【図13】図13は、このマイクロ総合分析システムにおけるシステム本体の内部構成を示した図である。
【符号の説明】
【0116】
1 マイクロリアクタ
2 マイクロ総合分析システム
3 システム本体
5a 流路
5b 流路
5c 混合流路
5d 送出流路
6 合流部
7a 試薬
7b 試薬
7c 混合試薬
7d 初期混合試薬
8 下流末端
9 能動弁
11 マイクロポンプユニット
12,12h〜12j マイクロポンプ
13 チップ接続部
14 開口
15,15a〜15c 開口
16a 貫通孔
16b 貫通孔
17 基板
18 基板
19 基板
20 流路
21 圧電素子
22 加圧室
23 第1流路
24 第2流路
25 第1液室
26 第2液室
31 ポンプ接続部
32a〜32k 開口
33a〜33c,33h〜33j 試薬収容部
34a,34b 端部
35 合流部
36 試薬混合部
37 試料受容部
38 合流部
39 反応部
40 検出部
51,51a〜51e 撥水バルブ
52 送液制御通路
53a,53b 流路
54 液
61 駆動液タンク
62 収納体
63 挿入口
64 表示部
65 搬送トレイ
66 ペルチェ素子
67 ヒーター
68 光源
69 検出器
【特許請求の範囲】
【請求項1】
板状のチップと、
複数の試薬が個別に収容される収容室からなる複数の試薬収容部と、
前記複数の試薬収容部から送出される複数の試薬を混合して混合試薬を生成する試薬混合部と、
外部から試料を注入するための注入口を有する試料受容部と、
前記試薬混合部から送出される混合試薬と、前記試料受容部から送出される試料とを混合して反応させる反応部と、を備え、
前記複数の試薬収容部、試薬混合部、試料受容部および反応部は、前記チップ内に組み込まれて流路により互いに連通され、
前記試薬混合部において生成された混合試薬のうち、初期に混合された初期混合試薬を前記反応部に送出することを防止する送出防止機構を備えることを特徴とするマイクロリアクタ。
【請求項2】
前記試薬混合部は、前記複数の試薬を混合する流路であって混合試薬の流れが停止される下流末端が設けられた混合流路からなり、
該混合流路の中間部において、前記反応部へ混合試薬を送出する送出流路が分岐され、
前記送出防止機構は、前記混合流路と送出流路とから構成されており、
前記初期混合試薬は、前記混合流路の中間部と下流末端との間に収容されて前記送出流路から前記反応部への送出が防止されることを特徴とする請求項1に記載のマイクロリアクタ。
【請求項3】
前記送出防止機構は、前記混合流路と送出流路との接続部に、混合流路内の圧力が所定圧以上となった際に送出流路へ混合試薬を送出する送液制御部を備えることを特徴とする請求項2に記載のマイクロリアクタ。
【請求項4】
前記送液制御部は、前記混合流路と送出流路との接続部における送出流路側に設けられた、送出流路の断面積よりも小さい断面積を有する細流路であることを特徴とする請求項3に記載のマイクロリアクタ。
【請求項1】
板状のチップと、
複数の試薬が個別に収容される収容室からなる複数の試薬収容部と、
前記複数の試薬収容部から送出される複数の試薬を混合して混合試薬を生成する試薬混合部と、
外部から試料を注入するための注入口を有する試料受容部と、
前記試薬混合部から送出される混合試薬と、前記試料受容部から送出される試料とを混合して反応させる反応部と、を備え、
前記複数の試薬収容部、試薬混合部、試料受容部および反応部は、前記チップ内に組み込まれて流路により互いに連通され、
前記試薬混合部において生成された混合試薬のうち、初期に混合された初期混合試薬を前記反応部に送出することを防止する送出防止機構を備えることを特徴とするマイクロリアクタ。
【請求項2】
前記試薬混合部は、前記複数の試薬を混合する流路であって混合試薬の流れが停止される下流末端が設けられた混合流路からなり、
該混合流路の中間部において、前記反応部へ混合試薬を送出する送出流路が分岐され、
前記送出防止機構は、前記混合流路と送出流路とから構成されており、
前記初期混合試薬は、前記混合流路の中間部と下流末端との間に収容されて前記送出流路から前記反応部への送出が防止されることを特徴とする請求項1に記載のマイクロリアクタ。
【請求項3】
前記送出防止機構は、前記混合流路と送出流路との接続部に、混合流路内の圧力が所定圧以上となった際に送出流路へ混合試薬を送出する送液制御部を備えることを特徴とする請求項2に記載のマイクロリアクタ。
【請求項4】
前記送液制御部は、前記混合流路と送出流路との接続部における送出流路側に設けられた、送出流路の断面積よりも小さい断面積を有する細流路であることを特徴とする請求項3に記載のマイクロリアクタ。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【公開番号】特開2007−83190(P2007−83190A)
【公開日】平成19年4月5日(2007.4.5)
【国際特許分類】
【出願番号】特願2005−276798(P2005−276798)
【出願日】平成17年9月22日(2005.9.22)
【出願人】(303000420)コニカミノルタエムジー株式会社 (2,950)
【Fターム(参考)】
【公開日】平成19年4月5日(2007.4.5)
【国際特許分類】
【出願日】平成17年9月22日(2005.9.22)
【出願人】(303000420)コニカミノルタエムジー株式会社 (2,950)
【Fターム(参考)】
[ Back to top ]

