Fターム[2G041JA04]の内容
その他の電気的手段による材料の調査、分析 (22,023) | イオン化前の処理 (1,172) | 標識付与 (186) | プローブ物質自体、ラベル物質自体 (95)
Fターム[2G041JA04]に分類される特許
41 - 60 / 95
翻訳後修飾蛋白質及び/又はペプチドの選択的富栄養化
本発明は、複合試料から翻訳後修飾された蛋白質及び/又はペプチドの選択的富栄養化に関し、翻訳後修飾は、グリコシル化であり、特定蛋白質/ペプチド標識化プロトコルを、分析すべき翻訳後修飾された蛋白質及び/又はペプチドの特定の選択物と組み合わせることによるものである。 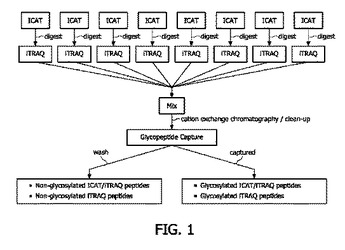 (もっと読む)
(もっと読む)
サンプル中の分析物を定量測定する際に使用するための内部標準および方法
本発明は、サンプル中の複数の分析物を定量分析するための方法を提供する。また、こうした分析に有用な一般的および特定内部標準も記載する。特定の実施形態において、これらの標準は、本明細書に記載もされる液体クロマトグラフィ/質量分析システムに有用であると記載される。さらに、特定の実施形態において、本発明の定量方法は、未知分析物に対して同時に検出され、比較される既知の分析物誘導体を用いて単一のサンプル混合物中に含有される分析物に関する複数の分析物定量についての精密度および/または正確度を増大させるのに有用である。 (もっと読む)
質量分析法
【課題】本発明の目的は、微量試料においてもMSn(n>1)解析を可能にするとともに、MSn(n>1)解析によって分子中の標識化合物の結合位置を同定することによって簡便、迅速に構造情報を得る方法を提供することである。
【解決手段】本発明においては、分子を安定に分子上の特定の部分に標識することによって、容易にイオンを生成、安定化させ、MSの感度を向上させる。このようにして生じたプリカーサーイオンは、MSn(n>1)解析に十分量であり、再現性よく構造特異的なイオンを生成させる。高感度で、簡便、迅速に構造情報を得ることができる。
(もっと読む)
化合物、診断薬、核磁気共鳴分析方法、核磁気共鳴イメージング方法、質量分析方法及び質量分析イメージング方法
【課題】(1)選択した生体内物質について、被爆のおそれや取扱時間の制約がある放射性同位体原子ではなく、安定同位体原子を用いて標識化合物を製造すること、(2)その標識化合物は、選択した生体内物質の自然界に存在する安定同位体原子の置換化合物と分離して感度良く測定可能であること。
【解決手段】生体内物質コリンについて、4級アンモニウム基の窒素原子及び該窒素原子に結合したメチル基の炭素原子の全てをそれぞれの同位体15N及び13Cに置換して標識し、診断薬として用いる。
(もっと読む)
核酸塩基の特徴づけ
本発明は、修飾核酸塩基化合物、修飾核酸模倣化合物、及びそれらの各種使用を提供する。加えて、本発明は、核酸塩基の特徴づけ、SNPの特徴づけ及び核酸の配列決定を提供する。 (もっと読む)
C末端逐次分解反応に由来する塩形成回避法
【課題】微量タンパク質に対しても適用でき、かつ確度の高い内部配列取得技術における反応副産物の効率的除去方法の確立。
【解決手段】解析対象とするペプチド群ないしペプチドが乾燥状態で塗布されているサンプルプレートに対して、C末端逐次分解工程の終了後、含窒素芳香環化合物と水分子を作用させ、アルカン酸と「揮発性塩」を形成させ、得られた「揮発性塩」を、減圧もしくは不活性ガスの送気によりサンプルプレート上から除去する。引き続き、第3アミン化合物と水分子による、加水分解反応工程を実施する際、アルカン酸と第3アミン化合物の「不揮発性塩」形成を抑制する。その結果、質量分析時に置ける高感度、高再現性が確保される。
(もっと読む)
非蛍光標識を用いる、リガンド対の結合を検出するための方法および組成物
【課題】広範な核酸ベースの手順またはタンパク質ベースの手順において有用とされ得る新規組成物を提供すること。
【解決手段】リガンド対の第1のメンバーの第2のメンバーへの結合を検出するための方法であって、
(a)第1のタグ化メンバーのセットを、1以上の第2のメンバーを含み得る生物学的サンプルと、第1のメンバーが第2のメンバーに結合するのに十分な時間および条件下で組み合わせる工程であって、該タグは、特定の第1のメンバーと相関しかつ非蛍光分光分析または電位差滴定により検出可能である、工程;
(b)結合した第1および第2のメンバーを、未結合のメンバーから分離する工程;
(c)該タグを、該第1のタグ化メンバーから切断する工程;および
(d)該タグを、非蛍光分光分析または電位差測定により検出し、そこから該第1のメンバーの該第2のメンバーへの結合を検出する工程;
を包含する、方法。
(もっと読む)
質量分析定量法
アナライトを分析する方法であって、(a)前記アナライトを含んでいてもよい試験サンプルと、各アリコートが既知の量のアナライトを含む少なくとも2の異なるアナライト含有アリコートを含むキャリブレーションサンプルとを混合する工程であって、前記試験サンプルと前記キャリブレーションサンプルの各アリコートとを質量分析法によって区別できるように、サンプル及び各アリコートを、質量分析上種類の異なる質量マーカー基をそれぞれ有する1以上の同重質量標識体を用いて相互に異なるように標識する工程と、(b)質量分析法によって、前記試験サンプル中のアナライトの量及び前記キャリブレーションサンプルの各アリコート中のアナライトの量を測定し、前記キャリブレーションサンプルのアリコート中の既知の且つ測定されたアナライトの量に対して、前記試験サンプル中のアナライトの量を較正する工程とを含むことを特徴とする方法。 (もっと読む)
コードされていない検出可能な標識を含む質量タグ付き試薬を用いる分析物決定
本発明は、レポーター部分およびコードされていない検出可能な標識を含む化合物を用いる質量分析による分析物決定および/または定量に関する方法、混合物、キットおよび組成物に関する。化合物は、標識された分析物の混合物の分析のために組にて用いることができる。本発明は、質量分析による分析物の決定に関する分析物(天然および/または合成物)の非限定例は、限定されないが、蛋白質、ペプチド、核酸、炭水化物、脂質、アミノ酸、ビタミン、ステロイド、プロスタグランジンおよび/または1500ダルトン(Da)未満の質量を有する他の小分子を含む。分析物は、複合混合物における分析物の相対的および/または絶対的定量を可能とする固有の標識試薬を用いて決定することができる。標識試薬は、複合試料混合物の分析のために異性体および/または同重体組で用いることができ、標識試薬は異性体および/または同重体であり得る。  (もっと読む)
(もっと読む)
サイジング技術を用いる核酸分子の分析のための方法および組成物
【課題】種々の核酸反応のために特別に設計されたタグおよびリンカーを提供すること。
【解決手段】広範な種々の核酸反応のために特別に設計されたタグおよびリンカーが開示される。これらは、広範な種々の核酸反応に適切であり、ここで、サイズに基づく核酸分子の分離が必要とされる。1つの局面において、本発明は、核酸分子の正体を決定する方法を提供する。この方法は、(a)1つ以上の選択された標的核酸分子からタグを付けた核酸分子を生成する工程であって、ここでタグが特定の核酸フラグメントと相関し、かつ非蛍光分光分析または電位差測定により検出可能である、工程;(b)サイズによって該タグを付けた分子を分離する工程;(c)該タグを付けた分子から該タグを切断する工程;および(d)非蛍光分光分析または電位差測定により該タグを検出し、それから該核酸分子の正体を決定する工程を包含する。
(もっと読む)
質量分析法を用いたペプチドのアミノ酸配列決定方法、該方法に使用されるペプチド誘導体化試薬、及び試薬キット
【課題】本発明の目的は、質量分析法により、簡便且つ効率的にペプチドのアミノ酸配列を完全に決定できる方法、及び当該方法に使用されるペプチド誘導体化試薬及び試薬キットを提供することである。
【解決手段】質量分析法を用いたペプチドのアミノ酸配列を決定する方法において、(1)ペプチドのN末端アミノ基に下記一般式(I)で示す基を結合させることによりペプチドを誘導体化する工程、(2)前記工程(1)で誘導体化されたペプチドに対して、フラグメントイオンの質量スペクトルを取得する工程、及び(3)前記工程(2)で得られた質量スペクトルに基づいて、ペプチドのアミノ酸配列を決定する工程を順次実施する。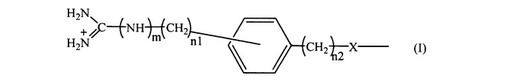 (もっと読む)
(もっと読む)
PCRにより増幅させた伸長DNA鎖の検出方法、および、標的配列の測定方法
【課題】定量性に優れ且つ同一反応液中の複数の増幅産物を各々検出可能な、新たなPCR増幅産物の検出方法を提供する。
【解決手段】標的配列を鋳型とし、これにプライマーと標識化プローブとをアニーリングさせる。DNAポリメラーゼのポリメラーゼ活性により、標的配列にアニーリングしたプライマーから標的配列に相補的なDNA鎖を5’→3’方向に伸長させ、且つ、DNAポリメラーゼの5’→3’エキソヌクレアーゼ活性により、標的配列にアニーリングした標識化プローブを分解し、標識化物質が結合した断片を遊離させる。この伸長反応(それに伴う分解反応)を繰り返し、標識配列に相補的な伸長DNA鎖を増幅する。この反応液について質量分析を行い、遊離した標識化物質結合断片の有無や量を検出して、標識配列に相補的な伸長DNA鎖の有無または増幅量を検出する。
(もっと読む)
質量分析を用いたアミノ酸配列解析方法、アミノ酸配列解析装置、アミノ酸配列解析用プログラム、及びアミノ酸配列解析用プログラムを記録した記録媒体
【課題】デノボ・シーケンスによるアミノ酸配列の推定の信頼性を向上させる。
【解決手段】マススペクトルデータに基づいてアミノ酸配列候補を選定する際に、その信頼度を示すスコアを最大化するアミノ酸配列候補を見い出す問題を、一方向の軸がアミノ酸配列上の位置、他方向の軸がマススペクトルの質量である2次元的な非巡回的グラフ上の最長路問題として定式化する。そして、被検ペプチドに由来するピークの質量と強度とを集めたピークリストに基づいて経路探索を実行することでピーク強度を加算したスコアを求め、スコアの大きなものを選択して経路を逆に辿りながら各アミノ酸を特定し、アミノ酸配列を求める。この方法によれば、高速の演算処理が可能であるため、正しいアミノ酸配列が漏れないように多数の候補を挙げることができる。
(もっと読む)
タンパク質ラベリングにおけるアリールボロン酸の使用
本発明は、アリールボロン酸タグ付け試剤によるポリペプチド中のヒスチジンのタグ付けに関する。本発明は、一つのタンパク質サンプル又はタンパク質サンプルのプールからヒスチジン含有ペプチドを単離して同定することによってサンプル中のタンパク質を同定するための方法及び装置をさらに説明する。本発明は、コンピュータで切断されたタンパク質からのヒスチジン含有ペプチドのデータベース及びタンパク質の同定におけるそれらの使用をさらに説明する。質量のみで同定できない場合は、ペプチドの質量以外の少なくとも一つ以上の物理化学的特性が考慮される。 (もっと読む)
質量分光によるタンパク質分解処理の分析
本発明は、N末端ペプチドの同位体ラベリングに基づいて特異なタンパク質分解処理を決定するためのサンプルの同時分析に関し、同位体ラベリングが、酵素タンパク質分解の間の18Oの組込みによって達成される。例えば本発明は、同位体ラベリングを用いて2つのタンパク質サンプルを分析するための装置であって、2つのサンプルソース、修飾試剤のソースを備えたタンパク質修飾ユニット、ラベリング及びタンパク質切断ユニット及び対応するラベルソース、N末端ペプチド単離ユニット、分離ユニット、質量分光器ユニット、並びにデータ分析ユニットを有する装置である。 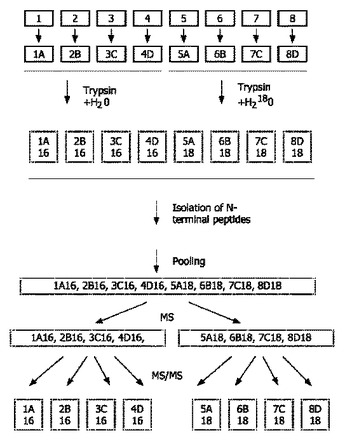 (もっと読む)
(もっと読む)
質量分光測定法の分析において多重化することを可能にするためのポリペプチドの二重のラベリングのための化合物及び方法
本発明は、差別的にラベリングする異なるタンパク質の試料に適切な同位体の及び等圧のラベル構成成分の両方を備えた二重のラベリング試薬を記載する。個々のタンパク質の試料のラベリングの後に、全ての試料は、貯留される。貯留された試料からのペプチドは、各々の差別的に二重にラベリングされたポリペプチドの相対的な濃度を決定するために質量分光測定法によって単離されると共に分析される。バランス基 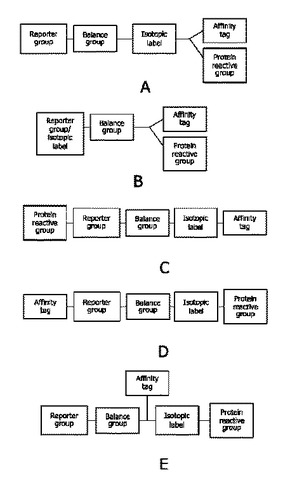 (もっと読む)
(もっと読む)
永続的な化学的マーカーおよびポリマー中の情報の識別
本発明は、ポリマーおよびその添加物(エイジング添加物、熱安定剤添加物、光安定剤添加物、可塑剤添加物または難燃性添加物、ならびに染料および他の高価値添加物など)へ化学的標識を行う方法およびその標識された情報を識別する方法に関する。製造中にポリマーマトリックスに配合されて定着する化合物中の好適な元素の、規定の原子質量を有する同位体を使用することにより、標識が行われる。結果として、高濃度の異物質によるポリマー特性への悪影響がなく、全製品寿命にわたって読み取り可能な化学的コードが得られる。この方法により、ポリマーの供給源を追跡したり、他の生産者からの化学的に同一な生成物と混合されている可能性を検証したり、あるいは、添加物が特定の濃度で添加されているかどうかを後に明らかにできることができる。 (もっと読む)
チロキシンを含む化合物の分析方法
本発明の教示は、アイソバリック標識および親・娘イオン遷移モニタリング(PDITM)を用いて1つ以上のサンプルにおいて1つ以上のチロキシン化合物を分析するための方法を提供する。種々の実施形態では、この方法は以下の工程を包含する:(a)1つ以上のチロ キシン化合物を、1セットのアイソバリックタグ由来の異なるアイソバリックタグで標識する工程と;(b)このアイソバリックに標識されたチロキシン化合物の各々の少なくとも一部を合わせて、合わされたサンプルを生成する工程と;(c)この合わせたサンプルの少なくとも一部をPDITMに供する工程と; (d)伝送レポーターイオンの1つ以上のイオンシグナルを測定する工程と;(e)標準化合物の1つ以上の測定されたイオンシグナルとレポーターイオンの測定されたイオンシグナルとの比較に少なくとも基づくアイソバリックに標識されたチロキシン化合物の1つ以上の濃度を決定する工程。 (もっと読む)
歯周病の予防に有用なポルフィロモナス・ジンジバリスポリペプチド
本発明は、歯周病の予防及び治療において用いられ得るヘム利用能により調節されると同定されるポルフィロモナス・ジンジバリスタンパク質を基礎にしたワクチン組成物及び方法に関する。特に2つの特定のインターナリン様ポルフィロモナス・ジンジバリスタンパク質、即ち宿主細胞によるポルフィロモナス・ジンジバリスのインターナリゼーションに関与するPG0350及びPG1374、細胞表面リポタンパク質であるとされる仮説的タンパク質PG1019、並びにアルキルヒドロペルオキシドレダクターゼタンパク質PG0618は、歯周病の予防及び治療のための有用な標的と同定された。 (もっと読む)
デノボシーケンス解析方法,解析ソフト,解析ソフトを記憶した記憶媒体,試薬キット
【課題】衝突誘起解裂を備えた液体クロマトグラフ質量分析計より得られたマススペクトルからデノボシーケンス解析を行う場合、N末端を含むb系列とC末端を含むy系列の値を区別ができないため、正確なアミノ酸配列が困難である。
【解決手段】酵素消化するさいに、縮合効率の高いリジルエンドペプチダーゼ(Lys−C)酵素などを用いてC末端側に質量数の大きな官能基を導入する。導入後、質量分析計で測定するとy系列(官能基の導入されていない)と官能基が導入されているb系列を質量分析計の質量数から簡単に判別できるにする。
(もっと読む)
41 - 60 / 95
[ Back to top ]



