Fターム[4H050BA51]の内容
第5−8族元素を含む化合物及びその製造 (19,778) | 反応の促進・抑制 (696) | 金属を含まない有機化合物触媒 (82) | 窒素を含む化合物 (44)
Fターム[4H050BA51]に分類される特許
1 - 20 / 44
エステルの不斉加水分解方法
【課題】人工触媒を用いたエステルの不斉加水分解方法を提供する。
【解決手段】下式(Ia)で表される四級アンモニウム塩を触媒として、常圧下、−60℃〜50℃で、塩基性水溶液または金属水酸化物の存在下に非水溶性溶媒中で加水分解するエステルの不斉加水分解方法。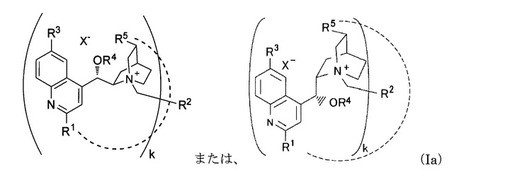
(式中、R1は水素原子等を表し、R2はアリール基等を表し、R3は水素原子等を表し、R4は水素原子等を表し、R5は低級アルキル基等を表し、X-はハロゲン原子等を表し、kは1または2の整数を表す。)
(もっと読む)
有機半導体リン含有化合物およびその製造方法
【課題】新規なアルコール系溶媒に可溶な有機半導体リン含有化合物およびその製造方法の提供。
【解決手段】ジアリールホスフィンオキシド誘導体とハロゲン化トリアリールホスフィンオキシド誘導体を、溶媒中、縮合触媒存在下に縮合させることからなる有機半導体リン含有化合物及びその製造方法。リン含有有機化合物としては、4,4’,4”−トリス(ジフェニルホスフィニル)−トリフェニルホスフィンオキシド、4,4’−ビス−(ジフェニルホスフィニル)−トリフェニルホスフィンオキシド、4,4’,4”−トリス−(ジ−p−トリル−ホスフィニル)−トリフェニルホスフィンオキシド等を提供する。リン含有有機化合物は、イオン化ポテンシャル、バンドギャップ、ガラス転移温度などの性質が十分であり、良好な電子輸送能、正孔阻止能、耐熱性を備えている。
(もっと読む)
ジアミノニトリル類縁体の製造方法
【課題】ジアミノニトリル類縁体を効率良く提供することである。
【解決手段】フルオレニリデン基を有するα−アミノアセトニトリルとイミンとを反応させてジアミノニトリル類縁体を生成するジアミノニトリル類縁体の製造方法。
(もっと読む)
ホスホロアミダイト化合物の製造法
【課題】新規なアミダイト化合物の製造法を提供する。
【解決手段】シリカ表面シラノールの全部または一部がアミノアルキルシリルで修飾されたシリカゲル(NHシリカゲル)を担体としたシリカゲルカラムを使用して、次の一般式(1)で表されるホスホロアミダイト化合物を精製する工程を含む、ホスホロアミダイト化合物(1)の製造法。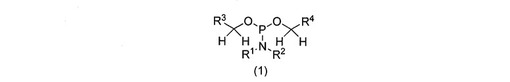 (もっと読む)
(もっと読む)
光学活性β−アシルオキシリン酸エステル誘導体の製造方法
【課題】ラセミ体のβ−ヒドロキシリン酸エステル誘導体から光学活性β−アシルオキシリン酸エステル誘導体を得る方法の提供。
【解決手段】下記式(I)
(式中、R1は、炭素数1〜5のアルキル基などの基である。)で示される光学活性オキサゾリン誘導体、銅塩、及び塩基の存在下、ラセミ体のβ−ヒドロキシリン酸エステル誘導体とカルボン酸ハライド化合物を反応させ、得られた反応物から下記式(IV)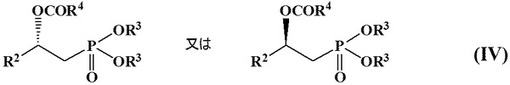
(式中、R3は、炭素数1〜3のアルキル基などの基で、R4は、置換基を有してもよいアリール基。)で示される光学活性β−アシルオキシリン酸エステル誘導体を分離する方法。
(もっと読む)
4置換不斉炭素を有するα−アミノリン酸化合物の製造方法
【課題】ケチミン類と亜リン酸エステルから4置換不斉炭素を有するα-アミノリン酸化合物を合成できるようにする。
【解決手段】下記化学式1で示されるケチミン類に触媒と塩基存在下で水酸基を有する亜リン酸を反応させて4置換不斉炭素を有するα-アミノリン酸化合物を製造する。
【化1】
ただし、R1は、2,4,6-トリメチルベンゼンスルホニル基などのアレーンスルホニル基であり、R2,R3は、アルキル基またはアリール基である。触媒は、ヒドロキニン、ヒドロキニジンなどであり、塩基は、炭酸ナトリウム、炭酸カリウムなどである。
(もっと読む)
テトラホスフィンテトラオキシド、その製造方法、並びにその用途
【課題】新規ホスフィンオキシド及びその製造方法、これを用いた希土類金属抽出方法の提供。
【解決手段】下式(1)で表されるテトラホスフィンテトラオキシド。
(R1〜R2は、アリール基等、nは2以上の整数。)該化合物と希土類金属塩を溶媒中で接触させるとテトラホスフィンテトラオキシドが配位した希土類金属錯体が得られる。該化合物は、下記化合物(4)とジフェニルホスフィンオキシド等を反応させ製造する。 (もっと読む)
(もっと読む)
N4−(2,2−ジメチル−4−[(二水素ホスホノオキシ)メチル]−3−オキソ−5−ピリド[1,4]オキサジン−6−イル)−5−フルオロ−N2−(3,4,5−トリメトキシフェニル)−2,4−ピリミジンジアミン二ナトリウム塩の合成
本発明は、製薬化学/プロセス化学の分野に関する。本明細書には、N4-(2,2-ジメチル-4-[(二水素ホスホノオキシ)メチル]-3-オキソ-5-ピリド[1,4]オキサジン-6-イル)-5-フルオロ-N2-(3,4,5-トリメトキシフェニル)-2,4-ピリミジンジアミン二ナトリウム塩、特に水和物(例えば六水和物)を調製するプロセスが開示されている。該化合物は、様々な疾患の治療および予防において有用である。また、N4-(2,2-ジメチル-4-[(ジアルキルホスホノオキシ)メチル]-3-オキソ-5-ピリド[1,4]オキサジン-6-イル)-5-フルオロ-N2-(3,4,5-トリメトキシフェニル)-2,4-ピリミジンジアミンを調製するプロセスも開示されている。いずれのプロセスもアミドの使用を伴う。 (もっと読む)
フルオレノンイミンを用いた炭素−炭素結合生成反応
【課題】ジアミン類縁体あるいはアミノアルコール類縁体を効率良く提供する。
【解決手段】炭素−炭素結合を生成する反応方法であって、フルオレノンイミン化合物と、下記の一般式[II]で表される化合物、またはカルボニル化合物を反応させてジアミン類縁体、またはアミノアルコール類縁体を合成する。一般式[II] (もっと読む)
(もっと読む)
遷移金属錯体の製造方法
【課題】収率及び純度に優れる遷移金属錯体の製造方法を提供すること。
【解決手段】アミン化合物の存在下、特定のシクロペンタジエン化合物と有機リチウム化合物とを反応後、続いて特定の遷移金属化合物を反応させて得た反応液に溶媒を添加した後アミン化合物と溶媒とを留去し、最後に濃縮液をろ過してろ液を得ることで下記一般式(3)で表される遷移金属錯体を製造する。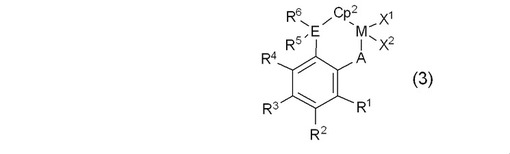
(式中、Mは第4族の遷移金属原子を表し、X1及びX2は、ハロゲン原子を表し、Aは、第16族の原子を表し、Eは、第14族の原子を表し、R1〜R6は、水素原子、アルキル基等を表し、Cp2はシクロペンタジエン形アニオン骨格を有する基を表す。)
(もっと読む)
難燃剤のための亜ホスホン酸誘導体のヒドロホスホリル化
本発明は、次式(I)で表されるアルキル亜ホスホン酸誘導体、
A−P(=O)(OX)−H (I)
(式中、Aは、場合により置換されているC2〜C18−アルキル、C2〜C18−アルキレン、C6〜C18−アリールアルキル、C6〜C18−アリールアルキルを意味し、および、Xは、H、場合により置換されている、C1〜C18−アルキル、C6〜C18−アリール、C6〜C18−アリールアルキル、C6〜C18−アルキルアリール、C2〜C18−アルキレン、Mg、Ca、Al、Sb、Sn、Ge、Ti、Fe、Zr、Zn、Ce、Bi、Sr、Mn、Cu、Ni、Li、Na、K、H、および/またはプロトン化された窒素塩基を意味する。)および、b) 次式(II)で表されるジエステル形成性オレフィン、からの付加物、
【化1】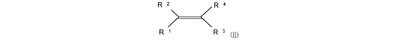
(式中、R2、R4は、同一または異なっていて、そしてCO2H、CO2R5、R6−CO2H、R6−CO2R5を意味し、およびR1、R3は、同一または異なっていて、そしてH、R5を意味し;または、R1、R4は、同一または異なっていて、そしてCO2H、CO2R5、R6−CO2H、R6−CO2R5を意味し、および、R2、R3は、同一または異なっていて、そしてH、R5を意味し;または、R2、R4は、同一または異なっていて、そして−CO−O−CO−、−CO−S−CO−、−CO−NR1−CO−、−CO−PR1−CO−を意味し、および、R1、R3は、同一または異なっていて、そしてH、R5を意味し;または、R1、R2は、同一または異なっていて、そしてCO2H、CN、CO2R5、R6−CO2H、R6−CO2R5を意味し、および、R3、R4は、同一または異なっていて、そしてH、R5を意味し;または、R1、R2は、同一または異なっていて、そして−CR23−CO−O−CO−、−CR23−CO−NR1−CO−、−CR23−CO−O−CO−CR23、−CR23−CO−NR1−CO−CR23を意味し、および、R3、R4は、同一または異なっていて、そしてH、R5を意味し;または、R2、R4は、それぞれ−CO−CR5=CR5−CO−を意味し、および、R1、R3は、同一または異なっていて、そしてH、R5を意味し;R5は、C1〜C18−アルキル、C6〜C18−アリール、C6〜C18−アリールアルキル、C6〜C18−アルキルアリールを意味し;R6は、C2〜C18−アルキレン、C6〜C18−アリーレン、C6〜C18−アルカリーレンおよび/またはC6〜C18−アラルキレンを意味する。);それの製造方法およびそれの使用に関する。 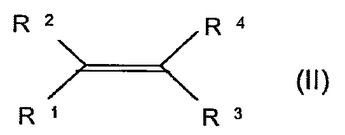 (もっと読む)
(もっと読む)
混合置換ジアルキルホスフィン酸、混合置換ジアルキルホスフィン酸エステル、および混合置換ジアルキルホスフィン酸塩の調製方法、およびそれらの使用
本発明は、a)ホスフィン酸ソース物質(I)を、オレフィン(IV)を用いて触媒Aの存在下でアルキル亜ホスホン酸、その塩またはそのエステル(II)に変換するステップ、および、b)それにより生じたアルキル亜ホスホン酸、その塩またはそのエステル(II)を、オレフィン(IV)を用いて、触媒Bの存在下で、混合置換ジアルキルホスフィン酸誘導体(III)に変換するステップからなることを特徴とする、混合置換ジアルキルホスフィン酸、混合置換ジアルキルホスフィン酸エステル、および混合置換ジアルキルホスフィン酸塩を調製する方法に関し、式(III)中、R1、R2、R3、R4、R11、R12、R13、R14は、同じであるか、または異なっており、相互に独立して、何よりも特にH、C1〜C18−アルキル、C6〜C18−アリール、C6〜C18−アラルキル、C6〜C18−アルキルアリールであり、Xは、H、C1〜C18−アルキル、C6〜C18−アリール、C6〜C18−アラルキル、C6〜C18−アルキルアリール、Mg、Ca、Al、Sb、Sn、Ge、Ti、Fe、Zr、Zn、Ce、Bi、Sr、Mn、Cu、Ni、Li、Na、K、および/またはプロトン化窒素塩基を表わしており、また触媒Aは、各種遷移金属および/または各種遷移金属化合物、および/または、いずれか一つの遷移金属および/またはいずれか一つの遷移金属化合物に、少なくとも一つのリガンドを結合した触媒系であり、また触媒Bは、過酸化物を生成する化合物および/またはペルオキソ化合物および/またはアゾ化合物である。  (もっと読む)
(もっと読む)
アリル化合物を用いる、モノアリル官能性ジアルキルホスフィン酸、それらの塩およびエステルの製造方法およびそれらの使用
この発明は、アリル化合物を用いる、モノアリル官能性ジアルキルホスフィン酸、同エステルおよび同塩の製造方法であって;a)ホスフィン酸源(I)をオレフィン(IV)と、触媒Aの存在下でアルキル亜ホスホン酸、その塩またはエステル(II)に変換させ、b)生成したアルキル亜ホスホン酸、その塩またはエステル(II)を、式(V)のアリル化合物と、触媒Bおよび塩基の存在下で、モノアリル官能性ジアルキルホスフィン酸誘導体(III)に変換させる方法に関し、ここに、R1、R2、R3、R4、R5、R6、R7、R8、R9は、同一または互いに異なって、また互いに独立して、とりわけH、C1〜C18アルキル、C6〜C18アリール、C6〜C18アラルキル、C6〜C18アルキルアリールであり、XはH、C1〜C18アルキル、C6〜C18アリール、C6〜C18アラルキル、C6〜C18アルキルアリール、Mg、Ca、Al、Sb、Sn、Ge、Ti、Fe、Zr、Zn、Ce、Bi、Sr、Mn、Cu、Ni、Li、Na、K、および/またはプロトン化窒素塩基を表し、触媒AおよびBは、遷移金属および/または遷移金属化合物および/または、遷移金属および/または遷移金属化合物および少なくとも1つの配位子から構成される触媒系である。 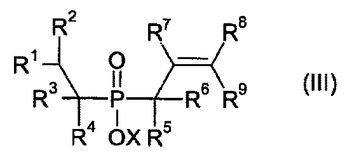 (もっと読む)
(もっと読む)
ホスホロモノクロリダイト合成のためのスラリー法
三塩化リン(PCl3)を2,2’−ビフェノールのような芳香族ジオールと、固体形態の一部の芳香族ジオールを含み且つ芳香族ジオールの残りの部分及び有機溶媒を含む溶液相を含んでなるスラリー中で、ホスホロモノクロリダイトを生成させるのに充分な反応条件下で接触させることによる、ホスホロモノクロリダイトを高収率で製造する方法。このスラリーは、芳香族ジオールの総モルに基づいて計算して、5モル%未満の窒素塩基を含み、有機溶媒は、その塩化水素溶解度が低いという基準で選ばれる。 (もっと読む)
ホスホロモノクロリダイト合成のための等温プロセス
本発明は、三塩化リン(PCl3)を、1種又はそれ以上の有機溶媒の溶液中の芳香族ジオールと、ホスホロモノクロリダイトを製造するために充分な反応条件下で、接触させることによる高収率でのホスホロモノクロリダイトの製造プロセスに関する。この反応は、第一の有機溶媒中に溶解された芳香族ジオールを含有する供給溶液を、PCl3及び任意的に1種又はそれ以上の第二の有機溶媒を含有する反応ゾーンの中に添加することによって実施し、前記添加は、実質的に等温のプロセス条件を維持するように実施する。この反応溶液は、5モル%よりも少ない窒素塩基を含有する。(式I、II)  (もっと読む)
(もっと読む)
[4−(2−ジフェニルホスファニルナフタレン−1−イル)フタラジン−1−イル]−(1−フェニルエチル)アミンの光学活性体の製造方法
【課題】カラムクロマトグラフィーによる分離を行うことなく簡便な方法によりN−PINAPの光学活性体を提供する。
【解決手段】(R)−または(S)−[4−(2−ジフェニルホスファニルナフタレン−1−イル)フタラジン−1−イル]−(1−フェニルエチル)アミンの混合物の溶液と、光学活性な有機スルホン酸とを混合して晶析させる、(R,P)−[4−(2−ジフェニルホスファニルナフタレン−1−イル)フタラジン−1−イル]−(1−フェニルエチル)アミンの光学活性な有機スルホン酸塩または(S,M)−[4−(2−ジフェニルホスファニルナフタレン−1−イル)フタラジン−1−イル]−(1−フェニルエチル)アミンの光学活性な有機スルホン酸塩の製造方法。
(もっと読む)
立体障害性フェニル基含有ホスホネート化合物、その製造方法、およびこれを含有する難燃性ポリカーボネート系樹脂組成物
【課題】立体障害性フェニル基含有ホスホネート化合物、その製造方法、およびこれを含有する難燃性ポリカーボネート系樹脂組成物の提供。
【解決手段】下記化学式(1)で表される立体障害性フェニル基含有ホスホネート化合物、その製造方法、およびこれを含有する難燃性ポリカーボネート系樹脂組成物。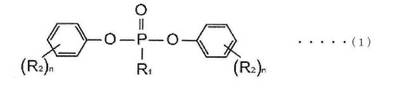
前記化学式(1)中、R1はC1〜C6の直鎖もしくは分岐鎖のアルキル基またはC6〜C14のアリール基であり、R2はC1〜C6の直鎖アルキル基、またはC3〜C6の分岐鎖アルキル基であり、nは、それぞれ独立して、1〜3の整数である。
(もっと読む)
有機リン化合物の連続製造方法及びその使用
本発明は、当該技術において長い間公知であった有機リン化合物、特に9,10−ジヒドロ−9−オキサ−10−ホスファフェナントレン−10−オキシド(DOPO)及びその誘導体の製造に関する。これらは、ポリマー用の添加剤として好ましく用いられる。特に、ポリマー、例えばポリエステル、ポリアミド、エポキシ樹脂のための難燃剤としてのDOPO及びその誘導体の使用が有利であることが見出された。 (もっと読む)
リン含有α−アミノ酸の製造法およびその製造中間体としてのリン含有ニトロ誘導体
【課題】除草剤D,L−2−アミノ−4−(ヒドロキシメチルホスフィニル)−ブタン酸を穏和な反応条件で、塩などの副生物が大量に生成することなく、安価に、良好な収率で、製造する方法を提供する。
【解決手段】次式(3)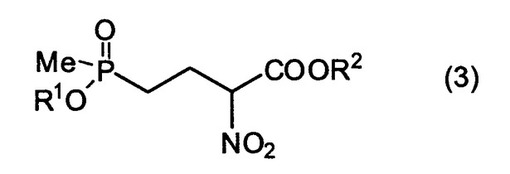
[式中、R1はアルキル基、クロロエチル基を表し、R2はアルキル基を表す]の化合物のニトロ基を還元することによってアミノ基に変換した後、さらにリン酸エステルおよびカルボン酸エステルを加水分解して脱保護することを含んでなる、D,L−2−アミノ−4−(ヒドロキシメチルホスフィニル)−ブタン酸の製造方法。
(もっと読む)
アミンおよびアミンオキシドで開始するアルキルホスフィン酸の合成方法
本発明は、アルキルホスフィン酸の新規製造方法に関する。より詳しくは、アミンおよびアミンオキシドの存在下でのアルキルハロゲン化物と次亜リン酸誘導体とのカップリング反応に関する。 (もっと読む)
1 - 20 / 44
[ Back to top ]