国際特許分類[C12P41/00]の内容
化学;冶金 (1,075,549) | 生化学;ビール;酒精;ぶどう酒;酢;微生物学;酵素学;突然変異または遺伝子工学 (115,607) | 発酵または酵素を使用して所望の化学的物質もしくは組成物を合成する方法またはラセミ混合物から光学異性体を分離する方法 (13,841) | 酵素または微生物を利用してラセミ混合物から光学異性体を分離する方法 (237)
国際特許分類[C12P41/00]に分類される特許
161 - 170 / 237
ヒンバシン類似物のキラルプロパルギルアルコールおよびエステル中間体の調製
本出願は、一連のラセミ体のプロパルギルアルコールの、対応する(R)−エネンチオマーへの変換のための、新規のプロセスを開示している。本出願はまた、(R)−エステルを調製するために、そのラセミ体からのプロパルギルアルコールのエナンチオ選択性のエステル化を開示している。エナンチオ選択性は、実験的に決定される酵素の使用により高められる。プロパルギルアルコールおよびキラルエステルは、例えば、トロンビン受容体アンタゴニストのような化合物の調製において、有用であり得る。合成経路のうち、以下:式(I)〜式(VI)が開示される。  (もっと読む)
(もっと読む)
光学活性クロマンカルボン酸エステルの製造方法
本発明の光学活性クロマンカルボン酸エステルの製造方法においては、ラセミ型クロマンカルボン酸の一方の対掌体を、生体触媒の存在下、アルコールを含む溶媒中でエステル化した後、未反応の他方のクロマンカルボン酸対掌体を分離して目的の光学活性エステルを得る。光学活性クロマンカルボン酸エステルは、医薬・農薬等の原料として有用であり、本発明の製造方法は、その効率的で工業的に実施可能な製造方法である。 (もっと読む)
トリプチセン類化合物の製造方法
【課題】
機能性材料や医薬品等の原料として広い分野で有効に利用されるトリプチセン誘導体の光学活性体を、より安価で、操作が煩雑でなく、かつ安全性にも優れた生化学的手法による方法で製造する方法を提供すること。
【解決手段】
エステル基などの加水分解され得る官能基を有するトリプチセン誘導体の光学異性体混合物に、コレステロールエステラーゼなどの不斉加水分解する能力を有する加水分解酵素を作用させ、光学活性なトリプチセン誘導体を得る。
(もっと読む)
2−アルキルシステインアミド又はその塩、並びに、それらの製造方法及び用途
一般式(2)で示される4−アルキルチアゾリジン−4−カルボン酸アミド又はその塩を加水分解して一般式(1)で示される2−アルキルシステインアミド又はその塩を得る、2−アルキルシステインアミド又はその塩の製造方法。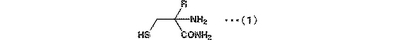
(一般式(1)中、Rは、炭素数1〜4の低級アルキル基を示す。)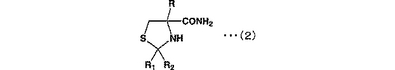
(一般式(2)中、Rは、炭素数1〜4の低級アルキル基を示し、R1及びR2は、各々独立に、水素若しくは炭素数1〜4の低級アルキル基、又は互いに結合して炭素数4〜7の脂環式構造をとる。但し、R1及びR2は両者が同時に水素であることはない。)
一般式(1)の化合物を2−アルキル−L−システインアミドを立体選択的に加水分解する活性を有する微生物の菌体又は菌体処理物を作用させて、2−アルキル−L−システインを生成せしめる。 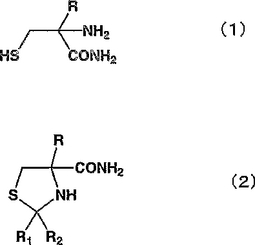 (もっと読む)
(もっと読む)
3−アミノ−3−アリールプロピオン酸n−アルキルエステル及びその製造方法並びに光学活性3−アミノ−3−アリールプロピオン酸及びその対掌エステルの製造方法
本発明は、式(I):
式中、Ar1は、置換基を有していても良いアリール基を表す、ただし、フェニル基及び4−メトキシフェニル基を除く、R1は、n−プロピル基又はn−ブチル基を表す、
で示される3−アミノ−3−アリールプロピオン酸n−アルキルエステル及びその製造方法、並びにその光学活性体及び式(III−a):
式中、Arは、置換基を有していても良いアリール基を表し、*は不斉炭素を表す、
で示される光学活性(S又はR)−3−アミノ−3−アリールプロピオン酸、及び式(IV−a):
式中、Ar及びR1は、前記と同義であり、*は不斉炭素を表す、ただし、一般式(III−a)の化合物とは逆の立体絶対配置を有する、
で示される光学活性(R又はS)−3−アミノ−3−アリールプロピオン酸n−アルキルエステルの製造方法を提供する。  (もっと読む)
(もっと読む)
化学的方法
インスリン抵抗性およびその他の代謝症候群の兆候に関連するかどうかにかかわらず、脂肪疾患(異常脂質血症)などの臨床症状の治療に有用である特定の3−フェニル−2−アリールアルキルチオプロピオン酸誘導体の酵素的および化学的製造方法が説明されており、さらに、これらの方法で用いられる特定の新規の中間体も説明されている。 (もっと読む)
光学活性な化合物の製造方法
【課題】 エポキシドヒドロラーゼ(EH)を有機合成試薬として使用して、ラセミ体のエポキシドから光学活性な化合物を製造する方法を提供すること。
【解決手段】 本発明の光学活性な化合物の製造方法は、エポキシドのラセミ体に、エポキシド加水分解活性を有する微生物または該微生物に由来する酵素を作用させて、該ラセミ体の一方の鏡像体を加水分解する工程;および反応液から目的の光学活性な化合物を回収する工程を包含し、該エポキシドは、式(I)で表される化合物:
【化1】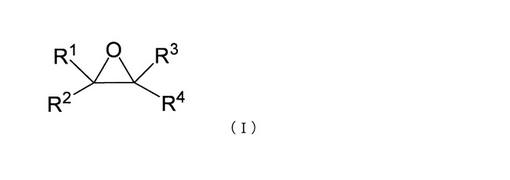
であり、そして該微生物は、バチルス属、クロモバクテリウム属、ノカルディア属、ステノトロホモナス属、ミクロバクテリウム属、シュードモナス属、ゴルドナ属、クレブシエラ属、キャンディダ属、ガラクトマイセス属、サッカロマイセス属、スポリジオボラス属、ロドスポリジウム属、ピチア属、またはロドトルラ属に属する。
(もっと読む)
(R)−γ−アミノ−β−ヒドロキシ酪酸((R)−GABOB)のエナンチオ収束的化学酵素合成
本発明は、特に、(R)−GABOBの調製にとって鍵となる3−ヒドロキシ−4−トリチルオキシブタンニトリルの両エナンチオマーの立体選択的な調製のための、そのラセミ体のリパーゼ媒介速度論的分割による化学酵素的方法、及び(R)−GABOBのエナンチオ収束的合成における有効な応用、に関する。 (もっと読む)
光学活性2−ヒドロキシエステル化合物の製造方法
【課題】反応後にpH調整を繰り返すことなく、容易に、式(2)
(式中、R1は置換されていてもよい低級アルキル基等を表わし、*は光学活性な炭素原子であることを表わす。)
で示される光学活性2−ヒドロキシエステル化合物や式(4)
(式中、*は上記と同一の意味を表わす。)
で示される光学活性2−ヒドロキシ酢酸化合物を製造する方法を提供すること。
【解決手段】式(1)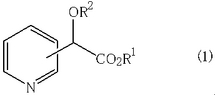
(式中、R1は上記と同一の意味を、R2は低級アシル基を表わす。)
で示される2−アシルオキシエステル化合物のアシルオキシ基部位を優先的に加水分解する能力を有する酵素、または該酵素の産生能を有する微生物の培養物あるいはその処理物を、前記式(1)で示される化合物に接触させることを特徴とする式(2)で示される光学活性2−ヒドロキシエステル化合物の製造方法。
(もっと読む)
熱安定性ωアミノ基転移酵素
熱安定性ωアミノ基転移酵素、特に高い反応速度を有し、高濃度のドナーアミンに耐性である熱安定性ωアミノ基転移酵素を用いて、キラルアミンの混合物を鏡像異性的に濃縮するか、またはアミノ基が非末端のキラル置換された炭素原子に結合する一対のキラルアミンの1つを立体選択的に合成することができる。 (もっと読む)
161 - 170 / 237
[ Back to top ]

