国際特許分類[G01N33/53]の内容
物理学 (1,541,580) | 測定;試験 (294,940) | 材料の化学的または物理的性質の決定による材料の調査または分析 (128,275) | グループ1/00から31/00に包含されない,特有な方法による材料の調査または分析 (37,154) | 生物学的材料,例.血液,尿 (30,164) | 生物学的材料,例.血液,尿,の化学分析;生物学的特異性を有する配位子結合方法を含む試験;免疫学的試験 (26,776) | 免疫分析;生物学的特異的結合分析;そのための物質 (18,208)
国際特許分類[G01N33/53]の下位に属する分類
免疫化学的試験物質の製造 (801)
液相中に形成された免疫複合体によるもの (424)
免疫化学物質を固定化するための不溶性担体によるもの (5,113)
動力学的測定,すなわち.抗原―抗体相互作用の進行速度,を用いるもの (9)
抗原または抗体の拡散または移動を用いるもの (28)
抗体フラグメントを含むもの (17)
あらかじめ存在する免疫複合体または自己免疫疾患のためのもの (102)
配位子結合試薬として,特異的キャリアまたは受容体蛋白質を用いるもの (714)
微生物,例.原生動物,細菌,ウィルス,のためのもの (1,041)
酵素またはイソ酵素のためのもの (282)
癌のためのもの (1,708)
肝炎のためのもの (131)
モノクローナル抗体を含むもの (445)
国際特許分類[G01N33/53]に分類される特許
1,081 - 1,090 / 7,393
直接的な化学的溶解のための方法および組成物
直接的な化学的溶解のための組成物は、アッセイ適合性のバッファー組成物およびアッセイ適合性の界面活性剤を含んでいる。検体貯蔵のための組成物と併せる場合、このような組成物は、生物学的試料中の細胞から溶解した核酸およびタンパク質に対する望ましくない修飾を防ぐ。このような組成物からの試料のアッセイは、遠心分離および長時間の高温処理加工などの高価で時間を要するステップを必要としない。本発明の直接的な化学的溶解のための組成物は、輸送媒体をデカントして除く必要なしに、または他の点で輸送媒体をアッセイ適合性のバッファーと交換する必要なしに、生物学的試料中の細胞から核酸の直接的な抽出を可能にする。細胞から核酸を抽出するために、試料をプロテイナーゼKまたは別の酵素と併せる必要はない。細胞を溶解してアッセイ用の標的核酸を得る方法および直接的な化学的溶解のための組成物を試料と併せるためのキットも企図される。 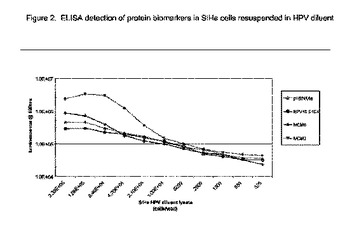 (もっと読む)
(もっと読む)
ブロッキング剤
【課題】本発明は、蛍光色素で標識した試料中の抗原を、抗原抗体反応を利用して測定する方法において、抗体と未反応蛍光色素の非特異反応自体を抑制するためのブロッキング剤を提供することを課題とする。
【解決手段】蛍光色素と抗体との非特異反応を抑制するためのブロッキング剤であって、トリス塩酸を含むことを特徴とするブロッキング剤を提供する。
(もっと読む)
遺伝子マーカー及びその利用
【課題】拒絶反応の診断、免疫抑制剤の薬効の評価、及び免疫寛容の有無の判定を行うことができる遺伝子マーカー、並びに、遺伝子マーカーを指標として迅速かつ簡便に行うことができる、拒絶反応の診断方法、免疫抑制剤の薬効を評価する方法、免疫抑制剤の同定方法、免疫抑制剤の選択方法、免疫抑制剤の用量決定方法、免疫寛容の有無を判定する方法、及びキットを提供する。
【解決手段】拒絶反応により発現量が1.5倍以上上昇し、免疫抑制剤により発現量が1.5倍以上抑制された免疫関連遺伝子、特にPSMB9遺伝子を遺伝子マーカーとして同定した。その遺伝子マーカーの発現量を指標とすることにより、拒絶反応の診断、免疫抑制剤の薬効の評価、及び免疫寛容の有無の判定を迅速かつ簡便に行うことが可能になる。
(もっと読む)
ハイブリダイゼーション装置及び方法
【課題】検体濃度が低い場合でもハイブリダイゼーション効率を高めることができる装置および方法を提供すること。
【解決手段】本発明ハイブリダイゼーション装置1、検体液を収容する検体液収容部8と、検体液収容部の深さ方向中間位置あるいはそれより下方に設けられバイオチップ14を水平に保持するバイオチップ取付部と、検体液収容部の両側の外方に対向して設けられた第1および第2のバッファ液収容部10、12と、検体液収容部と第1および第2のバッファ液収容部のそれぞれとを仕切る半透膜4、6と、第1および第2のバッファ液収容部のそれぞれに配置された第1の電極対18、20とを備えている。
(もっと読む)
バイオチップの製造方法、バイオチップ及びそれに用いる除去液
【課題】酸転写用組成物から形成される膜を除去する際、基板上の高分子にダメージを与えることなく、より精密に欠陥などなく膜を除去することができるバイオチップの製造方法を提供することを目的とする。
【解決手段】本発明は、(a)酸に不安定な保護基を有する第1化合物を基板に直接的又は間接的に結合して第1膜を形成する第1膜形成工程、
(b)前記第1膜上に酸転写用組成物を用いて第2膜を形成する第2膜形成工程、
(c)前記第2膜を露光して、露光された部分に対応する前記第1膜から前記保護基を除去する保護基除去工程、
(d)前記第2膜を、環状エステル化合物を含有する除去液を用いて、除去する第2膜除去工程、及び、
(e)前記第1膜のうち前記保護基が除去された部位に第2化合物を結合する第2化合物結合工程、を備える。
(もっと読む)
タウオリゴマーに結合する抗体
本発明の態様は、タウオリゴマーおよびタウオリゴマー特異的抗体に関連した組成物および方法に向けられる。 (もっと読む)
IL−17産生の阻害
【課題】本発明は、インターロイキン23(IL−23)のアンタゴニストを用いた、炎症誘発性サイトカインであるインターロイキン17(IL−17)のT細胞による産生の抑制に関係する。
【解決手段】さらに本発明は、IL−17濃度の上昇がみられることを特徴とする炎症性疾患の治療において、IL−23アンタゴニストを使用することに関係する。IL−23アンタゴニストには、サブユニットあるいはIL−17あるいはIL−17受容体に特異的に結合する抗体が含まれるがこれらに限定されない。さらに本発明はIL−23アゴニストを用いることによるIL−17産生に関係する。
(もっと読む)
抗VEGFモノクローナル抗体およびその抗体を含む薬学的組成物
本発明は、抗VEGFモノクローナル抗体であって、その重鎖の可変ドメインが配列番号l、配列番号2、および配列番号3のアミノ酸配列を含み、および/またはその軽鎖の可変ドメインが配列番号4、配列番号5、および配列番号6のアミノ酸配列を含むモノクローナル抗体を提供する。該抗体は保存番号CGMCC No.3233の細胞系から産生される。本発明はまたVEGF関連疾患を治療するための薬物を調製する際の該抗体の使用も提供し、該抗体を含む薬学的組成物、薬剤、キット及びチップ、並びに、保存番号CGMCC No.3233の細胞系も提供する。 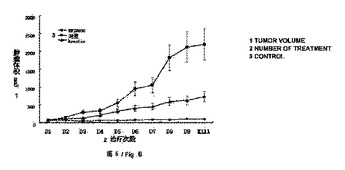 (もっと読む)
(もっと読む)
新規のIgEエピトープの同定
【課題】IgEに特異的に結合するが既にその高親和性レセプターに結合したIgEには結合しない高親和性の非アナフィラキシー性抗体、ならびに、アナフィラキシー性抗体を誘導しない能動免疫のためのペプチドを提供すること。
【解決手段】本発明は、IgEに特異的に結合する高親和性抗体によって認識される、IgEのCH3ドメインに由来する新規のペプチドエピトープに関する。これらの新規のペプチドは、被験体においてこれらのペプチドを投与して高親和性抗体を産生させることによる、被験体の能動免疫のため、ならびに被験体の受動免疫のために、非ヒト宿主においてIgEのこれらの領域に特異的に結合する高親和性抗IgE抗体を産生するための、両方に使用され得る。
(もっと読む)
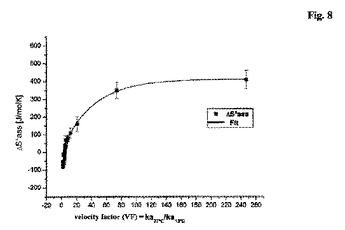
速度因子
本発明は速度因子に関する。この速度因子に基づき抗体を分類することができる、すなわち、抗体を、それらの結合特性に従い、例えばエントロピーまたはエンタルピー的な抗原結合体として特徴づけることができる。速度因子に基づく分類は、詳細な熱力学的測定および/または算出を必要としない。速度因子は、37℃および13℃で測定された抗原・抗体複合体の会合速度定数kaの比である。本発明は、この速度因子を算出するのに2つの実験的測定しか必要とせず、高速・高スループットに適した方法である。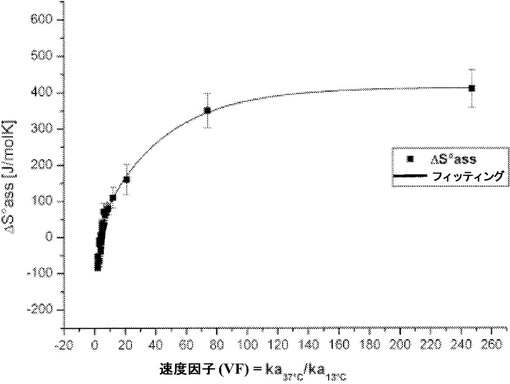
 (もっと読む)
(もっと読む)
1,081 - 1,090 / 7,393
[ Back to top ]