Fターム[4C076CC27]の内容
医薬品製剤 (238,651) | 医療活性成分 (34,824) | 組織細胞の機能に作用 (3,428) | 抗ガン剤 (2,996)
Fターム[4C076CC27]に分類される特許
2,161 - 2,180 / 2,996
RHCCペプチドおよびその使用
本発明は、RHCCペプチドおよび/またはそのフラグメントの様々な使用に関する。該RHCCペプチドおよび/またはそのフラグメントは、目的とする標的部位に物質および/または薬物を送達および放出するために、または液体または非液体材料から、例えば体組織または体液体から物質を除去するために、該ペプチドおよび/またはフラグメントの空洞中への薬物および/または物質の取込みおよび結合を可能にする。RHCCペプチドおよび/またはそのフラグメントは、ある文脈において、ナノ粒子の生成または化学反応における触媒として使用され得る。好ましい態様において、該RHCCペプチドおよび/またはそのフラグメントは、生物体内で所望の部位に薬物を送達するための薬物送達システムを含む。 (もっと読む)
PEG−ワートマニンコンジュゲート
本発明は、水溶性ポリマーを薬物担体として用いるワートマニンの可溶性誘導体に関し、明細書中に記載のような構造を有する化合物を包含する。 (もっと読む)
中性脂質組成物によるsiRNAの送達
本発明は、分子生物学および薬物送達の分野に関する。ある態様において、本発明は、中性(非電荷)リポソームを介する細胞へのsiNA(例えば、siRNA)の送達方法を提供する。これらの方法は、癌などの病気を治療するために用いられ得る。 (もっと読む)
抗腫瘍剤及び新規DNアーゼ
【課題】正常細胞には作用せず、癌にのみ特異的に作用する抗腫瘍剤、及びその有効成分として有用な新規DNアーゼを提供する。
【解決手段】前記抗腫瘍剤は、DNアーゼを有効成分として含有する。前記新規DNアーゼは、ヒト由来胃癌培養細胞MKN−28又はヒト由来子宮頚癌培養細胞HeLa由来のDNアーゼである。
(もっと読む)
アスコルビン酸の安定化誘導体
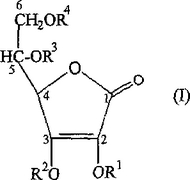
一般式I(式中、R1は、C2〜C22アシル基、アミノ酸基又はC1〜C17アルキル基であり、R2は、アンモニウム又は金属カチオンであり、R3又はR4のそれぞれは、独立に、水素、C2〜C22アシル基、アミノ酸残基又はC1〜C17アルキル基である)のアスコルビン酸誘導体は、アスコルビン酸よりも安定で、薬剤組成物、栄養補給組成物及び化粧品組成物においてビタミンC源として使用することができる。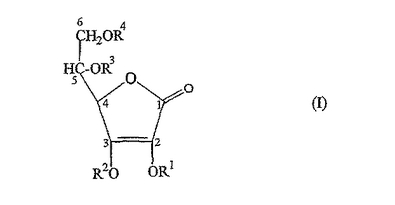
 (もっと読む)
(もっと読む)
機能性ナノ粒子充填カーボンナノチューブおよびその製造のための方法
機能性ナノ粒子の懸濁液またはコロイド溶液で充填されたカーボンナノチューブ、および機能性ナノ粒子で充填されたカーボンナノチューブの製造のための方法を提供する。  (もっと読む)
(もっと読む)
腫瘍内の不均一または混合細胞集団を排除する方法
不均一または混合細胞集団からなる腫瘍を死滅または阻害する方法を記載する。腫瘍の死滅または阻害は、特定の細胞集団に発現すると推測されるユニークリガンドを選択的にターゲティングし、かつそのユニークリガンドを欠如する細胞集団をも死滅させることにより達成される。これらのコンジュゲートは特定の細胞集団へ送達されてこれらの細胞を死滅させ、かつ細胞毒性薬物が放出されて非ターゲット細胞を死滅させ、これにより腫瘍を排除するので、療法用として有用である。 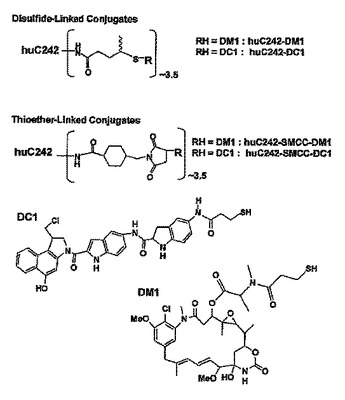 (もっと読む)
(もっと読む)
ピロリドン側基を含む生分解性ポリホスファゼン
ピロリドン側基を含む生分解性のポリホスファゼンポリマおよびこのようなポリホスファゼンポリマの生物医学用途が開示されている。 (もっと読む)
新規ペプチド
本発明は、血管内皮増殖因子受容体2(VEGFR2)をターゲティングするための新規ペプチドに関する。本発明はさらに治療上有効な処置及び画像診断法における当該ペプチドの使用に関する。VEGFR−2は血管新生内皮細胞、造血幹細胞、骨髄中の内皮前駆体細胞及び数種の悪性細胞で発現されるので、これらのペプチド系造影剤は、例えば悪性疾患、心疾患、子宮内膜症、炎症関連疾患及び関節リウマチの診断に使用し得る。さらに、かかる薬剤は血管新生の阻害によるこれらの疾患の治療に使用し得る。 (もっと読む)
ヌクレオチド・ワクチン組成、ヌクレオチド及び細胞ワクチン組成の産出方法、ワクチン組成、ワクチン組成使用、免疫反応産出方法、疾患の治療または予防方法、抗原提示細胞から成るキット
【課題】本発明は、ヌクレオチドおよびセルのワクチン構成の新規な組み合わせに関し、また薬剤の組成およびその使用にも関し、癌、感染病、アレルギー、自己免疫疾患、血液疾患等の病気の予防及び/または治療に使用可能なものに関する。
【解決手段】抗原分子をコード化するヌクレオチド配列、そして、樹状細胞が好ましいがこれに制限されない組換抗原提示細胞で構成されるワクチンを組成する。したがって、造血系のプロフェッショナル抗原提示細胞(APC)APCは好ましくは混合する。そしてAPCは免疫を調整する分子を表すために変更される。本発明のワクチン構成を備えた免疫化は、本発明の目的において、本発明のワクチン構成を備えた免疫化は、ホスト免疫系を引き起こし、効率的な免疫に応答、生成し、何らかの存在する疾病あるいはその病気からホストを保護する。  (もっと読む)
(もっと読む)
ジンセノサイドRg5量を増加させるべく処理された朝鮮人参の新規調製方法
【課題】ジンセノサイドRg5含有量が増加した薬理学的に強力な朝鮮人参製品の調製方法を提供する。
【解決手段】本発明は、薬理学的に強力な朝鮮人参製品及びその抽出物を調製するための調製方法に関し、厳選された範囲の圧力と温度を前記方法に適用することで、様々な薬理活性を示すジンセノサイドRg5を多量提供することができ、本発明による処理された朝鮮人参及びその抽出物を含む組成物は、各種疾患、特に癌疾病の予防又は治療における薬剤又はヘルスケア食品として有用である。
(もっと読む)
医薬品のホスフェート誘導体
本発明に従って、(a)フェノール、第一級アルコール、第二級アルコール、又は第三級アルコールの水酸基を有する1以上のオピオイド、ステロイド・ホルモン、チロイド・ホルモン、麻酔薬、又は化学療法薬の1以上のホスフェート誘導体;と(b)両性界面活性剤、カチオン性界面活性剤、窒素官能基を有するアミノ酸、及び当該アミノ酸を多く含むタンパク質を含む群から選ばれる複合体形成剤との反応生成物を含むオピオイド、ホルモン、麻酔薬、及び化学療法薬からなる群から選ばれる医薬品の複合体が提供される。 (もっと読む)
CCK−B/ガストリン受容体に対する免疫原性組成物および腫瘍の治療法
本発明は、ガストリン依存性腫瘍を治療するための、免疫原、免疫原性組成物、および方法に関する。免疫原は、免疫原性キャリアと抱合したガストリン受容体免疫模倣ペプチドを含む。免疫原は、ガストリン応答性悪性腫瘍または前悪性腫瘍のガストリン受容体(GR)に結合する抗体をin vivoで誘導し、それにより増殖刺激ペプチドホルモンが受容体に結合するのを阻止して、腫瘍細胞増殖を阻害する能力を有する。本発明はまた、受動免疫化のための、ガストリン受容体に対する特異的抗体に関する。そのうえさらに、本発明は細胞毒性分子で誘導体化された抗GR抗体を含む。本発明はまた、本発明の抗体を用いて、in vivoで、または組織生検からガストリン依存性腫瘍を検出する診断法に関する。能動および受動免疫化は、組み合わせて、GR、G17および/またはG17−Glyに対する免疫応答を提供することができる。 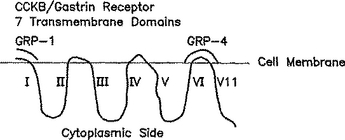 (もっと読む)
(もっと読む)
標的部位で選択的に活性化される新規化合物およびその利用
【課題】癌の標的療法に適したプロドラッグとして利用可能であり、標的部位に効率良く送達させるため水溶性を向上させた新規な化合物、および癌など低酸素性疾患の画像診断用プローブを提供する。
【解決手段】機能部と抑制部とを、水溶性を向上させる構造を有するリンカー部分を介して結合させる。抑制部には癌細胞等の低酸素条件下の細胞で選択的に遊離するユニットを用い、機能部には抗癌剤、または画像診断用プローブ等を用いる。
(もっと読む)
羊ヒアルロニダーゼを単離し精製する方法
【課題】医薬の用途に適した純度の高いヒアルロニダーゼ製剤の調製方法を提供する。
【解決手段】好ましい実施態様では、そのプロセスは、最終製品の純度を上げるウイルス濾過ステップの使用を含む。そのプロセスは、現在市販されているヒアルロニダーゼ製剤の純度を高める方法を提供する。その方法は、哺乳類のソースからヒアルロニダーゼを精製するために好ましく使用される。別の実施態様では、開示されている方法は、組換えヒアルロニダーゼを精製するために使用することができる。  (もっと読む)
(もっと読む)
薬剤併用物送達用組成物
【課題】併用薬を投与するときの非拮抗的な効果を達成する。
【解決手段】抗悪性腫瘍薬などの2又はそれ以上の薬剤を非拮抗的な組み合わせで安定的に相互作用した送達媒体を含む組成物。
(もっと読む)
癌の治療のための、フルオロシチジン誘導体を含む改変放出組成物
本発明は、フルオロシチジン誘導体、好ましくはカペチタビンを含む複数粒子性改変放出組成物、及び、改変放出コーティング、改変放出マトリックス物質又はその両方を含む改変放出組成物に関する。経口送達に続いて、該組成物は、操作において、投与後約6〜約12時間で、拍動性の様式で、該フルオロシチジン誘導体を送達する。 (もっと読む)
化合物および病気に関連する遺伝子の特異的かつ同時阻害のための化合物の使用、および関連薬物
式:
A−B−C
[式中、
Aは、病理学的に重要な遺伝子に共通する配列を同時にかつ特異的に認識することができるDNA配列−特異的リガンドであり;
Bはリンカーアームであり、前記リンカーアームはAの3’末端に結合しており;
CはトポイソメラーゼIポイズンである]
の化合物の、遺伝子の発現によってもたらさせる病気の治療用の医薬品の調製のための使用であって、前記遺伝子は安定化されたトポイソメラーゼI−媒介DNA開裂によって阻害される、使用である。
(もっと読む)
薬剤を含んだ所定のレイヤパターンを有する複層構造体
【課題】制御された治療を改善する、微細加工された所定の空間的パターンを有するポリマからなる複層構造体を提供する。
【解決手段】微細加工された概ね予め定められた幾何学的構成をなす空間的パターン(貯蔵室及びチャネルなど)を有するポリマからなる複層構造体を提供する。本発明によって提供される幾何学的なパターンは、パターンの制御を向上させたものであり、制御された治療の改善を可能にする。好適な実施態様では、本発明のポリマ複層構造体は、生分解可能であり、その生体内での寿命は、供給する薬の持続時間よりも長い。したがって、ポリマ構造体の幾何学的なパターンは、治療中にその形状が著しく変化することなく治療薬の送達を制御し、その構造体は、治療薬がなくなった後に分解する。この方法では、治療薬の分解副産物による干渉が最小限になり、治療薬の送達は、分解の進行具合に依存しない。
(もっと読む)
MCP−1/CCR2関連疾患を治療するための分子およびその使用方法
CCR2/MCP−1関連疾患の治療およびMCP−1の単離のための分子及びそれを含む組成物。 (もっと読む)
2,161 - 2,180 / 2,996
[ Back to top ]



