Fターム[4B063QR35]の内容
酵素、微生物を含む測定、試験 (178,766) | 試薬 (61,469) | 試薬としての核酸(←オリゴマー(3以上)) (12,299) | RNA (3,372)
Fターム[4B063QR35]の下位に属するFターム
mRNA (935)
Fターム[4B063QR35]に分類される特許
2,341 - 2,360 / 2,437
核酸のプライマーに基づく増幅のための方法及びキット
診断又は疾患因子と二次疾患因子の鑑別診断のための新規方法を開示する。開示された方法は、その核酸配列が公知であるいずれかの疾患因子及び/又は二次疾患因子からの標的配列の感受性の高い特異的な増幅を可能にする、TemPCRと称する新規増幅戦略を用いる。TemPCR法は、検出すべき疾患因子又は二次疾患因子に特異的な標的富化プライマーの少なくとも1セット(低濃度で存在する)及び共有標的増幅プライマーの少なくとも1対(高濃度で存在する)を利用する。前記標的富化プライマーの少なくとも1対は、標的増幅プライマーのための結合配列を含む。従って、TemPCR法の使用は、多重増幅パラメータの経験的最適化を必要とせずに多重増幅反応を実施することを可能にする。TemPCR法と共に使用するための、核酸単離及び標的配列の検出のための方法も開示する。  (もっと読む)
(もっと読む)
トマトhighpigment−1突然変異表現型(hp−1及びhp−1W)に関与する単離ヌクレオチド配列及びその使用
本発明は、トマト high pigment 1(hp−1)及びhigh pigment 1w(hp−1w)表現型に関与する単離ヌクレオチド配列(該配列は、改変トマトDDB1遺伝子配列又はその断片を含有し、該改変配列又は断片における該改変は、hp−1の場合は該DDB1遺伝子配列のヌクレオチド931でのAからTへの塩基転換を、hp−1wの場合は該DDB1遺伝子配列のヌクレオチド2392でのGからAへの転位を含有する。)を提供する。 (もっと読む)
SNOW1はICE1と結合し、CBF発現およびシロイヌナズナにおける凍結耐性を制御する
本発明は、タンパク質(Snow1)、その突然変異体、および前記タンパク質をコード化している核酸に関し、これはIce1と相互作用し、これはCBF3プロモーター活性を活性化し、このようにして植物における凍結耐性を制御する。 (もっと読む)
生物サンプル中の核酸を検出するための器具および方法
帯電物を包含する、具体的には生物サンプル中の標的DNAを包含する生物学的方法に関する電場援用促進のために開示された器具および方法が存在する。反応セルは、誘電性表面を提供し、電場は、誘電物質と接触している電極に電位を加えることにより誘電物質における電荷分離を誘導することによって発生される。
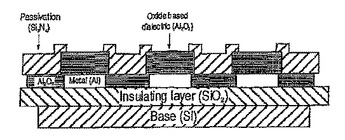 (もっと読む)
(もっと読む)
アルツハイマー病の発症年齢に関連するNTRK1遺伝子マーカー
アルツハイマー病の発症年齢マーカーに関連するNTRK1遺伝子のハプロタイプが、開示される。種々の臨床適用においてこれらのNTRK1ハプロタイプを検出および使用するための組成物および方法が、開示される。このような適用としては、これらNTRK1ハプロタイプの一つを有するADを発症する危険のある個体においてADの発症年齢の遅延において効果的な化合物を含む製造物、個体のハプロタイププロファイルに基づいてADを発症する危険のある個体においてADの発症年齢を予測するための方法およびキット、ならびに患者のハプロタイププロファイルに基づいてADを発症する危険のある個体においてADの発症年齢を遅延するための方法が挙げられる。 (もっと読む)
酸化還元機能性アミノ酸のタンパク質への部位特異的組み入れ
組成物ならびに酸化還元機能性アミノ酸をタンパク質に組み入れる直交性tRNA、直交性アミノアシルtRNAシンテターゼ、およびtRNA/シンテターゼの直交性の対を含むタンパク質生合成機構の成分を産生させる方法を提供する。これらの直交性の対を使用して酸化還元機能性アミノ酸を伴うタンパク質を産生させる方法と共に、これらの直交性の対を同定する方法も提供する。 (もっと読む)
ラマン散乱によりヌクレオチド信号を増加する方法
本明細書に開示の方法および装置は、増強ラマン分光法による核酸配列決定に関する。本発明のある態様において、ヌクレオチドは、核酸に組み込まれる前にラマン標識に共有結合する。他の態様においては、未標識核酸を使用する。核酸をエキソヌクレアーゼ処理すると、標識または未標識ヌクレオチドが放出され、ラマン分光法によって検出される。本発明の別の態様において、エキソヌクレアーゼ処理によって核酸から放出されるヌクレオチドはナノ粒子に共有結合で架橋し、表面増強ラマン分光法(SERS)、表面増強共鳴ラマン分光法(SERRS)、および/またはコヒーレント反ストークスラマン分光法(CARS)によって検出される。本発明の他の態様は核酸配列決定のための装置に関する。
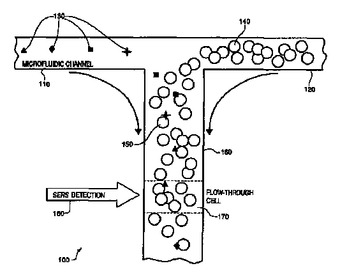 (もっと読む)
(もっと読む)
マイコバクテリウム・アビウム亜種パラツベルクローシスの分子レベルの検出
本発明は、マイコバクテリウム・アビウム亜種パラツベルクローシス(MAP)の分子レベルの検出および同定に関する。より詳細には、MAPに特異的なIS900因子の種々のゲノム領域を標的とした1以上のオリゴヌクレオチドプライマーを用いたPCRアッセイの開発がもたらされる。 (もっと読む)
B細胞慢性リンパ性白血病の診断及び治療のための方法及び組成物
抗体軽鎖遺伝子と抗体重鎖遺伝子との結合体である、単離且つ精製された製剤が提供され、ここで、軽鎖及び抗体重鎖遺伝子は、B細胞慢性リンパ性白血病(B−CLL)を有する1体以上の患者間で同じである。これらの遺伝子を含むベクター、及びこれらのベクターを含む細胞もまた、抗体遺伝子によりコードされた単離且つ精製された抗体として提供される。抗体遺伝子によりコードされる抗体の抗原結合領域に結合する、抗イディオタイプ抗体、ペプチド及びアプタマーがさらに、抗体遺伝子によりコードされる抗体の抗原結合領域に結合する複数の結合部位を含む多量体分子として提供される。B細胞慢性リンパ性白血病(B−CLL)を有する患者が、イディオタイプ特異的B細胞受容体を有するB−CLL細胞を消失させることを対象とする治療の影響を受けやすいB−CLLの形態を有するかを決定する方法も、患者におけるB−CLLの治療の進行を追う方法として提供される。さらに、B−CLLを有する患者を治療する方法も、B−CLLに対する治療薬を同定する方法として提供される。 (もっと読む)
固定化された核酸の検出
本発明は、チアゾールオレンジの誘導体である非対称シアニン色素、染色溶液、および本質的に非遺伝子毒性として特徴付けられる精選された蛍光発生的化合物を用いる、固定化された核酸の存在を決定するための方法を提供する。上記方法は、一本鎖または二本鎖のDNA、RNA、またはそれらの組み合わせである核酸を、固体または半固体の支持体上に固定化する工程、上記固定化した核酸を、非対称シアニン色素化合物と接触させる工程、次いで上記固定化させた核酸を、それによって上記核酸の存在が決定される適切な波長を照射する工程を包含する。 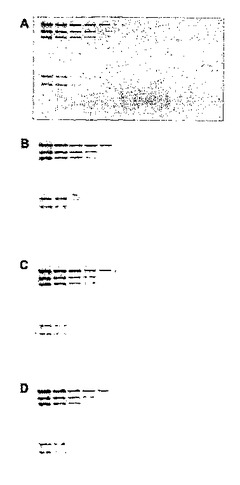 (もっと読む)
(もっと読む)
細胞学的サンプルの自動分類
【課題】
【解決手段】 細胞学的サンプルを自動分類する方法が提供されている。この方法は、サンプルを一又はそれ以上の光波長を用いて尋問して結果を得るステップと、この結果が所定の基準に合致するかどうかに基づいてサンプルに一又それ以上の識別子を付するステップとを具える。本方法によれば、サンプルの特徴についての迅速なフィードバックが可能であり、サンプルを所定の特徴に対して正であるとの自動識別子を可能とし、サンプルが基準に合わない場合に、直ちに治療行動をとることができる。
(もっと読む)
TIM−3ポリペプチド
本発明は、tim−3 IgVドメインおよびtim−3細胞内ドメインを含み、tim−3ムチンドメインまたはtim−3膜貫通ドメインを含まない単離ポリペプチドおよびポリペプチドをコードする核酸に関する。さらに、本発明は、治療有効量のtim−3活性を調整する薬剤を被験体に投与する工程を含む、被験体の免疫応答を調整する方法に関する。免疫応答には、免疫寛容、移植免疫寛容、Th1応答、およびTh2応答が含まれるが、これらに限定されない。 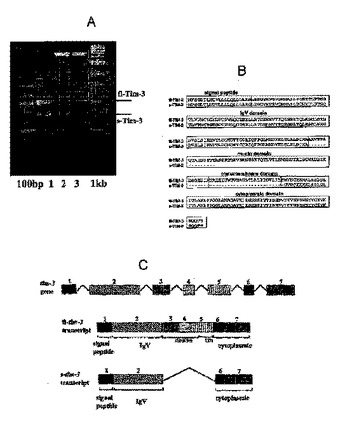 (もっと読む)
(もっと読む)
生合成経路遺伝子産物を同定するための方法
本発明は、単離された遺伝子操作された宿主細胞であって、生合成経路の酵素をコードするヌクレオチド配列を含む核酸を用いて遺伝子操作されている宿主細胞を提供する。宿主細胞における酵素の合成によって、酵素の基質の生合成経路中間体への変換が生じ、中間体は遺伝子操作されている宿主細胞の増殖を阻害するのに有効な量で産生される。本発明はさらに、本遺伝子操作された宿主細胞を含む組成物およびキットを提供する。本宿主細胞は、生合成経路において活性を有する遺伝子産物を同定するのに有用である。本発明はさらに、生合成経路において活性を有する遺伝子産物を同定する方法を提供する。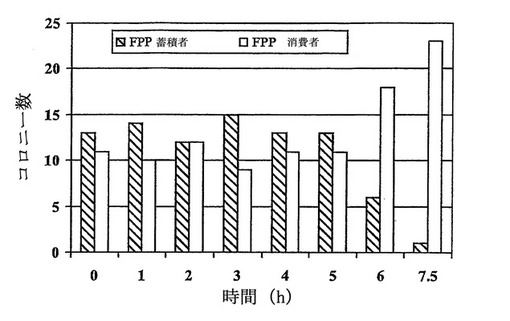
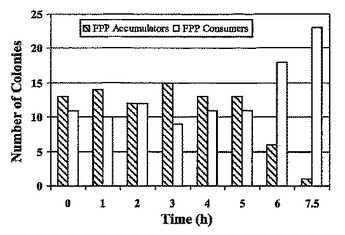 (もっと読む)
(もっと読む)
プログラム可能な分子バーコード
本開示は、分子バーコードを作製および/または使用する方法に関する。本発明の特定の態様において、バーコードは、1つまたは複数の分岐構造を含んでもよいポリマー骨格を含む。タグは、骨格および/または分岐構造に付着してもよい。バーコードはまた、タンパク質、核酸および他の生体分子または凝集体のような標的に結合できるプローブを含んでもよい。異なるバーコードは、タグの型および位置により識別されうる。他の態様において、バーコードは、コンテナ部およびプローブ部を含む鋳型への1つまたは複数のタグ付きオリゴヌクレオチドのハイブリダイゼーションにより作製されうる。タグ付きオリゴヌクレオチドは、異なる標的に特異的な異なるバーコードを形成するように、モジュラーコード部として設計されてもよい。代替の態様において、バーコードは、モノマーユニットの重合により調製されうる。結合したバーコードは、表面プラズモン共鳴、蛍光またはラマン分光法のような様々なイメージング様式により検出されうる。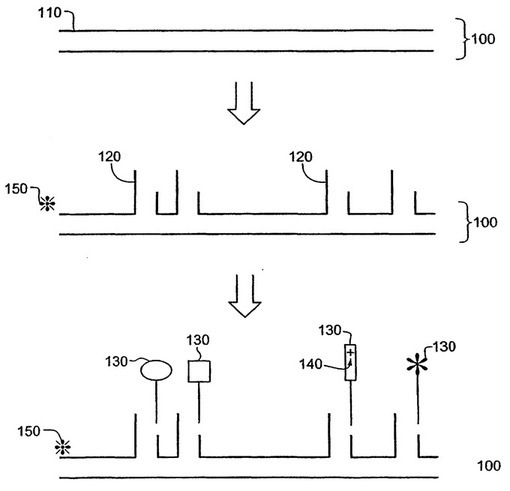
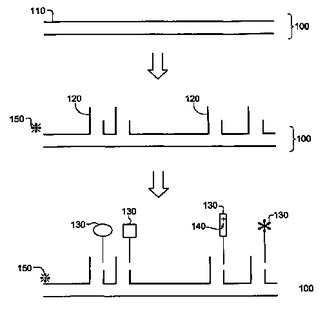 (もっと読む)
(もっと読む)
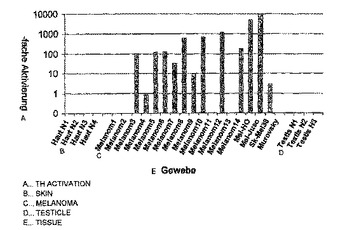
診断および治療のための腫瘍関連細胞表面抗原の同定
本発明に従って、腫瘍関連遺伝子産物およびそれをコードする核酸が同定された。本発明は、該腫瘍関連遺伝子産物が異常発現される疾病の治療および診断方法に関する。本発明は、腫瘍関連様式で発現されるタンパク質、ポリペプチドおよびペプトイドおよびそれらをコードする核酸に関する。
 (もっと読む)
(もっと読む)
フラビウィルス感染の処置のためのオリゴヌクレオチドアナログおよび方法
動物細胞内でのフラビウィルスの複製の阻害の方法、および、その方法における使用のためのオリゴヌクレオチド化合物が開示される。そのオリゴヌクレオチドアナログは、(i)ヌクレアーゼ抵抗性の骨格を有し、(ii)細胞に取り込まれ得、(iii)8〜40個の間のヌクレオチド塩基を含み、そして、(iv)配列番号1−4の少なくとも一部分を含む上記ウィルスの正鎖RNAゲノムの領域に相補的な、少なくとも8塩基の配列を有する。フラビウィルスに感染した細胞を、上記のアナログに曝すことは、その細胞内での、ウィルスのssRNAおよび上記のオリゴヌクレオチドから構成されるヘテロ二重鎖の形成に有効であり、そのヘテロ二重鎖は少なくとも45℃で解離するTmによって特徴付けられ、そしてウィルスの5’末端環化配列および3’末端環化配列の間に崩壊した塩基対合を有する。 (もっと読む)
SenecaValleyウイルスベースの組成物および疾患の処置方法
【解決課題】 本発明は、Seneca Valleyウイルス(「SVV」)と称される新規RNAピコルナウイルス、及び、単離されたSVV核酸およびこれらの核酸によってエンコードされるタンパク質と該SVVタンパク質に対して産生される抗体を提供する。
【解決手段】SVVはいくつかのタイプの腫瘍を選択的に死滅させる能力を有するため、癌の処置にSVVおよびSVVポリペプチドを使用する方法と、SVVは特定の腫瘍を特異的に標的にするため、癌の検出にSVV核酸およびタンパク質を使用する方法、さらに、SVVの腫瘍特異的機構によって提供される情報に基づいて、新規腫瘍溶解性ウイルス誘導体を作成する方法および腫瘍特異的親和性を有するようにウイルスを改変する方法を提供する。
(もっと読む)
Gタンパク質共役受容体およびそのシグナル伝達経路の断片相補アッセイ
本発明は一般に、生物学、分子生物学、化学および生化学の分野に関する。本発明は、Gタンパク質共役受容体(GPCR)およびそのシグナル伝達経路の多数の新規なアッセイを対象とする。GPCR経路における1つまたは複数のステップについてそのようなアッセイを構築する方法が記載される。本発明は、GPCRの機能上の特徴付け、標的検証、受容体の脱オーファン化、高処理能スクリーニング、高容量スクリーニング、薬理学的プロファイリング、および他の創薬適用技術に使用することができる。本アッセイを直接使用して、化合物ライブラリーまたは生体抽出物が受容体のアゴニストまたはアンタゴニストを含むかどうかを評価することができる。アッセイ組成物も提供される。本アッセイの開発が直接的であり、それによってGPCRまたはその同系の経路に作用する新規薬剤および天然リガンドの発見に関する広範、柔軟かつ生物学的に適切な土台が提供されることが示される。  (もっと読む)
(もっと読む)
Gタンパク質共役受容体AdipoR1(AdipoR1)に関連する疾患の診断および治療
本発明は、心循環器疾患、皮膚病、胃腸疾患、癌、血液病、炎症、呼吸器疾患、神経系疾患および泌尿器疾患に関連するヒトAdipoR1を提供する。本発明はまた、心循環器疾患、皮膚病、胃腸疾患、癌、血液病、炎症、呼吸器疾患、神経系疾患および泌尿器疾患の治療または予防に有用な化合物の同定のためのアッセイを提供する。本発明はさらに、AdipoR1へ結合する化合物および/またはAdipoR1の活性を活性化または阻害する化合物ならびにかかる化合物を含む医薬組成物を特徴とする。 (もっと読む)
神経ペプチドFF受容体2アゴニストによる神経因性疼痛の処置
本願発明は、急性侵害受容および慢性神経因性疼痛を媒介する神経ペプチドFF受容体サブタイプ、この受容体サブタイプと選択的に相互作用する化合物、および急性疼痛および慢性神経因性疼痛を処置する方法の発見に関する。 (もっと読む)
2,341 - 2,360 / 2,437
[ Back to top ]



