Fターム[4B063QS33]の内容
酵素、微生物を含む測定、試験 (178,766) | 処理,操作 (34,251) | 検出処理 (14,617) | 検出用プローブの成分への結合 (9,560) | 抗原抗体反応により結合させるもの (1,520)
Fターム[4B063QS33]に分類される特許
1,301 - 1,320 / 1,520
塩基多型の同定方法
【課題】 迅速で容易に再現性の良い結果が得られる、塩基多型を明確にまた簡便に検出できる方法を提供。
【解決手段】 特定の核酸配列を含む試料溶液に第一のリガンドが結合した該特定核酸配列増幅用オリゴヌクレオチドを用いて、増幅反応後、第二のリガンドが結合された結合体を接触させ、特定の核酸配列と結合した第二のリガンド結合体との複合体を検出することによって塩基多型を同定する方法において、上記第一のリガンドの補捉剤が結合された通液性フィルターに滴下して、該複合体の第一のリガンド部分を、該リガンド補捉剤に結合させる工程;該通液性フィルターの表面に、上記第二のリガンドに結合する、標識された生理活性物質の溶液を滴下して、この標識を持つ生理活性物質を、第一のリガンド補捉剤とリガンド部分とを介して通液性フィルターに結合している第二のリガンドに結合させる工程;通液性フィルターに結合した標識を測定する工程、からなる塩基多型の同定方法。
(もっと読む)
脱メチル化および/または酸化された膜DNA、ならびに自己免疫疾患の診断におけるその使用
酸化および/または脱メチル化された抗原の調製のためのプロセスであって、このプロセスは、以下の工程を包含する:細胞を、UV照射、酸化試薬、重金属塩、薬物、ヌクレオシドアナログおよびヌクレオチドアナログ、ならびに酵素インヒビターからなる群より選択されるストレス因子で処理する工程;この細胞を溶解して、細胞溶解産物を得る工程;酸化および/または脱メチル化した抗原をこの細胞溶解産物から精製する工程。このプロセスによって調製された酸化および/または脱メチル化された抗原もまた提供される。 (もっと読む)
FALPタンパク質
インスリンへの応答を示す新規の脂肪組織の低分子量タンパク質(FALPs)が、記載されている。 (もっと読む)
新規TFIIHサブユニット
【課題】哺乳類に於けるDNA修復機構の解明及び関連疾患の治療法、診断法の提供。
【解決手段】ヒトTFIIH 8kDaサブユニットおよび関連する配列をコード化している核酸配列に関する。前記核酸は、TFIIHサブユニットを産生するための方法に使用し得る、また転写およびNER欠乏(特に裂毛症(TTD)のいくつかの形態における)を診断する又は治療するための方法に使用し得る。hTFB5/TTDA遺伝子およびコード化されたタンパク質は、先天性のNER障害を治療することを対象とする、治療の又は遺伝子治療の製品のために使用でき、またTTDAに特異的な分子プローブまたは抗体を用いて、哺乳類の基礎の転写、NERおよびTCR活性における障害を診断する方法に使用し得る。
(もっと読む)
糖尿病およびインスリン抵抗性の診断および治療の方法
本発明は、糖尿病およびインスリン抵抗性の診断および治療のための組成物および方法を提供する。特に、本発明は、本発明のポリヌクレオチドまたはポリペプチドの修飾物質を同定する方法、およびそのような修飾物質を糖尿病の治療のために用いる方法、さらには患者における本発明のポリヌクレオチドまたはポリペプチドのレベルを測定することによって糖尿病を診断する方法を提供する。 (もっと読む)
塩基多型の同定方法
【課題】塩基多型を明確にまた簡便に検出する方法を提供する。
【解決手段】特定の核酸配列を含む試料溶液に第一のリガンドが結合した該特定核酸配列増幅用オリゴヌクレオチドを用いて、増幅反応し、該核酸配列の塩基多型部位に特異的に結合する第二のリガンドが結合された結合体を接触させ、特定の核酸配列と結合した第二のリガンド結合体との複合体を検出する方法であって、上記第二のリガンドの補捉剤が結合された通液性フィルターの表面に滴下して、該複合体の第二のリガンド部分を、該リガンド補捉剤に結合させる工程;該通液性フィルターの表面に、上記第一のリガンドに結合する、標識された生理活性物質の溶液を滴下して、この標識を持つ生理活性物質を、第二のリガンド補捉剤とリガンド部分とを介して通液性フィルターに結合している第一のリガンドに結合させる工程;そして通液性フィルターに結合した標識を測定する。
(もっと読む)
蛋白間相互作用を調節することによる新規アポトーシス調節方法と、それを用いる医薬
本発明は、Omiを介するカスパーゼ非依存性アポトーシス機構の優れた調節法、即ち、WARTS蛋白質とOmi蛋白質の相互作用を亢進または抑制することを含む、細胞の新規アポトーシス調節方法、例えば(1)細胞に外部よりOmiおよび/またはWARTS、またはそれらに実質的に同質な蛋白質を加えること、(2)Omiおよび/またはWARTSをコードするDNAで組換えた組換えベクターを与えて細胞を形質転換すること、(3)Omiおよび/またはWARTSをコードするDNAで形質転換した細胞を被検患者に戻すこと、等によってWARTSとOmiの相互作用を亢進または抑制することを特徴とする、前記アポトーシス調節方法、を提供するとともに、アポトーシスが関与する各種疾患の治療または予防に有効な新規医薬組成物を提供する。  (もっと読む)
(もっと読む)
糖尿病およびインスリン抵抗性の診断および治療の方法
本発明は、糖尿病およびインスリン抵抗性の診断および治療のための組成物および方法を提供する。特に、本発明は、本発明のポリヌクレオチドまたはポリペプチドの修飾物質を同定する方法およびこれらの修飾物質を糖尿病の治療に用いる方法、さらには患者における本発明のポリヌクレオチドまたはポリペプチドのレベルを測定することによって糖尿病を診断する方法を提供する。 (もっと読む)
RS7抗体
本発明は、一価および多価の単一特異性結合タンパク質、ならびに多価多重特異性タンパク質に関する。これらの結合タンパク質の一つの実施態様は一以上の結合部位を有し、各結合部位は標的抗原または標的抗原上のエピトープと結合する。これらの結合タンパク質のもう一つの実施態様は二以上の結合部位を有し、各結合部位は標的抗原上の異なるエピトープに対して親和性を有するか、または標的抗原かハプテンのいずれかに対して親和性を有する。本発明はさらに、宿主においてこれらの機能的結合タンパク質を発現させるために有用な組換えベクターに関する。より詳しくは、本発明は、RS7と呼ばれる腫瘍関連抗原結合タンパク質、およびその他のEGP−1結合タンパク質に関する。本発明はさらに、ヒト化、ヒトおよびキメラRS7抗原結合タンパク質、ならびに診断および治療におけるこのような結合タンパク質の使用に関する。 (もっと読む)
卵巣癌の検出のための方法および組成物
患者サンプル中の卵巣癌を同定するための方法および組成物が提供される。本発明の方法は、身体サンプル中での少なくとも1つのバイオマーカーの過剰発現を検出する工程を包含し、ここでバイオマーカーは卵巣癌において選択的に過剰発現される。好ましい実施形態において、身体サンプルは血清サンプルである。本発明のバイオマーカーは、卵巣癌において選択的に過剰発現される任意の遺伝子またはタンパク質を含む。本発明のある態様において、目的のバイオマーカーの過剰発現が、バイオマーカー特異的抗体を使用してタンパク質レベルにて、または核酸ハイブリダイゼーション技法を使用して核酸レベルにて検出される。本発明の方法を実施するためのキットも提供される。 (もっと読む)
診断方法
感染に対する被検体の感受性を決定する方法を提供する。本方法は、(i)被検体から試料を得る段階; (ii)試料に存在する任意のLL-37を検出する段階; (iii)任意で、試料中のLL-37レベルと対照を比較する段階; および(iv)感染に対する被検体の感受性を提供する段階であり、LL-37が存在しないことまたはLL-37が低レベルであることが、被検体が感染に対して感受性であることを示す段階を含む。  (もっと読む)
(もっと読む)
C−マンノシルトランスフェラーゼに関するアッセイ
本発明は、C−マンノシルトランスフェラーゼ(CMT)活性を検出するための細胞に基づくアッセイ、およびCMT活性の調節に有効な薬剤に関するスクリーニングアッセイを提供する。 (もっと読む)
治療ポリペプチド、それをコードする核酸、および使用方法
本発明は、細胞、組織、器官もしくは生物において、生化学的または生理学的な応答の刺激に関連した特性を有する新規ポリペプチド、およびそれらをコードする核酸に関する。より詳細には、新規ポリペプチドは、新規遺伝子の遺伝子産物であるか、または特定の生物学的に活性なそれらのフラグメントもしくは誘導体である。使用方法は、診断および予後アッセイの手順、ならびに種々の病理状態の治療方法を包含する。 (もっと読む)
腎腫瘍の分子サブ分類および新規診断マーカーの発見
腎細胞癌のサブタイプ中に示差的に発現される遺伝子をそのポリペプチド産物として開示する。本情報を利用して核酸および抗体プローブおよびこれらの遺伝子およびその産物に特異的なこのようなプローブのセットを作成する。ハイブリダイゼーションおよび免疫学的方法を包含するこれらのプローブを用いた方法を用いて、癌のサブタイプに特徴的なこのような遺伝子の示差的な発現に基づいて対象に由来する腎細胞腫瘍試料のサブタイプを決定する。 (もっと読む)
分泌酸性ホスファターゼ(sapM)は病原性マイコバクテリアのみに存在し、ファゴソームpHで選択的に発現する
本発明は、低pHによって誘導可能であるマイコバクテリア分泌酸性ホスファターゼプロモーターまたはプロモーターフラグメントを含む単離DNA構築物に関する。本発明は、さらに、病原性Mycobacterium疾患または感染の治療または予防のための診断方法およびワクチンに関する。本発明はまた、マイコバクテリア分泌酸性ホスファターゼの活性、産生、または分泌を調整することができる化合物のスクリーニング方法に関する。  (もっと読む)
(もっと読む)
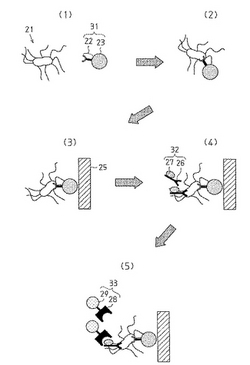
磁気ビーズ及び微生物検出方法
【課題】 より簡易かつ高感度に微生物の検出を行うための磁気ビーズ及び微生物検出方法を提供する。
【解決手段】 サルモネラ21の細胞表層の構成成分であるリポポリサッカライドと特異的に反応するポリミキシンBを固定化した磁気ビーズ(ポリミキシンB固定化磁気ビーズ31)を用いて、サルモネラ21を捕捉する。そして、そのポリミキシンB固定化磁気ビーズ31を磁気ビーズ分離用磁石25により分離し、分離されたポリミキシンB固定化磁気ビーズ31により捕捉されているサルモネラ21に、ビオチン標識抗体32を結合させ、さらに、アビジン・ルシフェラーゼ複合体33を結合させる。そして、ルシフェリンを基質とする発光反応により、サルモネラ21を検出する。
(もっと読む)
細胞培養
(a)各々が1以上の細胞を含む細胞ユニットの群の第1の組を提供し、次いで、前記群を所望の培養条件に暴露するステップと、(b)前記群の2以上をプールして、少なくとも1つの第2のプールを形成するステップと、(c)第2のプールをサブ分割して、細胞ユニットの群のさらなる組を作るステップと、(d)前記さらなる群を所望の培養条件に暴露するステップと、(e)任意選択により、必要に応じて、ステップ(b)〜(d)を繰り返し反復するステップと、(f)所望によりそれは暴露された培養条件の所与の細胞ユニットに対する効果を評価するステップとを含む、細胞に対する複数の培養条件の効果を測定する方法。 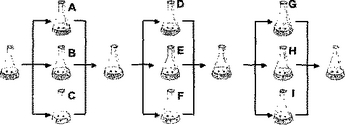 (もっと読む)
(もっと読む)
ヒト癌胎児性抗原(CEA)用の特異的抗体断片
本発明は、組換えDNA技術を用いて、抗癌胎児性抗原(CEA)モノクローナル抗体(McA)CB/ior−CEA.1から得られる一価及び二価(二重特異性抗体)の単鎖Fv型(scFv)抗体断片に関する。前述のMcAはCEAに対する高い親和性を有しており、ヒトにおける結腸直腸腫瘍の診断及びモニターリングに使用されている。元のMcAと同様に、二重特異性抗体及び一価scFv断片はヒトCEAに対する高い親和性、及び炭水化物の保存に依存的なエピトープ認識を示す。二重特異性抗体及び一価scFv断片はそれぞれ(5.0±0.4)×109L mol−1及び(2.8±0.3)×1010L mol−1のCEAに対する親和定数を有する。前述の2つの断片は、CEAがしばしば存在する正常な結腸粘膜を除いては、正常なヒト組織及び細胞と交差反応性を示さない。前記断片は、CB/ior−CEA.1 McAによって産生されるハイブリドーマから得られうる可変領域をコードしている核酸配列のクローニングから、組換え微生物中で発現させることによって産生できる。元のMcAと同様に、二重特異性抗体及び一価scFvは、腫瘍の形成を増殖するヒトCEA産生細胞をラット内でin vivoで同定する能力を有している。一価scFv及び二重特異性抗体はFcドメインを有さず、前記一価scFv及び二重特異性抗体の分子量はラットMcAよりもそれぞれ5倍及び2.5倍小さい。その結果、前述の一価scFv及び二重特異性抗体はin vivoで組織により良好に浸透することができ、且つヒトにおいて免疫原性がより低い。 (もっと読む)
ヒト5T4腫瘍関連抗原由来のMHCクラスIペプチドエピトープ
5T4抗原に由来するMHCクラスIペプチドエピトープを提供する。特に、(i)配列番号2として表示されるアミノ酸配列、(ii)配列番号3として表示されるアミノ酸配列に由来する最小エピトープ、(iii)配列番号4として表示されるアミノ酸配列に由来する最小エピトープ、(iv)配列番号5として表示されるアミノ酸配列に由来する最小エピトープ、(v)配列番号6として表示されるアミノ酸配列に由来する最小エピトープ、(vi)配列番号7として表示されるアミノ酸配列に由来する最小エピトープの1つを含む、5T4のペプチドエピトープを提供する。このようなペプチド(またはその前駆体)を含むワクチン、および疾患、特にがん疾患を治療および/または防止するためのその使用も提供する。 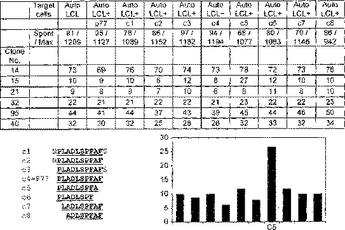 (もっと読む)
(もっと読む)
コラーゲンの分解を制御するための生成物およびその同定方法
本発明はII型コラーゲンなどのコラーゲンの分解を制御するための生成物および方法を提供する。II型コラーゲンペプチドフラグメントの変異体、インヒビター、および擬似物質、並びにコラーゲンの分解を修飾し、それによりコラーゲン破壊の増加の病理学的影響を低減させることができるこれらのペプチドフラグメントを生成するプロテアーゼのインヒビターもまた包含される。加えて、本発明は疾患状態が直接的または間接的に1つまたはそれ以上のコラーゲン種の分解の結果である疾患状態を処置するための方法を提供する。さらに、本発明は診断目的でのこれらのペプチドフラグメントのスクリーニングを包含する。 (もっと読む)
1,301 - 1,320 / 1,520
[ Back to top ]