Fターム[4B064AG27]の内容
微生物による化合物の製造 (77,679) | 生産物−ペプチド、タンパク質 (8,409) | ペプチド、タンパク質 (8,405) | 免疫グロブリン (3,940) | モノクローナル抗体 (3,170)
Fターム[4B064AG27]に分類される特許
3,001 - 3,020 / 3,170
M−CSFに対する抗体
本発明は、M-CSF、好ましくはヒトM-CSFに特異的に結合し、またM-CSFを阻害するように機能する抗体、およびこの抗原結合部分に関する。本発明はまた、ヒト抗M-CSF抗体、およびこの抗原結合部分にも関する。本発明はまた、キメラ抗体、二重特異性抗体、誘導体化抗体、単鎖抗体、または融合タンパク質の一部である抗体にも関する。本発明はまた、ヒト抗M-CSF抗体に由来する、単離された重鎖および軽鎖の免疫グロブリン、ならびにこのような免疫グロブリンをコードする核酸分子にも関する。本発明はまた、ヒト抗M-CSF抗体、このような抗体を含む組成物を作製する方法、ならびに抗体および組成物を診断および治療に使用する方法にも関する。本発明はまた、本発明のヒト抗M-CSF抗体を含む、重鎖および/または軽鎖の免疫グロブリン分子をコードする核酸分子を用いる遺伝子治療法も提供する。本発明はまた、本発明の核酸分子を含むトランスジェニック動物またはトランスジェニック植物にも関する。
 (もっと読む)
(もっと読む)
癌における新規の治療標的
本発明は癌、特にリンパ腫の検出、診断および治療における使用のための新規の配列に関する。本発明は発現が癌に関連する癌関連(CA)ポリヌクレオチド配列を提供する。本発明は細胞表面に存在し、癌に対する新しい治療標的となる癌に関連するCAポリペプチドを提供する。本発明はさらに癌の検出のための診断用組成物および方法を提供する。本発明はCAポリペプチドに特異的なモノクローナルおよびポリクローナル抗体を提供する。本発明はまた癌のスクリーニング、防止および治療のための、診断用ツールおよび治療用組成物および方法を提供する。 (もっと読む)
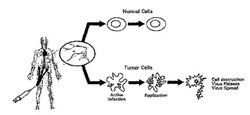
SenecaValleyウイルスベースの組成物および疾患の処置方法
【解決課題】 本発明は、Seneca Valleyウイルス(「SVV」)と称される新規RNAピコルナウイルス、及び、単離されたSVV核酸およびこれらの核酸によってエンコードされるタンパク質と該SVVタンパク質に対して産生される抗体を提供する。
【解決手段】SVVはいくつかのタイプの腫瘍を選択的に死滅させる能力を有するため、癌の処置にSVVおよびSVVポリペプチドを使用する方法と、SVVは特定の腫瘍を特異的に標的にするため、癌の検出にSVV核酸およびタンパク質を使用する方法、さらに、SVVの腫瘍特異的機構によって提供される情報に基づいて、新規腫瘍溶解性ウイルス誘導体を作成する方法および腫瘍特異的親和性を有するようにウイルスを改変する方法を提供する。
(もっと読む)
ヒトインスリン様成長因子に対する遺伝子組換え抗体
IGFが病態の亢進に関与している癌、末端肥大症、糖尿病性合併症等の疾患の治療のための医薬品が求められている。ヒトIGF−IおよびヒトIGF−IIと特異的に結合し、ヒトIGF−IおよびヒトIGF−IIの生物活性を阻害する能力を有する遺伝子組換え抗体または該抗体断片、該抗体または該抗体断片を生産する形質転換体、該抗体または該抗体断片の製造法および該抗体または該抗体断片を有効成分として含有する医薬を提供する。 (もっと読む)
KID3およびKID3に結合するKID3抗体
本発明は、疾患および癌に関連するエピトープであるKID3の同定および特徴付けを提供する。本発明は、KID3に結合する1ファミリーのモノクローナル抗体、KID3を発現する様々なヒトの癌および疾患を診断および治療する方法もさらに提供する。本発明の目的は、ヒトKID3の疾患関連活性を阻害できるそのアンタゴニストを同定することである。また別の目的は、KID3のアッセイにおいて使用するため、免疫原として使用するため、そして抗ヒトKID3抗体を選択するための新規化合物を提供することである。 (もっと読む)
従来の低免疫原性の抗原に特異的なモノクローナル抗体の開発、及び使用のための方法、キット、及び組成物
本発明は、従来の低免疫原性の抗原に特異的なモノクローナル抗体の開発、及び使用に関する。本発明は、対象の抗原を担体分子に化学的に結合させ、免疫系を該結合された抗原での免疫感作へ反応可能にすることによる、モノクローナル抗体を製造する方法を提供する。また、該発明は、結合された抗原の具体的な組成物を、これらの結合された抗原に特異的なモノクローナル抗体の組成物と同様に提供する。また、本発明は、該モノクローナル抗体を用いて疾患状態を検出する際に使用するキットを提供する。 (もっと読む)
IL−6の生物学的効果を減じる化合物の使用
【解決手段】インターロイキン−6(IL−6)及び/またはIL−6受容体またはその部分、好ましくはヒトIL−6に結合するかその拮抗剤である構造体を少なくとも含む化合物であって、内皮の損傷、破壊、内皮の損傷もしくは破壊のリスクの増加または慢性関節リウマチ以外の免疫障害、及びそれらの組み合わせよりなる群から選択される疾病の治療または予防用の医薬を製造するための溶液からIL−6を除去する化合物、あるいは、細胞表面上、または、該溶液中で、少なくとも1つ以上のIL−6の機能を遮断する化合物の使用。 (もっと読む)
sPLA2の効果の失効方法
【解決手段】分泌ホスホリパーゼA2 IIA(sPLA2 IIA)またはその部分、より具体的にはヒトsPLA2 IIAに結合する構造体を少なくとも含む化合物であって、かつ構造体が、
a)細胞表面上、または、溶液中で、好ましくは血液または他の体液または組織からの溶液中で、最も好ましくはインビボで、少なくとも1つ以上のsPLA2 IIAの機能を遮断し、
b)及び/または、溶液から、好ましくは血液または他の体液または組織からの溶液から、最も好ましくはインビボで、sPLA2 IIAを除去する、化合物。
(もっと読む)
NOGO−A結合分子およびその医薬的使用
本発明は、ヒトNogoAポリペプチドまたはヒトNiGまたはヒトNiG−D20またはヒトNogoA_342−357に、解離定数<1000nMで結合する能力のある結合分子、かかる結合分子をコードするポリヌクレオチド;該ポリヌクレオチドを含む発現ベクター;結合分子を産生する能力のあるポリヌクレオチドを含む発現系;上記定義の発現系を含む単離宿主細胞;医薬としての、特に神経修復の処置における、かかる結合分子の使用;該結合分子を含む医薬組成物;および神経修復に関連する疾患の処置方法を提供する。 (もっと読む)
ヒトサイトカインの生物活性をブロッキングするヒト抗体を高収率で産生する方法
【課題】ヒトサイトカインの生物活性をブロッキングするヒト抗体の高収率な産生方法。
【解決方法】VEGF、IFNα、IL−4、TNFα、TGFβの中から選択されるヒトサイトカインの活性を中和するIgGアイソタイプのヒト天然抗体を活性成分として含み、この中和抗体が0.006〜0.05ngの量のサイトカインによってインビトロで誘発される最大生物活性を少なくとも50%抑制する医薬組成物。
(もっと読む)
癌の診断及び治療に用いられる示差的に発現する腫瘍特異的ポリペプチド
本発明は、癌の診断、予後及び治療のための作用薬及び方法に関する。具体的には、本発明は、膜貫通スーパーファミリ・メンバ6 (TM4SF6)、シナプトフィジン様たんぱく質
(SYPL)、ストマチン様2 (STOML2)、Ras−関連GTP−結合 たんぱく質 RAGA)、ヌクレオチド感受性クロリドチャンネル1A (CLNS1A)、プリオンたんぱく質
(p27-30) (PRNP)、グアニンヌクレオチド結合たんぱく質ベータ2-様1 (GNB2L1)、グアニンヌクレオチド結合たんぱく質 4 (GNG4)、一体型膜たんぱく質 2B (ITM2B)、一体型膜たんぱく質 1 (ITM1)、膜貫通9 スーパーファミリ・メンバ 2 (TM9SF2)、アヘン受容体様1 たんぱく質 (OPRL1)、低密度リポたんぱく質受容体関連たんぱく質 4 (LRP4)、ヒト糸球体上皮たんぱく質 1
(GLEPP1)、toll様受容体 3 (TLR3)、及び/又は透明帯糖たんぱく質 3A (ZP3)をコードする核酸及びアミノ酸配列の、 早期及び後期の両方の非ステロイド特異的癌の診断及び癌予後や、前記たんぱく質の遺伝子発現及び/又は生物学的活性を調節する作用薬のスクリーニングのための使用に関する。更に本発明は、ここで解説されたスクリーニング検定で同定される作用薬の使用、アンチセンスポリヌクレオチド配列のベクタ送達、及び、前記たんぱく質の抗体ターゲティングを含め、前記たんぱく質の遺伝子発現及び/又は生物学的活性を阻害するようにデザインされた生物学的技術に関する。具体的な実施態様では、前記たんぱく質はヒト由来である。
 (もっと読む)
(もっと読む)
CD99アンタゴニストを用いる慢性関節リウマチの処置
本発明は、慢性関節リウマチおよびその症状を処置する新規な方法ならびに慢性関節リウマチおよびその臨床症状の処置において有用な薬物を同定およびスクリーニングする新規な方法を含む。ヒトリウマチ関節のコンピュータモデルの標的化操作は、一部の癌に対する効果を有することが既知である接着分子、CD99の活性が慢性関節リウマチの病態生理学に著しい影響を有するという驚くべき結果を提供した。CD99の活性の阻害は、慢性関節リウマチの症状を軽減することが予想される。 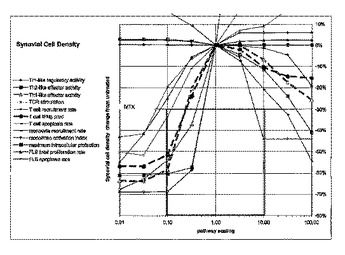 (もっと読む)
(もっと読む)
HMGB1に対するモノクローナル抗体
種々の実施形態において、本発明は、脊椎動物高移動度グループボックス(HMGB)ポリペプチドに結合する抗体またはその抗原結合断片、HMGBポリペプチドに結合する薬剤を検出および/または同定する方法、被験体において炎症性サイトカインカスケードの活性化を特徴とする状態を治療する方法、および試料中のHMGBポリペプチドを検出する方法に関する。 (もっと読む)
治療用結合分子
配列に超可変領域CDR1、CDR2およびCDR3を含み、該CDR1はアミノ酸配列Asn−Tyr−Ile−Ile−His(NYIIH)を有し、該CDR2はアミノ酸配列Tyr−Phe−Asn−Pro−Tyr−Asn−His−Gly−Thr−Lys−Tyr−Asn−Glu-Lys−Phe−Lys−Gly(YFNPYNHGTKYNEKFKG)を有し、そして該CDR3はアミノ酸配列Ser−Gly−Pro−Tyr−Ala−Trp−Phe−Asp−Thr(SGPYAWFDT)を有しており;例えばさらに配列に超可変領域CDR1’、CDR2’およびCDR3’を含み、CDR1’はアミノ酸配列Arg−Ala−Ser−Gln−Asn−Ile−Gly−Thr−Ser−Ile−Gln(RASQNIGTSIQ)を有し、CDR2’はアミノ酸配列Ser−Ser−Ser−Glu−Ser−Ile−Ser(SSSESIS)を有し、そしてCDR3’はアミノ酸配列Gln−Gln−Ser−Asn−Thr−Trp−Pro−Phe−Thr(QQSNTWPFT)を有している少なくとも1つの抗原結合部位を含む分子。 (もっと読む)
脂肪細胞補体関連タンパク質ZACRP12
新規zacrp12ポリペプチド、ポリペプチドをコードするポリヌクレオチド、ならびに関連する組成物および方法を開示する。zacrp12タンパク質に対する抗体またはその断片もまた開示する。 (もっと読む)
種々の配列を有するタンパク質から形成されたアミロイドに共通の高分子量凝集中間体に特異的なモノクローナル抗体
アミロイド疾患(例えばアルツハイマー病)に罹患しているヒトまたは動物のアミロイド原線維形成の一因となる前原線維凝集物の配座エピトープに特異的なモノクローナル抗体の製造方法、並びにハイブリドーマおよび前記から生成されるモノクローナル抗体が提供される。さらにまた、アルツハイマー病または他のアミロイド疾患に対するヒトまたは動物の免疫におけるそのようなモノクローナル抗体の使用、及び/又はアルツハイマー病または他のアミロイド疾患の診断または検出のためのそのようなモノクローナル抗体の使用が提供される。前記モノクローナル抗体は、抗炎症剤(例えば金または金含有化合物)と同時にまたは前記と併用して投与され、アミロイド疾患(例えばアルツハイマー病)に付随する神経の炎症を減少させることができる。 (もっと読む)
第VIIIa因子様活性を示す第IXa因子特異抗体
本発明は、第IX因子/第IXa因子に結合可能で第IXa因子(FIXa)の凝血促進活性を増大させることが可能な抗体のようなリガンド、そのようなリガンドを含む薬学的組成物、そのようなリガンドを用いた血液凝固を患う患者を処置する方法、ならびにそのようなリガンドをコードする核酸、もしくはそのようなリガンドを発現する細胞を提供する。あるリガンドでは、第VIII因子を抑制しない抗体が第IXa因子の凝血促進活性を打ち消さずに、第IXa因子に結合可能である。 (もっと読む)
腫瘍において示差的に発現される遺伝子産物およびこの使用
本発明は、腫瘍に関連して発現された遺伝子産物の同定および前述の産物のためのコード核酸に関する。本発明はまた、遺伝子産物が腫瘍、タンパク質、ポリペプチドおよび腫瘍に関連して発現されるペプチドに関連して異常に発現される疾患の療法および診断、並びに、前述のタンパク質、ポリペプチドおよびペプチドのためのコード核酸に関する。  (もっと読む)
(もっと読む)
アテローム硬化症および/または心血管性疾患の処置および予防のためのコレステロールのオゾン化産物
本発明は、アテローム硬化病変において産生されるコレステロールのオゾン化産物の作用に妨げることによって、アテローム硬化症および/または循環器病を治療および予防するための組成物および方法に関する。本出願中に説明される通り、コレステロールは、アテローム硬化プラーク中に存在する際、酸化される。この反応により細胞傷害性のコレステロール酸化またはオゾン化産物が生成される。本出願は、コレステロールオゾン化産物、その産物に対して指向性を有する結合性実体、および、各種疾病の治療のためにそれら結合性実体および細胞傷害性物質を用いる方法に向けられる。 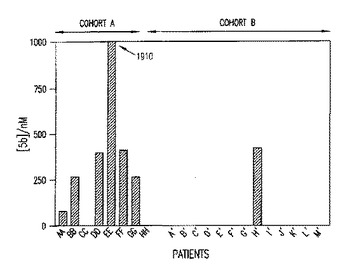 (もっと読む)
(もっと読む)
フィブロネクチンED−Bに対する放射性ラベルされた抗体L19を用いての腫瘍脈管構造の標的化
本発明は、ヒトED-Bに結合する特異的結合メンバーであって、この特異的結合メンバーは76Br、77Br、123I、124I、131I 及び2llAtから成る群から選択された同位体によりラベルされており、そして抗体VHドメイン及び抗体VLドメインを含んで成る抗原−結合部位を含んで成り、ここで抗体VHドメインは、L19 VHドメイン、及びVH CDR1, VH CDR2及びVH CDR3を含んで成るVHドメインから成る群から選択され、前記VH CDR3が配列番号3のL19 VH CDR3であり、前記VH CDR1が任意には、配列番号1のL19 VH CDR1であり、そして前記VH CDR2が任意には、配列番号2のL19 VH CDR2であり;そして前記抗体VLドメインが、L19 VLドメイン、並びにVL CDR1, VL CDR2及びVL CDR3を含んで成るVLドメインから成る群から、任意には選択され、前記VL CDR3が配列番号6のL19 VL CDR3であり、前記VL CDR1が任意には、配列番号4のL19 VL CDR1であり、そして前記VL CDR2が任意には、配列番号5のL19 VL CDR2であり;前記L19 VHドメインの配列及びL19 VLドメインの配列がPiniなど. (1998) J. Biol. Chem. 273: 21769-21776に開示されており;ここで前記特異的結合メンバーは、εS2−CH4に融合されそして二重体化された抗体VLドメイン及び抗体VHドメインを含んで成るミニ−免疫グロブリンを含んで成るか、又は完全なIgG1抗体分子を含んで成り;また、そのような特異的結合メンバーの使用方法及び使用に関する。 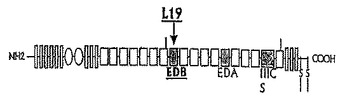 (もっと読む)
(もっと読む)
3,001 - 3,020 / 3,170
[ Back to top ]