Fターム[4C084DA39]の内容
蛋白脂質酵素含有:その他の医薬 (348,545) | 生体防御機能関連蛋白物質 (6,180) | グロブリン (294) | 免疫グロブリン (246)
Fターム[4C084DA39]に分類される特許
181 - 200 / 246
RAGE関連疾患の治療用組成物及び方法
糖化最終産物受容体のリガンド結合要素(RAGE−LBE)と免疫グロブリン要素とを含む融合蛋白質を開示する。また、RAGE−LBEと二量化ドメインとを含む融合蛋白質も開示する。また、このような融合蛋白質をコードする核酸、及び開示される核酸と蛋白質を使用して、例えば、RAGE関連疾患を治療するための方法も開示する。また、追加の組成物及び方法も開示する。 (もっと読む)
補体関連障害の予防および処置のためのCRIgポリペプチド
本発明は、最近発見されたマクロファージ特異的受容体CRIg、ならびに、例えば、加齢性黄斑変性(AMD)および慢性脈絡膜新生血管(CNV)などの補体が関係している眼の症状を含む、補体が関係している障害の予防および処置におけるその使用に関する。1つの態様においては、本発明は、補体が関係している眼疾患の予防または処置のための方法に関する。これには、その必要がある被験体に、予防有効量または治療有効量の補体阻害因子(例えば、代替補体経路の阻害因子(例えば、CRIgポリペプチドまたはそのアゴニスト))を投与する工程が含まれる。  (もっと読む)
(もっと読む)
制御細胞溶解による癌の免疫療法のための装置と方法
治療装置は、溶解機構に連結した、患者または腫瘍から組織サンプルを採取するように構成された採取機構を含む。溶解機構は、溶解組織サンプルへの組織サンプルの溶解を誘導するように構成されている。治療装置はまた、採取機構と溶解機構の両方に連結した投与機構を含む。治療装置には、溶解組織サンプルを患者に投与する前に、追加の溶液を溶解組織サンプルに加えるように構成された追加の機構がさらに含まれる。さらに本発明はまた、癌を治療する方法を与える。本方法は、患者または腫瘍からの組織サンプルを治療装置のチャンバーに採取する工程を含む。組織サンプルを溶解して溶解組織サンプルにして治療装置のチャンバー内に入れ、溶解組織サンプルを治療装置から直接患者に投与する。 (もっと読む)
乳汁生産方法
a) i) 乳汁の半減期を低下させる原因となる少なくとも1つの微生物の生存のために必要な分子;ii) 乳汁の半減期を低下させる原因となる少なくとも1つの微生物の増殖のために必要な分子;iii) 他の微生物が乳汁の半減期を低下させるのを補助する少なくとも1つの微生物の生存に必要な分子;iv) 他の微生物が乳汁の半減期を低下させるのを補助する少なくとも1つの微生物の増殖に必要な分子;のうちの少なくとも1つに対して作製された抗体を乳汁に接触させる段階、を含む乳汁の半減期を改善する方法。 (もっと読む)
哺乳類EAG1イオンチャネルタンパク質に対する新規の抗体
本発明は、哺乳類EAG1イオンチャネルの細胞外または細胞内ドメインの少なくとも1つのエピトープと特異的に結合/相互作用するのに特に有利な抗体、抗体断片またはその誘導体、およびそれらをコードする核酸分子、ならびに該核酸分子を含有するベクターに関する。本発明は、さらに該抗体、抗体断片またはその誘導体の調製のための方法、およびそれらを含有する医薬組成物に関する。さらに本明細書では、該抗体、抗体断片またはその誘導体の使用および該成分を含有する診断用組成物も開示される。本発明は、EAG1発現細胞の存在について評価する方法および該細胞内でのEAG1機能を遮断する方法にも関する。本発明は、さらに該抗体または抗体断片またはその誘導体を活用して疾患を治療する方法に関する。 (もっと読む)
Wntタンパク質ならびに癌の検出および治療の方法
本発明は、とりわけ、癌の診断および治療における、ならびに癌を治療する能力について試験化合物をスクリーニングするための、WntおよびFZDのタンパク質、その遺伝子、WntおよびFZDの特異的抗体、およびそのプローブを使用する方法を提供する。肝臓癌のような癌を治療するために有用な化合物もまた開示される。 (もっと読む)
2,3−ベンゾジアゼピンによる炎症性疾患の治療
式Iの化合物(但し、R1、R2、R3、R4、R5及びnは本発明で定義される。)を、炎症性疾患、好ましくはLTB4により伝達される炎症性疾患の治療用に投与する方法。
【化1】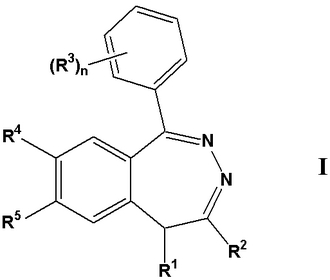
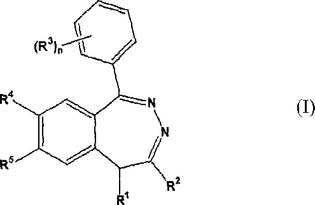 (もっと読む)
(もっと読む)
β−カテニンシグナル伝達経路の調節による細胞傷害剤からの幹細胞の保護
抗増殖剤による幹細胞の死滅を低減させるために、β-カテニンの細胞外活性化をブロックする試薬を用いて、正常幹細胞の静止状態を誘導する。 (もっと読む)
CXC−ケモカインレセプターリガンドおよびCC−ケモカインレセプターリガンドとしてのチアジアゾールジオキシドおよびチアジアゾールオキシド
式(IA)の新規化合物ならびにそれらの薬学的に受容可能な塩および溶媒和物が開示される。置換基Aを含む基の例としては、ヘテロアリール、アリール、ヘテロシクロアルキル、シクロアルキル、アリール、アルキニル、アルケニル、アミノアルキル、アルキルまたはアミノが挙げられる。置換基Bを含む基の例としては、アリールおよびヘテロアリールが挙げられる。式(IA)の化合物を使用して、ケモカイン関連疾患(例えば、癌、血管新生、血管新生性眼疾患、肺疾患、多発性硬化症、慢性関節リウマチ、骨関節炎、脳卒中および心再灌流障害、急性疼痛、急性炎症性疼痛および慢性炎症性疼痛、ならびに神経障害性疼痛)を処置する方法もまた、開示される。 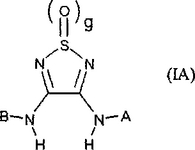 (もっと読む)
(もっと読む)
新規な抗IGF−IR抗体及びその使用
本発明は、ヒトインスリン様成長因子I受容体IGF−IRと特異的に結合することができ、且つ/又はそのIGF−IRのチロシンキナーゼ活性を特異的に阻害することができる新規な抗体、特にマウスのモノクローナル抗体、キメラモノクローナル抗体及びヒト化モノクローナル抗体、並びにこれらの抗体をコードするアミノ酸配列及び核酸配列に関する。本発明はまた、IGF−IRを過剰発現する癌又はその受容体の過剰発現に関連した病状の予防的処置及び/又は治療的処置を目的とした薬剤としての、並びにIGF−IRの過剰発現に関連した疾患の診断のための方法又はキットにおけるこれら抗体の使用を含む。本発明は最後に、このような抗体と、抗EGFR抗体、及び/又は抗VEGF抗体、及び/又は腫瘍進行もしくは転移に関与する他の成長因子に対する抗体、及び/又は化合物、及び/又は抗癌剤、又は毒素と共役した物質とを組み合わせて含む、製品及び/又は組成物、並びに特定の癌の予防及び/又は治療のためのその使用に関する。
【配列表】
SEQUENCE LISTING
<110> PIERRE FABRE MEDICAMENT
<120> Novel anti-IGF-IR antibodies and uses thereof
<130> D22514
<140> PCT/IB2005/002619
<141> 2005-07-27
<150> US 60/591 932
<151> 2004-07-29
<150> FR 04/08379
<151> 2004-07-29
<160> 26
<170> PatentIn version 3.1
<210> 1
<211> 16
<212> PRT
<213> Mus musculus
<400> 1
Arg Ser Ser Gln Thr Ile Ile His Ser Asn Gly Asn Thr Tyr Leu Glu
1 5 10 15
<210> 2
<211> 7
<212> PRT
<213> Mus musculus
<400> 2
Lys Val Ser Asn Arg Phe Ser
1 5
<210> 3
<211> 10
<212> PRT
<213> Mus musculus
<400> 3
Phe Gln Gly Ser His Val Pro Tyr Thr Phe
1 5 10
<210> 4
<211> 5
<212> PRT
<213> Mus musculus
<400> 4
Asp Tyr Trp Met Asn
1 5
<210> 5
<211> 17
<212> PRT
<213> Mus musculus
<400> 5
Leu Ile His Pro Ser Asp Ser Glu Thr Arg Leu Asp Gln Asn Phe Tyr
1 5 10 15
Asp
<210> 6
<211> 13
<212> PRT
<213> Mus musculus
<400> 6
Ser Val Ile Tyr Tyr Gly Asn Tyr Arg Trp Tyr Phe Asp
1 5 10
<210> 7
<211> 11
<212> PRT
<213> Mus musculus
<400> 7
Lys Ala Ser Gln Asn Val Val Thr Asn Val Ala
1 5 10
<210> 8
<211> 7
<212> PRT
<213> Mus musculus
<400> 8
Ser Ala Ser Tyr Arg Tyr Ser
1 5
<210> 9
<211> 9
<212> PRT
<213> Mus musculus
<400> 9
His Gln Tyr Asn Asn Phe Pro Leu Thr
1 5
<210> 10
<211> 5
<212> PRT
<213> Mus musculus
<400> 10
Glu Tyr Gly Val Ser
1 5
<210> 11
<211> 16
<212> PRT
<213> Mus musculus
<400> 11
Val Ile Trp Gly Gly Arg Asp Thr Tyr Tyr His Ser Pro Leu Lys Ser
1 5 10 15
<210> 12
<211> 6
<212> PRT
<213> Mus musculus
<400> 12
His Glu Gly Met Asp Tyr
1 5
<210> 13
<211> 11
<212> PRT
<213> Mus musculus
<400> 13
Ile Thr Ser Thr Asp Ile Asp Asp Asp Met Asn
1 5 10
<210> 14
<211> 7
<212> PRT
<213> Mus musculus
<400> 14
Glu Gly Asn Thr Leu Arg Pro
1 5
<210> 15
<211> 9
<212> PRT
<213> Mus musculus
<400> 15
Leu Gln Ser Asp Lys Met Pro Leu Thr
1 5
<210> 16
<211> 5
<212> PRT
<213> Mus musculus
<400> 16
Asn Tyr Ala Met Ser
1 5
<210> 17
<211> 16
<212> PRT
<213> Mus musculus
<400> 17
Ser Ile Gly Ser Ala Gly Tyr Ile His Tyr Pro Asp Ser Val Lys Gly
1 5 10 15
<210> 18
<211> 9
<212> PRT
<213> Mus musculus
<400> 18
Glu Gly Gly Leu Val Trp Phe Ala Tyr
1 5
<210> 19
<211> 112
<212> PRT
<213> Mus musculus
<400> 19
Asp Val Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Thr Ile Ile His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Val Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 20
<211> 123
<212> PRT
<213> Mus musculus
<400> 20
Gln Ala Gln Leu Gln Gln Pro Gly Ala Val Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Ser Tyr Ser Phe Thr Asp Tyr
20 25 30
Trp Met Asn Trp Val Lys Arg Arg Pro Gly Gln Gly Leu Gln Trp Ile
35 40 45
Gly Leu Ile His Pro Ser Asp Ser Glu Thr Arg Leu Asp Gln Asn Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Phe Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Asn Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser Val Ile Tyr Tyr Gly Asn Tyr Arg Trp Tyr Phe Asp Val
100 105 110
Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 21
<211> 107
<212> PRT
<213> Mus musculus
<400> 21
Asp Ile Val Met Thr Gln Ser Gln Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Val Thr Asn
20 25 30
Val Ala Trp Tyr Gln His Lys Pro Gly His Ser Pro Lys Pro Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Ala Glu Tyr Phe Cys His Gln Tyr Asn Asn Phe Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 22
<211> 114
<212> PRT
<213> Mus musculus
<400> 22
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Asn Glu Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Gly Gly Arg Asp Thr Tyr Tyr His Ser Pro Leu Lys
50 55 60
Ser Arg Leu Ser Ile Thr Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Lys His Glu Gly Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val
100 105 110
Ser Ser
<210> 23
<211> 114
<212> PRT
<213> Mus musculus
<400> 23
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Asn Glu Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Gly Gly Gly Asp Thr Tyr Tyr His Ser Pro Leu Lys
50 55 60
Ser Arg Leu Ser Ile Thr Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Lys His Glu Gly Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val
100 105 110
Ser Ser
<210> 24
<211> 107
<212> PRT
<213> Mus musculus
<400> 24
Glu Thr Thr Val Thr Gln Ser Pro Ala Ser Leu Ser Val Ala Thr Gly
1 5 10 15
Glu Lys Val Thr Ile Arg Cys Ile Thr Ser Thr Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Pro Pro Lys Leu Leu Ile
35 40 45
Ser Glu Gly Asn Thr Leu Arg Pro Gly Val Pro Ser Arg Phe Ser Ser
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Val Leu Thr Ile Glu Asn Thr Leu Ser
65 70 75 80
Glu Asp Val Ala Asp Tyr Tyr Cys Leu Gln Ser Asp Lys Met Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 25
<211> 117
<212> PRT
<213> Mus musculus
<400> 25
Glu Val Asn Leu Val Glu Ser Gly Gly Ile Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Ser Ile Gly Ser Ala Gly Tyr Ile His Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Glu Gly Gly Leu Val Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ala
115
<210> 26
<211> 16
<212> PRT
<213> Mus musculus
<400> 26
Val Ile Trp Gly Gly Gly Asp Thr Tyr Tyr His Ser Pro Leu Lys Ser
1 5 10 15
(もっと読む)
Man3GlcNAc2グリコフォームを支配的に含む免疫グロブリン
本発明は、特定エフェクター機能を与える、免疫グロブリン糖タンパク質上の支配的グリコフォーム構造を有する免疫グロブリン糖タンパク質組成物に関する。加えて、本発明は、特定の富化N−グリカン構造を有する抗体を含み、前記N−グリカン構造がMan3GlcNAc2である医薬組成物に関する。 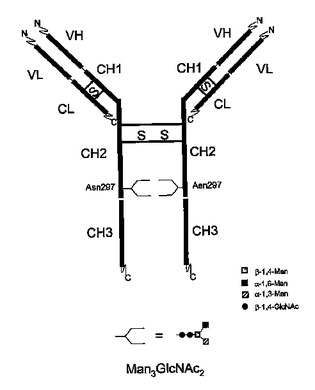 (もっと読む)
(もっと読む)
DKK−1に対する抗体
本発明は、Dkk−1ポリペプチド類に特異的に結合する抗体およびその免疫機能性フラグメントを提供する。対象の抗体およびフラグメントは、Dkk−1タンパク質のカルボキシ領域に位置する配座エピトープに高親和性で結合する。このような抗体またはそのフラグメント、ならびに抗体またはそのフラグメントを含有する生理的に受容可能な組成物を調製する方法もまた提供する。骨疾患、炎症性疾患、神経系疾患、眼疾患、腎疾患、肺疾患および皮膚疾患など、種々の疾患を治療するための抗体およびフラグメントの使用法もまた開示する。  (もっと読む)
(もっと読む)
モノクローナル抗体5c8が特異的に結合するタンパク質
【課題】ATCC受付番号HB10916のハイブリドーマによって産生されるモノクローナル抗体に関連する技術を提供する。
【解決手段】ATCC受付番号HB10916のハイブリドーマによって産生されるモノクローナル抗体5c8により特異的に認識されるタンパク質に結合することが可能なモノクローナル抗体を提供する。この発明はまたATCC受付番号HB10916のハイブリドーマによって産生されるモノクローナル抗体5c8により特異的に認識される単離タンパク質を提供する。この発明は、さらに、ATCC受付番号HB10916のハイブリドーマによって産生されるモノクローナル抗体5c8により特異的に認識されるタンパク質をコードする単離核酸分子を提供する。この発明はまたB細胞に接触依存性ヘルパー機能を本質的に付与し得るD1.1と呼ばれるATCC受付番号CRL10915のヒトCD4-T細胞白血病細胞を提供する。
(もっと読む)
VEGF媒介性活性をブロックすることによるI型糖尿病を処置する方法
VEGF媒介性活性をブロックまたは阻害することによって、哺乳動物、特にヒトにおける糖尿病を処置する方法。VEGF媒介性活性の好ましいインヒビターは、VEGFに結合および阻害し得る配列番号2のVEGF融合タンパク質トラップのようなVEGFアンタゴニストである。本発明の方法は、インスリン治療法のような他の治療法と組み合わせられ得る。特定の実施形態において、本発明の処置する方法は、血清グルコースレベルの低下、グルコース耐性の改善、および/または血糖コントロールの改善を生じる。 (もっと読む)
Gal2GlcNAc2Man3GlcNAc2グリコフォームを支配的に含む免疫グロブリン
本発明は、特定エフェクター機能を与える、免疫グロブリン糖タンパク質の支配的グリコフォーム構造を有する免疫グロブリン糖タンパク質組成物に関する。加えて、本発明は、特定の富化N−グリカン構造を有する抗体を含み、前記N−グリカン構造がフコースを欠くGal2GlcNAc2Man3GlcNAc2である医薬組成物に関する。 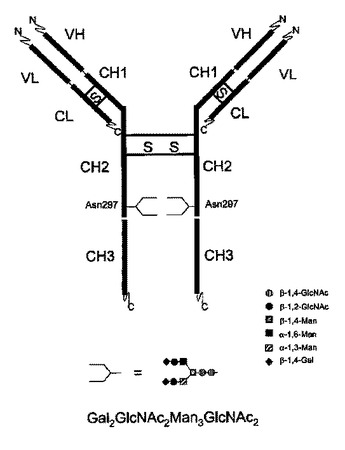 (もっと読む)
(もっと読む)
β−アミロイドペプチドを認識するヒト化抗体
本発明は、患者の脳中のAβのアミロイド沈着物を伴う疾患の処置のための改良された作用物質および方法を提供する。好ましい作用物質はヒト化抗体を包含する。 (もっと読む)
遺伝子およびポリペプチド配列
本発明は、(i)(a)分泌プレ配列、および(b)以下のモチーフ:−X1−X2−X3−X4−X5−(式中、X1はフェニルアラニン、トリプトファンまたはチロシンであり、X2はイソロイシン、ロイシン、バリン、アラニンまたはメチオニンであり、X3はロイシン、バリン、アラニンまたはメチオニンであり、X4はセリンまたはトレオニンであり、かつ、X5はイソロイシン、バリン、アラニンまたはメチオニンである)を含んでなるリーダー配列、ならびに(ii)そのリーダー配列に対して異種の目的タンパク質を含んでなるポリペプチドを提供する。本発明のポリペプチドは、リーダー配列の一部として、分泌プロ配列をさらに含んでなってよい。本発明はまた、本発明のポリペプチドをコードする配列を含んでなるポリヌクレオチドおよび該ポリヌクレオチドを含んでなる細胞、好ましくは、酵母細胞を提供する。  (もっと読む)
(もっと読む)
HCVの複製を抑制するスカベンジャー受容体B1に対する抗原結合性タンパク質
本発明は、HCV E2の結合に関与する領域として本明細書中に特定されているSR-BI標的領域に結合する抗原結合性タンパク質に関する。特定された標的領域は、配列番号1、2、3または4の一本鎖抗体が結合する領域である。  (もっと読む)
(もっと読む)
マクロファージ−刺激タンパク質受容体(RON)の阻害
本発明は、マクロファージ-刺激タンパク質受容体(“MSP-R”又は“RON”)に特異的な抗体を投与することを含む、哺乳動物における腫瘍及び他の疾患を治療する方法に関する。本発明は、RON活性化を阻害する、ヒト抗体を含む、Ronに特異的な抗体又は(of)抗体断片を含有する組成物を更に提供する。 (もっと読む)
抗体−薬物結合体および方法
本発明は、式I:Ab−(L−D)pの抗体−薬物結合体化合物に関し、ここで、1以上のメイタンシノイド薬物部分(D)は、Lによって抗体(Ab)に共有結合し、その抗体(Ab)は、ErbBレセプターに結合するかあるいは1以上の腫瘍関連抗原または細胞表面レセプターに結合する。これらの化合物は、癌、ならびに他の疾患および障害の診断方法または処置方法において使用され得る。本発明は、癌細胞に対する生物学的活性を有する新規化合物を提供する。その化合物は、哺乳動物において腫瘍増殖を阻害し得、そしてヒト癌患者を処置するのに有用であり得る。 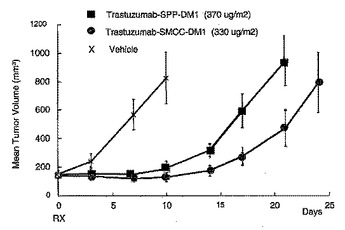 (もっと読む)
(もっと読む)
181 - 200 / 246
[ Back to top ]

