Fターム[4H006BB70]の内容
有機低分子化合物及びその製造 (186,529) | 反応媒体、分離、精製、回収用溶媒 (10,350) | 溶媒の不存在を特徴とするもの(←有機溶媒の不存在) (105)
Fターム[4H006BB70]の下位に属するFターム
無水条件下 (31)
Fターム[4H006BB70]に分類される特許
21 - 40 / 74
不飽和アルファ,オメガジカルボン酸および/または不飽和アルファ,オメガジカルボン酸ジエステルの製造方法
本発明は、2つのルテニウム複合触媒を用いた、不飽和アルファ,オメガジカルボン酸および/または不飽和アルファ,オメガジカルボン酸ジエステルの製造方法に関する。請求項に記載する方法により得られた、不飽和アルファ,オメガジカルボン酸および/または不飽和アルファ,オメガジカルボン酸ジエステルは、特に日焼け止め化粧料組成物に適する。 (もっと読む)
アルコールおよびアンモニアからアミンを調製する方法
本発明は、新規ルテニウムに基づく触媒、およびアミンの調製方法を、1級アルコールおよびアンモニアを、前記触媒の存在下にて反応し、アミンおよび水を生成することによるアミンを調整する方法を提供する。本発明の方法にしたがって、1級アルコールは直接アンモニアと反応させて、1級アミンおよび水を、高収率および高い転換数にて生成する。この反応は新規ルテニウム複合体によって触媒され、好ましくはピンサー型リガンドに基づくキノリニルまたはアクリジニルから構成されるものによって触媒される。 (もっと読む)
2,3,3,3−テトラフルオロプロペンの製法
本発明は、下記反応工程を含む2,3,3,3−テトラフルオロプロペンの製造方法を提供するものである:(i)一般式(1):ACF2CF2CHxFyAz(式中、AはCl、BrまたはIであり、xは0〜2の整数、y及びzは、それぞれ0〜3の整数であって、x、y及びzの合計は3である。)で表されるハロゲン化フルオロプロパンを還元して、一般式(2):ACF2CF2CH3で表される1−ハロゲン化−1,1,2,2−テトラフルオロプロパンとする工程、(ii) 上記(i)工程で得られた1−ハロゲン化−1,1,2,2−テトラフルオロプロパンを気相において触媒に接触させて2,3,3,3−テトラフルオロプロペンとする工程。本発明によれば、安価な原料を用いて高収率で2,3,3,3−テトラフルオロプロペン(HFO−1234yf)を製造することができる。 (もっと読む)
有機カルボン酸をN−アシル化剤とするアミド類の製造方法
【課題】特殊な装置を必要とせず、特別の脱水縮合剤を使用することなく、副生するH2Oを系外へ除去することなく、一段反応で、有機カルボン酸をアミン類の共存下、無溶媒又は適当な非プロトン性溶媒中加熱することでアシル化反応を行い、高収率でアミド化合物を製造する簡便な、環境に害を与えない製造法の開発。
【解決手段】本発明によれば、特殊な装置を必要とせず、特別の脱水縮合剤を使用することなく、副生するH2Oを系外へ除去することなく、一段反応で、有機カルボン酸をアミン類の共存下、無溶媒又は適当な非プロトン性溶媒中加熱することでアシル化反応を行い、高収率でアミド化合物を製造することができる
(もっと読む)
トリフルオロ酢酸をアシル化剤とするトリフルオロアセタミド類の製造方法
【課題】特殊な装置を必要とせず、脱水縮合剤を使用することなく、副生するH2Oを系外へ除去することなく、一段反応で、トリフルオロ酢酸をアミン類の共存下、無溶媒又は適当な非プロトン性溶媒中加熱することでトリフルオロアセチル化反応を行い、高収率でアミド化合物を製造する方法を提供する。
【解決手段】トリフルオロ酢酸をアミン類の共存下、無溶媒又は適当な非プロトン性溶媒中加熱することでアシル化反応を行い、高収率でアミド化合物を製造することができる。アミン類の塩基性が強い場合は、トリフルオロ酢酸を3級アミンと共に使用するか、3級アミンの塩として使用するとよい。
(もっと読む)
3−ヒドロキシアクリロニトリルの金属塩の製造方法
【課題】工業的に適した3−ヒドロキシアクリロニトリルの金属塩の製造方法を提供する。
【解決手段】金属アルコキシドの存在下、アセトニトリルのほかに溶媒を用いず、一酸化炭素とアセトニトリルを反応させることにより、3−ヒドロキシアクリロニトリルの金属塩を製造する。
(もっと読む)
芳香族アルファ−ヒドロキシケトンの調製方法
塩素、塩化スルフリルまたは臭素を用いることを必要とせず、中間体の芳香族ケトンをハロゲン化水素で、酸化作用を有する化合物の存在下でハロゲン化することを含む、芳香族アルファ−ヒドロキシケトン(芳香族α−ヒドロキシケトン)の調製方法。 (もっと読む)
エステル化合物の製造方法
【課題】本発明は、少なくともエステル化反応の段階では溶媒や特殊な触媒を用いることなく、ほぼ等モル量のカルボン酸とアルコールからエステル化合物を製造する方法を提供することを目的とする。
【解決手段】本発明に係るエステル化合物の製造方法は、等モルまたは略等モルのカルボン酸化合物とアルコール化合物を無溶媒でトルエンスルホン酸基担持シリカゲルと混合することを特徴とする。
(もっと読む)
1−アルキルカルボニルオキシ−3−置換フェニル−プロペン化合物の製造方法
【課題】香料、医農薬品、有機合成薬品の中間体として有用である1−アルキルカルボニルオキシ−3−置換フェニルプロペン化合物を、簡便且つ収率良く得る製法を提供する。
【解決手段】11〜13族元素、スズ及びランタノイド元素のトリフラート化合物及びハロゲン化合物からなる群から選ばれた少なくとも1種を含む触媒の存在下、アルコキシ置換ベンゼンとα,β−不飽和アルデヒドとカルボン酸無水物を反応させることを特徴とする、式(4)で表わされる1−アルキルカルボニルオキシ−3−置換フェニルプロペン化合物の製造法。 (もっと読む)
(もっと読む)
ジフルオロメチレン−及びトリフルオロメチル−含有化合物を製造するための方法及び組成物
フェニルイオウトリフルオリド又は第1級アルキル置換フェニルイオウトリフルオリドを用いてジフルオロメチレン含有化合物を製造する新規な方法を開示する。また、フェニルイオウトリフルオリド又は第1級アルキル置換フェニルイオウトリフルオリドを用いてトリフルオロメチル含有化合物を製造する新規な方法も開示する。 (もっと読む)
アシルグリシネートの製造方法
本発明は、式(I)、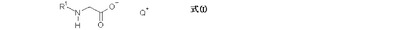
(式中、
R1は、6〜30個、好ましくは8〜22個、特に好ましくは8〜18個の炭素原子を有する直鎖若しくは分岐の飽和アルカノイル基、又は、6〜30個、好ましくは8〜22個、特に好ましくは12〜18個の炭素原子を有する直鎖若しくは分岐のモノ不飽和若しくはポリ不飽和アルケノイル基であり、そして、
Q+は、アルカリ金属カチオンLi+、Na+及びK+から選択されるカチオン、好ましくはNa+及びK+から選択されるカチオン、特に好ましくはNa+である)
で表されるアシルグリシネートの製造方法において、
水中で、かつ、Li+、Na+及びK+から選択されるカチオン、好ましくはNa+及びK+から選択されるカチオン、特に好ましくはNa+であるカチオンQ+を与える塩基性アルカリ金属化合物の存在下で、しかし、有機溶媒の不存在下で、グリシンを脂肪酸クロライドR1Cl(R1は、式(I)に定義したとおりである)と30〜35℃で反応させ、そして、18個若しくは19個以上の炭素原子を含むアシル基R1を持つ脂肪酸クロライドR1Clの割合が、使用する脂肪酸クロライドの全量をベースにして2.0重量%未満であることを特徴とする前記方法に関する。 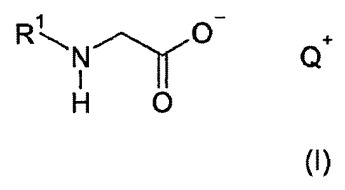 (もっと読む)
(もっと読む)
3,3−ジアルコキシプロピオン酸アルキルを調製するためのプロセス
酸性触媒の存在下で、ケテンを式(RO)3CHのオルトギ酸エステルと反応させることによって、RがC1-6アルキルである式(RO)2CHCH2CO2Rの3,3-ジアルコキシプロピオン酸アルキルを調製するためのプロセスであって、前記反応がループ反応器中で実行されることを特徴とするプロセス。 (もっと読む)
光学活性α−フルオロカルボン酸エステルの精製方法
【課題】医農薬および光学材料の重要中間体である光学活性α−フルオロカルボン酸エステルの大量規模での生産に適した脱弗方法を提供する。
【解決手段】光学活性α−フルオロカルボン酸エステルを有機塩基の存在下に蒸留することにより、前記課題は解決する。この方法により、光学活性α−フルオロカルボン酸エステル中に含まれるフッ化物イオン痕の濃度を、比較的容易な操作で大幅に低減することができる。有機塩基の中でも、第三級アミンが好ましく、中でもトリn−ブチルアミンが特に好ましい。
(もっと読む)
イソプレゴールの水素化によるメントールの製造方法
【解決手段】本発明は、水素、ならびにニッケル、銅、ジルコニウムおよびモリブデンを含有する化合物を含む触媒の存在下にラセミ体もしくは光学活性のイソプレゴールを触媒的に水素化することで、ラセミ体もしくは光学活性のメントールを製造する方法に関するものである。本発明は具体的には、L−イソプレゴールを連続的に触媒的に水素化してL−メントールとする、相当する方法に関するものである。 (もっと読む)
アルファ、ベータ−不飽和カルボニルハロゲン化物を形成するプロセス
マイクロリアクター中でα,β−不飽和カルボニルハロゲン化物を形成するプロセスが記述される。この反応物質は、α,β−不飽和カルボン酸、ハロゲン化剤、及び触媒を含む。第1の流入ストリーム、第2の流入ストリーム、及び任意選択の第3の流入ストリームが貫流マイクロリアクターの反応チャンバに流入し、α,β−不飽和カルボニルハロゲン化物を含む反応生成物を生成する。 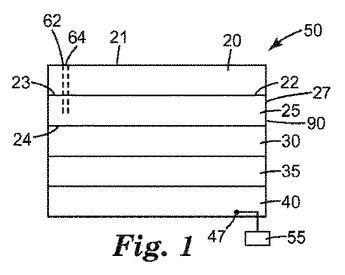 (もっと読む)
(もっと読む)
接触還元方法及びカップリング方法
【課題】有機化合物を合成する際に有利に用いられ得る接触還元方法及びカップリング方法であって、環境への負荷が小さいものを提供すること。
【解決手段】基質及び不均一系白金族触媒を、溶媒としての液体が存在しない水素ガス雰囲気中にて混合し、攪拌する。又は、有機ホウ素化合物と、有機ハロゲン化物又はその等価体と、塩基と、不均一系白金族触媒とを、溶媒としての液体が存在しない状態下において、混合し、攪拌する。
(もっと読む)
光学活性α−フルオロカルボン酸エステルの製造方法
【課題】医農薬および光学材料の重要中間体である光学活性α−フルオロカルボン酸エステルの量産に適した製造方法を提供する。
【解決手段】光学活性α−ヒドロキシカルボン酸エステルを、有機塩基の存在下かつ反応溶媒の非存在下に、スルフリルフルオリド(SO2F2)、トリフルオロメタンスルホニルフルオリド(CF3SO2F)またはノナフルオロブタンスルホニルフルオリド(C4F9SO2F)と反応させることにより、光学活性α−フルオロカルボン酸エステルを製造する。さらに好ましくは、反応終了液に酸を加えて蒸留精製することにより、一層純度の高い光学活性α−フルオロカルボン酸エステルを製造することができる。
この方法により光学活性α−フルオロカルボン酸エステルを大量規模で有利に製造することができる。
(もっと読む)
テトラカルボン酸およびその酸二無水物の製造方法
【課題】従来技術におけるテトラカルボン酸テトラエステルの加水分解反応速度が低いという問題点を解決し、効率のよいテトラカルボン酸の製造方法、およびテトラカルボン酸二無水物の製造方法を提供すること。
【解決手段】メカノケミストリーを利用した加アルカリ分解により、テトラカルボン酸エステルの加水分解反応を従来にない高い反応速度にて進行せしめる。
(もっと読む)
2,2−ジフルオロ−フェニルアセト酢酸エステルの製造方法
【課題】工業的規模での製造に適した2,2−ジフルオロ−フェニルアセト酢酸エチルエステルの製造方法を提供する。
【解決手段】フェニルアセチルクロリドを塩素(Cl2)と反応させ、2,2−ジクロロ−フェニルアセチルクロリドを得る。次いで、得られた2,2−ジクロロ−フェニルアセチルクロリドを、アルコールと反応させ、2,2−ジクロロ−フェニルアセト酢酸エステルを得る。次いで得られた2,2−ジクロロ−フェニルアセト酢酸エステルを液相でフッ化水素(HF)と反応させ、2,2−ジフルオロ−フェニルアセト酢酸エステルを得る。
(もっと読む)
置換2−アリールマロン酸エステルの製造方法
本発明は、マロン酸エステルを銅塩の存在下で塩基及び臭化アリールを用いて変換させる一般式(I):
【化1】
(式中、RはC1-C6アルキルまたはC1-C4-アルコキシ-C1-C4-アルキルを表し;Arはフェニルまたはヘテロ芳香族5または6員環を表し、上記基中に含まれる各C原子は置換基RAを有していてもよく;RAはF、Cl、CN、NO2、C1-C4-アルキル、C1-C4-ハロアルキル、C1-C4-アルコキシ、C1-C4-ハロアルコキシ等を表すか、または2個の隣接するRAはこれらが結合している炭素原子と一緒になって環を形成する)
の置換2-アリールマロン酸エステルの製造方法に関し、マロン酸エステル1モル当量あたり0.1〜0.65モル当量の塩基が使用されることを特徴とする。
(もっと読む)
21 - 40 / 74
[ Back to top ]



