Fターム[4H006BV22]の内容
有機低分子化合物及びその製造 (186,529) | カルボン酸アミド (2,553) | C−CON< (1,525) | C−CON−CR (583)
Fターム[4H006BV22]の下位に属するFターム
Fターム[4H006BV22]に分類される特許
41 - 60 / 572
希土類金属抽出剤の合成方法
【解決手段】ジアルキルジグリコールアミド酸を抽出剤成分とする希土類金属抽出剤を、ジグリコール酸Xmol、エステル化剤Ymol中、モル比Y/Xを2.5以上、反応温度70℃以上、反応時間1時間以上で反応させ、減圧濃縮することで、未反応物及び反応残分を除去して反応中間生成物を得、更に、反応溶媒として、希土類金属の溶媒抽出における有機相を形成する有機溶媒であり、かつジアルキルジグリコールアミド酸を溶解可能である無極性又は低極性溶媒を加え、反応中間生成物とジアルキルアミンZmolとを、モル比Z/Xを0.9以上として反応させることにより合成する。
【効果】軽希土類元素の分離に優れたジアルキルジグリコール酸を、高価な無水ジグリコール酸及び有害なジクロロメタンを用いることなく、低コストで、効率よく、かつ高収率で合成できるため、工業的利用価値が高い。
(もっと読む)
希土類金属抽出剤の合成方法
【解決手段】下記一般式(1)
(式中、R1及びR2は、互いに同一又は異種のアルキル基であり、少なくとも一方は炭素数6以上の直鎖又は分岐鎖状のアルキル基を示す。)
で表されるジアルキルジグリコールアミド酸からなる希土類金属抽出剤を合成する方法であって、前記ジアルキルジグリコールアミド酸の原料であるジグリコール酸無水物とジアルキルアミンとを、溶媒抽出における有機相を形成する有機溶媒として、ジアルキルジグリコールアミド酸を溶解可能な無極性又は低極性溶媒を合成溶媒に用い、ジグリコール酸無水物(A)とジアルキルアミン(B)とのモル比B/Aを1.0以上として反応させることを特徴とする希土類金属抽出剤の合成方法。
【効果】軽希土類元素の分離性に優れたジアルキルジグリコールアミド酸を有害なジクロロメタンを用いることなく、効率よく、かつ高い収率で合成できるため、工業的利用価値が大きい。
(もっと読む)
希土類金属抽出剤の合成方法
【解決手段】ジアルキルジグリコールアミド酸を抽出剤成分とする希土類金属抽出剤を、ジグリコール酸Xmol、エステル化剤Ymol中、モル比Y/Xを2.5以上、反応温度70℃以上、反応時間1時間以上で反応させ、減圧濃縮することで、未反応物及び反応残分を除去して反応中間生成物を得、更に、反応溶媒として、非プロトン性極性溶媒を加え、反応中間生成物とジアルキルアミンZmolとを、モル比Z/Xを0.9以上として反応させ、非プロトン性極性溶媒を除去することにより合成する。
【効果】軽希土類元素の分離に優れたジアルキルジグリコール酸を、高価な無水ジグリコール酸及び有害なジクロロメタンを用いることなく、低コストで、効率よく、かつ高収率で合成できるため、工業的利用価値が高い。
(もっと読む)
希土類金属抽出剤の合成方法
【解決手段】下記一般式(1)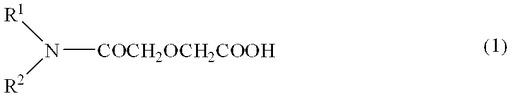
(式中、R1及びR2は、互いに同一又は異種のアルキル基であり、少なくとも一方は炭素数6以上の直鎖又は分岐鎖状のアルキル基を示す。)
で表されるジアルキルジグリコールアミド酸からなる希土類金属抽出剤を合成する方法であって、前記ジアルキルジグリコールアミド酸の原料であるジグリコール酸無水物とジアルキルアミンとを非プロトン性極性溶媒中で、ジグリコール酸無水物(A)とジアルキルアミン(B)とのモル比B/Aを1.0以上として反応させる工程、及び前記非プロトン性極性溶媒を除去する工程を含むことを特徴とする希土類金属抽出剤の合成方法。
【効果】軽希土類元素の分離性に優れたジアルキルジグリコールアミド酸を有害なジクロロメタンを用いることなく、効率よく、かつ高い収率で合成できるため、工業的利用価値が大きい。
(もっと読む)
ビフェニルアセトアミド誘導体からなる医薬
【課題】部分発作及び/又は全般発作の種々てんかん発作に対する治療薬若しくは予防薬として有用な化合物からなる医薬の提供。
【解決手段】式(I)の化合物からなる医薬[式中R1、R2及びR3は、水素原子、フッ素原子、塩素原子、臭素原子、C1-6アルキル、フッ素原子で置換されたC1-6アルコキシ等を表し、R4及びR5は、水素原子、フッ素原子、塩素原子、C1-6アルキル、フッ素原子で置換されたC1-6アルコキシ等を表し、R6及びR7は、水素原子、フッ素原子、メチル、エチル、水酸基等を表し、R8及びR9は、水素原子、C1-6アルキル等を表す]。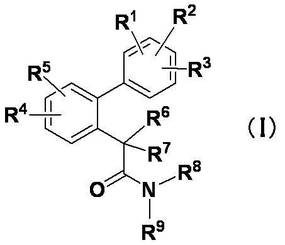 (もっと読む)
(もっと読む)
タンパク質チロシンホスファターゼの調節因子としての置換メチレンアミド誘導体
【課題】インスリン抵抗性または高血糖症による代謝異常の治療および/又は予防に有用な新規置換メチレンアミド誘導体を提供する。
【解決手段】下式(I)で示される置換メチレンアミド誘導体、その幾何異性体、その光学活性体、その医薬として許容される塩、およびその医薬として活性な誘導体。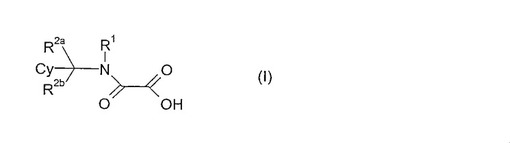
[式中、R1は、(C1−C15)アルキル基、(C2−C12)アルケニル基、(C2−C12)アルキニル基、アリール基、ヘテロアリール基等を表し、R2aとR2bは、それぞれ互いに独立して、水素原子又は(C1−C12)アルキル等を表し、Cyは、アリール基、ヘテロアリール基、シクロアルキル基又は複素環基を表す。]
(もっと読む)
ノイラミニダーゼ阻害剤として有用な置換シクロペンタン及びシクロペンテン化合物
【課題】ノイラミニダーゼ阻害剤として有用な置換シクロペンタン及びシクロペンテン化合物を提供する。
【解決手段】具体的には例えば下式等で表される化合物、並びに、その医薬上許容される塩等例示される。
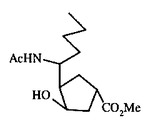 (もっと読む)
(もっと読む)
フッ素化ポリエーテル組成物
【課題】環境に優しく、かつ加工上の難点を伴うことなく調製することのできるフルオロケミカル組成物を提供する。
【解決手段】式Rf−(Q−Tk)y [式中、Rfは分子量が約750g/モル〜約4000g/モルの1価または2価のペルフルオロ化ポリエーテル基を表し、Qは化学結合あるいは2価または3価の有機結合基を表し、Tは−C(O)F、−CO2R3(ここで、R3は水素、低級アルキル、シクロアルキルまたはアルカノールである)、−C(O)N(R1)(R2)(ここで、R1およびR2は独立に、低級アルキル、シクロアルキルまたはアルカノールである)、−OH、−SH−および−NH2からなる群から選択され、kは1または2であり、yは1または2である]のフッ素化ポリエーテル、またはその混合物を含む、フルオロケミカル組成物。
(もっと読む)
アラレマイシン誘導体
【課題】ポルホビリノーゲン合成酵素(PBGS)の阻害活性を有し、抗菌剤として有用な新規アラレマイシン(Alaremycin)誘導体を提供する。
【解決手段】式(I)で表わされるアラレマイシン誘導体又は薬理学的に許容される塩。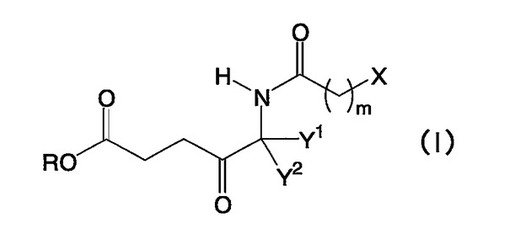
Rは、水素原子又は低級アルキル基、Xは、ハロゲン置換メチル基、Y1及びY2は、一方が水素原子を表すとき、他方は、水素原子、ヒドロキシメチル基又は低級アルコキシメチル基を表すか、又はY1とY2が一緒になって二重結合を表し、mは、0〜5の整数
(もっと読む)
イオン液体ゲル化剤及びゲル
【課題】イオン液体を少量でゲルを形成できるポリオール誘導体からなるイオン液体ゲル化剤、並びに該ゲル化剤とイオン液体よりなるゲルの提供。
【解決手段】式(1):
(式中、R1は炭素原子数10至20の飽和脂肪族基又は1個の二重結合を持つ炭素原子
数10乃至20の不飽和脂肪族基を表し、R2はアミノ酸が有する置換基を表し、Xは酸
素原子またはNHを表す。)で表されるポリオール誘導体及び薬学的に使用可能な塩から成る事を特徴とするイオン液体ゲル化剤、該ゲル化剤の自己集合化により形成される自己集合体、及び、該ゲル化剤又は自己集合体とイオン液体より成るゲル。
(もっと読む)
芳香族末端基を有するアミドゲル化化合物
【課題】十分なゲル化強度、高い熱安定性を有するゲル化剤の提供。
【解決手段】下式で表される化合物。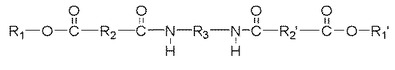
〔R1およびR1’は同じであり、R1およびR1’は、芳香族基であり;R2、R2’およびR3は、アルキレン基、アリーレン基、アリールアルキレン基またはアルキルアリーレン基であるか;又は、実施形態では、R1およびR1’は、同じであっても異なっていてもよく、R1およびR1’は、少なくとも1箇所のエチレン系不飽和部を有するアルキル基、少なくとも1箇所のエチレン系不飽和部を有するアリールアルキル基、少なくとも1箇所のエチレン系不飽和部を有するアルキルアリール基、又は芳香族基であり、ただし、R1およびR1’のうち、少なくとも1つが芳香族基であり;ただし、R1もR1’も光開始性基ではない。]
(もっと読む)
無機/有機ハイブリッド触媒材料とその製造方法、選択的プロセスへの応用及びそれを利用した反応容器
カルボン酸アミド類の新規合成法
【課題】有機カルボン酸と有機アミンとの脱水反応でカルボン酸アミド類を製造する際に、水を反応媒体として、温和な反応条件で製造する方法を提供する。
【解決手段】一般式(1)で表されるカルボン酸と有機アミンとを、水を反応媒体としてマイクロ波を照射して反応させることにより比較的低温で、高収率でカルボン酸アミド類を製造する。
R−(COOH)n (1)
(一般式(1)中、Rは、炭素数9以上の置換若しくは無置換のn価の飽和又は不飽和脂肪族基を表し、nは1又は2を表す。)
(もっと読む)
新規ジカルボン酸型化合物
【課題】加水分解安定性、生分解性を有し、優れた界面活性を示す新規ジカルボン酸型化合物を提供する。
【解決手段】ジカルボン酸型化合物は、式(1)で示される化合物である。
CnH2n+1は直鎖状の又は分岐状のアルキル基を示し、nは1〜22の整数を示し、R1は炭素原子数1〜22のアルキレン基を示し、R2は炭素原子数1〜22のアルキル基を示し、R3は、水素原子または、メチル基を示し、Xは、水素イオン、アルカリ金属イオン、アルカリ土類金属イオン、又はアンモニウムイオンを示すが、但し、前記R1及びR2は−R1−CH−CH−R2部分が炭素原子数9〜25の炭化水素構造をなすように選択される。
(もっと読む)
鉄欠乏症および鉄欠乏性貧血の治療および予防用の鉄(III)錯体化合物
アゴメラチン塩酸塩水和物およびその製造
有機ナノチューブからなる核酸導入剤
【課題】毒性のない優れた核酸キャリアとなる、自己集合性の有機ナノチューブを提供をする。
【解決手段】下記化学式(1)、(2)の脂質化合物等が混合されて、有機ナノチューブ構造体を形成していることを特徴とする複合ナノチューブ。<化学式(1)>(化合物1)
〔式中、mは12〜20の整数。〕<化学式(2)>(化合物2)
〔式中、mは12〜20の整数等、Xは(CH2)nでnが2〜8の整数等を表す。〕
(もっと読む)
アゴメラチン臭化水素酸塩水和物およびその製造
N−長鎖アシル酸性アミノ酸ジエステル化合物及びこれを用いた化粧料及び洗浄料
【課題】従来のN−長鎖アシル酸性アミノ酸アルカリ塩やN−長鎖アシル酸性アミノ酸ジエステルと同性能であって、且つ、従来に比べ低凝固点であるN−長鎖アシル酸性アミノ酸ジエステル化合物を提供する。
【解決方法】N−長鎖アシル酸性アミノ酸ジエステル化合物は、炭素数8〜22のアシル基を有するN−長鎖アシル酸性アミノ酸と、炭素数の平均が18となる分岐鎖高級アルコールの混合物とをエステル化反応させて得られる。
(もっと読む)
置換アセトフェノン化合物及びその用途
【課題】有害生物防除剤として有用な置換イソキサゾリン化合物の新規な製造中間体を提供する。
【解決手段】一般式(1):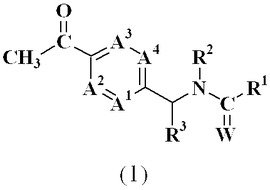
[式中、A1、A2、A3及びA4はC-Y又は窒素原子を表し、Wは酸素原子又は硫黄原子を表し、Yは水素原子、ハロゲン原子等を表し、R1はアルキル、ハロアルキル、R6によって任意に置換されたアルキル、-N(R11)R10等を表し、R2は水素原子、メチル等を表し、R3は水素原子、シアノ、メチル等を表し、R6はシクロアルキル、-S(O)pR16等を表し、R10はアルキル、ハロアルキル、シクロプロピル等を表し、R11は水素原子等を表し、R16はメチル、エチル等を表し、pは0〜2の整数を表す。]で表される置換アセトフェノン化合物。
(もっと読む)
41 - 60 / 572
[ Back to top ]