Fターム[4H045BA12]の内容
Fターム[4H045BA12]に分類される特許
341 - 360 / 638
抗血管形成ペプチドおよび治療のためのその使用
抗走化性、抗血管形成、および抗腫瘍活性を有するアンギオスタチンペプチドフラグメント、それを含む薬学的組成物、ならびに炎症、結合組織変性、血管および新生物の状態の処置のためのその使用。 (もっと読む)
皮膚のトリートメントにおいて有用な合成ペプチド類および化粧品または皮膚薬剤組成物中でのその用途
本発明は、原線維発生を制御することができる一般式(I)のペプチド類、その立体異性体類およびラセミ体であってもよいその混合物類、およびその化粧学的または皮膚薬剤学的に許容できる塩類に関し、式中、Zはアラニル、アロ−イソロイシル、グリシル、イソロイシル、イソセリル、イソバリル、ロイシル、ノルロイシル、ノルバリル、プロリル、セリル、スレオニル、アロ−スレオニルまたはバリルであり;nおよびmは、1と5の間で変動し;AAは、LまたはD体でコードされた天然アミノ酸類およびコードされないアミノ酸類により形成される群から選択され;xおよびyは、0と2の間で変動し;R1はHまたはアルキル、アリール、アラルキルまたはアシル基であり;およびR2は、アミノ、ヒドロキシルまたはチオールであり、これら全てが、脂肪族または環状基により置換されているかまたは置換されていない。それらを含有する化粧品または皮膚薬剤学組成物類を得る方法、および皮膚、好適には、加齢および/または瘢痕外観の柔軟化のような原線維発生制御を必要とする皮膚状態のトリートメントのためのその用途。
【化1】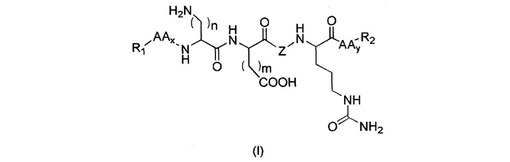
 (もっと読む)
(もっと読む)
還元型グルタチオンの製造法
【課題】食品、医薬品、化粧品等に使用される還元型グルタチオンを簡便で工業的に有利に製造できる、特殊な設備を必要とすることなく、水溶液中でも収率よく反応が進行する、酸化型グルタチオンの還元方法を提供する。
【解決手段】酸化型グルタチオンを、鉄化合物、硫黄及び硫化水素存在下、還元する。
(もっと読む)
ペプチド
【課題】食品の風味や栄養価等を損ない、品質の劣化を引き起こすだけではなく、生体において疾病や老化等の悪影響を及ぼす活性酸素やフリーラジカル等による生体の酸化的障害を抑制する抗酸化剤及びこの抗酸化剤を配合した飲食品、化粧品または飼料の提供。
【解決手段】Gly-Ile-His あるいは Pro-Gly-Pro-Ile-Hisで表されるアミノ酸配列からなるペプチドは抗酸化作用があり、しかも低用量で効果を有する。
(もっと読む)
還元型グルタチオンの製造方法
【課題】食品、医薬品、化粧品等に使用される還元型グルタチオンを簡便で工業的に有利に製造できる、特殊な設備を必要とすることなく、水溶液中でも収率よく反応が進行する、酸化型グルタチオンの還元方法を提供する。
【解決手段】酸化型グルタチオンを、銅化合物、鉄化合物及び硫化水素存在下、還元する。
(もっと読む)
ペプチド精製物の製造方法
【課題】ゼラチンまたはコラーゲンの酵素消化精製物のようなペプチド混合物(例えば、トリペプチドGly-X-Yの含有率が2〜35%のペプチド混合物)から、大量生産に適した方法で、トリペプチドGly-X-Yの含有率が40%以上のペプチド精製物を製造できる方法を提供する。
【解決手段】トリペプチドGly-X-Y(Gly-X-Yはアミノ酸配列であり、X、YはGly以外のアミノ酸残基を示す)を含有するペプチド混合物を塩基性陰イオン交換樹脂と接触させて、トリペプチドGly-X-Yを前記イオン交換樹脂に吸着させ、トリペプチドGly-X-Yを吸着した前記イオン交換樹脂からトリペプチドGly-X-Yを溶出することを含む、トリペプチドGly-X-Yの含有率が前記ペプチド混合物より高められたペプチド精製物の製造方法。
(もっと読む)
重水素化C型肝炎プロテアーゼインヒビター
式(I)
【化1】
で示される重水素化α−ケトアミド立体特異的化合物(ここで、Dは、立体特異的炭素原子上の重水素原子を示す。)。  (もっと読む)
(もっと読む)
成長刺激タンパク質の使用
本発明は、個体における新たに発見された成長刺激タンパク質の阻害に関する。さらに、本発明は、前記成長刺激タンパク質の発現を下方調節し、又は前記タンパク質を不活性化することにより、個体において癌を予防若しくは治療し、又は癌の成長、浸潤、若しくは転移を予防若しくは治療し、又は他の過剰増殖性疾患を予防若しくは治療する方法に関する。さらに、本発明は、前記成長刺激タンパク質に基づいて、個体において癌又は他の過剰増殖性疾患を診断する方法に関する。 (もっと読む)
放射線障害の制御の為にペプチドを使用する方法
本発明は、高エネルギー電磁波(X線、ガンマ線)又は粒子(アルファー粒子、ベータ粒子、ニュートロン)への被曝により引き起こされる急性放射線障害に対する薬剤開発の分野に関する。今日までに、電離照射への不測の被曝後に放射線障害を改善するための有効な薬剤はない。本発明は、放射線障害の処置が必要な対象の放射線障害を処置する方法であって、30アミノ酸より小さいペプチド又はその機能的類似体若しくは誘導体を投与することを含む上記方法を提供する。さらに、本発明は、放射線障害を患う又は患っていると考えられる対象の処置のための医薬組成物の製造の為の30アミノ酸より小さいペプチド又はその機能的類似体若しくは誘導体を使用する方法を提供する。特に、本発明は、少なくとも1.10の急性ガンマ照射に対する線量減少係数(DRF)を有する抗放射線ペプチドを提供し、該DRFは、どのくらいの放射線量が、全身照射(WBI)後30日で50%死亡率を結果するか(LD50/30)を、WBI後72時間で該ペプチドにより処理されたマウスの試験群において試験すること、及びどのくらいの放射線量が、全身照射(WBI)後30日で50%死亡率を結果するか(LD50/30)を、WBI後72時間で該ペプチドの媒体によってだけ処置されたマウスの対照群において試験すること、及びここで該DRFは該ペプチドにより処置された動物のLD50/30を、該媒体により処置された動物のLD50/30により割り算することにより計算される、によって決定可能である。 (もっと読む)
ペプチド結合に基づく多数の細胞株のプロファイリングに関連した組成物および方法
多数の細胞または細胞株に特定の特徴的パターンで会合または結合する細胞および/またはペプチドを分類するための方法および組成物が説明される。本発明の局面はまた、細胞または細胞集団へ薬物を送達するための適切な結合特性を有するペプチドの使用も含む。 (もっと読む)
ペプチド脂質を含んだキャリア及びそれを用いた化合物の細胞内導入法
本発明は、下記式: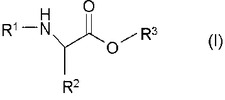
(式中、R1はアミノ酸残基数1〜10のアミノ酸もしくはペプチドを示し、R2は任意のアミノ酸側鎖を示し、R3は炭素数1〜30の炭化水素基を示す。但し、R2がカルボキシル基を有する場合、該カルボキシル基は炭素数1〜30の炭化水素基とのエステルであってもよい)で表わされるペプチド脂質を含有する細胞毒性が低く、かつ高効率で化合物を細胞内に導入することのできる、化合物の細胞内導入用キャリア、および該キャリアを用いた化合物の細胞内導入方法を提供する。
(もっと読む)
ペプチド類の安定化剤
【課題】病原体の感染や病原性因子の伝達を生じる危険性がなく、高い安全性を有し、生理活性又は薬理活性を有するペプチド類を有効に安定化できる安定化剤及びペプチド類が有効に安定化されたペプチド組成物を提供する。
【解決手段】本発明の安定化剤は、生理活性又は薬理活性を有するペプチド類を安定化させるための安定化剤であって、少なくとも式Pro-Y-Gly(式中、YはPro又はHypを示す)で表されるアミノ酸配列を有する合成ポリペプチドで構成されている。前記合成ポリペプチドは、コラーゲン様の構造を有してもよい。また、合成ポリペプチドの分子量は3×104〜500×104の範囲にピークを示してもよい。
(もっと読む)
抗酸化性ペプチド
【課題】ローヤルゼリー蛋白質由来の抗酸化性ペプチドを提供する。
【解決手段】抗酸化性ペプチドは、ローヤルゼリー蛋白質のプロテアーゼ分解産物であって、特定のアミノ酸配列を有するペプチドである。ローヤルゼリー蛋白質に由来するので安全性が高く、酸化ストレス細胞の生存率を高めることができる。従って、抗酸化剤及び細胞死抑制剤として、機能性食品、食品、医薬品等の添加剤などとして広く利用することができる。
(もっと読む)
C末端におけるポリペプチドの結合
本発明は、新規のポリペプチド、それらの合成方法、新規のポリペプチドを含有する医薬組成物、並びに治療用途の医薬におけるそれらの使用に関する。 (もっと読む)
虚血および神経変性の処置のための化合物
【課題】
【解決手段】TPPII(トリペプチジルペプチダーゼII)阻害剤は、神経変性疾患、例えばアルツハイマー病、パーキンソン病もしくはハンチントン舞踊病、または虚血性状態、例えば脳卒中および心筋梗塞の処置に役立つ。適当な化合物には、一般式RN1RN2N−A1−A2−A3−CO−RC1のトリペプチド化合物が含まれ、上式で、RN1、RN2、A1、A2、A3およびRC1は本明細書で定義される通りであり、上の例としては、例えばトリペプチド配列GLAおよびGPGが含まれる。
(もっと読む)
連続合成装置および方法
【課題】 原料の成分の濃度を一定にした状態で反応を進行させ、効率よく連続ペプチド合成を行うことができる連続合成装置を提供する。
【解決手段】 この連続合成装置は、水溶性縮合剤と、N保護アミノ酸およびC保護ペプチドの混合液とを連続流れで混合し反応させる混合反応手段5と、合成後の液中から未反応の水相成分を分離し除去する油水分離手段6と、水相成分が除去された有機相成分液中に水素ガスを混合させ、触媒を介して生成したペプチドの脱保護反応を行う気体触媒反応手段7とを有する。
(もっと読む)
癌の処置のためのγ線照射と組み合わせた化合物の使用
【課題】
【解決手段】TPPII(トリペプチジルペプチダーゼII)阻害剤は、γ線照射癌療法の効力を強化するか、腫瘍細胞のin vivoγ線照射感受性を増加させるために有用である。適当な化合物には、一般式RN1RN2N−A1−A2−A3−CO−RC1のトリペプチド化合物が含まれ、RN1、RN2、A1、A2、A3およびRC1は本明細書で定義された通りであり、その例としては、例えばトリペプチド配列GLAおよびGPGが含まれる。γ線照射と併用した処理の間、TPPII阻害剤を注射したマウスで、完全なin vivo腫瘍退縮が観察される。
(もっと読む)
CXCR4および/または細胞運動の阻害
本発明は、フェニルアラニン、システイン、該アミノ酸の誘導体、それらを含むペプチド、ならびに病状がCXCR4活性および/または細胞の運動性によって引き起こされるかまたは関連する疾患、障害または症状におけるそれらの使用に関する。  (もっと読む)
(もっと読む)
ペプチド含有抗癌剤(ANTICANCERAGENTCOMPRISINGAPEPTIDE)
本発明の1実施例による抗癌剤は配列番号:4、配列番号:11及びこれらの組み合わせからなる群より選択されるアミノ酸配列を有するペプチドを含む。前記抗癌剤は大腸、膵臓、乳房、肺、脳、前立腺、扁平上皮細胞、リンパ細胞または白血球から由来する癌を抑制するのに使用することができる。 (もっと読む)
リガンド結合用新規捕捉剤
本発明は、少なくとも第1ペプチド鎖および第2ペプチド鎖を含む、リガンド結合用多量体型捕捉剤であって、上記第1ペプチド鎖および第2ペプチド鎖はそれぞれ、2〜50アミノ酸の鎖を含んでおり、上記アミノ酸のそれぞれは実質的に鏡像異性的に単一であり、かつ上記少なくとも第1ペプチド鎖と第2ペプチド鎖とが共有結合している、ことを特徴とするリガンド結合用多量体型捕捉剤に関する。  (もっと読む)
(もっと読む)
341 - 360 / 638
[ Back to top ]