Fターム[4B063QQ79]の内容
酵素、微生物を含む測定、試験 (178,766) | 検体,検出物 (39,509) | 酵素,核酸以外の有機物質 (4,619) | 蛋白質,ペプチド,その構成成分,その誘導体 (2,970)
Fターム[4B063QQ79]の下位に属するFターム
アミノ酸 (75)
Fターム[4B063QQ79]に分類される特許
2,161 - 2,180 / 2,895
腫瘍の診断と治療のための組成物と方法
本発明は、哺乳動物の腫瘍の診断と治療のために有用な物質の組成物と、同用途のために当該物質の組成物を使用する方法に関するものである。 (もっと読む)
相互作用測定方法
【課題】本発明の課題は、コスト的にも有利で、ハイスループットに蛋白質の結合DNAサイトをチップ上でスクリーニングする相互作用測定方法を提供することにある。
【解決手段】蛋白質との相互作用できる核酸配列を測定する方法であって、蛋白質が相互作用できる配列を含む標的核酸配列から、遺伝子増幅法を用いて長さの異なる増幅産物を複数、別々に取得し、該増幅産物を同一の固体基板上に混じり合うことなくそれぞれ異なる位置に固定化し、該蛋白質との相互作用を観察することを特徴とする相互作用測定方法。
(もっと読む)
ナチュラルキラー細胞関連疾患の治療のための組成物と方法
本発明は、新規のタンパク質を含む組成物と、免疫関連疾患の診断と治療のためのその組成物の使用法とに関する。 (もっと読む)
HIV感染症の治療方法
【課題】HIV感染症の治療方法を提供する。
【解決手段】HIV感染症の治療を必要とする患者に、逆転写酵素阻害剤のような少なくとも1種の抗HIV薬を投与し、その少なくとも1種の抗HIV薬の投与後にワクシニアウイルス接種炎症組織抽出物を該患者に投与することを含むHIV感染症の治療方法。例え少なくとも1種の抗HIV薬の投与が中止されても、前記抽出物はHIV複製に対する抑制作用を維持する。
(もっと読む)
腫瘍の診断と治療のための組成物と方法
本発明は、哺乳動物の腫瘍の診断と治療のために有用な物質の組成物と、同用途のためにその物質の組成物を使用する方法に関するものである。 (もっと読む)
アッセイ
本発明は、胎児中に存在する2,3−ビスホスホグリセリン酸ムターゼ(2,3−BPGM)の量及び質を測定することによって、ヒト等の哺乳動物において子癇前症をスクリーニングする方法に関する。この方法を行う試薬及びキットも提供される。  (もっと読む)
(もっと読む)
α−フェトタンパク質Immu31抗体および融合タンパク質ならびにその使用方法
本発明は、ヒト化、キメラおよびヒト抗α−フェトタンパク質抗体、融合タンパク質、およびそれらのフラグメントを提供する。この抗体、融合タンパク質、およびそれらのフラグメント、ならびに他の好適な抗体との組み合わせは、肝細胞癌腫、肝芽細胞腫、生殖系細胞腫瘍および他のAFP産生腫瘍の治療および診断に有用である。 (もっと読む)
薬物の代謝及び毒性を評価するためのトランスジェニック動物
本発明は、トランスジェニック非ヒト動物、該動物由来の組織又は細胞、及びその作出方法に関する。本発明のトランスジェニック非ヒト動物、或いは該動物由来の組織又は細胞により、相同内在性非ヒト動物タンパク質に代わって薬物代謝に関与すると共に、該動物に導入されたヒト遺伝子の発現の調節がヒトにおいてインビボで見られるものと一層同様になされるように該遺伝子を制御することに関与するヒトタンパク質を発現することが可能な系が得られる。 (もっと読む)
内因性トロンビン活性を自動的に測定するための方法
【課題】 本発明は、血液または血漿検体の内因性トロンビン活性を自動的に測定する方法に関する。
【解決手段】 a)総反応速度の飽和相の直線領域を、所定の試験特有の時間枠の範囲内で測定し、そして、次に、
b)トロンビンのα2−マクログロブリンに対する結合定数Cを、飽和相の直線領域における総反応速度の勾配Aを用いて反復測定し、ここで該勾配はα2MTの反応速度の勾配に対応しており、そして、次に、
c)α2MTの反応速度の値を測定して、総反応速度の対応する値から差引き、そして、次に、
d)飽和相の総反応速度の直線領域について測定した、遊離トロンビンの反応速度の値を平均化することによって、生のETP値を測定する、
時間の関数として、測定すべきトロンビン基質のターンオーバー速度を用いる、凝固する血液または血漿の検体の内因性トロンビン活性(ETP)の測定。
(もっと読む)
自己免疫障害を治療する方法
本発明は、自己免疫疾患を治療するための方法に関する。ある具体例において、本発明は、TCCRアゴニストを投与することを含む自己免疫疾患を治療する方法に向けられる。ある具体例において、該自己免疫疾患はTh1応答によって少なくとも部分的に媒介される。ある具体例において、該自己免疫疾患はCD8+T−細胞増殖によって少なくとも部分的に媒介される。本発明は、IL−27のようなIL27R(TCCR)のアゴニストを投与することによって、多発性硬化症(MS)および慢性関節リウマチ(RA)を含めた自己免疫疾患を治療する方法を提供する。TCCRの有用なアゴニストは、IL27Rの改変体および断片、IL−27のようなIL27Rリガンド、およびその改変体および断片ならびにIL27RまたはIL27Rリガンドに結合し、IL27−媒介応答を刺激し、誘導し、または増強するアゴニスト抗体を含む。 (もっと読む)
養子免疫療法のためのIL−21の使用法および腫瘍抗原の同定法
養子免疫療法で使用するためのIL-21組成物を用いるエクスビボT細胞培養物を調製するための方法を記載する。単離されたか、または末梢血単核細胞に存在するかいずれかの、最終分化していないT細胞集団の培養物へIL-21が添加され、1つまたは複数の腫瘍抗原に曝露され、ならびにIL-21組成物および抗原提示細胞(APC)の存在下で、結果として生じるT細胞集団は増強された抗原特異性を有し、かつ患者の中に再導入することができる。また、腫瘍物質の存在下で、IL-21組成物およびAPCに曝露されたT細胞集団を培養することによって、腫瘍抗原を同定する方法も開示する。
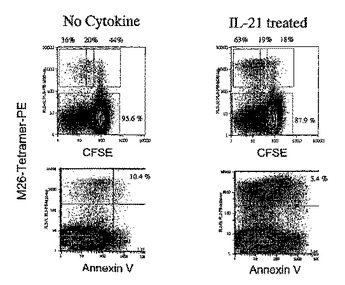 (もっと読む)
(もっと読む)
熱ショックタンパク質結合性のCD91断片およびその使用
本発明は、熱ショックタンパク質結合性タンパク質として、天然および組換えのp95形態および断片を使用するための組成物および方法に関する。本発明は、一部には、p95を組換えにより発現させることができるという本発明者らの発見に基づいている。本発明はまた、少なくともp95と、CD91のドメインII、IIIおよびIVからの追加の連続配列とを含むCD91ポリペプチド断片に関する。本発明は、CD91ポリペプチド断片またはその類似体、誘導体もしくは擬似体をコードする核酸分子、CD91ポリペプチド断片またはその類似体、誘導体もしくは擬似体、CD91ポリペプチド断片をコードする核酸分子を含有するベクター、CD91ポリペプチド断片をコードする核酸分子を含有する発現ベクター、CD91ポリペプチド断片を組換えにより発現する真核および原核細胞、CD91ポリペプチド断片と相互作用する化合物またはCD91ポリペプチド断片とCD91リガンドとの相互作用を同定する方法、本発明の組成物および方法により免疫応答をモジュレートする方法、ならびに本明細書に記述する組成物および方法を用いた治療方法を提供する。  (もっと読む)
(もっと読む)
細胞上および生物学的混合物中の抗原の検出のための組成物、方法およびキット
本発明は、既知の結合対の一方のメンバー(「受容体」と命名される)がバクテリオファージにより発現され、その後そのファージを使用して該対の他方のメンバー(「リガンド」若しくは「標的」と命名される)の存在を検出する、細胞を包含するサンプル中の既知の結合対の一メンバーの新規検出方法に関する。抗体に基づく技術を使用してファージの結合を検出するよりはむしろ、本発明はファージと会合する核酸を検出することに関する。一局面において、本発明は、抗体を表示するバクテリオファージを使用して細胞、例えば赤血球上に存在する目的の抗原をもつ部分(例えば赤血球抗原)を同定すること、ならびに抗グロブリン試薬を表示するバクテリオファージを使用しかつ該ファージと会合する核酸を検出してサンプル中の抗赤血球自己若しくは同種抗体および/または補体を検出することに関する。  (もっと読む)
(もっと読む)
MCAMインヒビタ
本発明は自然発生性腫瘍細胞におけるMCAMの機能を阻害するポリペプチド類およびそれらの使用、および癌治療において、特に特殊の癌細胞の侵襲性、増殖、接着および/または転移能力を軽減するためにMCAMの機能を阻害するその他の分子類を使用することに関するものである。さらに、自然発生性腫瘍細胞がその侵襲性、接着性、増殖および/またはその転移能力に関して機能的MCAMに依存するかどうかを確認できる方法が提供される。最後に、腫瘍細胞の侵襲性、増殖性または接着性を阻害できる抗体または抗体フラグメントを同定できる方法が提供される。  (もっと読む)
(もっと読む)
癌を有する個体の層別化のためのPTAペプチドの使用
本発明は癌を患っている個体の層別化の方法に関する。より詳細には、本発明は、PTA断片が抗内分泌療法に感受性である癌細胞と前記療法には感受性がない癌細胞の区別を可能にすることの発見に関する。それ故、PTA断片は、免疫組織学によるエストラジオールレセプター検出のための代替であることができ、抗エストラジオール療法に対する癌細胞の耐性をモニターするためのマーカーであることができ、再発をモニターするために使用することができ、及び脱分化の状態、例えば、癌細胞の状態を決定するために使用することができる。PTA断片は、血清又は血漿のような容易に入手できる患者サンプルから決定されるという利点を有する。本発明はさらに、特異的PTAペプチド及び核酸、それらの抗体、試験キット及び診断及び治療法、及び組成物を包含する。  (もっと読む)
(もっと読む)
カルシウム感知受容体2(CaR2)およびその使用方法
本開示は、CaR2と名づけられた新規なヒトカルシウム感知受容体および、該受容体をコードするヌクレオチド配列を提供する。本開示はさらに、CaR2に特異的な抗体を提供する。また、受容体のモジュレーターを同定する方法および同定されたモジュレーターを用いて、カルシウム受容体媒介性の症状を治療する方法も開示する。 (もっと読む)
蛍光タンパク質マイクロドメインを使用するタンパク質−タンパク質相互作用検出システム
本発明は、フラグメントの会合を駆動するために融合された相互作用ポリペプチドを必要とし、さらに、可溶性かつ安定であり、そしてそれらが融合されるポリペプチドの安定性を変えない蛍光タンパク質および発色団タンパク質に基づく、タンパク質の標識化および相互作用検出のシステムを提供する。1つの実施形態では、試験タンパク質Xが、GFPの16アミノ酸のフラグメント(β鎖10、アミノ酸198〜214)に融合され、融合タンパク質の可溶性を変動させないように操作される。第2の試験タンパク質Yは、GFPの16アミノ酸のフラグメント(β鎖11、アミノ酸215〜230)に融合され、融合タンパク質の可溶性を変動させないように操作される。XとYとが相互作用する場合、それらは、そのGFP鎖を接近させ、そしてGFPアミノ酸1〜198(鎖1〜9)からなる第3のGFPフラグメントとの補完によって検出される。 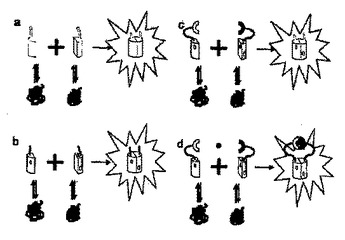 (もっと読む)
(もっと読む)
リガンドに特異的に結合するタンパク質を効率的に選別する手法
【課題】特定のリガンドに対し特異的に結合するタンパク質を選別する方法を提供する。
【解決手段】多様化ライブラリーから、目的リガンドに特異的に結合するタンパク質を選択する方法であって、該ライブラリー中に存在するタンパク質と目的リガンドを接触させ、目的リガンドに結合するタンパク質を選択する工程、得られたタンパク質を対照リガンドと接触させ、該タンパク質と対照リガンドとの結合性の有無を判定する工程、および、対照リガンドとの結合性を有しないと判定された該タンパク質を選択する工程、を含んで成る方法からなる。
(もっと読む)
糖化タンパク質割合の測定方法
【課題】特定タンパク質の糖化割合、中でもグリコアルブミン割合、グリコヘモグロビン割合、とりわけグリコヘモグロビン割合の中ではヘモグロビンA1cを測定するにあたって、簡便かつ精度良く測定できる測定方法、および糖化タンパク質割合測定用キットの提供を課題とする。
【解決手段】特定タンパク質量及び糖化された特定タンパク質量につき、これらの分解反応で生じる同一の特定アミノ酸及び/又は特定ペプチドの量を絶対量として測定する方法を見出し、キャリブレーターや標準品を用いた補正を必要としない測定方法および糖化タンパク質割合測定用キットを提供する。
(もっと読む)
α1β1インテグリンの誘導性リガンドおよび使用
本発明は、特にコラーゲンXIII とα1β1インテグリンとの間の相互作用を阻害するペプチドおよびモノクローナル抗体である薬剤の同定および使用について示す。 (もっと読む)
2,161 - 2,180 / 2,895
[ Back to top ]



